乙酰丙酸还原胺化制备5-甲基-2-吡咯烷酮
2017-04-12王彦钧蒋叶涛曾宪海
王彦钧, 李 铮, 蒋叶涛, 陈 伟, 曾宪海, 孙 勇, 林 鹿
(厦门大学 能源学院;厦门市现代农业生物质高值化技术重点实验室, 福建 厦门 361005)
·研究报告——生物质化学品·
乙酰丙酸还原胺化制备5-甲基-2-吡咯烷酮
王彦钧, 李 铮, 蒋叶涛, 陈 伟, 曾宪海, 孙 勇*, 林 鹿
(厦门大学 能源学院;厦门市现代农业生物质高值化技术重点实验室, 福建 厦门 361005)
以甲酸铵为氢源和氮源,N,N-二甲基甲酰胺为溶剂,探讨了甲酸铵直接还原胺化乙酰丙酸制备5-甲基-2-吡咯烷酮的反应途径及机理。通过实验分别考察了反应温度、 反应时间、 乙酰丙酸与甲酸铵的总质量分数和物质的量比、 体系pH值等反应条件对5-甲基-2-吡咯烷酮得率的影响趋势。结果表明,适当提高反应温度、 延长反应时间、 提高乙酰丙酸与甲酸铵的物质的量比和总质量分数、 增加体系pH值均有利于提高5-甲基-2-吡咯烷酮的得率。同时,考察了不同溶剂和乙酰丙酸衍生物在该反应体系中的应用,结果表明极性非质子溶剂甲酰胺、 N,N-二甲基乙酰胺、 二甲亚砜亦可作为该中体系反应的反应溶剂,乙酰丙酸甲酯、α-当归内酯可作为反应底物在该体系下制备5-甲基-2-吡咯烷酮。
吡咯烷酮;还原胺化;乙酰丙酸;生物质
随着全球变暖、 能源危机等问题不断加剧,由可再生能源替代传统的化石能源作原料生产大宗化学品和材料成为了研究热点[1-4]。生物质经过高效化学转化合成高附加值化学品为替代石油基产品提供了一条可持续和环境友好的路径[5]。生物质作为唯一可以提供有机碳源的可再生能源,可通过化学转化合成平台化合物,如糠醛[6]、 5-羟甲基糠醛[7]和乙酰丙酸[8]等。在这些平台化合物中,乙酰丙酸可较容易地通过生物质直接酸水解来得到[3],并可继续转化制备高附加值的生物基下游产品,如γ-戊内酯[9]、 乙酰丙酸酯[10]、 吡咯烷酮类化合物[11]等。其中,乙酰丙酸及其衍生物与伯胺还原胺化制备吡咯烷酮类化合物已引起科研界广泛的关注。吡咯烷酮类化合物因其良好的溶解性能和低毒性,广泛应用于制备医药中间体、 个人护肤品、 工业溶剂、 农药和家居清洗剂等[11]。目前,乙酰丙酸制备吡咯烷酮类化合物的研究主要以氢气为还原剂,以贵金属(Pt、 Pd、 Ir和Ru)[12-13]、 Cu和雷尼镍(Raney Ni)[11]等作为催化剂。Manzer[11]以贵金属(Pt和Ru等)和过渡金属(Cu和Co等)为催化剂,采用伯胺、 硝基化合物、 氰基化合物等作为氮源,通过一步法直接合成了吡咯烷酮类化合物,但这些合成均需在高压下进行,反应不易控制,安全性较低。Touchy等[14]制备了Pt-MoOx/TiO2固体催化剂,在无溶剂体系下,以乙酰丙酸和正辛胺为原料,100 ℃下反应20 h,5-甲基-N-正辛基-2-吡咯烷酮的得率可达99 %。然而从经济性和工业化角度来分析,昂贵的贵金属催化剂不利于乙酰丙酸还原胺化反应的工业化生产。因此,Wei等[15]建立了以二甲亚砜(DMSO)作为溶剂,采用三乙胺来调节体系的pH值,无催化剂的体系,在该体系下以乙酰丙酸、 甲酸和正辛胺为原料,100 ℃下反应12 h,5-甲基-N-正辛基-2-吡咯烷酮得率达到93 %,但二甲亚砜溶剂的高沸点不利于产物的分离。Ledoux等[16]报道了一种以乙酰丙酸、 甲酸和伯胺按照等物质的量比加料,无催化剂的反应体系,在高温(150~200 ℃)下反应4 h吡咯烷酮化合物得率可达80 %以上,但较高的甲酸浓度增加了反应的危险性。基于以上分析,乙酰丙酸还原胺化反应仍然需要更简便和安全的路径。甲酸铵已经被证明可应用于酮类化合物的刘卡特(Leuckart)反应中[17],将反应底物分子内酮羰基还原胺化为氨基。乙酰丙酸分子内就含有酮羰基,但目前还未有报道甲酸铵应用于乙酰丙酸的还原胺化反应。因此,本研究建立了以甲酸铵作为氢源和氮源,在无催化剂存在的N,N-二甲基甲酰胺(DMF)中直接还原胺化乙酰丙酸制备5-甲基-2-吡咯烷酮的反应体系,以期为乙酰丙酸及其衍生物的还原胺化提供更简便和安全的方法。
1 材料与方法
1.1 材料、 试剂和仪器
乙酰丙酸(LA)、γ-戊内酯、α-当归内酯和5-甲基-2-吡咯烷酮(5-MeP),纯度均为98 %。N,N-二甲基甲酰胺(DMF)、 甲酰胺、 甲酸铵、 N,N-二甲基乙酰胺(DMA)和二甲亚砜,均为分析纯。乙酰丙酸甲酯纯度为99 %。
安捷伦7890A气相色谱仪和美国Thermofisher Trace 1300&ISQ LT气相色谱质谱联用仪。
1.2 5-甲基-2-吡咯烷酮的制备
将1.00 g乙酰丙酸、 2.72g甲酸铵(n(乙酰丙酸)∶n(甲酸铵)=1∶5)与10.00 g N,N-二甲基甲酰胺(DMF)混合后置于50 mL带有磁子的圆底烧瓶中,待油浴锅温度升至130 ℃时将烧瓶置于油浴锅中,在500 r/min的转速下反应4 h后,取出烧瓶,待烧瓶冷却后取样分析反应液中5-甲基-2-吡咯烷酮(5-MeP)的含量。此外,在讨论pH值对反应的影响时,另外向体系中加入甲酸,调节反应体系的pH值。
1.3 产物分析
1.3.1 定性分析 采用气相色谱质谱联用仪检测反应过程中的中间体,分析条件为TR-5MS型气相毛细色谱柱(30 m×0.25 mm×0.25 mm)、 载气为氦气、 流速为1.2 mL/min、 分流比为1∶50,程序升温条件为373 K保持2 min,然后以10 K/min的升温速率升至523 K,保持5 min;质谱为EI源、 70 eV。
1.3.2 定量分析 乙酰丙酸与5-甲基-2-吡咯烷酮的含量采用气相色谱仪进行检测,分析条件为HP-INNOWAX型气相毛细色谱柱(30 m×0.25 mm×0.25 mm)、 离子火焰检测器(FID)温度543 K、 载气为氮气、 流速为24 mL/min、 分流比为1∶20,程序升温条件为373 K保持2 min,然后以10 K/min的升温速率升至523 K,保持5 min。
1.3.3 转化率、 得率及选择性 乙酰丙酸的转化率(C,%)与5-甲基-2-吡咯烷酮的得率(Y,%)和选择性(S,%)用下列公式计算:
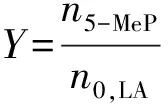
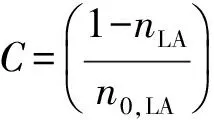
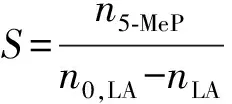
式中:n5-MeP—5-MeP的物质的量,mol;nLA—反应后LA的物质的量,mol;n0,LA—LA的初始物质的量,mol。
2 结果与讨论
2.1 反应条件对产物得率的影响
2.1.1 反应时间 反应时间对产物得率的影响如表1所示,设定其他反应条件为1.00 g乙酰丙酸、 2.72 g甲酸铵、 10.00 g N,N-二甲基甲酰胺、 温度130 ℃、 搅拌速度500 r/min。乙酰丙酸的转化率在1 h达到77.7 %, 24 h时达到100 %。5-甲基-2-吡咯烷酮的得率和选择性随着反应时间的延长逐步提高,在48 h时得率和选择性均达到54 %。值得注意的是,在反应最初8 h,乙酰丙酸转化率由77.7 %升至83.0 %,升高了5.3个百分点,而5-甲基-2-吡咯烷酮的得率由26.1 %升至40.3 %,升高了14.2个百分点。由此可以看出,乙酰丙酸的转化速率明显高于5-甲基-2-吡咯烷酮的生成速率,随着反应时间的延长,5-甲基-2-吡咯烷酮的得率增速高于乙酰丙酸的转化率,这说明在乙酰丙酸还原胺化反应过程中存在速率控制的中间步骤。结合反应时间和5-甲基-2-吡咯烷酮得率来看,反应8 h,5-甲基-2-吡咯烷酮得率达到40.3 %为较优条件。
2.1.2 反应温度 反应温度对反应的影响如表1所示,其他反应条件为1.00 g乙酰丙酸、 2.72 g甲酸铵、 10.00 g N,N-二甲基甲酰胺、 反应时间4 h、 搅拌速度500 r/min。随着温度由90 ℃升至155 ℃,5-甲基-2-吡咯烷酮的得率由17.3 %升至41.6 %,选择性由24.1 %升至51.2 %,乙酰丙酸的转化率在71.5 %到81.3 %之间变化。这表明在乙酰丙酸还原胺化反应过程中高温条件有利于甲酸的转移加氢反应。当温度进一步由155 ℃升高到175 ℃, 5-甲基-2-吡咯烷酮的选择性和得率变化不大。这可能是由于实验检测到反应液的沸点为148 ℃,进一步升高温度只是加剧了反应液沸腾回流的程度,对还原胺化反应本身并没有影响。从提高能效的角度考虑,在130 ℃下反应,5-甲基-2-吡咯烷酮得率达到35.8 %为较优条件。
2.1.3 乙酰丙酸与甲酸铵的总质量分数 乙酰丙酸与甲酸铵的物质的量比固定为1∶5,溶剂N,N-二甲基甲酰胺质量为10.00 g,通过改变乙酰丙酸与甲酸铵的总质量来探究底物总质量分数对目标产物得率的影响,结果如表1 所示。其他反应条件为反应温度130 ℃、 反应时间4 h和搅拌速度500 r/min。表1显示,随着乙酰丙酸与甲酸铵的总质量分数由3.6 %提高到35.7 %,5-甲基-2-吡咯烷酮的得率由24.9 %提高到35.3 %,乙酰丙酸的转化率由63.3 %提高到83.7 %。随着底物总质量分数由35.7 %进一步提高到55.6 %,产物得率和乙酰丙酸的转化率保持稳定。当底物总质量分数超过55.6 %,乙酰丙酸转化率保持稳定,但产物得率和选择性逐步降低。这表明适当增加底物总质量分数有利于提高产物得率,但过高会导致产物选择性的下降并影响后期产物的分离提纯。从投料和提高产率的角度看,当乙酰丙酸与甲酸铵总质量分数为55.6 %时,5-甲基-2-吡咯烷酮得率达到35.0 %为较优条件。
2.1.4 乙酰丙酸与甲酸铵物质的量比 胺与酮羰基(乙酰丙酸分子内4号位上有酮羰基)的比例会直接影响还原胺化反应[17]。本研究探讨了乙酰丙酸与甲酸铵不同物质的量比对产物得率的影响,其他反应条件为1.00 g乙酰丙酸、 10.00 g N,N-二甲基甲酰胺、 反应温度130 ℃、 反应时间4 h和搅拌速度500 r/min。如表1所示,随着乙酰丙酸与甲酸铵的物质的量比由1∶1提高到1∶25,5-甲基-2-吡咯烷酮的得率由13.1 %提高至50.7 %。当乙酰丙酸与甲酸铵的物质的量比达到1∶10时,乙酰丙酸的转化率达到100 %。随着物质的量比由1∶10逐渐提高至1∶25,产物的得率和选择性由45.3 %缓慢增至50.7 %,增大了5.4个百分点。这可能是由于随着甲酸铵用量的增加,分解产生的甲酸含量升高,促进了反应的正向进行,但过多的甲酸铵会导致副反应发生,对提高产物得率贡献不大。从节约投料成本的角度考虑,乙酰丙酸与甲酸铵物质的量比为1∶10,5-甲基-2-吡咯烷酮的得率达到45.3 %为较优条件。
2.1.5 体系pH值 反应体系的pH值被认为是影响还原胺化反应的重要因素[18]。固定其他反应条件为1.00 g乙酰丙酸、 2.72 g甲酸铵、 10.00 g N,N-二甲基甲酰胺、 反应温度130 ℃、 反应时间4 h和搅拌速度500 r/min,通过向体系中加入不同含量甲酸来调节体系的pH值,研究体系pH值对反应的影响,结果见表1。随着体系pH值由8.38降至3.86,5-甲基-2-吡咯烷酮的得率由35.8 %降至15.1 %,与此同时,乙酰丙酸的转化率由79.8 %降至50.0 %。产物得率和乙酰丙酸转化率下降可能的原因在于,在本研究中,氨由甲酸铵的分解产生,而高甲酸添加量会抑制甲酸铵分解产生甲酸和氨的反应,同时酸性条件下氨基的质子化也可导致氨基亲核反应活性下降,这2种原因导致了产物得率和乙酰丙酸转化率大幅降低[15]。因此,当体系pH值为6.99时,5-甲基-2-吡咯烷酮的得率为37.7 %为较优条件。
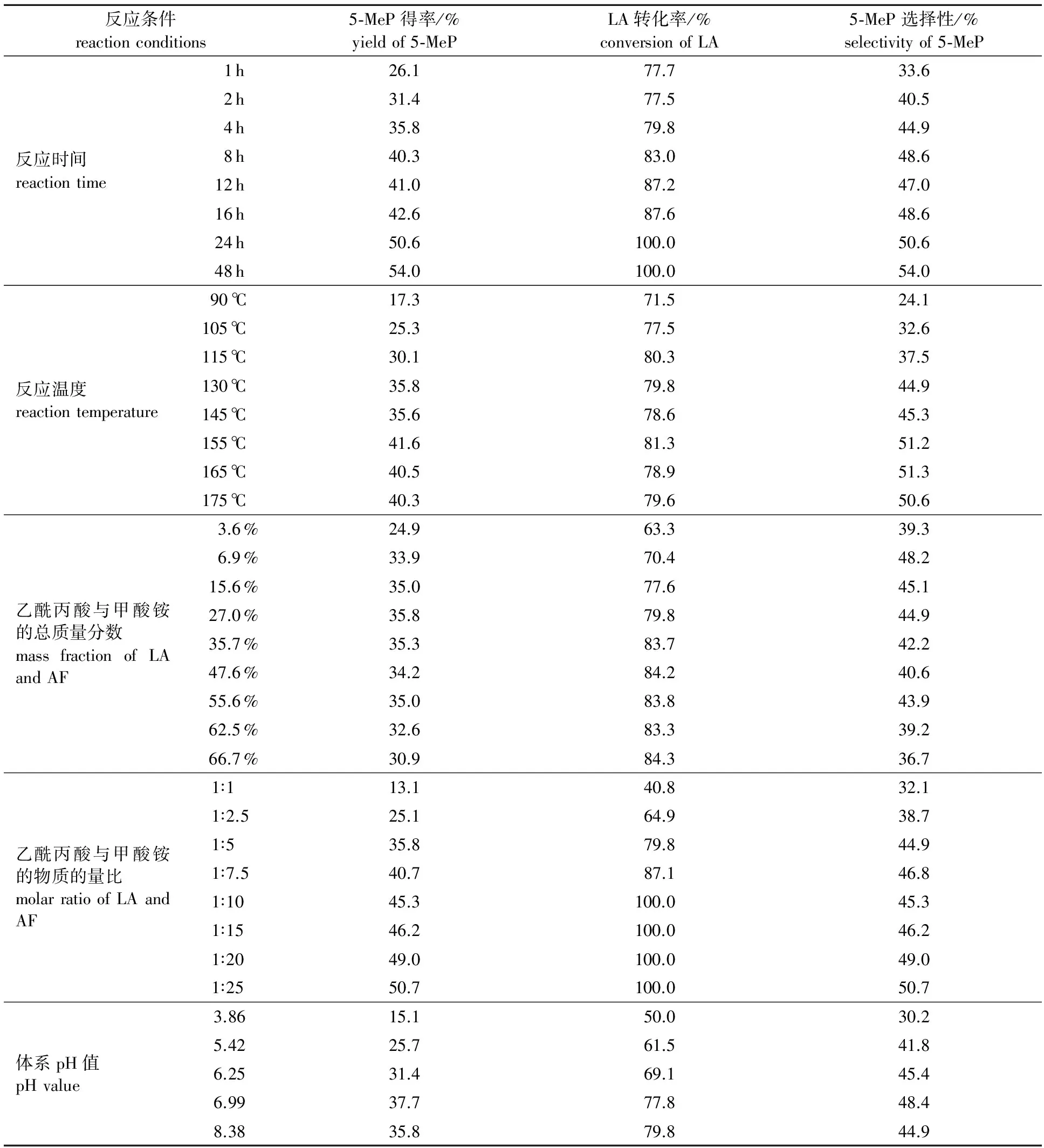
表1 反应条件对5-甲基-2-吡咯烷酮得率的影响
2.2 反应机理的探讨
综合以上分析可知,乙酰丙酸还原胺化反应存在速率控制步骤。同时,实验发现以乙酸铵代替甲酸铵作为氮源在该体系同样条件下反应1 h,主要生成不饱和吡咯烷酮化合物5-甲基-3,4-二氢-2-吡咯酮。由前期文献报道[19-20]和本研究的检测结果来看,反应中的速率控制步骤很可能是甲酸的转移加氢,导致中间产物不易还原。推测反应机理如图1所示,路径A为: 1)乙酰丙酸的羰基被氨取代生成亚胺中间体γ-亚胺戊酸; 2)亚胺中间体在甲酸转移加氢作用下还原生成γ-氨基戊酸; 3)γ-氨基戊酸分子内脱水成环生成5-甲基-2-吡咯烷酮。路径B为: 1)乙酰丙酸的羰基被氨取代生成亚胺中间体γ-亚胺戊酸; 2)亚胺中间体γ-亚胺戊酸直接脱水成环,生成环状化合物5-甲基-3,4-二氢-2-吡咯酮; 3) 5-甲基-3,4-二氢-2-吡咯酮在甲酸转移加氢作用下还原生成5-甲基-2-吡咯烷酮。后期研究中该体系的反应机理仍有待进一步探讨。
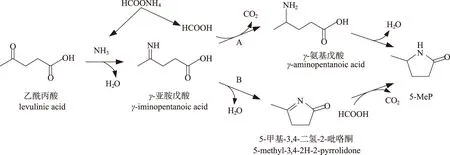
图1 乙酰丙酸还原胺化制备5-甲基-2-吡咯烷酮的反应机理
2.3 不同溶剂及乙酰丙酸衍生物在反应中的应用
除了上述所讨论的影响因素外,Touchy等[14]和Wei等[15]在研究中指出,溶剂的极性和溶剂化作用也是影响吡咯烷酮合成的重要因素。本研究探讨了不同溶剂在该体系的应用,反应条件为1.00 g乙酰丙酸、 乙酰丙酸与甲酸铵的物质的量比为1∶5、 10.00 g溶剂、 反应温度130 ℃、 反应时间4 h和搅拌速度500 r/min,结果如表2所示。

表2 不同溶剂及乙酰丙酸衍生物在该体系的应用
在使用极性质子溶剂水和甲酸作为体系溶剂时,产物得率分别为0和14.1 %。然而,在使用极性非质子溶剂甲酰胺、 N,N-二甲基甲酰胺、 N,N-二甲基乙酰胺和二甲亚砜作为反应溶剂时,5-甲基-2-吡咯烷酮的得率分别为28.4 %、 35.8 %、 50.7 %和62.1 %,产物得率明显高于极性质子溶剂。这可能是由于极性非质子溶剂的高pKa有助于氨基以大量自由态存在于体系中,避免被质子化,从而有利于氨基与羰基的亲核反应[15],而以不同极性非质子溶剂作为体系溶剂时产物得率差异较大则可能是由于不同极性非质子溶剂自身的理化性质不同。
此外,本研究还探讨了乙酰丙酸的衍生物如乙酰丙酸甲酯、α-当归内酯和γ-戊内酯在该反应体系中的应用,反应条件为1.00 g乙酰丙酸衍生物、 乙酰丙酸衍生物与甲酸铵的物质的量比为1∶5、 10.00 g N,N-二甲基甲酰胺、 反应温度130 ℃、 反应时间4 h和搅拌速度500 r/min。乙酰丙酸甲酯与α-当归内酯作为底物时产物得率分别为38.3 %和30.8 %,而γ-戊内酯做底物时并没有反应发生,这可能是由于其羧酸中的羰基亲核反应活性较低的缘故。
综上讨论,极性非质子溶剂如甲酰胺、 N,N-二甲基乙酰胺和二甲亚砜同样可作为该体系的反应溶剂。乙酰丙酸衍生物如乙酰丙酸甲酯和α-当归内酯也可作为反应底物在该体系下制备5-甲基-2-吡咯烷酮。
3 结 论
3.1 在无催化剂的N,N-二甲基甲酰胺(DMF)溶剂体系下,研究了由甲酸铵直接还原胺化乙酰丙酸制备高附加值化合物5-甲基-2-吡咯烷酮,提出了可能的反应机理,并对反应条件进行了优化。结果显示,适当提高反应温度、 延长反应时间、 提高乙酰丙酸与甲酸铵的物质的量比和总质量分数、 增加体系pH值均有利于提高5-甲基-2-吡咯烷酮的得率。
3.2 在优化反应条件的基础上,还研究了溶剂及乙酰丙酸衍生物对反应体系的影响,结果表明,极性非质子溶剂有助于氨基自由基的存在和亲核攻击,甲酰胺、 N,N-二甲基乙酰胺、 二甲亚砜同样可作为该体系的反应溶剂。此外,乙酰丙酸衍生物如乙酰丙酸甲酯、 α-当归内酯也可作为反应底物在该体系下制备5-甲基-2-吡咯烷酮。
[1]LIU S J,ZHANG Z S,SCOTT G M. The biorefinery:Sustainably renewable route to commodity chemicals,energy,and materials[J]. Biotechnology Advances,2010,28(5):541-542.
[2]BOZELL J J. Connecting biomass and petroleum processing with a chemical bridge[J]. Science,2010,329(5991):522-523.
[3]BOZELL J J,PETERSEN G R. Technology development for the production of biobased products from biorefinery carbohydrates:The US Department of Energy’s “Top 10” revisited[J]. Green Chemistry,2010,12(4):539-554.
[4]TANG X,ZENG X H,Li Z,et al. Production ofγ-valerolactone from lignocellulosic biomass for sustainable fuels and chemicals supply[J]. Renewable and Sustainable Energy Reviews,2014,40:608-620.
[5]MASCAL M,NIKITIN E B. Direct,high-yield conversion of cellulose into biofuel[J]. Angewandte Chemie International Edition,2008,47(41):7924-7926.
[6]WEINGARTEN R,TOMPSETT G A,CONNER W C,et al. Design of solid acid catalysts for aqueous-phase dehydration of carbohydrates:The role of Lewis and Brønsted acid sites[J]. Journal of Catalysis,2011,279(1):174-182.
[7]ZHAO H B,HOLLADAY J E,BROWN H,et al. Metal chlorides in ionic liquid solvents convert sugars to 5-hydroxymethylfurfural[J]. Science,2007,316(5831):1597-1600.
[8]RACKEMANN D W,DOHERTY W. The conversion of lignocellulosics to levulinic acid[J]. Biofuels Bioproducts and Biorefining,2011,5(2):198-214.
[9]LI Z,TANG X,JIANG Y T,et al. Atom-economical synthesis ofγ-valerolactone with self-supplied hydrogen from methanol[J]. Chemical Communications,2015,51:16320-16323.
[10]HU X,LI C Z. Levulinic esters from the acid-catalysed reactions of sugars and alcohols as part of a bio-refinery[J]. Green Chemistry,2011,13:1676-1679.
[11]MANZER L E. Production of 5-methyl-N-aryl-2-pyrrolidone and 5-methyl-N-cycloalkyl-2-pyrrolidone by reductive amination of levulinic acid with aryl amines:US 6863722[P]. 2005-03-08.
[12]DU X L,HE L,ZHAO S,et al. Hydrogen-independent reductive transformation of carbohydrate biomass intoγ-valerolactone and pyrrolidone derivatives with supported gold catalysts[J]. Angewandte Chemie International Edition,2011,50(34):7815-7819.
[13]HUANG Y B,DAI J J,DENG X J,et al. Ruthenium-catalyzed conversion of levulinic acid to pyrrolidines by reductive amination[J]. ChemSusChem,2011,4(11):1578-1581.
[14]TOUCHY A S,SIDDIKI S H,KON K,et al. Heterogeneous Pt catalysts for reductive amination of levulinic acid to pyrrolidones[J]. ACS Catalysis,2014,4(9):3045-3050.
[15]WEI Y W,WANG C,JIANG X,et al. Catalyst-free transformation of levulinic acid into pyrrolidinones with formic acid[J]. Green Chemistry,2014,16:1093-1096.
[16]LEDOUX A,KUIGWA L S,FRAMERY E,et al. A highly sustainable route to pyrrolidone derivatives:Direct access to biosourced solvents[J]. Green Chemistry,2015,17:3251-3254.
[17]KITAMURA M,LEE D,HAYASHI S,et al. Catalytic leuckart-wallach-type reductive amination of ketones[J]. Journal of Organic Chemistry,2002,67(24):8685-8687.
[18]OGO S,UEHARA K,ABURA T,et al. pH-Dependent chemoselective synthesis ofα-amino acids. Reductive amination ofα-keto acids with ammonia catalyzed by acid-stable iridium hydride complexes in water[J]. Journal of the American Chemical Society,2004,126(10):3020-3021.
[19]WEI Y W,WANG C,JIANG X,et al. Highly efficient transformation of levulinic acid into pyrrolidinones by iridium catalysed transfer hydrogenation[J]. Chemical Communications,2013,49:5408-5410.
[20]ORTIZ-CERVANTES C,FLORES-ALAMO M,GARCIA J J. Synthesis of pyrrolidones and quinolines from the known biomass feedstock levulinic acid and amines[J]. Tetrahedron Letters,2016,57(7):766-771.
《生物质化学工程》征稿简约
《生物质化学工程》是中国林科院林产化学工业研究所主办的技术类刊物。报道范围是可再生的木质和非木质生物质资源的化学加工与利用,包括生物质能源、生物质化学品、生物质新材料、生物质天然活性成分和制浆造纸等。主要报道内容为松脂化学、生物质能源化学、生物质炭材料、生物基功能高分子材料、胶黏剂化学、森林植物资源提取物化学利用、环境保护工程、木材制浆造纸为主的林纸一体化和林产化学工程设备研究设计等方面的最新研究成果。为了保证刊物的质量,根据国家的有关标准和本刊的实际,特制定本简约。
1 文稿具体要求
1.1 基本要求 论文应有一定的科学性、创新性、实用性和可读性,要求内容充实,数据可靠,论点明确,文字精练。
1.2 书写顺序 题目(题目应简洁、明确地反映研究成果的实质及特点,字数不超过20字),作者姓名、单位(署名顺序按对文章贡献大小排列),中文摘要,关键词(关键词3~5个),中图分类号,英文摘要,正文,致谢,参考文献。
我国基坑在施工过程中已发生较多事故,大部分原因为基坑周边和地下水位之间没有做好处理,导致倾覆危险,本文通过介绍使用三轴搅拌桩应用于止水帷幕中的优点,今后在实际施工过程中应更多的使用此类安全、快捷的方法,最大程度的保护施工人员的安全,为我国建筑行业树立更加优秀的形象。
1.3 摘要 论文摘要的基本要素包括研究的目的、方法、结果和结论。应具有独立性和自明性,即不阅读全文,就能获得必要的信息(中文摘要以200~300字为宜)。英文摘要与中文摘要内容一致,语句通顺(长度一般不超过150 words)。
1.4 前言 论文的前言部分不编号,不计算进正文层次。文字应尽可能的简明扼要,对之前的同类研究数据简短概括并标注参考文献即可,且前言部分应少分段,尽可能不分段,不出现图、表、分子式和化学式等。
1.5 正文层次标注 层次标题应简短明确,各层次一律用阿拉伯数字连续编号,不同层次的数字之间用下圆点“.”相隔,最末数字后面不加标点,如:“1”、“2.1”、“3.1.2”,一律左顶格。
1.6 外文、计量单位及符号 论文中的外文及符号要求区分文种、正/斜体、黑/白体、上/下角和大/小写,动植物及微生物名称在正文中第一次出现时,须加注拉丁文学名(斜体)。计量单位按GB/T 3100~3102—1993,符号按GB/T 15834—2011的规定执行。
1.7 图、表 图、表应具有自明性,其内容要与正文相呼应,并附相应的英文对照。表格设计要合理,一律用三线表(必要时可加辅助线)。
1.8 参考文献 参考文献必须标全并注意引用国内外及本刊的最新文献,以公开发表的、作者亲自阅读的文献为限,并由作者对照原文一一核实。格式按GB/T 7714—2015的规定,采用顺序编码制,即所引文献应按文中出现的顺序随文标注,在正文引用处右上角用方括号标出文献序号。
1.9 作者简介(加注在论文的首页页脚) 来稿请注明第一作者的出生年,性别(民族——汉族可省略),籍贯(含省、县),职称,学位及研究方向。如有通讯作者的,请注明职称、学位、博(硕)导等状况及专业领域。
2 投稿约定
[][]
2.2 稿件经编辑部初审后送1~2位专家审阅,之后编辑部将审稿意见反馈给作者,对于拟发表的稿件,作者应根据审稿人和编辑部的意见对稿件进行修改,在指定时间内修回,同时提供电子文档,交纳版面费。修改后的稿件统一由主编终审后再排版印刷(稿件一经发排,不得擅自修改或变更作者署名,且一般不得对文稿进行增删)。来稿一经发表,即按篇酌付稿酬,并赠送当期期刊2册、单行本5份。
2.3 所有稿件均需提供“版权转让协议书”,内容包括:文章题名、作者姓名及其排序,无泄密情况,无一稿多投;若为基金项目请给出项目名称及编号(加注在论文的首页页脚)。
2.4 来稿文责自负,请勿一稿多投。编辑部对来稿有权作技术性和文字修饰,但实质性内容的修改须征得作者同意。
2.5 凡本刊发表的文章将有可能进入国内外相关数据库并在互联网上运行,其作者著作权使用费与本刊稿酬一次性给付。如作者不同意将文章编入相关数据库,请在来稿时声明,本刊将做适当处理。
3 编辑部联系方式
地址:210042 南京市锁金五村16号 林化所内《生物质化学工程》编辑部;电话:(025)85482492;传真:(025)85482492;E-mail:bce@vip.163.com;http: ∥www.bce.ac.cn。
Reductive Amination of Levulinic Acid to 5-Methyl-2-pyrrolidone
WANG Yanjun, LI Zheng, JIANG Yetao, CHEN Wei, ZENG Xianhai, SUN Yong, LIN Lu
(College of Energy;Key Laboratory of High-valued Conversion Technology of Agricultural Biomass in Xiamen,Xiamen University, Xiamen 361005, China )
The reductive amination of levulinic acid with ammonium formate as hydrogen and nitrogen donor to synthesize 5-methyl-2-pyrrolidone(5-MeP) in DMF solvent was developed and the mechanism of this process was proposed. The effects of various reaction conditions including temperature,reaction time,mass fraction and molar ratio of levulinic acid with ammonium formate and pH value on 5-methyl-2-pyrrolidone yield were investigated. Meanwhile,different solvents and levulinate derivatives were investigated in this system. The results showed that the properly increasing temperature,reaction time,the molar ratio and total mass fraction of levulinic acid and ammonium formate,and the pH value of system could improve the yield of 5-methyl-2-pyrrolidone. The polar aprotic solvents including formamide,DMA,DMSO and levulinate derivatives,such as methyl levulinate andα-angelica lactone,could also be respectively used as solvents and substrates in this system,too.
pyrrolidone;reductive amination;levulinic acid;biomass
10.3969/j.issn.1673-5854.2017.02.004
2016-05-11
福建省自然科学基金资助项目(2016J01077);厦门大学校长基金资助项目(20720160087)
王彦钧(1989— ),男,山东文登人,硕士生,主要从事制备生物质基产品的研究工作
*通讯作者:孙 勇,副教授,硕士生导师,研究领域为生物炼制和生物能源化学;E-mail:sunyong@xmu.edu.cn。
TQ31;TQ35
A
1673-5854(2017)02-0019-07
