腹腔镜胃癌D2根治术联合腹腔内热灌注化疗治疗胃癌的疗效研究①
2017-04-12郭明浩
郭明浩
(南阳医学高等专科学校第一附属医院,河南 南阳,473000)
·论 著·
腹腔镜胃癌D2根治术联合腹腔内热灌注化疗治疗胃癌的疗效研究①
郭明浩
(南阳医学高等专科学校第一附属医院,河南 南阳,473000)
目的:探讨腹腔镜下胃癌D2淋巴结根治术联合术后腹腔内热灌注化疗治疗胃癌的临床疗效。方法:选取2010年1月至2013年9月收治的120例胃癌患者作为研究对象,采用前瞻性研究方法随机分为观察组与对照组,观察组行腹腔镜胃癌D2根治术联合术后腹腔内热灌注化疗、术后化疗;对照组行腹腔镜胃癌D2根治术联合术后化疗,观察两组术后并发症、复发率、生存率。结果:观察组术后并发症发生率为26.67%,对照组为25%,两组差异无统计学意义。随访1年、2年,两组复发率、生存率差异无统计学意义。随访3年,观察组复发率为30%,生存率为81.67%;对照组复发率为50%,生存率为58.33%,差异均有统计学意义。结论:腹腔镜胃癌D2根治术联合术后腹腔内热灌注化疗安全、有效,不增加术后并发症发生率,且可提高生存率,降低复发率,值得临床推广应用。
胃肿瘤;胃癌D2根治术;腹腔镜检查;腹腔内热灌注化疗;治疗结果
目前胃癌的治疗以手术切除结合放化疗的综合治疗为主。其中手术治疗是主要方式,新版的胃癌治疗指南与共识将胃癌D2根治术作为胃癌的标准术式(适应证:Ⅰb期、Ⅱ期、Ⅲ期)[1]。腹腔镜下胃癌根治性切除术具有术野清晰、解剖操作精准、出血少、腹腔组织损伤小、术后患者疼痛轻、康复快、住院时间短等优势,被广大患者及临床医师接受[2-3]。研究表明,大多数胃癌患者死于肿瘤复发或转移。文献报道,胃癌根治术后5年生存率仅为39%~45%,而术后切除部位复发率为60%~90%,腹膜转移率高达50%,肝转移率30%[4]。如何防止肿瘤腹腔内转移复发,改善胃癌患者的预后,成为临床研究的热点。术后腹腔内热灌注化疗(intraperitoneal hyperthermic chemotherapy,IPHC)作为进展期胃癌治疗的有机组成部分受到越来越广泛的重视,我院也取得了令人欣喜的效果。本研究采用腹腔镜胃癌D2根治术联合术后IPHC及辅助化疗治疗Ⅱ~Ⅲ期胃癌取得了满意疗效。现将结果报道如下。
1 资料与方法
1.1 临床资料 选取2010年1月至2013年9月我院收治的120例胃癌病例,入组标准:(1)术前均经胃镜病理检查确诊;(2)未进行任何治疗(包括手术、化疗、放疗、生物免疫治疗等);(3)术前肿瘤分期Ⅱ~Ⅲ期;(4)术前检查心肺肝肾功能良好,无IPHC及全身化疗禁忌证;(5)均行腹腔镜胃癌根治D2淋巴结清扫术,淋巴结数量在15枚以上;(6)术后能按时复诊;(7)38~75岁,平均(59.5±4.3)岁。根据治疗方案分为观察组与对照组,观察组(n=60)行腹腔镜下胃癌D2根治术联合术后IPHC治疗3次+术后辅助全身化疗;对照组(n=60)行腹腔镜胃癌D2根治术联合术后辅助全身化疗。两组患者临床资料见表1。随访截至2016年9月。本研究经我院道德伦理委员会批准并签订相关治疗知情同意书。


组别性别(n)男女年龄(岁)手术方式(n)近端胃切除术远端胃切除术全胃切除术病理分型(n)高分化中分化低分化印戒细胞癌粘液腺癌TNM分期(n)Ⅱ期Ⅲ期观察组352561.5±6.2301416123010353228对照组322859.7±5.5321315152515233525t/χ2值2.5360.4000.1360.4000.950P值0.2810.8190.9340.8190.622
1.2 手术方法 根据肿瘤位置、大小、受侵犯范围选择全胃切除、近端胃大部切除、远端胃大部切除,手术均严格按日本胃癌公约(2010版)行腹腔镜下胃癌D2根治术淋巴结清扫标准操作,使用切割闭合器及吻合器分别行食管-空肠吻合、食管-胃吻合、胃-空肠吻合等消化道重建。观察组术后于肝肾隐窝、脾窝、左下腹及右下腹部交叉放置IPHC专用导流管,对照组于小网膜孔及吻合口周围放置腹腔引流管1~2根。观察组术后采用BR-TRG-Ⅱ型体腔热灌注治疗系统进行治疗,具体操作:按说明书连接循环器套管,先将3 000~4 000 ml灌注液(含顺铂60 mg/m2+5-氟尿嘧啶1 000 mg/m2)预热至40℃后进行治疗,灌注液注入腹腔的容量、时间根据患者耐受力确定。通常设置腹腔灌注温度43℃,灌注速度为350~500 ml/min,灌注60~90 min。连续灌注3次,一般于术后72 h内完成,每天一次。化疗药物总量控制铂类<200 mg,5-FU<5 g。两组术后6个月内均采用FOLFOX6方案进行术后全身辅助化疗:第1天静脉滴注奥沙利铂100 mg/m2,维持3 h;亚叶酸钙200 mg/m2维持2 h;随后5-氟尿嘧啶按照(2.4~3.6) g/m2持续48 h泵入,每3周重复1次,共计6次。全身静脉化疗结束后对两组患者进行近期疗效评价。
1.3 观察指标 对比分析两组术后并发症(吻合口瘘、腹腔感染、吻合口出血、胸腔积液、肺部感染、切口液化感染、淋巴瘘及术后胃瘫)。术后定期随访,观察术后1年、2年、3年肿瘤复发率及生存率。

2 结 果
2.1 两组术后并发症的比较 观察组术后并发症发生率为26.67%(16/60);对照组为25%(15/60),两组相比差异无统计学意义(P>0.05),见表2。
2.2 两组远期疗效的比较 两组患者定期随访,随访1年、2年,两组复发率、生存率差异无统计学意义(P>0.05);随访3年,观察组复发率为30%(18/60),对照组为50%(30/60);观察组生存率为81.67%(49/60),对照组为58.33%(35/60),两组复发率、生存率差异有统计学意义(P<0.05)。见表3。
表2 两组患者术后并发症发生率的比较[n(%)]
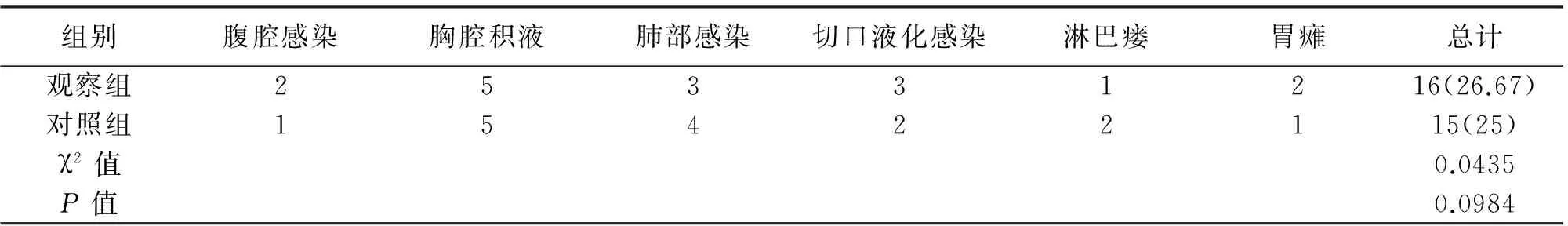
组别腹腔感染胸腔积液肺部感染切口液化感染淋巴瘘胃瘫总计观察组25331216(26.67)对照组15422115(25)χ2值0.0435P值0.0984
表3 两组患者复发率与生存率的比较[n(%)]

组别随访1年复发率生存率随访2年复发率生存率随访3年复发率生存率观察组5(8.33)59(98.33)15(25)55(91.67)18(30)49(81.67)对照组8(13.33)57(95)20(33.33)48(80)30(50)35(58.33)χ2值0.77640.25861.00843.35815.0007.7778P值0.2540.09850.6375.2410.00240.001
3 讨 论
我国是胃癌大国,目前胃癌的治疗原则仍以手术根治性切除为主加放化疗为辅的综合治疗方案。近年,腹腔镜下胃癌D2根治术在临床已被广泛应用于进展期胃癌的治疗,其可行性已被多次证实。但如何降低术后肿瘤复发率、减少术中肿瘤细胞或微小癌结节的脱落问题[5-6],各大肿瘤诊疗中心进行了大量实验,但效果均不是特别理想。
腹腔镜下癌细胞或微小癌结节的脱落是造成肿瘤复发的重要因素之一,已引起外科医生们的高度关注[7-8]。腹腔镜胃癌根治术后腹腔内复发的机制目前公认的有“种子-土壤学说”:(1)术前肿瘤一旦侵及浆膜层就有可能脱落于腹腔,腹腔镜操作时,持续较长时间的腹腔高压状态,使肿瘤细胞的脱落、移位更可能沿胃肠壁、血管、淋巴管甚至腹壁切口弥散,使肿瘤细胞及微小癌结节脱落后的移位种植播散性增大。(2)腹腔镜操作时,腹腔存在较长时间的CO2充盈状态,可改变腹腔pH值,加重腹腔组织缺氧,降低患者的免疫功能,促进脱落肿瘤细胞的转移种植。(3)术中应用超声刀等设备,切割组织时超声雾化效应使肿瘤转移种植的可能性更大。(4)切断胃肠道行消化道重建时,胃肠腔内的癌细胞随胃肠液也可进入腹腔内。这些脱落于腹腔的游离癌细胞就成为复发的“种子”。因此术中及术后进行IPHC有助于及时杀灭脱落癌细胞,控制微病灶,减少术后复发与转移。
IPHC是根据腹腔特有的解剖学特点设计的选择性区域化疗,综合了温热效应、化疗药物、腹腔灌洗三方面的作用以杀灭癌细胞。其治疗原理包括以下几点[9-11]:(1)温热效应对癌细胞的直接杀伤作用。癌细胞主要以无氧糖酵解为获能方式,43℃温度条件下细胞内乳酸堆积,增加了癌细胞对热的敏感性,同时癌细胞含水量明显高于一般软组织,蓄热潜能大,导致恶性肿瘤细胞较正常细胞更容易受到热损伤。适当的高温就达到杀伤癌细胞又保护正常组织的目的。(2)热疗联合化疗可发挥出1+1>2的效果。实验证明,由于温热效应可促进药物与癌细胞的结合,并能改变癌细胞的通透性,利于化疗药物渗入癌细胞内发挥作用,丝裂霉素、顺铂、5-FU等化疗药物在加温条件下抗癌作用明显增强。(3)扩大化疗药物的作用范围。腹腔灌注除了通过机械灌洗作用可清除腹腔内的残留癌细胞,从而减少种植的机会外,还可促使腹腔所有脏器、腹膜表面都能与化疗药物直接接触,从而使化疗药物对肿瘤细胞的杀伤范围最大化。(4)延长化疗药物的作用时间。由于存在“腹膜-血浆屏障”作用,化疗药物腹腔内给药在腹膜表面所达到的浓度要远高于静脉血管给药。由于腹膜超强的吸收能力,即使腹腔灌注液体排出后仍有部分药物留在体内发挥作用。
但在实际临床工作实践中,部分医师及患者家属往往担心IPHC的副作用,如在43℃和化疗药物充满腹腔的环境下吻合口的安全问题,会不会引起腹腔感染、肺部感染及残胃功能恢复延迟等问题。本研究结果显示,患者术后经过3次腹腔热灌注化疗联合6次辅助化疗后,对比单纯6次辅助化疗,吻合口瘘、腹腔感染、吻合口出血、胸腔积液、肺部感染、切口液化感染、淋巴瘘及术后胃瘫等并发症发生率并无明显增加,反而经过腹腔热灌注化疗3年后肿瘤复发率明显降低,生存率有所上升,表明腹腔热灌注化疗是安全、有效的,对吻合口生长没有影响,不会引起腹腔及肺部感染,术后胃肠道功能的恢复不会产生延迟,且可降低远期复发率、提高生存率。这与文献研究结果相似[12-14]。
综上所述,腹腔镜胃癌D2根治术联合术后腹腔热灌注化疗治疗胃癌安全、有效,不仅不增加并发症发生率,还可降低远期复发率、提高3年生存率,值得临床推广。
[1] 中华医学会外科学分会腹腔镜与内镜外科学组,中国研究型医院学会机器人与腹腔镜外科专业委员会.腹腔镜胃癌手术操作指南(2016版)[S].中华消化外科杂志,2016,15(9):851-857.
[2] Lu J,Wei ZQ,Huang CM,et al.Small-volume chylous ascites after laparoscopic radical gastrectomy for gastric cancer:results from a large population-based sample[J].World J Gastroenterol,2015,21(8):2425-2432.
[3] Zang L.Laparoscopic radical gastrectomy for gastric cancer:traps and strategies[J].Ann Transl Med,2015,3(9):125.
[4] 吴晓江,贾永宁,季加孚.腹腔热灌注化疗在胃癌腹腔转移治疗中的价值[J].中国实用外科杂志,2015,35(10):1071-1075.
[5] 夏渭超,胡彦锋,牟廷裕,等.胃癌并腹膜转移腹腔镜姑息性切除术后腹腔热灌注化疗的安全性及疗效[J].中华胃肠外科杂志,2014,17(11):1087-1091.
[6] 李帅超,任柯,朱元增,等.腹腔镜根治联合术后热灌注并SOX方案化疗治疗进展期胃癌临床疗效分析[J].中国实用医刊,2015,42(8):60-62.
[7] Suda K,Man-I M,Ishida Y,et al.Potential advantages of robotic radical gastrectomy for gastric adenocarcinoma in comparison with conventional laparoscopic approach:a single institutional retrospective comparative cohort study[J].Surg Endosc,2015,29(3):673-685.
[8] Gong JQ,Cao YK,Wang YH,et al.Three-step hand-assisted laparoscopic surgery for radical distal gastrectomy:an effective surgical approach[J].Int J Clin Exp Med,2014,7(8):2156-2164.
[9] 莫德龙,万进,刁德昌,等.循环腹腔热灌注化疗用于老年胃肠肿瘤患者的安全性[J].广东医学,2015,36(14):2213-2215.
[10] 吴引兵,巴明臣,崔书中,等.进展期胃癌腹腔热灌注化疗临床疗效与安全性Meta分析[J].中华肿瘤防治杂志,2013,20(21):1686-1690.
[11] Hu MG,Ou-yang CG,Zhao GD,et al.Outcomes of open versus laparoscopic procedure for synchronous radical resection of liver metastatic colorectal cancer:a comparative study[J].Surg Laparosc Endosc Percutan Tech,2012,22(4):364-369.
[12] 胡娜,梁家铭,苏莹莹,等.老年胃癌腹腔热灌注化疗联合静脉化疗治疗恶性腹水的临床疗效[J].中国老年学杂志,2015,35(16):4578-4579.
[13] 李欣.老年胃癌患者术后腹腔热灌注化疗联合静脉化疗的疗效和安全性[J].中国老年学杂志,2015,35(13):3642-3644.
[14] 姬忠贺,孙建华,武海涛,等.腹腔热灌注化疗对腹腔游离癌细胞杀灭效果的评价[J].中国肿瘤临床,2015,42(19):963-968.
(英文编辑:杨庆芸)
Research on clinical effects of laparoscopic D2 radical gastrectomy and intraperitoneal hyperthermic chemotherapy for gastric cancer
GUOMing-hao.
DepartmentofGeneralSurgery,theFirstHospitalofNanyangMedicalCollege,Nanyang473000,China
Objective:To investigate the clinical effect of laparoscopic D2 radical gastrectomy and postoperative intraperitoneal hyperthermic chemotherapy (IPHC) for gastric cancer.Methods:A retrospective analysis was conducted on the data of 60 patients (control group) who underwent laparoscopic D2 radical gastrectomy for gastric cancer and 60 patients (observation group) who underwent laparoscopic D2 radical gastrectomy combined with IPHC from Jan.2010 to Sep.2013.The two groups were given chemotherapy after surgery.The indexes related to the complications,recurrence rate and survival rate were compared between the two groups.Results:The incidence of postoperative complications was 26.67% in the observation group,the control group was 25%,there was no statistically significant difference.After follow-up for one to two years,the recurrence rate and survival rate were not significantly different.After 3 years,in observation group the recurrence rate was 30%,the survival rate was 81.67%;in control group the recurrence rate was 50%,the survival rate was 58.33%,the differences were statistically significant.Conclusions:For gastric cancer,the laparoscopic D2 radical gastrectomy combined with IPHC is safe and effective,dose not increase postoperative complicatios, can increase survival rate and decrease recurrence rate.It is worthy to be popularized in clinical application.
Stomach neoplasms;D2 radical gastrectomy;Laparoscopy;Intraperitoneal hyperthermic chemotherapy;Treatment outcome
1009-6612(2017)01-0042-04
10.13499/j.cnki.fqjwkzz.2017.01.042
R735.2
A
2016-09-18)
①*作者简介:郭明浩(1981—)男,河南省南阳医学高等专科学校第一附属医院普通外科主治医师,主要从事腹腔镜下胃肠手术方面的研究。
