一种含酯基的咪唑啉型季铵盐化合物的合成及性能研究
2017-04-10樊国栋魏晓晓
樊国栋, 魏晓晓
(陕西科技大学 化学与化工学院 教育部轻化工助剂化学与技术重点实验室, 陕西 西安 710021)
一种含酯基的咪唑啉型季铵盐化合物的合成及性能研究
樊国栋, 魏晓晓
(陕西科技大学 化学与化工学院 教育部轻化工助剂化学与技术重点实验室, 陕西 西安 710021)
以咪唑啉与己二酰氯为原料,三乙胺为缚酸剂,二氯甲烷为溶剂首先合成酸酯,然后以氯乙酸对合成的酸酯进行季铵化反应,得到一种含酯基的咪唑啉型季铵盐化合物.采用红外光谱对合成的物质进行结构表征,利用静态挂片失重法和电化学方法考察了该季铵盐化合物对A3钢片在盐酸介质中的缓蚀效果,并通过扫描电镜对缓蚀剂使用前后的A3钢片形貌进行了表征.静态挂片失重法结果表明,在温度为60 ℃,当咪唑啉型季铵盐化合物添加量为90 mg/L时,对A3钢片在15%的HCl溶液中缓蚀率可达95.94%,缓蚀效果明显.电化学实验表明该缓蚀剂为混合型缓蚀剂,溶液中加入缓蚀剂后,交流阻抗半径变大,腐蚀电流减小.形貌观察显示加入缓蚀剂后碳钢表面腐蚀迹象明显减弱.
酯基; 咪唑啉型季铵盐化合物; 盐酸; 缓蚀性能
0 引言
目前,我国主要依靠管道来完成石油和天然气等资源的输送过程,这些输送管道的主要材质为钢铁,由于管道穿越的地形及环境复杂,它会受到一些微生物的侵蚀以及土壤介质的腐蚀,土壤介质中由于有CO2和H2S这些气体的存在而略显酸性.
CO2是石油开采过程中的伴生气体,也是天然气的组分之一,其溶于水很容易形成碳酸,腐蚀性极强.CO2腐蚀主要是去氢极化腐蚀,当它溶于水时,发生CO2+H2O=HCO3-+H+反应,从而使介质酸性增强,且腐蚀产物易溶于水而使金属管道表面裸露在酸性介质中[1],而加快了其腐蚀速率,缩短了其使用寿命,进而也带来了巨大的经济损失[2].因此,对管道及设备的保护显得尤为重要.由于缓蚀剂具有成本低、操作简单、使用时间长等优点,在其介质中添加一定量的缓蚀剂可有效减小腐蚀速率[2].
研究认为:到达金属的缓蚀剂能牢固吸附在金属表面,其分子结构要具有较低的能量和稳定的构象,咪唑啉型缓蚀剂在酸性介质中,能在金属表面形成单分子吸附膜,改变金属表面的电荷分布,其良好的稳定性使它在高温条件下也可以使用[3].因其能够在金属表面发生物理吸附和化学吸附从而减缓金属的腐蚀速率而备受关注[4-10].另外,在使用过程中不存在相溶性及挥发性等问题而被广泛应用[11],咪唑环上氮原子的孤电子对及其大的共轭体系增大了其在金属表面的吸附能力,可以在金属表面形成保护膜,提高缓蚀性能.
在环境保护法规日益严格的今天,可降解的分子越来越引起了人们的关注.分子中含有酯基的季铵盐化合物因疏水链中含有酯基很容易水解为一些小分子片段,是一类可生物降解性好,毒性小,性能优良的化合物[12].
本文以己二酰氯和自制含羟基的咪唑啉反应生成酸酯,再以氯乙酸对该酸酯进行季铵化得目标产物.采用静态挂片失重法、电化学方法研究其缓蚀性能,并通过扫描电镜观察加入该缓蚀剂后A3钢片在HCl溶液中的腐蚀形貌.
1 实验部分
1.1 试剂与仪器
(1)主要试剂:实验室自制咪唑啉[13];己二酰氯,分析纯,上海达瑞精细化学品有限公司;三乙胺,分析纯,天津市科密欧化学试剂有限公司;二氯甲烷,分析纯,天津市富宇精细化工有限公司;氯乙酸,分析纯,国药集团化学试剂有限公司;异丙醇,分析纯,天津市科密欧化学试剂有限公司;A3钢片杭州冠洁工业清洗水处理科技公司;HCl,分析纯,天津市科密欧化学试剂有限公司;溴化钾,光谱纯,国药集团化学试剂有限公司.
(2)主要仪器:旋转蒸发仪,上海予华仪器设备有限公司;电化学工作站,上海辰华仪器有限公司;饱和甘汞电极,上海精密科学仪器有限公司;铂电极,上海精密科学仪器有限公司;扫描电镜,日立S-4800;VECTOR-2傅里叶变换红外光谱仪,德国Bruker公司.
1.2 合成方法
图1为咪唑啉型季铵盐化合物的合成路线图.
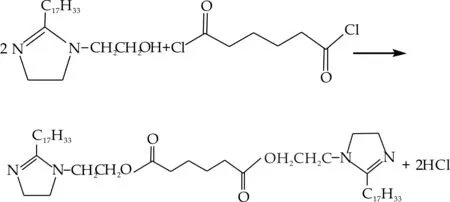
(a)酸酯的合成
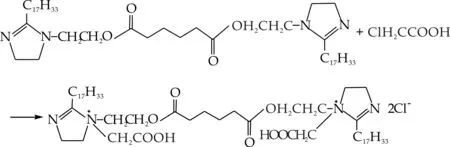
(b)酸酯的季铵化图1 合成路线图
1.2.1 酸酯的合成
在装有电动搅拌器和滴液漏斗的100 mL三口烧瓶中,加入一定量的自制咪唑啉,加少量二氯甲烷将其溶解,再加入一定量的三乙胺,在冰水浴条件下边搅拌边缓慢滴加己二酰氯的二氯甲烷溶液,滴加完毕后反应一段时间,待反应物变为淡黄色糊状物,减压旋蒸除去溶剂,重结晶得到酸酯.
1.2.2 咪唑啉型季铵盐化合物的合成
在装有电动搅拌器、回流冷凝管和滴液漏斗的100 mL三口烧瓶中加入一定量的异丙醇作溶剂,取一定量制得的酸酯溶于异丙醇中,边搅拌边加氯乙酸,在75 ℃下反应4 h,减压蒸馏除去溶剂,得棕黄色膏状物质.
1.3 结构表征与性能测试
1.3.1 红外分析
用光谱纯KBr压片,将所得产物采用涂膜法进行红外表征.
1.3.2 缓蚀性能测试
缓蚀性能测试采用静态挂片失重法.
A3钢片在使用前用360目和1 000目的砂纸打磨,用去离子水冲洗,用丙酮进行脱脂后在常温条件下真空干燥,以备使用.
腐蚀溶液的配制:选用分析纯的浓盐酸配制成质量分数为15%的HCl溶液,在其中分别加入不同质量的自制咪唑啉型季铵盐化合物.
静态挂片失重法参照中华人民共和国石油与天然气行业标准SY5405-1996《酸化用缓蚀剂性能试验方法及评价指标》[14],在常压、温度为60 ℃时,将A3钢片在质量分数为15%的盐酸溶液中加入不同质量缓蚀剂所配制成的腐蚀溶液中静置6 h,分别测定其腐蚀速率Vi和缓蚀率μ,按式(1)、(2)计算:
Vi=Δmi×106/AiΔt
(1)
μ=(V0-Vi)/V0×100%
(2)
式(1)中:Vi—加入缓蚀剂后试片腐蚀速率,g·( m2·h)-1;Δmi—试片腐蚀失重,g;Ai—试片的表面积,mm2;Δt—腐蚀时间,h.式(2)中:μ—缓蚀率,%;V0—空白腐蚀速率,g·( m2·h)-1.
1.3.3 极化曲线与电化学阻抗分析
用电化学工作站测定极化曲线和电化学阻抗谱,采用三电极体系:铂电极和饱和的甘汞电极(SCE)分别作为辅助电极和参比电极,将规格为50 mm×10 mm×3 mm的A3钢片作为工作电极.在试验温度为60 ℃,扫描范围为-1.5~+2.0 V,扫描速度为10 mV/s的条件下测试试样在加入不同质量的含酯基的咪唑啉型季铵盐化合物的HCl溶液中的动电位极化曲线.在开路电位下,设定频率范围为0.1~105Hz,交流电压信号幅度为10 mV的情况下测其电化学阻抗谱.
1.3.4 扫描电镜对钢片腐蚀形貌的分析
分别将两块相同的A3钢片静置于未加缓蚀剂和加了缓蚀剂的质量分数为15%的盐酸溶盐酸溶液中,6 h后取出,用去离子水冲洗三次,干燥.采用扫描电子显微镜观察形貌.
2 结果与讨论
2.1 红外表征
图2为自制咪唑啉与目标物的红外光谱图.两图相比较可以看出,3 332 cm-1处出现一个较强的峰,且该峰峰形较胖,为-COOH上的-OH的伸缩振动峰;1 734 cm-1出现了羰基的特征吸收峰;2 923 cm-1处为甲基的伸缩振动特征吸收峰;2 851 cm-1处为亚甲基的伸缩振动峰;1 625 cm-1处为咪唑环上C=N的伸缩振动峰,表明产物为咪唑啉的衍生物.由此可见合成得到了咪唑啉型季铵盐目标物.

(a)自制咪唑啉的FTIR谱图

(b)目标物的FTIR谱图图2 自制咪唑啉与目标物的FTIR谱图
2.2 静态挂片失重法
2.2.1 缓蚀剂加入量对缓蚀率的影响
常压下,缓蚀温度为60 ℃的条件下,在质量分数为15%的HCl溶液中加入不同质量的缓蚀剂,配制成质量浓度分别为10、20、30、40、50、60、70、80、90、100 mg/L腐蚀溶液,对A3钢片进行静态挂片失重试验6 h,考察缓蚀剂含量对缓蚀率的影响.结果如图3所示.
由图3可知,随着缓蚀剂含量的增加,缓蚀率逐渐增大,继续增大缓蚀剂含量,缓蚀率反而稍有下降.这可能是由于随着加入缓蚀剂后,这些分子逐渐取代了A3钢片表面的水分子,在A3钢片表面慢慢形成一层保护膜,阻止了H+与钢片的反应,因此随着缓蚀剂含量的增加,缓蚀剂分子在钢片表面的覆盖度增加从而引起缓蚀率增大.但当溶液中缓蚀剂含量增加到某个值时,其在A3钢片表面的吸附量达到饱和,再增加缓蚀剂的浓度,钢片表面覆盖度不会增加,反而会由于浓差扩散的存在引起钢片表面局部吸附不均匀造成缓蚀率稍有下降.实验表明当缓蚀剂添加量为90 mg/L 时,缓蚀率可达95.94%,该缓蚀剂缓蚀效果良好.

图3 缓蚀剂含量对缓蚀率的影响
2.2.2 温度对缓蚀率的影响
常压下,温度分别为30 ℃、40 ℃、50 ℃、60 ℃、70 ℃、80 ℃分别对A3钢片在缓蚀剂质量浓度为90 mg/L的15%的HCl溶液中进行静态挂片失重试验6 h,考察温度对缓蚀率的影响.结果如图4所示.
由图4可知,当温度低于60 ℃时,缓蚀剂的缓蚀率随着温度升高而增大.这是因为低温区属于动力学控制区,和H+相比缓蚀剂分子运动缓慢,这时就会有较多的H+与Fe接触并发生反应,导致Fe的腐蚀速率相对较快,随着温度升高,缓蚀剂分子运动速度和吸附速率均增大,在金属表面的吸附量也会随着温度的升高而增加,更多的缓蚀剂分子在金属表面形成一层保护膜而阻碍腐蚀反应发生,因此缓蚀率逐渐增大.但当温度高于60 ℃时,缓蚀率呈现下降趋势,主要原因是温度高于60 ℃时,属于热力学控制区,由于吸附为放热过程,因此平衡吸附量会随着温度的升高而降低.另外,高温时H+的反应活性增大引起腐蚀速度增大也是其原因之一.实验表明,当温度为60 ℃时,缓蚀效果最佳.

图4 温度对缓蚀率的影响
2.2.3 盐酸含量对缓蚀率的影响
常压下,温度为60 ℃,对A3钢片在均含90 mg/L缓蚀剂的不同质量分数盐酸介质中进行静态挂片失重试验,考察盐酸含量对缓蚀率的影响.结果如图5所示.
由图5可知,随着盐酸含量的增加,A3钢片腐蚀速率增大,表明高浓度盐酸对A3钢片的腐蚀性大,缓蚀效率下降.这是因为随着HCl含量的增大,H+浓度也增大,导致单位时间内进攻金属的H+增加,使腐蚀速率增加,缓蚀率下降.质量分数为15%盐酸溶液中缓蚀剂对A3钢片具有较好的缓蚀性能,因此当使用质量分数为15%以上盐酸溶液做腐蚀介质时,应适当增加缓蚀剂的量才能达到较好的缓蚀效果.实验表明:缓蚀剂含量应适当随腐蚀介质的pH而调整,才能发挥更好的缓蚀作用.

图5 HCl含量对缓蚀率的影响
2.3 电化学法
2.3.1 动电位极化曲线
将工作电极表面用环氧树脂包裹,只留1 cm2表面积与腐蚀介质接触,并将辅助电极与参比电极插入缓蚀剂含量不同的HCl溶液中,分别测其极化曲线,结果如图6所示.
由图6可见,与空白试样相比,添加了缓蚀剂后,阳极出现明显的钝化区域,钝化区域的出现正是缓蚀剂作用的结果.缓蚀剂添加量较小时,对阴极反应的抑制作用较小,自腐蚀电位负移,随着缓蚀剂添加量的增大,缓蚀剂对阴极过程的抑制作用减弱,对阳极过程的抑制作用增强,当添加量在90~100 mg/L时,自腐蚀电位由负移转变为正移,缓蚀作用类型由阴极型变为阳极型.这种随缓蚀剂添加量的增大,缓蚀作用类型变化的电化学行为,是绝大多数咪唑啉类缓蚀剂的共同特征[15,16].实验表明该缓蚀剂对A3钢片表面起到了良好的保护作用.

图6 A3钢片在含不同质量浓度缓蚀剂的HCl溶液中的极化曲线
2.3.2 电化学阻抗谱
图7为电化学阻抗谱图.由图7可见,Nyquist图为半圆形,且只有容抗弧,出现阻抗谱“退化”现象,表明该缓蚀剂作用方式为几何覆盖效应,为混合型缓蚀剂[17].这与极化曲线结果一致.随缓蚀剂含量的增加,容抗弧半径逐渐增大,电极表面极化电阻变大,界面电容减小,表明缓蚀剂分子吸附在电极表面阻碍界面电荷的转移,从而使极化电阻增大[18].由于缓蚀剂分子含有咪唑环和氮、氧等杂原子而吸附在A3钢片表面,取代了水分子的位置,缓蚀剂含量增大,覆盖度增加,进而起到保护作用.当溶液中缓蚀剂含量增大到一定值时,缓蚀剂分子在钢片表面吸附达到饱和,再增大缓蚀剂的含量,极化电阻减小,缓蚀率也减小.这与失重法测得的缓蚀率及极化曲线所得结果一致.
2.4 表面形貌
图8是加缓蚀剂前后A3钢片的SEM表面形貌图.由图8可见,A3钢片在未加缓蚀剂的HCl溶液中浸泡过后,表面粗糙不平,腐蚀比较严重,在加入缓蚀剂的HCl溶液中浸泡过后,表面较平整,腐蚀明显减轻.这表明该缓蚀剂缓蚀效果良好.

图7 A3钢片在含不同质量浓度缓蚀剂的HCl溶液中电化学阻抗谱

(a)A3钢片在无缓蚀剂HCl溶液中腐蚀后的SEM图

(b)A3钢片在含缓蚀剂HCl溶液中腐蚀后的SEM图图8 A3钢片腐蚀后的SEM图
3 结论
合成的含酯基的咪唑啉型季铵盐化合物在质量分数为15%的盐酸溶液中对A3钢片的缓蚀性能良好.在60 ℃下,当其质量浓度为90 mg/L时,缓蚀率可达95.94%.极化曲线表明其为混合型的缓蚀剂,电化学阻抗谱表明,随着缓蚀剂的加入,阻抗增大,对A3钢片起到了保护作用.扫描电镜下观察A3钢片的腐蚀形貌,也证明了该缓蚀剂可以起到良好的缓蚀作用.
[1] 宋佳佳,裴峻峰,邓学峰,等.海洋硫化氢的腐蚀与防护进展[J].腐蚀与防护,2012,33(8):648-651,667.
[2] 李 孟,岳为超,徐吉晨,等.季铵盐双子型表面活性剂的合成及其缓蚀性能[J].腐蚀与防护,2013,34(12):1 058-1 061,1 071.
[3] 马文军,范 峥,李稳宏,等.咪唑啉类缓蚀剂性能的评价及其机理研究[J].化学工程,2014,42(2):9-12.
[4] 张光华,王腾飞,孙卫玲,等.硫脲基烷基咪唑啉类缓蚀剂的制备、缓蚀性能及其机理[J].材料保护,2011,44(2):21-23.
[5] Achouri M E,Kertit S,Gouttaya H M,et al.Corrosion inhibition of iron in 1M HCl by some gemini surfactants in the series of alkanediyl-α,ω-bis-(dimethyl tet-radecyl ammonium bromide)[J].Progress in Organic Coatings,2001,43(4):267-273.
[6] Achouri M E,Kertit S,Gouttaya H M,et al.Synthesis of some cationic gemini surfactants and their inhibitive effect on iron corrosion in hydrochloric acid medium[J].Corrosion Science,2001,43(1):19-35.
[7] Qiu L G,Xie A J,Shen Y H.Understanding the effect of spacer length on adsorption of gemini surfactants onto steel surface in acid medium[J].Applied Surface Science,2005,246(1):1-5.
[8] Hegazy M A.A novel shiff base-based cationic gemini surfactants:Synthesis and effect on corrosion inhibition of carbon steel in hydrochloric acid solution[J].Corrosion Science,2009,51(11):2 610-2 618.
[9] Wang X M,Yang H Y, Wang F H.A cationic gemini-surfactant as effective inhibitor for mild steel in HCl solution[J].Corrosion Science,2010,52(4):1 268-1 276.
[10] Assefi D A R, Ami M,Mahmoodi N M.Electrochemical effect of cationic gemini surfactant halide salts on corrosion inhibition of low carbon steel in acid medium[J].Corrosion Science,2010,52(3):794-800.
[11] 徐宝军,媵洪丽,王金波,等.咪唑啉衍生物缓蚀剂的研究[J].腐蚀与防护,2003,24(8):340-344.
[12] Tehrani Bagha A R,Oskarsson H,Holmberg K.Cationic ester-containing gemini surfactants:Chemical hydrolysis and biodegradation[J].Journal of Colloid and Interface Science,2007,312(2):444-452.
[13] 葛 君,樊国栋,柴玲玲.咪唑啉基季铵盐双子表面活性剂的合成与性能[J].精细化工,2011,28(5):448-450.
[14] SY/T5405—1996,酸化用缓蚀剂性能实验方法及评价指标[S].
[15] 刘公召,杨振声,张 艳,等.咪唑啉酰胺在HCl/NH4Cl-H2O和H2S/NH4HS-H2O体系中对碳钢的缓蚀性能[J].腐蚀与防护,2016,37(3):189-195,201.
[16] 方晓君,彭伟华.一种曼尼希碱缓蚀剂在盐酸溶液中的缓蚀行为[J].石油化工应用,2016,35(7):116-120,130.
[17] 何 爽,张凤华,李 飞,等.曼尼希碱酸化缓蚀剂的合成及缓蚀性能[J].材料保护,2014,47(6):42-44.
[18] 龙小柱,周荣星,刘婧雯,等.咪唑啉季铵盐缓蚀剂的合成及缓蚀行为的研究[J].腐蚀研究,2015,29(11):72-77.
【责任编辑:陈 佳】
Synthesis and performance of quaternary ammonium salt compound of imidazoline containing ester
FAN Guo-dong, WEI Xiao-xiao
(College of Chemistry and Chemical Engineering, Key Laboratory of Auxiliary Chemistry & Technology for Chemical Industry, Ministry of Education, Shaanxi University of Science & Technology, Xi′an 710021, China)
The ester synthesized with imidazoline and adipoyl chloride as raw materials,three trimethylamine as acid binding agent,dichloromethane as solvent.A quaternary ammonium salt compound of imidazoline obtained via quaternary ammonium reaction between the ester and chloroacetic acid.The aimed material was characterized using infrared spectroscopy.Weight-loss method,electrochemical methods and scanning electron microscopy were used to study the corrosion inhibition performance of quaternary ammonium salt gemini surfactant for A3 carbon steel in HCl solution at 60 ℃.The results showed that the inhibition rate was close to 95.94% when 90 mg/L corrosion inhibitor was added.Electrochemical methods experiments revealed that the corrosion inhibitor is a mixed type corrosion inhibitor.After adding the inhibitor,long passivation range for the steel was formed,AC impedance radius became bigger,corrosion current decreased obviously.Microscopy result demonstrated that the gemini surfactant could form a compact film on the surface of the carbon steel specimen to protect it form corrosion.
ester; quaternary ammonium salt compound of imidazoline; HCl; corrosion inhibition performance
2016-09-29 基金项目:陕西省教育厅重点实验室科研计划项目(14JS015); 陕西省科技厅工业科技攻关计划项目(2014K08-12)
樊国栋(1944-),男,山西永济人,教授,博士,研究方向:油田缓蚀剂的开发与应用
1000-5811(2017)02-0072-05
TG174.42
A
