高效液相色谱法测定利肺片中五味子醇甲、五味子甲素及五味子乙素含量
2017-04-07杨立志姜雪敏
杨立志,姜雪敏
(黑龙江省鸡西市食品药品检验检测中心,黑龙江鸡西 158100)
高效液相色谱法测定利肺片中五味子醇甲、五味子甲素及五味子乙素含量
杨立志,姜雪敏
(黑龙江省鸡西市食品药品检验检测中心,黑龙江鸡西 158100)
目的建立测定利肺片中五味子醇甲、五味子甲素、五味子乙素含量的高效液相色谱(HPLC)法。方法采用Agilent Extend-C18色谱柱(250 mm×4.6 mm,5 m),以乙腈-水为流动相梯度洗脱,流速为1.0 mL/min,检测波长为220 nm。结果3种成分进样量线性范围分别为五味子醇甲0.025 8~0.515 0 g(r=1.000 0),五味子甲素0.026 5~0.530 9 g(r=1.000 0),五味子乙素0.026 0~0.521 0 g (r=1.000 0);平均回收率依次为97.35%,97.54%,97.58%,RSD分别为0.48%,0.55%,0.44%(n=6)。结论该方法操作简便,重复性好,结果准确,可用于利肺片的质量控制。
高效液相色谱法;利肺片;五味子醇甲;五味子甲素;五味子乙素;含量测定
利肺片是由五味子、白及、枇杷叶、牡蛎、百部、甘草、百合、冬虫夏草、蛤蚧粉制成的中成药,具有驱痨补肺、镇咳祛痰的功效,可用于治疗肺结核咳嗽、咯痰咯血、气虚哮喘、慢性支气管炎[1]。目前,该药品的质量标准中未对方中任何药物进行定性或定量测定,不能有效控制产品的质量。为此,笔者参考文献[2-14],建立了测定利肺片中五味子醇甲、五味子甲素、五味子乙素含量的高效液相色谱(HPLC)法,并进行了方法学验证,为更好地控制该药品的质量提供了科学依据。
1 仪器与试药
1.1 仪器
岛津LC-2010A型高效液相色谱仪(株式会社岛津制作所);AG285型电子分析天平(瑞士梅特勒托利多公司);KQ-400KDE型超声波清洗器(昆山市超声仪器有限公司)。
1.2 试药
五味子醇甲对照品(批号为110857-200608,纯度为100.00%),五味子甲素对照品(批号为110764-201010,纯度为99.60%),五味子乙素对照品(批号为110765-200508,纯度为100.00%),均购于中国食品药品检定研究院;利肺片(通化民泰药业股份有限公司,批号为140101,吉林百姓堂药业有限公司,批号为150602,150801);水为超纯水,乙腈(Merck公司)为色谱纯。
2 方法与结果
2.1 色谱条件
色谱柱:Agilent Extend-C18柱(250 mm×4.6 mm,5 μm);流动相:流动相A为乙腈,流动相B为水,梯度洗脱(0~20 min,A为30%;20~70 min,A为30%~80%);流速:1.0 mL/min;柱温:30℃;进样量:10 μL;检测波长:220 nm。理论板数按五味子乙素峰计算均应不低于3 000。
2.2 溶液制备
混合对照品溶液:称取五味子醇甲对照品10.30 mg,五味子甲素对照品10.66 mg,五味子乙素对照品10.42 mg,精密称定,加甲醇溶解并稀释,制成质量浓度分别为0.515,0.533,0.521 mg/mL的对照品贮备液。再分别量取对照品贮备液各1 mL,置20 mL容量瓶中,制成每1 mL含五味子醇甲25.75 μg、五味子甲素26.54 μg、含五味子乙素26.05 μg的混合对照品溶液。
供试品溶液:取本品适量,研细,称取2.0 g(平均片重为0.435 7 g),精密称定,置50 mL具塞锥形瓶中,精密加入甲醇25 mL,密塞,称定质量,超声处理40 min(功率400 W,频率40 Hz),放冷至室温,用甲醇补足减失的质量,摇匀,滤过,即得。
阴性对照品溶液:按照利肺片处方工艺制成不含五味子的空白样品,按供试品溶液制备方法制成阴性对照品溶液。
2.3 方法学考察
阴性干挠试验:精密吸取混合对照品溶液、供试品溶液、阴性对照品溶液,按2.1项下色谱条件进样测定,记录色谱图(见图1)。结果供试品溶液色谱中,在与对照品溶液相应位置上有相同保留时间的色谱峰,表明阴性对照无干扰。
线性关系考察:分别精密吸取五味子醇甲、五味子甲素、五味子乙素对照品混合溶液1,2,5,10,15,20 μL,注入液相色谱仪,记录峰面积,以对照品进样量(X,μg)为横坐标、峰面积积分值(Y)为纵坐标进行线性回归,得回归方程,五味子醇甲为Y=7.000 0×106X-9.856 5× 102,r=1.000 0(n=6);五味子甲素,Y=8.000 0× 106X+1.909 9×103,r=1.000 0(n=6);五味子乙素,Y=8.000 0×106X+1.323 1×103,r=1.000 0(n=6)。结果表明,五味子醇甲、五味子甲素、五味子乙素进样量分别在0.0258~0.5150μg,0.0265~0.5309μg,0.0260~0.521 0 μg范围内与峰面积积分值线性关系良好。
精密度试验:精密吸取混合对照品溶液10 μL,连续进样6次,计算峰面积。结果,五味子醇甲峰面积平均值为1 877 849,RSD=0.86%(n=6);五味子甲素峰面积平均值为2 049 349,RSD=0.92%(n=6);五味子乙素峰面积平均值为2 031 295,RSD=1.02%(n=6)。表明仪器精密度良好。

图1 高效液相色谱图
稳定性试验:精密吸取同一供试品溶液,在室温下放置0,2,4,8,12,24 h后,分别进样10 μL,记录峰面积。结果,五味子醇甲峰面积平均值为1 820 881,RSD=0.82%(n=6);五味子甲素峰面积平均值为2 027 508,RSD=0.79%(n=6);五味子乙素峰面积平均值为2 019 439,RSD=0.90%(n=6)。表明供试品溶液在24 h内稳定。
重复性试验:称取同一批样品(批号为140101)6份,依法制备供试品溶液,测定含量。结果五味子醇甲平均含量为0.070 mg/片,RSD=0.75%,五味子甲素平均含量为0.072 mg/片,RSD=0.91%,五味子乙素平均含量为0.071 mg/片,RSD=1.01%。表明方法重复性良好。
加样回收试验:精密称取已知含量的同一批样品(批号为140101,五味子醇甲含量为0.070 mg/片,五味子甲素含量为0.072mg/片,五味子乙素含量为0.071mg/片)约1.0 g,以2份为1组,共3组,分别置25 mL容量瓶中,分别精密加入五味子醇甲对照品溶液(161.0μg/mL)、五味子甲素对照品溶液(165.0 μg/mL)和五味子乙素对照品溶液(163.0 μg/mL)0.8,1.0,1.2 mL,加甲醇稀释至刻度,称定质量,超声处理40 min,放冷至室温,用甲醇补足减失的质量,摇匀,滤过,作为供试品溶液。按2.1项下色谱条件进样测定,并计算回收率。结果见表1。

表1 加样回收试验结果(n=6)
2.4 样品含量测定
取市售利肺片3批,依法制备供试品溶液,按拟订色谱条件测定五味子醇甲、五味子甲素、五味子乙素含量。结果见表2。
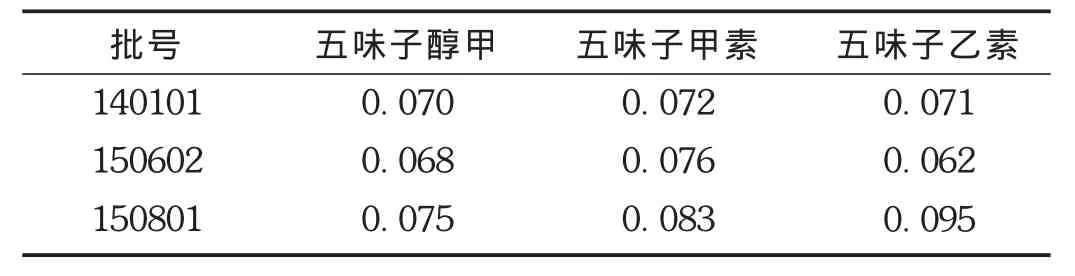
表2 含量测定结果(mg/片,n=9)
3 讨论
3.1 检测波长选择
经检测,五味子醇甲、五味子甲素、五味子乙素最大紫外吸收波长均在(220±2)nm,本研究中采用220 nm,则3种被测成分均有较大吸收。
3.2 流动相选择
应用2015年版《中国药典(一部)》中五味子含量测定项下的流动相,3种被测成分未能达到较好分离,以乙腈-水为流动相,梯度洗脱,则使分离度更好,故选用后者为流动相。
3.3 检测对象选择
方中五味子为主药,五味子醇甲、五味子甲素、五味子乙素是其主要成分,且含量高,易于测定,故采用测定处方中五味子的成分含量来控制该制剂的质量。
3.4 样品提取溶剂选择
分别考察了甲醇、70%甲醇、乙酸乙酯,结果表明,以甲醇为溶剂提取效果较好,故以甲醇为溶剂。
3.5 样品提取时间选择
用甲醇分别提取20,40,60 min,结果表明,20 min提取的含量低于提取40 min和60 min,且提取40 min 和60 min含量基本相同,故确定提取时间为40 min。
[1]WS3-B-2152-96.卫生部药品标准·中药成方制剂(第十一册)[S].
[2]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2015:66-67.
[3]单鑫,陆兔林,毛春芹,等.HPLC同时测定复方五味含片中葛根素、甘草苷、甘草酸铵、五味子醇甲、五味子甲素、五味子乙素[J].南京中医药大学学报,2014,30(1):82-84.
[4]李正国,于立佐,张爱岑.RP-HPLC测定降酶灵胶囊中五味子醇甲、五味子甲素和五味子乙素的含量[J].中成药,2004,26(8):618-621.
[5]谭生建,屈雪莲,杨成勇,等.肝复康丸中五味子甲素和五味子乙素含量测定方法研究[J].解放军药学学报,2000,16(5):270-272.
[6]何海雁,张叶,刘宏明.HPLC法同时测定五酯胶囊中五味子醇甲、五味子酯甲、五味子甲素和五味子乙素的含量[J].药学研究,2015,34(11):642-644.
[7]史敏,林超,秦华.HPLC测定养肝片中五味子醇甲、五味子甲素、五味子乙素含量[J].食品与药品,2014,16(6):433-435.
[8]张广春,陈明明.高效液相色谱法测定安神养心丸中五味子醇甲的含量[J].时珍国医国药,2011,22(7):1783-1784.
[9]唐秋竹,王艺纯,孟庆妍,等.HPLC法同时测定护肝片中五味子醇甲、五味子甲素、五味子乙素的含量[J].中国药品标准,2012,13(4):258-261.
[10]古海锋,张小茜,郭洪祝.HPLC法测定复方益肝灵片中五味子醇甲的含量[J].药物分析杂志,2009,29(2):295-297.
[11]陈恩瑜,施夏蓉,洪可俊.RP-HPLC法同时测定补肾益脑胶囊中五味子醇甲、五味子甲素和五味子乙素的含量[J].海峡药学,2012,24(12):49-52.
[12]潘建锋,庄波阳.HPLC法测定太太静心助眠口服液中五味子醇甲、五味子甲素和五味子乙素的含量[J].福建医药杂志,2013,35(2):75-77.
[13]郭禹彤,弥宏,赵宏峰.RP-HPLC法测定制剂中五味子醇甲、五味子甲素与五味子乙素的含量[J].西部中医药,2015(4):33-35.
[14]杨孝容,向清祥,熊俊如,等.HPLC测定柏子养心丸中五味子酯甲、五味子甲素和五昧子乙素的含量[J].药物分析杂志,2006,26(11):1558-1561.
Content Determination of Schisandrin,Deoxyschizandrin and Schisandrin B in Lifei Tablets by HPLC
Yang Lizhi,Jiang Xuemin
(Jixi Inspection and Testing Center for Food and Drug,Jixi,Heilongjiang,China158100)
ObjectiveTo develop an HPLC method for the content determination of Schisandrin,Deoxyschizandrin and Schisandrin B in Lifei Tablets.MethodsThe separation was performed on an Agilent Extend-C18column(250 mm×4.6 mm,5 m).The mobile phase was Acetonifrile-Water,gradient elution,with the flowing rate of 1.0 mL/min.The detection wave length was 220 nm.ResultsThe linear ranges of Schisandrin,Deoxyschizandrin and Schisandrin B were 0.025 8-0.515 0 μg(r=1.000 0),0.026 5-0.530 9 μg (r=1.000 0)and 0.026 0-0.521 0 μg(r=1.000 0),respectively.The average recoveries were 97.35%,97.54%and 97.58% respectively,RSD=0.48%,0.55%,0.44%(n=6),respectively.ConclusionThe method is simple,reproducidle and accurate,and can be used in the content determination of Schisandrin,Deoxyschizandrin and Schisandrin B in Lifei Tablets.
HPLC;Lifei Tablets;Schisandrin;Deoxyschizandrin;Schisandrin B;content determination
R284.1;R286.0
A
1006-4931(2017)02-0038-03
10.3969/j.issn.1006-4931.2017.02.011
2016-09-23;
2016-10-15)
杨立志(1977-),男,大学本科,副主任药师,主要从事食品药品检验检测工作,(电话)0467-6103377。
