2种含碘制剂《中华人民共和国药典》(2015年版)微生物限度检查方法的建立
2017-04-07刘文张广求朱立刚
刘文,张广求,朱立刚
(1.黄冈市中心医院药剂科,湖北 黄冈 438000;2.黄冈市第二人民医院药剂科,湖北 黄冈 438000)
2种含碘制剂《中华人民共和国药典》(2015年版)微生物限度检查方法的建立
刘文1,张广求1,朱立刚2
(1.黄冈市中心医院药剂科,湖北 黄冈 438000;2.黄冈市第二人民医院药剂科,湖北 黄冈 438000)
目的:建立2种含碘制剂(碘乳康口服溶液和复方碘口服溶液)的微生物限度检查方法。方法:按《中华人民共和国药典》(2015年版)四部规定,以硫代硫酸钠为中和剂,采用金黄色葡萄球菌、枯草芽孢杆菌、铜绿假单胞菌、白色念珠菌和黑曲霉等5种试验菌株,进行需氧菌总数、霉菌和酵母菌总数计数方法的适用性试验,并进行控制菌大肠埃希菌检查方法的适用性试验。结果:采用中和法,可消除抑菌成分碘的干扰,5种试验菌株的回收比值均在0.5~2.0;控制菌大肠埃希菌可检出。结论:建立的方法简便可行,结果准确可靠,可用于这2种含碘制剂的微生物限度检查。
碘乳康口服溶液;复方碘口服溶液;含碘制剂;《中华人民共和国药典》(2015年版);微生物限度检查;硫代硫酸钠
碘乳康口服溶液是黄冈市中心医院的自制制剂,用于乳腺增生症,安全性好,疗效显著。复方碘口服溶液调节甲状腺功能,用于甲状腺功能亢进的术前准备[1]。2种制剂均主要由碘、碘化钾组成,由于碘具强有力的消毒防腐作用,能杀死细菌、霉菌[2],文献[3]亦证实碘注射液中的碘有抑菌作用。笔者曾采用培养基稀释法,较好地消除了碘乳康口服溶液中抑菌成分碘的干扰[4]。文献[5-6]采用淀粉吸附或淀粉吸附与薄膜过滤相结合的方法,分别消除聚维酮碘泡腾片、聚维酮碘溶液中碘的抑菌活性。
根据《中华人民共和国药典》(2015年版)[7]规定,对这2种含碘制剂进行微生物限度检查时,应先消除供试品中碘的抑菌活性,再依法进行检查,以保证方法的适用性。本文利用硫代硫酸钠能将碘分子还原为无抑菌作用的碘离子,消除了碘的抑菌作用,建立了2种含碘制剂有效的微生物限度检查方法。
1 仪器与试药
1.1 仪器
高压蒸汽灭菌器(上海三申医疗器械有限公司);DB-102-1型电热干燥箱(武汉市武昌实验仪器厂);HHB11420电热恒温培养箱(湖北省黄石市医疗器械厂);LRH-250B生化培养箱(广东省医疗器械厂);HSGIC-2型电热恒温水浴箱(浙江临海市东方仪器厂);SZK202净化工作台(蚌埠净化设备厂);BSC-1300ⅡA2生物安全柜(苏州安泰空气技术有限公司);FA1604型电子天平(上海越平科学仪器有限公司);YJK015菌落计数器(江苏金坛市荣华仪器制造有限公司)。
1.2 供试品
碘乳康口服溶液(批准文号:鄂药制字H20110227,批号:160319,160407,160421)、复方碘口服溶液(批准文号:鄂药制字H20110213,批号:160128,160307,160425),均为黄冈市中心医院自制。
1.3 菌株
金黄色葡萄球菌[CMCC(B)26003]、枯草芽孢杆菌[CMCC(B)63501]、铜绿假单胞菌[CMCC(B)10104]、白色念珠菌[CMCC(F)98001]、黑曲霉[CMCC(F)98003]、大肠埃希菌[CMCC(B)44102],均为第2代冷冻保藏菌株,由湖北省食品药品监督检验研究院提供。
1.4 培养基及试剂、稀释剂
胰酪大豆胨琼脂培养基(批号:20150802),胰酪大豆胨液体培养基(批号:20150722),沙氏葡萄糖琼脂培养基(批号:20150919),沙氏葡萄糖液体培养基(批号:20150226),麦康凯琼脂培养基(批号:20150708),麦康凯液体培养基(批号:20150624),均由青岛高科园海博生物技术有限公司生产。蛋白胨(北京三药科技开发公司,批号:150320)。硫代硫酸钠、磷酸二氢钾、无水磷酸氢二钠、氯化钠均为分析纯。
2 方法与结果
2.1 溶液的制备
2.1.1 pH7.0无菌氯化钠-蛋白胨缓冲液[4]取磷酸二氢钾3.56 g、无水磷酸氢二钠5.77 g、氯化钠4.30 g、蛋白胨1.00 g,加纯化水1 000 mL,微温溶解,滤清,分装,灭菌,备用。
2.1.2 中和剂溶液取硫代硫酸钠0.3 g、7 g,分别加入pH7.0无菌氯化钠-蛋白胨缓冲液至1 000 mL,微温溶解,灭菌,制成含0.03%硫代硫酸钠的pH7.0无菌氯化钠-蛋白胨缓冲液(以下简称中和剂溶液A)、含0.7%硫代硫酸钠的pH7.0无菌氯化钠-蛋白胨缓冲液(以下简称中和剂溶液B)。
2.1.3 供试品溶液取碘乳康口服溶液、复方碘口服溶液各10 mL,分别加中和剂溶液A、中和剂溶液B至100 mL,摇匀,制成1∶10的碘乳康口服溶液、复方碘口服溶液供试液,备用。
2.2 菌悬液的制备
按《中华人民共和国药典》(2015年版)四部规定,取经30~35℃培养18~24 h的金黄色葡萄球菌、枯草芽孢杆菌、铜绿假单胞菌的胰酪大豆胨液体培养物,或经20~25℃培养2~3天的白色念珠菌沙氏葡萄糖液体培养物,分别用pH7.0无菌氯化钠-蛋白胨缓冲液制成含菌数为3 000~10 000 cfu/mL的菌悬液,备用。
取经20~25℃培养5~7天的黑曲霉沙氏葡萄糖琼脂斜面培养物,加含0.05%(mL / mL)聚山梨酯80的pH7.0无菌氯化钠-蛋白胨缓冲液3~5 mL,将孢子洗脱,用管口带有薄无菌脱脂棉的无菌毛细吸管,吸取孢子悬液至无菌试管内,用含0.05%(mL / mL)聚山梨酯80的pH7.0无菌氯化钠-蛋白胨缓冲液,制成含菌数为3 000~10 000 cfu/mL的黑曲霉孢子悬液,备用。
2.3 需氧菌总数、霉菌和酵母菌总数计数方法的适用性试验
2.3.1 试验组分别取“2.1.3”项下制备的1∶10碘乳康口服溶液、复方碘口服溶液供试液9.9 mL于灭菌试管中,加“2.2”项下制备的金黄色葡萄球菌菌悬液0.1 mL,充分混匀,使每1 mL供试液中含试验菌不大于100 cfu,同法制备每1 mL含枯草芽孢杆菌、铜绿假单胞菌、白色念珠菌、黑曲霉不大于100 cfu的供试液。分别取1 mL注入2个直径90 mm无菌平皿中,立即倾注不超过45℃融化的胰酪大豆胨琼脂培养基,用于需氧菌总数计数。再分别取含白色念珠菌、黑曲霉的供试液1 mL注入2个直径90 mm无菌平皿中,立即倾注不超过45℃融化的沙氏葡萄糖琼脂培养基,用于霉菌和酵母菌总数计数。轻轻摇匀,待凝固后倒置,含每株试验菌的供试液各平行制备2个平皿。需氧菌置33℃培养3~5 d,霉菌和酵母菌置23℃培养5~7 d,观察菌落生长情况,点计平板上生长的所有菌落数,以平均菌落数作为计数结果。
2.3.2 供试品对照组取“2.1.3”项下制备的1∶10碘乳康口服溶液、复方碘口服溶液供试液9.9 mL于灭菌试管中,分别加“2.1.2”项下制备的中和剂溶液A、中和剂溶液B 0.1 mL,充分混匀,同试验组操作,测定供试品中的菌落数。
2.3.3 菌液对照组取“2.1.1”项下制备的pH7.0无菌氯化钠-蛋白胨缓冲液9.9 mL,分别加入“2.2”项下制备的5种试验菌菌悬液0.1 mL,充分混匀,同试验组操作,测定菌液中的菌落数。
2.3.4 中和剂对照组取“2.1.2”项下制备的中和剂溶液A、中和剂溶液B 9.9 mL于灭菌试管中,分别加入“2.2”项下制备的5种试验菌菌悬液0.1 mL,充分混匀,同试验组操作,以确认中和剂对试验菌无毒性。
2.3.5 结果碘乳康口服溶液、复方碘口服溶液的5种试验菌株各进行3次独立的平行试验,计算回收比值:
试验组的回收比值=(试验组平均菌落数-供试品对照组平均菌落数)/ 菌液对照组平均菌落数,
回收比值均在0.5~2[7]。
中和剂对照组的回收比值=中和剂对照组的平均菌落数 / 菌液对照组平均菌落数,
回收比值均在0.8~1.2,见表1。
2.4 控制菌大肠埃希菌检查方法的适用性试验
2.4.1 大肠埃希菌菌液的制备取经30~35℃培养18~24 h的大肠埃希菌的胰酪大豆胨液体培养物,用pH7.0无菌氯化钠-蛋白胨缓冲液制成含菌数不大于100 cfu/mL的菌悬液,备用。
2.4.2 供试品组取“2.1.3”项下制备的碘乳康口服溶液、复方碘口服溶液供试液10 mL,分别加入到胰酪大豆胨液体培养基100 mL中,作为供试品组。
2.4.3 试验组取“2.1.3”项下制备的碘乳康口服溶液、复方碘口服溶液供试液10 mL和“2.4.1”项下制备的含菌数不大于100 cfu/mL的大肠埃希菌菌悬液1 mL,分别加入到胰酪大豆胨液体培养基100 mL中,作为试验组。
2.4.4 中和剂对照组取“2.1.2”项下制备的中和剂溶液A、中和剂溶液B 10 mL和“2.4.1”项下制备的含菌数不大于100 cfu/mL的大肠埃希菌菌悬液1 mL,分别加入到胰酪大豆胨液体培养基100 mL中,作为中和剂对照组。
2.4.5 阴性对照组取“2.1.2”项下制备的中和剂溶液A、中和剂溶液B 10 mL,分别加入到胰酪大豆胨液体培养基100 mL中,作为阴性对照组。
上述各培养物置33℃培养24 h,分别取培养物1 mL,接种至100 mL麦康凯液体培养基中,置43℃培养48 h。取麦康凯液体培养物划线接种于麦康凯琼脂培养基平板上,置33℃培养24 h,判断是否检出大肠埃希菌。
2.4.6 结果供试品组、阴性对照组均未见有菌生长,试验组、中和剂对照组麦康凯液体培养基均浑浊,麦康凯琼脂培养基平板上均有菌落生长,经分离、纯化,鉴定为大肠埃希菌。
表明该方法消除了抑菌成分碘的干扰,且中和剂对试验菌大肠埃希菌无毒性,适用于碘乳康口服溶液、复方碘口服溶液的大肠埃希菌检查见表2。
2.5 3批样品的微生物限度和控制菌检查
取供试品,分别按“2.1.3”项下方法制备供试液,依法检查,2种含碘制剂的微生物限度检查结果见表3。
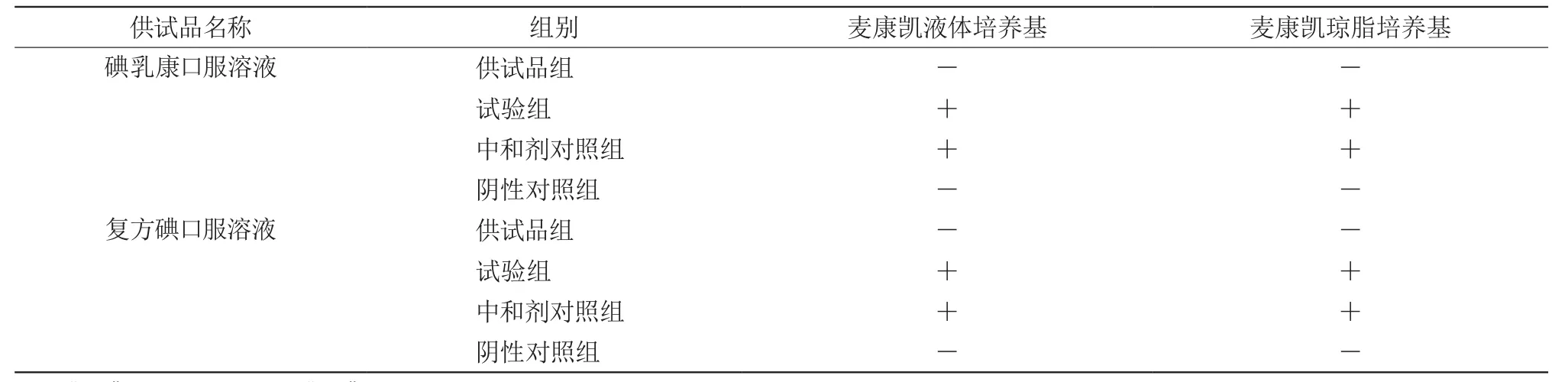
表2 大肠埃希菌检查方法的适用性试验结果

表3 微生物限度检查结果
3 讨论
《中华人民共和国药典》(2015年版)微生物限度检查培养体系在培养基、培养温度、培养时间等方面都做了较大修订,与国际通用标准高度一致[8],采用更优良的广谱培养基,有利于受损微生物的修复及生长,提高了方法的灵敏度。将试验菌加入供试液中模拟样品污染微生物,进行方法适用性试验,取消了稀释剂对照组,结果判定以变化范围进行规定,符合微生物计数规律,结果更为准确。微生物计数法中,按微生物的培养条件来区分,将细菌数及霉菌和酵母菌数,修订为需氧菌总数及霉菌和酵母总数。需氧菌总数是指胰酪大豆胨琼脂培养基上生长的总菌落数,包括真菌菌落数;霉菌和酵母菌总数是指沙氏葡萄糖琼脂培养基上生长的总菌落数,包括细菌菌落数。
碘与硫代硫酸钠在中性或弱酸性溶液中,发生氧化还原反应,生成无抑菌作用的连四硫酸钠和碘化钠:
I2+2Na2S4O6= Na2S4O6+2NaI。
由化学反应方程式得知,1 moL碘(I)与1 moL硫代硫酸钠相当,即中和100 mL碘乳康口服溶液1∶10溶液,需消耗硫代硫酸钠0.022 g;中和100 mL复方碘口服溶液1∶10溶液,需消耗硫代硫酸钠0.623 g。试验结果表明,在所用的中和剂溶液A、中和剂溶液B中,加入一定量的中和剂硫代硫酸钠,能分别有效中和碘乳康口服溶液、复方碘口服溶液供试品溶液中的碘,且中和剂、中和产物对试验菌的生长无干扰。此法作为碘乳康口服溶液和复方碘口服溶液的微生物限度检查方法,较好地消除了碘的抑菌作用,简化了试验操作,提高了工作效率,保证了方法的科学性和检查结果的准确可靠。
[1] 湖北省食品药品监督管理局.湖北省医疗机构制剂规范(2011年版)[S].武汉:湖北科学技术出版社,2012:318-319.
[2] 国家药典委员会.中华人民共和国药典临床用药须知(化学药和生物制品卷)[M].北京:人民卫生出版社,2005:859.
[3] 张广求.碘注射液无菌检查方法学验证[J].中国医院药学杂志,2010,30(2):165-166.
[4] 张广求,刘文,田祥学.碘乳康口服溶液微生物限度检查方法学验证[J].中国执业药师,2015,12(8):10-13.
[5] 王立华,杨谊,马靖,等.含碘药物控制菌检查方法的探讨[J].中国药事,2000,14(5):310-311.
[6] 徐雄利,林永丽,刘玉明,等.聚维酮碘溶液的微生物限度检查[J].海军医学杂志,2007,28(4):326-327.
[7] 国家药典委员会.中华人民共和国药典(四部) [S].北京:中国医药科技出版社,2015:140-151.
[8] 杨晓莉,李辉,马英英,等.《中华人民共和国药典》(2015年版)非无菌产品微生物限度检查:控制菌检查法解读与对策[J].中国药师,2016,19(4):748-752.
本文编辑:苏日力嘎
Establishment of a Microbial Limit Test Method for Two Iodine Preparations in Chinese Pharmacopoeia (2015 Edition)
Liu Wen1, Zhang Guang-qiu1, Zhu Li-gang2
(1. Department of Pharmacy, Huanggang Central Hospital, Hubei Huanggang 438000, China; 2.Department of Pharmacy, The Second People’s Hospital of Huanggang City, Hubei Huanggang 438000, China)
Objective:The establish a microbial limit test method for two iodine preparations (oral dianrukang solution and oral compound iodine solution).Methods:According to the requirements in Chinese Pharmacopoeia (volume Ⅳ, 2015 edition), the method for counting of total aerobic bacteria, yeast and mould as well as the test method for E. coli were verf ed for suitability with f ve test bacteria, i.e. Staphylococcus aureus, Bacillus subtilis, Pseudomonas aeruginosa, Candida albicans and A. niger, using sodium thiosulfate as a neutralizing agent.Results:The interference of iodine as a antibacterial component was eliminated by neutralization method. All the recovery ratios of f ve test bacterial strains were 0. 5 ~ 2. 0; E. coli as a control bacterium could be detected.Conclusion:The established method is simple, feasible, accurate and reliable, which may be used for the microbial limit test for the two iodeine preparations.
Oral Dianrukang Solution; Oral Compound Iodine Solution; Iodine Preparation; Chinese Pharmacopoeia (2015 Edition); Microbial Limit Test; Sodium Thisulfate
R286.0
A
10.3969/j.issn.2096-3327.2017.02.004
2016 - 08 - 22
刘文,男,副主任药师。研究方向:医院药学。E-mail:liuwen.cn@163.com
张广求,男,副主任药师。研究方向:医院药学,药物分析。E-mail:ccnpa@163.com
