白蛋白结合型紫杉醇单药作为三线及以上方案治疗晚期非小细胞肺癌的临床研究
2017-03-30蒋侃黄诚吴标林根张晶
蒋侃 黄诚 吴标 林根 张晶
白蛋白结合型紫杉醇单药作为三线及以上方案治疗晚期非小细胞肺癌的临床研究
蒋侃 黄诚★吴标 林根 张晶
目的观察白蛋白结合型紫杉醇单药三线及以上治疗晚期非小细胞肺癌的近期疗效及不良反应。方法选取2013年10月至2015年3月在福建省肿瘤医院已接受过二线治疗的晚期非小细胞肺癌患者46例,予以白蛋白结合型紫杉醇260 mg/m2D1,每21天为一周期,每个周期复查CT评价疗效,观察其疗效及不良反应。结果完全缓解(CR)0例,部分缓解(PR)6例,疾病稳定(SD)26例,疾病进展(PD)14例,客观缓解率(ORR)13%,疾病控制率(DCR)70%,中位无进展生存期(PFS)4.7月,主要不良反应为血液学毒性、肝功能损害,外周神经毒性,无毒性相关死亡病例。结论白蛋白结合型紫杉醇用于三线及以上治疗晚期非小细胞肺癌,ORR及DCR高,不良反应可以耐受。
白蛋白结合型紫杉醇;多线化疗;非小细胞肺癌
目前肺癌的死亡率已占恶性肿瘤的第一位,严重威胁人类的健康。其中非小细胞肺癌(non⁃small cell lung cancer,NSCLC)占75%~80%[1]。大部分的患者在确诊肺癌时已属晚期,错失手术机会。化疗在NSCLC治疗中占据重要的地位。白蛋白结合型紫杉醇(nanoparticle albumin⁃bound pa⁃clitaxel,Nab⁃P)是一种新型的以白蛋白为溶剂的紫杉醇,紫杉醇是活性成分,人血白蛋白作为辅料起分散、稳定颗粒及运载主药的作用[2⁃3]。其高效低毒的优势使其2004年在美国上市,2009年在中国上市。Nab⁃P已广泛应用于头颈部鳞癌、转移性乳腺癌、胰腺癌、卵巢癌、前列腺癌、黑色素瘤等肿瘤[4⁃5],显示出肯定的疗效。2012年10月美国食品药品监督管理局(Food and Drug Administration,FDA)批准Nab⁃P一线治疗局部进展或转移性的无手术及放疗指征的NSCLC[6]。美国国立综合癌症网(National Comprehensive Cancer Network,NCCN)指南中晚期NSCLC只有一线及二线的化疗方案。而部分患者在二线治疗以后仍要求继续治疗。但经过多程治疗后的患者通常无法耐受不良反应较大的药物。因此选择高效、低不良反应的化疗药物成为三线及以上患者的选择。而Nab⁃P就属于此类药物。国内已有数家医院进行了Nab⁃P单药/和化疗药物联用三线及以上治疗晚期NSCLC的研究,显现出较好的近期疗效。但此方面的探索较少。为弥补这方面的不足,本研究经伦理委员会批准,收集了46例在我院住院的予以Nab⁃P单药作为三线及以上方案治疗晚期NSCLC患者的资料,观察其疗效及不良反应。
1 资料与方法
1.1 一般资料
(1)2013年10月至2015年3月在我院住院的晚期NSCLC患者46例:男性34例,女性12例;(2)年龄范围40~75岁,中位年龄58岁;(3)美国东部肿瘤协作组(Eastern Cooperative Oncology Group,ECOG)[7]评分:0分5例,1分36例,2分5例;(4)临床分期:Ⅲb期8例,Ⅳ期38例;(5)经组织学确认的病理类型:鳞癌30例,非鳞癌16例;(6)三线及三线以上治疗:3线方案化疗的32例,4线方案化疗的6例,5线以上方案化疗的8例;其中表皮生长因子受体(epidermal growth factor re⁃ ceptor,EGFR)基因突变10例已接受过靶向药物及一种化疗方案后进展,未突变的36例接受二种化疗方案后进展;(7)至少有一处影像学电子计算机断层扫描(computed tomography,CT)或磁共振成像(magnetic resnane iamge,MRI)可测量或可评估病灶;(8)预计生存期≥3月;(9)符合化疗的指征:外周血象基本正常,心、肝、肾功能无明显异常,心电图基本正常;(10)获得患者知情同意,签署知情同意书。
1.2 治疗方法
所有患者均接受Nab⁃P(美国阿斯利斯公司生产,100g/瓶)260 mg/m2化疗。化疗第1天30 min内静滴完成。每21天为1个周期。至少完成2个周期的化疗。
1.3 疗效评价
治疗前患者进行影像学基线评估。每周期结束后下一周期开始前复查CT评价疗效。按照美国国立癌症研究所实体瘤疗效评价标准(Response Evaluation Criteria in Solid Tumours,RECIST)[8]对患者进行疗效评价,分为:完全缓解(complete response,CR)、部分缓解(partial response,PR)、疾病稳定(stable disease,SD)和疾病进展(progression disease,PD)。客观缓解率(objective response rate,ORR)是指CR+PR患者占全组患者的百分率。疾病控制率(disease control rate,DCR)是指CR+PR+SD患者占全组患者的百分率。无进展生存期(progression free survival,PFS)是指患者从首次用药到疾病进展或任何原因死亡的时间(以发生在先的事件计算)。
1.4 不良反应
化疗期间每周查2次血常规、一次肝肾功能。按照美国国立癌症研究所不良反应评价标准(common toxicity criteria,CTC)[9]第4版进行分级。
1.5 统计方法
采用SPSS 17.0统计软件进行统计分析。组间比较采用χ2检验。PFS采用Kaplan⁃Meier法计算。以P<0.05有统计学意义。
2 结果
2.1 近期疗效
46例NSCLC患者均可评价疗效,共化疗148个周期,中位周期数为3个周期(2~5周期)。其中:CR 0例(0%),PR 6例(13%),SD 26例(57%),PD 14例(30%),ORR 13%(6/4),DCR 70%(32/46)。EGFR突变患者1例为PR,1例PD,其余均为SD。近期疗效和各临床病理特征均无关(表1)。
2.2 远期疗效
从治疗开始进行随访,随访截止至2016年1月30日,12例存活,34例死亡。中位PFS为4.7个月(1.4个月至22.7个月)(图1)。
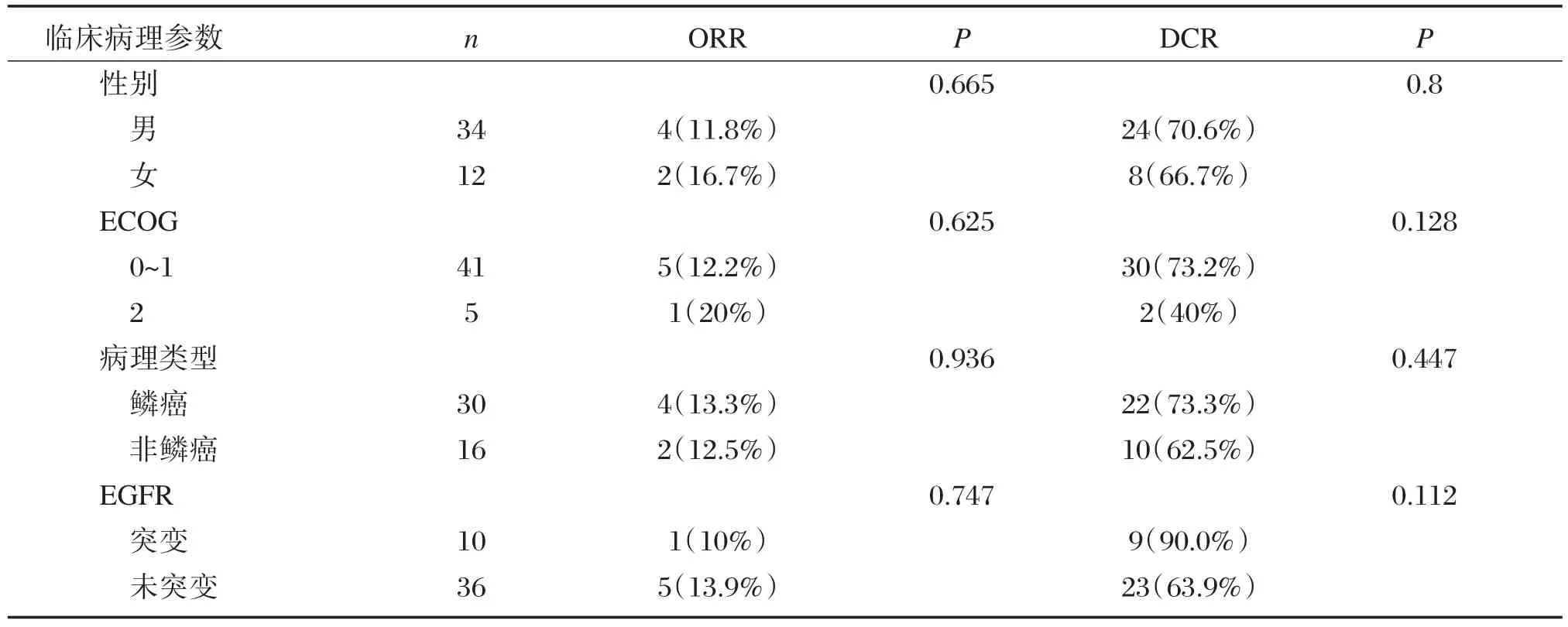
表1 Nab⁃P疗效与临床病理特征的关系Table 1 Relations of Nab⁃P efficacy and clinical pathological features
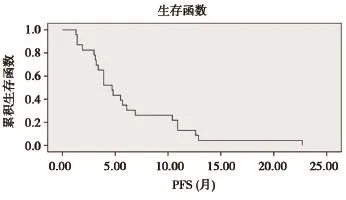
图1 46例患者的生存曲线Figure 1 Survival curve of 46 patients
2.3 不良反应
本组患者治疗后均出现不同程度的不良反应,最常见为骨髓抑制、肝功能损害、周围神经毒性、关节及肌肉酸痛。骨髓抑制主要表现为白细胞及中性粒细胞下降,未观察到贫血及血小板减少。Ⅰ度骨髓抑制2例,Ⅱ度骨髓抑制18例,Ⅲ度骨髓抑制5例,Ⅳ度骨髓抑制0例,经粒细胞集落刺激因子治疗后好转。肝功能损害表现为谷丙转氨酶及谷草转氨酶的升高。仅为Ⅰ~Ⅱ度,Ⅰ度5例,Ⅱ度5例,予以保肝治疗后好转。周围神经毒性主要表现为手足末端麻木。骨关节疼痛、肌肉酸痛和疲乏多为Ⅰ~Ⅱ级不良反应;恶心、呕吐等不良反应少见,经治疗后均好转(表2)。
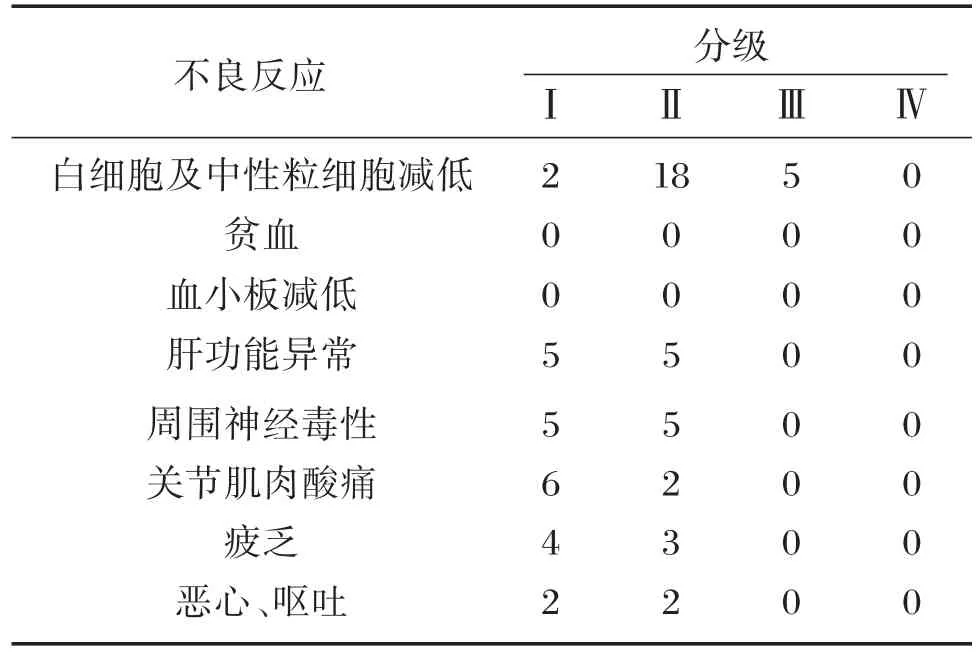
表2 Nab⁃P治疗晚期非小细胞肺癌的不良反应Table 2 Adverse events of Nab⁃P treatment for advanced NSCLC
3 讨论
近几年来,针对NSCLC的靶向治疗已获得巨大的进步,其中针对EGFR基因突变及间变性淋巴瘤激酶(anaplastic lymphoma kinase,ALK)基因重排的药物,已被NCCN指南推荐用于一线治疗NSCLC。但化疗仍是NSCLC治疗的一个重要手段。特别是基因检测阴性的患者,化疗为治疗的首选。NCCN指南推荐:一线标准化疗方案是含铂双药方案,二线方案为培美曲塞、多西他赛或分子靶向治疗。三线以后就无标准治疗方案。但在临床工作中,相当一部分患者在接受一线、二线治疗失败后仍有较好的状态,渴望继续治疗。但是,这部分患者的体力状态又不如一线二线化疗的时候。因此,为这一部分患者选择高效、低毒的治疗方案成为临床医师面临的难题。
紫杉醇是重要的化疗药物,能促进微管蛋白聚合,抑制微管蛋白解聚,使细胞生长停滞于G2/ M后期,有效抑制癌细胞分裂与增殖。但其水溶性极差,选用聚氧乙烯蓖麻油/乙醇作为溶剂,容易产生严重的过敏反应。并且聚氧乙烯蓖麻油/乙醇在血液中易形成胶束,阻碍紫杉醇的释放,影响疗效。Nab⁃P作用机制与紫杉醇相似。制备过程中将紫杉醇和人血白蛋白经高压振动技术制成平均直径为130 nm的颗粒[10]。白蛋白通过受体介导的胞转作用、高通透性和滞留效应(enhanced permea⁃bility and retention effect,EPR)通过内皮细胞到达肿瘤组织[11]。研究显示Nab⁃P血清中的游离紫杉醇是普通紫杉醇的10倍,瘤内Nab⁃P紫杉醇浓度较同剂量普通紫杉醇高33%[2]。由于不存在聚氧乙烯蓖麻油类的助溶剂,Nab⁃P在给药前无需用类固醇或抗组织胺预防过敏反应[12],输注时间短,仅需30 min,故便于在临床使用。
Socinski等[6]的Nab⁃P联合铂类一线治疗NSCLC的Ⅱ期临床研究显示出其高效性和良好的耐受性。Ⅲ期临床试验(VA031)中[6]:Nab⁃P组的ORR、PFS、OS均高于普通紫杉醇组。在鳞癌患者中,ORR提高了71%。其3级以上的周围神经炎,中性粒细胞减低、关节肌肉酸痛明显低于紫杉醇组。非鳞癌患者中两组相当[13]。日本学者[14]进行了周剂量Nab⁃P联合卡铂与普通紫杉醇联合卡铂比较治疗晚期NSCLC的研究,进一步证明了Nab⁃P对亚洲人疗效佳,安全性可。二线治疗方面:日本学者 Sakata进行的Ⅱ期临床研究[15]:ORR为31.7%,PFS为4.9个月,OS为13.0个月。Weill Cornell医学院[16]收集了该学院31例复发或铂类耐药后予以Nab⁃P治疗的患者的资料,ORR为16.1%,DCR为64.5%,PFS为3.5个月,1位患者予以Nab⁃P维持治疗了3年。Nab⁃P与培美曲塞二线比较的Ⅱ期临床研究中[17],Nab⁃P疗效与不良反应与培美曲塞相当。国内相关的Ⅱ期临床研究也显示:ORR为16.1%,PFS为3.5个月,OS为6.8个月[18]。故Nab⁃P可考虑作为晚期NSCLC的二线治疗的选择。在多线治疗晚期NSCLC方面,国内学者开展的研究较多。陈秀等[19]的Nab⁃P单药多线治疗晚期NSCLC的研究:ORR为18.75%,DCR为50%,TTP为2.15个月,对既往使用过紫杉醇类药物化疗的患者,Nab⁃P仍然有效。方瑛等[20]将Nab⁃P与替吉奥联合三线以上治疗晚期NSCLC,ORR为22.2%,DCR为72.2%,PFS达3个月,副反应可耐受。Ho等[21]将Nab⁃P与培美曲塞联合,也显示出了较好的疗效。Zheng等[22]研究显示了Nab⁃P对老年患者的高效性,可作为紫杉类药物或TKI耐药的患者的解救治疗。本研究中,ORR及DCR与国内学者所得数据相似,PFS较国内学者所得数据稍长。个别患者的PFS达到22.7个月。说明Nab⁃P对个别患者的特异性。不良反应方面:仅血液学毒性方面显示出了Ⅲ度的白细胞减低,其余均为Ⅰ~Ⅱ度的不良反应,患者耐受性较好。本研究也充分证明了Nab⁃P可用于多线治疗晚期NSCLC,且不良反应可以耐受。但无论是国内还是国外,二线还是多线,相关研究的病例数均较少,故期待着大样本量的临床研究。并且,随着国际上化疗药物与靶向药物/抗血管生成药物/免疫制剂联用的风潮兴起,结合Nab⁃P高效低毒的优点,可考虑进行研究将Nab⁃P与这些药物进行“强强联合”,争取更好的疗效。
总之,Nab⁃P高效低毒的特性,可考虑将其作为晚期NSCLC多线治疗的一种选择,延长患者的生存期。
[1]Ferlay J,Dikshit R,Eser S,et al.Cancer incidence and mortality worldwide:IARC Sources,methods and major patterns in GLOBOCAN 2012[J].International Journal of Cancer,2014,136(5).
[2]Yardley DA.Nab⁃Paclitaxel mechanisms of action and delivery[J].J Control Release,2013,170(3):365⁃372.
[3]Hirsh V.Nab⁃paclitaxel for the management of patients with advanced non⁃small⁃cell lung cancer[J].Expert Rev Anticancer Ther,2014,14(2):129⁃141.
[4]von Hoff DD,Ervin T,Arena FP,et al.Increased sur⁃vival in pancreatic cancer with nab⁃paclitaxel plus gem⁃citabine[J].N Engl Med,2013,369(18):1691⁃1703.
[5]O’Shaughnessy J,Gradishar WJ,Bhar P,et al.Nab⁃paclitaxel for first⁃line treatment of patients with meta⁃static breast cancer and pool prognostic factors:a retro⁃spective analysis[J].Breast Cancer Res Treat,2013,138(3):829⁃837.
[6]Socinski MA,Bondarenko I,Karaseva NA,et al. Weekly nab⁃paclitaxel in combination with carboplatin versus solvent⁃baesd paclitaxel plus carboplatin as first⁃line therapy in patients with advanced non⁃small⁃cell lung cancer:final results of a phaseⅢtrial[J].J Clin Oncol,2012,30(17):2055⁃2062.
[7]Malalasekera A,Tan CSY,Phan V,et al.Eastern co⁃operative oncology group score:agreement between non⁃small⁃cell lung cancer patients and their oncolo⁃gists and clinical implications[J].Cancer Treatment Communications,2016,5:17⁃21.
[8]Eisenhauer EA,Therasse P,Bogaerts J,et al.New re⁃sponse evaluation criteria in solid tumours:revised RE⁃CIST guideline(version 1.1)[J].European Journal of Cancer,2009,45(2):228⁃247.
[9]Hay JL,Atkinson TM,Reeve BB,et al.Cognitive in⁃terviewing of the US national cancer institute’s patient⁃reported outcomes version of the common terminology criteria for adverse events(PRO⁃CTCAE)[J].Quali⁃ty of Life Research An International Journal of Quality of Life Aspects of Treatment Care&Rehabilitation,2014,23(1):257⁃269.
[10]Madaan A,Singh P,Awasthi A,et al.Efficiency and mechanism of intracellular paclitaxel delivery by novel nanopolymer⁃based tumor⁃targeted delivery system,Nanoxel(TM)[J].Clinical&Translational Oncolo⁃gy,2013,15(1):26⁃32.
[11]Neesse A,Frese KK,Chan DS,et al.SPARC inde⁃pendent drug delivery and antitumour of Nnb⁃paclitax⁃el in genetically engineered mice[J].Gut,2014,63(6):974⁃983.
[12]Viúdez A,Ramírez N,Hernández⁃García I,et al.Nab⁃paclitaxel:a flattering facelift[J].Crit Rev Oncol He⁃ma,2014,92(3):166⁃180.
[13]Socinski MA,Okamoto I,Hon JK,et al.Safety and efficacy by histology of weekly nab⁃paclitaxel in com⁃ bination with carboplatin as fist⁃line therapy in patients with advanced nonsmall⁃cell lung cancer[J].Ann On⁃col,2013,24(9):2390⁃2396.
[14]Saouchi M,Okamato I,Sakai H,et al.Efficacy and safety of weekly nab⁃paclitaxel plus carboplatin in pa⁃tients with advanced non⁃small cell lung cancer[J]. Lung Cancer,2013,81(1):97⁃101.
[15]Sakata S,Saeki S,Okamoto I,et al.Phase II trial of weekly nab⁃paclitaxel for previously treated advanced non⁃small cell lung cancer:kumamoto thoracic oncolo⁃gy study group(KTOSG)trial 1301[J].Lung Can⁃cer,2016,99:41⁃45.
[16]Saxena A,Schneider BJ,Christos PJ,et al.Treat⁃ment of recurrent and platinum⁃refractory stage IV non⁃small cell lung cancer with nanoparticle albumin⁃bound paclitaxel(nab⁃paclitaxel)as a single agent[J].Medi⁃cal Oncology,2016,33(2):1⁃9.
[17]Liu Z,Wei Z,Hu Y,et al.A phase II open⁃label clin⁃ical study of comparing nab⁃paclitaxel with pemetrexed as second⁃line chemotherapy for patients with stage IIIB/IV non⁃small⁃cell lung cancer[J].Medical Oncol⁃ogy,2015,32(8):1⁃6.
[18]Hu W,Zhang Z.A phase II clinical study of using nab⁃paclitaxel as second⁃line chemotherapy for Chinese pa⁃tients with advanced non⁃small cell lung cancer[J]. Medical Oncology,2015,32(6):1⁃5.
[19]陈秀,任胜祥,李雪飞,等.白蛋白结合型紫杉醇治疗多线治疗晚期非小细胞肺癌的疗效分析[J].中国肿瘤临床,2012,39(22):1824⁃1827.
[20]方瑛,王丽,夏国豪,等.白蛋白结合型紫杉醇联合替吉奥作为三线及以上方案治疗晚期非小细胞肺癌的临床观察[J].临床肿瘤学杂志,2013,18(12):1131⁃1134.
[21]Ho C,Davies AM,Sangha RS,et al.PhaseⅠ/Ⅱtri⁃al of pemetrexed plus nab⁃paclitaxel in advanced solid tumor patients with emphasis on non⁃small cell lung cancer[J].Invest New Drugs,2013,31(6):1587⁃1591.
[22]Zheng Q,Yao Y,Nan K.et al.Weekly intravenous nanoparticle albumin⁃bound paclitaxel for elderly pa⁃tients with stage IV non⁃small⁃cell lung cancer:a series of 20 cases[J].J Biomed Res,2012,26(3):159⁃164.
Clinical study of nanoparticle albumin⁃bound paclitaxel(single⁃agent regimen) as third⁃and further⁃line therapy in advanced non⁃small cell lung cancer patients
JIANG Kan,HUANG Cheng★,WU Biao,LIN Gen,ZHANG Jing
(Department of Medical Oncology,Fujian Provincial Cancer Hospital,Fujian Affiliated Hospital of Fujian Medical University,Fuzhou,Fujian,China,350014)
ObjectiveTo observe the efficacy and toxicity of nanoparticle albumin⁃bound paclitaxel(Nab⁃P)as third⁃and further⁃line chemotherapeutic approach for advanced non⁃small cell lung cancer (NSCLC)patients.MethodsA total of 46 advanced NSCLC patients that have received second⁃line therapy were recruited from Fujian Province Cancer Hospital from October 2013 to March 2015.Nab⁃P 260 mg/m2D1 was applied as a single⁃agent regimen for third⁃and further⁃line chemotherapy by intravenous administration for a 21 day cycle.Efficacy was estimated by imaging every cycle.ResultsOut of the 46 total patients,6 patients was achieved partial relief(PR),26 patients were disease stable(SD),and 14 patients had disease progression(PD).The objective response rate(ORR)was 13%.The disease control rate(DCR)was 70%.The median progression free survival(PFS)was 4.7 months.The most commonly seen adverse events(AEs)were myelosuppression,liver dysfunction,and peripheral neurotoxicity.There were no treatment⁃related deaths.ConclusionUsing Nab⁃P as a signle⁃agent regimen for third⁃and further⁃line chemotherapy in advanced NSCLC patients was both effective and safe.The adverse events were well tolerated.
Nanoparticle albumin⁃bound paclitaxel(Nab⁃P);Multi⁃line chemotherapy;Non⁃small cell lung cancer(NSCLC)
福建省青年课题基金(2015⁃1⁃14)
福建医科大学教学医院福建省肿瘤医院内科,福建,福州350014
★通讯作者:黄诚,E⁃mail:cheng671@sina.com
