解答化学计算题新主张
2017-03-29刘希
刘希

近几年,根据课标思想,中考化学计算题打破传统的单一计算形式,以灵活多样的形式展现在我们面前,这些题型着重考查同学们的分析能力、思维能力、各科间的融合能力以及创新能力等,下面笔者对2016年中考计算题的命题热点作一个归类分析,供大家参考。
一、联系生活实际,考查有关化学式的计算
例1(2016·巴中)巴中某超市卖的纯碱(Na2C03)产品往往含有少量的氯化钠(NaCl),化学兴趣小组的同学通过实验来测定该纯碱样品中纯碱的质量分数,他们取12g纯碱样品放人烧杯中,逐滴加入稀盐酸至不再产生气泡为止,共消耗盐酸100g,烧杯中没有残留不溶物,称得反应后溶液的质量为107.6g计算:
(1)生成二氧化碳___g
(2)样品中纯碱的质量分数是多少?(要求写出计算过程,结果精确到0.1%)
研析与解析:(1)根据质量守恒定律可知,生成二氧化碳的质量为:100g+12g-107.6g=4.4g(2)根据化学方程式和生成二氧化碳的质量能够得出参加反应的碳酸钠的质量,进而求出纯碱的质量分数。
答案:(1)4.4
(2)88.3%
三、培养同学们定量分析的能力,考察数学模型在化学中的应用
例3(2016·遂宁)某校化学小组的同学为了测定某石灰石中碳酸钙的质量分数,他们取该石灰石样品10g加入烧杯中,再把80g稀盐酸分4次加入,实验过程所得数据如表1(已知石灰石样品中含有的杂质既不溶于水,也不与稀盐酸反应),
分析表中数据,完成下列问题:
(1)表中m的数值为——一,
(2)该石灰石样品中碳酸钙的质量分数为__。
(3)计算第1次实验反应结束后所得溶液中溶质的质量分数(计算结果精确到0,1%),
研析与解答:(1)因为第1、2次加入盐酸后,固体质量都减少3g,第3次加入盐酸后固体质量减少1.4g,可知第3次加入盐酸后,碳酸钙反应完了,所以m的数值是2.6,(2)根据杂质不会与盐酸反应可知,剩余固体的质量就是杂质的质量,然后计算碳酸钙的质量分数,(3)根据碳酸钙和盐酸反应的化学方程式和碳酸钙的质量计算生成氯化钙的质量,然后计算溶质的质量分数(计算过程中不要漏掉逸出的CO2的质量)。
答案:(1)2,6(2)74%(3)15-4%,
四、培養同学们探究能力,考察对化学问题的计算性评价
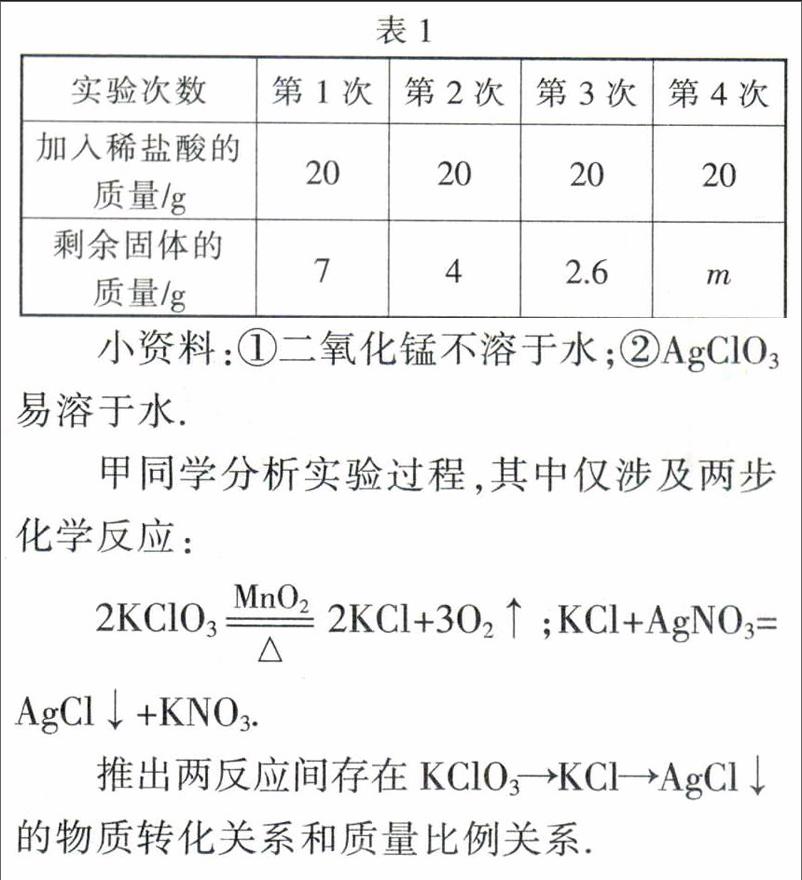
例4(2016·济宁)化学兴趣小组的同学为体验加热同体制取气体的操作步骤和方法,利用6g氯酸钾和2g二氧化锰的混合物加热制取氧气。
(1)实验结束后,甲同学认为氯酸钾可能未分解完全,又设计了下面的实验:
实验1:将实验加热后的残留物加水至充分溶解,过滤;
实验2:向实验1的滤液中滴加硝酸银溶液至不再产生沉淀,过滤、干燥,称得沉淀质量为5.74g。
请你利用上述关系,通过计算帮甲同学判断KCIO3是否完全分解?(简单写出计算过程、说明判断依据,计算结果精确到0.1)。
(2)乙同学对甲同学的方案提出质疑:通过称量加热后残留物质的质量,利用加热前后的质量差进行计算,同样能达到目的,你赞同乙同学的观点吗?说明理由。
研析与解答:(1)由KCIO3、KCl、AgCl之间的物质转化关系和质量比例关系,可计算出参加反应的氯酸钾的质量,进而判断KCIO3是否完全分解,由题意知,生成的AgCl沉淀的质量是5.74g,可计算出参加反应的KCIO3的质量为4.9g。(2)由质量守恒定律可知,加热前后固体混合物减少的质量即为生成氧气的质量,由生成氧气的质量可计算出参加反应的氯酸钾的质量,进而判断氯酸钾是否完全分解。
答案:(1)KCIO3没有完全分解。(2)赞同,由质量守恒定律,反应前后固体混合物减少的质量即为生成氧气的质量,由反应的化学方程式可计算出参加反应的氯酸钾的质量。
