玄麦甘桔中指标性成分血药浓度的UPLC-MS/MS法测定及药代动力学研究
2017-03-28刘洪涛董占军
吴 茵,魏 欣,刘洪涛,董占军
玄麦甘桔中指标性成分血药浓度的UPLC-MS/MS法测定及药代动力学研究
吴 茵,魏 欣,刘洪涛,董占军*
目的 建立玄麦甘桔颗粒中指标性成分甘草苷和哈巴俄苷在大鼠血浆中的超高效液相-质谱/质谱定量测定方法,并研究其体内药动学过程。方法 色谱柱:菲罗门Kinetex C18柱(50 mm×3 mm,2.6 μm);柱温:20 ℃;流动相为0.1%甲酸(A)-乙腈(B);梯度洗脱;流速为0.3 mL/min;进样量:5 μL。采用ESI源,多反应监测模式(MRM)负离子模式下检测各成分血药浓度。6只雄性大鼠灌胃玄麦甘桔颗粒药液后分别于给药后0.03、0.08、0.16、0.33、0.67、1、1.5、2、3、4、6、8、12 h,眼内眦取血0.5 mL测定血药浓度,并用DAS 3.0 软件计算药动学参数。结果 以芦丁为内标,甘草苷、哈巴俄苷的检测范围分别为0.78~50.0 ng/mL(r=0.997 9)和1.66~106.10 ng/mL(r=0.995 8)。方法回收率>82.3%,日内精密度与日间精密度RSD均<8.8%。甘草苷、哈巴俄苷大鼠体内的t1/2分别为(3.46±2.08)、(3.28±1.17)h,Cmax分别为(27.55±21.12)、(16.28±14.53)μg/L,tmax分别为(0.31±0.19)、(0.33±0.18)h,AUC0~12 h分别为(48.82±11.35)、(64.85±46.70)μg ·h/L。结论 该方法快速、灵敏,重复性好,可用于玄麦甘桔颗粒2种指标性成分在大鼠体内的药代动力学研究。
玄麦甘桔颗粒;甘草苷;哈巴俄苷;超高效液相色谱-质谱/质谱;药动学
0 引言
玄麦甘桔颗粒是2015年版药典的载入品种,由玄参、麦冬、甘草、桔梗4味药材组方,具有祛痰利咽、滋阴养肺之功。方中以玄参为君,清热凉血、滋阴解毒;以麦冬为臣,养阴润肺、益胃生津;佐以桔梗化痰宣肺,使以甘草调和诸药、祛痰止咳。该药临床应用广泛,主要用于治疗阴虚火旺所致的咳嗽、咽炎等呼吸道系统疾病[1-2]。哈巴俄苷为玄参的主要有效成分,有抗炎、抗氧化的作用[3];甘草中的甘草苷在抗病毒、抑制溃疡方面有较强的生物活性[4]。这些成分既是玄麦甘桔颗粒的物质基础,也是质量控制常用的指标性成分[5]。
目前,国内学者对该药的研究主要集中在含量测定和质量控制,而尚未见该药入血活性成分的药代动力学研究报道。中药复方制剂成分复杂,药代动力学代谢特点独特。本文首次建立了大鼠灌胃玄麦甘桔颗粒后血浆中甘草苷及哈巴俄苷的UPLC-MS/MS法。该方法灵敏度高、可操作性强,为该药的物质基础研究和临床应用提供了理论依据。
1 仪器、试药与动物
AB Sciex QTRAPTM 5500型三重四极杆质谱仪,美国Applied Biosystems公司,含有Turbo V离子源和三重四极杆质量分析器。超高效液相色谱系统,Shimadzu 30A UPLC System,Kyoto,日本,配有Shimadzu 30AD二元高压梯度泵、Shimadzu SIL30AC自动进样器和Shimadzu CTO30AD柱温箱,Analyst 1.6.1数据采集软件。BP211D型分析天平,德国Sartorius公司;雷勃尔LG16-B高速离心机,北京雷勃尔离心机有限公司。
对照品哈巴俄苷(批号:20141015)、甘草苷(批号:20140923)购自南京春秋生物科技有限公司,纯度均>98%。乙腈、甲酸为色谱纯,水为娃哈哈纯净水。玄麦甘桔颗粒由药店购得,规格:10 g/袋,批号:51078,宁夏多维药业有限公司生产。
清洁级SD(Spraque-Dawley)大鼠,体重200~250 g,雄性(河北省实验动物中心提供,合格证编号:1508018号)。实验动物喂养环境:温度23~25 ℃;相对湿度50%±5%。给药前12 h禁食,自由饮水。
2 方法
2.1 检测条件 液相条件:色谱柱为菲罗门Kinetex C18柱(50 mm×3 mm,2.6 μm);柱温20 ℃;流动相为乙腈-0.1%甲酸水溶液,梯度洗脱:0~6 min,10%~60%乙腈;6~6.1 min,60%~10%乙腈;体积流量0.3 mL/min;进样量5 μL;进样前平衡2 min。
质谱条件:电喷雾离子源(ESI源),离子源温度为600 ℃,负离子模式监测。离子源电压为-4 500 V,雾化气(gas 1)和加热气(gas 2)分别为414、448 kPa,气帘气为172 kPa,采用负离子模式扫描模式监测,甘草苷和哈巴俄苷的去簇电压(DP)、碰撞能(CE)分别为-100 V、-28 V,-110 V、-14 V;检测离子对分别为m/z 417.1/255.0、m/z 493.2/345.2,内标芦丁的去簇电压(DP)、碰撞能(CE)分别为:-90 V、-24 V;检测离子对为m/z 609.1/300.0。
2.2 血浆样品的制备 取内标溶液20 μL于离心管中,40 ℃水浴下氮气吹干,备用。精密吸取大鼠血浆200 μL,置于离心管中,涡流混旋1 min;再加入400 μL乙腈,混旋2 min,以14 000 r/min离心10 min,取上清液于离心管中,氮气流吹干。残渣加入10%乙腈100 μL复溶,涡流混旋1 min,14 000 r/min离心10 min,取上清液10 μL进UPLC-MS/MS分析,记录色谱图。
2.3 标准曲线和质控样品的制备 分别精密称取2种待测成分对照品适量,定量溶解于甲醇作为储备液。分别精密量取上述各储备液适量至同一容量瓶中,用甲醇稀释至刻度,制备成混合对照品溶液。取混合对照品溶液和内标各20 μL加入离心管氮气吹干后,再将200 μL空白血浆加入其中,按“2.2”项下方法处理,制得系列甘草苷含量为0.78、1.56、3.13、6.25、12.50、25.00、50.0 ng/mL,哈巴俄苷为1.66、3.31、6.63、13.26、26.53、53.05、106.10 ng/mL的标准样品;内标芦丁的浓度为17.5 ng/mL。同法配制低、中、高3种浓度的标准溶液[甘草苷(1.56、6.25、40.00 ng/mL),哈巴俄苷(3.31、13.26、84.88 ng/mL)],作为质控(QC)样品。
2.4 方法学考察
2.4.1 专属性 通过比较空白血浆、模拟生物样品和灌胃给药后的实际生物样品发现,被测物和内标不受血浆内源性物质和代谢产物的干扰,见图1。
2.4.2 线性关系考察 按“2.3”项下方法处理,记录各被测物系列浓度色谱图,以甘草苷、哈巴俄苷与内标物峰面积比值对甘草苷、哈巴俄苷质量浓度进行线性回归,回归方程分别为Y=0.194 X-0.059 2 (r=0.997 9)和Y=0.011 X-0.003 78 (r=0.995 8)。结果表明,甘草苷、哈巴俄苷血药浓度分别在0.78~50.00、1.66~106.10 ng/mL范围内线性关系良好。
2.4.3 提取回收率和基质效应 取空白血浆200 μL,分别制备低、中、高3种浓度的含药QC样品,按“2.5”项下操作,进样分析,记录峰面积,每一浓度平行测定5份,记录待测物和内标的峰面积比值为A;另取空白血浆200 μL,按“2.2”项下操作处理后,加入对应的低、中、高3种浓度的标准系列溶液进样分析,记录待测物和内标的峰面积比值为B,每一浓度平行测定5份;A/B×100%即得提取回收率。另用初始比例流动相将标准系列溶液配制成与上述理论浓度相同的低、中、高3种浓度溶液直接进样分析,每一浓度平行测定5份,记录待测物和内标的峰面积比值为C,基质效应的计算方法为 B/C×100%。甘草苷和哈巴俄苷低、中、高3种浓度的回收率和基质效应见表2。内标的回收率和基质效应分别为91.4%和87.2%。结果表明,所建方法能够满足生物样品的测定要求。
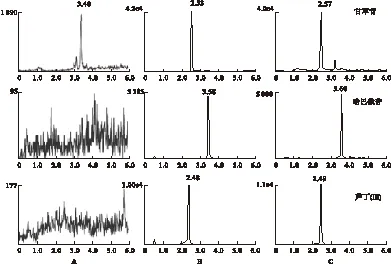
图1 大鼠血浆中2种指标成分的MRM提取离子流图
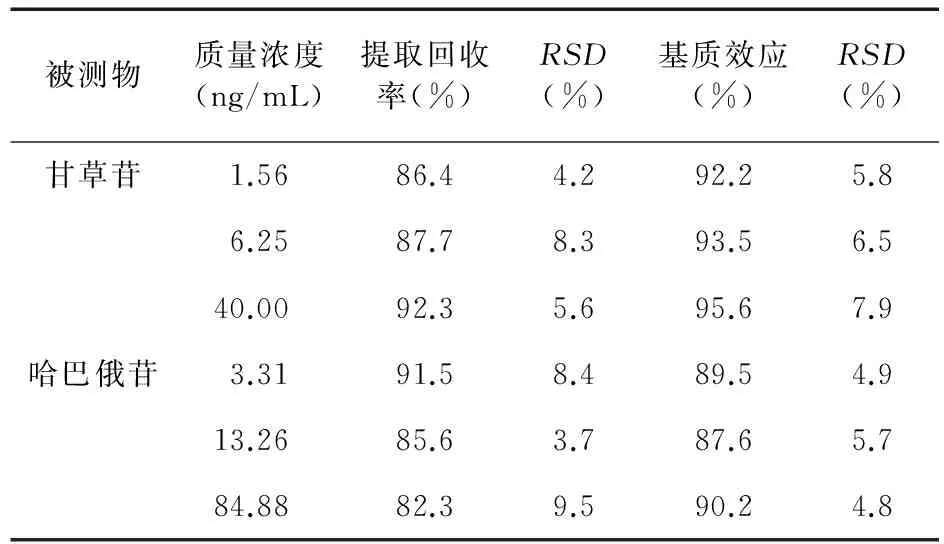
表2 2种成分的提取回收率和基质效应(n=5)
2.4.4 精密度与准确度 取空白血浆,按“2.3”项下方法制备高、中、低3个浓度的QC样品各6份,测定并计算2种待测成分与内标的峰面积比,用当日随行的标准曲线计算QC样品的测定浓度,考察方法的日内精密度和准确度。连续测定3 d,考察日间精密度和准确度,RSD均<15%,结果见表3。
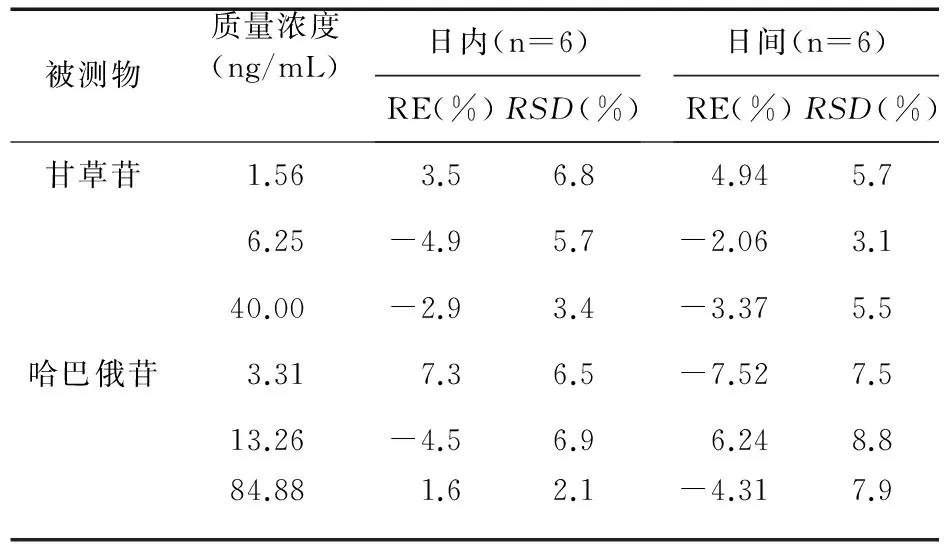
表3 2种成分的精密度和准确度(%)
2.5 稳定性试验 按“2.3”项下方法制备含甘草苷和哈巴俄苷低、中、高3种浓度的含药血浆QC品,考察上述2种成分血浆样品反复冻融3次、-20 ℃放置15 d、室温放置4 h以及经“2.3”方法处理后的分析物放置12 h的稳定性,被测物浓度变化在85%~115%,结果表明,甘草苷和哈巴俄苷上述条件下稳定性良好。
2.6 药代动力学试验 雄性SD大鼠6只,给药前12 h禁食,自由饮水。取玄麦甘桔颗粒,外标法测定,甘草苷和哈巴俄苷的含量分别为107.2 μg/g和28.7 μg/g。用适量水溶解,按1 g/mL配成灌胃液,并以8 mL/kg的剂量灌胃给予玄麦甘桔颗粒水溶液,分别于给药后0.03、0.08、0.17、0.33、0.67、1、1.5、2、3、4、6、8、12 h,眼内眦取血0.5 mL,放在肝素化离心管中,以4 000 r/min离心10 min,取上层大鼠血浆冷冻于-20 ℃冰箱中。按“2.2”项下同法操作,记录各待测物与内标的峰面积比,用当日的标准曲线计算甘草苷、哈巴俄苷的浓度,并绘制药-时曲线(见图2),采用DAS 3.0计算各物质药代动力学参数,主要药代动力学参数见表4。

图2 甘草苷和哈巴俄苷的药时曲线图
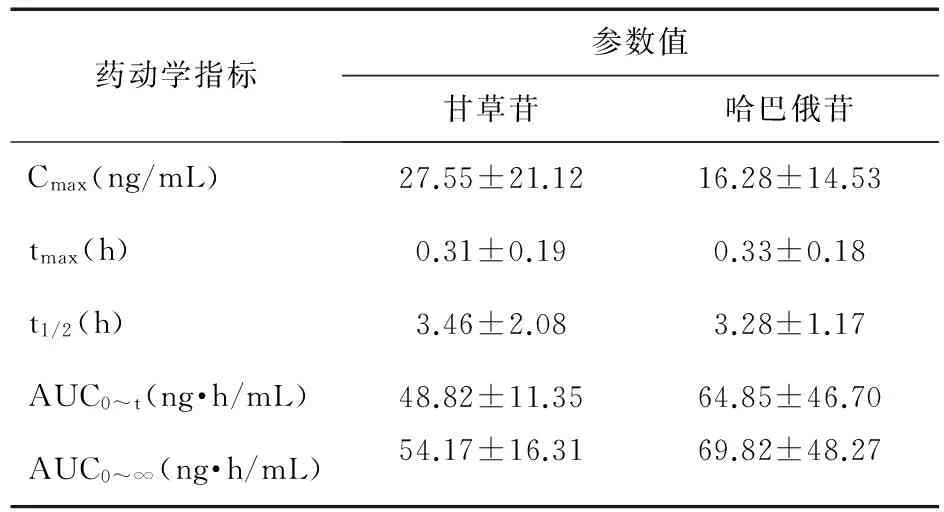
药动学指标参数值甘草苷哈巴俄苷Cmax(ng/mL)27.55±21.1216.28±14.53tmax(h)0.31±0.190.33±0.18t1/2(h)3.46±2.083.28±1.17AUC0~t(ng·h/mL)48.82±11.3564.85±46.70AUC0~∞(ng·h/mL)54.17±16.3169.82±48.27
3 讨论
本实验分别考察了常用流动相甲醇-水、乙腈-水和乙腈-甲酸水,结果发现,使用乙腈-0.1%甲酸水体系作为流动相时,被分析成分分离效果好,峰形对称。对加入水相的甲酸比例进一步进行考察,结果表明,水相中加入0.1%甲酸能够达到良好的分离效果和稳定的响应值,最后采用0.1%甲酸-乙腈水溶液为流动相进行梯度洗脱。
在样品处理过程中,本实验分别比较了蛋白沉淀(PP)和液-液萃取(LLE)2种前处理方法。分别采用乙酸乙酯、氯仿、乙醚为萃取试剂进行液-液萃取,发现方法回收率较低,且处理过程复杂。蛋白沉淀法操作简单,重现性好。本实验对不同的蛋白沉淀剂如甲醇、乙腈等分别进行考察,结果显示,采用乙腈作为蛋白沉淀剂,提取效率高,操作方便,且得到的样品内源性干扰较少。
药代动力学结果显示,大鼠灌胃玄麦甘桔颗粒后,甘草苷和哈巴俄苷的达峰时间分别为0.31、0.33 h;消除半衰期分别为3.46、3.28 h;说明玄麦甘桔颗粒后这些成分入血吸收和消除都较为迅速。与文献[6-7]相比,玄麦甘桔颗粒中这2种被测物的药动学行为与其单一成分、单味药材或复方配伍中的不同,这可能由于复方中药体系中多种组分相互作用所致。复方中药制剂的药代动力学特点不同于单一成分或单味药材的药代动力学,反映了复杂中药体系中多种组分相互作用的结果。因此,玄麦甘桔颗粒的药代动力学研究为明确该药的作用机制、揭示配伍的合理性和临床应用有重要的意义。
[1] 李方.玄麦甘桔汤治疗咽炎性咳嗽30例[J].辽宁中医药大学学报,2008,10(8):90-92.
[2] 唐华平,郝月琴,王宏,等.加味玄麦甘桔汤治疗咳嗽变异性哮喘100例临床观察[J].中国实验方剂学杂志,2008,14(10):64-65.
[3] 许福泉,许旭东,陈士林.玄参化学成分及药理活性研究进展[J].中国现代中药,2013,15(9):752-759.
[4] 高雪岩,王文全,魏胜利,等.甘草及其活性成分的药理活性研究进展[J].中国中药杂志,2009,34(21):2695-2700.
[5] 国家药典委员会.中华人民共和国药典(一部)[S].北京:中国医药科技出版社,2010.
[6] 赵瑞芝,王银洁,冯丽敏,等.大鼠口服芍苓消银片后血液中芍药苷、落新妇苷、迷迭香酸、异嗪皮啶、甘草苷的药物动力学研究[J].中国中药杂志,2014,39(13):2559-2563.
[7] 徐多多,庞欢欢,江美芳,等.玄参提取物化学成分及其大鼠血浆移行成分的LC-LTQ-Orbitrap分析[J].中国中药杂志,2016,41(3):521-527.
Determination of plasma concentration of indicative components in Xuanmai ganjie granules by UPLC-MS/MS and their pharmacokinetic study
WU Yin,WEI Xing,LIU Hong-tao,DONG Zhan-jun*
(Department of Pharmacy,Hebei General Hospital,Shijiazhuang 050051,China)
Objective To establish a UPLC-MS/MS method for the determination of indicative components such as liquiritin and harpagoside in Xuanmai ganjie granules in rats′ plasma,and to study the pharmacokinetics of them.Methods Phenomenex Kinetex C18column(50 mm×3 mm,2.6 μm)was used,and the column temperature was 20 ℃.The chromatography was eluted with mobile phase consisting of 0.1% formic acid solution(A) and acetonitrile(B) at the flow rate of 0.3 mL/min by gradient elution,the volume was 5 μL.Multiple-reaction monitoring (MRM) scanning mode was employed for quantification with switching electrospray ion(ESI) source polarity in negative mode.Six SD male rats were docked to collect blood 0.5 mL from angular vein at 0.03,0.08,0.16,0.33,0.67,1,1.5,2,3,4,6,8 and 12 h after administration of Xuanmai ganjie granule solution to determine the blood concentration of drugs.The pharmacokinetic parameters were calculated by using DAS 3.0 software.Results The linear ranges of liquiritin and harpagoside were 0.78~50.00 ng/mL (r=0.997 9) and 1.66~106.10 ng/mL (r=0.995 8),respectively.The intra-dayRSDand inter-dayRSDwere all lower than 8.8%,and the average recoveries were more than 82.3%.The pharmacokinetic parameters of liquiritin and harpagoside were as follows:t1/2:(3.46±2.08) and (3.28±1.17)h,Cmax:(27.55±21.12) and (16.28±14.53)μg/L,tmax:(0.31±0.19) and (0.33±0.18)h,AUC0~12 h:(48.82±11.35)and (64.85±46.70)μg·h/L.Conclusion The method is efficient,sensitive and reproducible,and can be used for pharmacokinetic analysis of liquiritin and harpagosideinvivo.
Xuanmai ganjie granules;Liquiritin;Harpagoside;UPLC-MS/MS;Pharmacokinetic
2016-08-09
河北省人民医院药学部,石家庄 050051
河北省卫生厅青年科技课题(ZL20140340);河北省中医药管理局指导性项目(2014152)
10.14053/j.cnki.ppcr.201703022
*通信作者
