CPB-LAR-GFP表达载体的构建及其在紫花苜蓿愈伤组织中的表达
2017-03-28陈春艳马晖玲董文科杨江伟李玉珠
陈春艳,马晖玲,董文科,杨江伟,李玉珠
(1.甘肃农业大学 草业学院/草业生态系统教育部重点实验室/甘肃省草业工程实验室/中-美草地畜牧业可持续发展研究中心,甘肃 兰州 730070; 2.河南科技大学 农学院,河南 洛阳 471003;3.甘肃农业大学 生命科学院,甘肃 兰州 730070)
CPB-LAR-GFP表达载体的构建及其在紫花苜蓿愈伤组织中的表达
陈春艳1,2,马晖玲1,董文科1,杨江伟3,李玉珠1
(1.甘肃农业大学 草业学院/草业生态系统教育部重点实验室/甘肃省草业工程实验室/中-美草地畜牧业可持续发展研究中心,甘肃 兰州 730070; 2.河南科技大学 农学院,河南 洛阳 471003;3.甘肃农业大学 生命科学院,甘肃 兰州 730070)
以无色花青素还原酶编码基因LAR为靶序列,构建携带绿色荧光蛋白GFP和抗除草剂bar基因的双标记选择植物表达载体,通过农杆菌介导法对紫花苜蓿进行遗传转化,经PCR检测和PPT筛选出抗性愈伤组织,转基因紫花苜蓿愈伤组织的缩合单宁含量比对照高30.8%。试验证明重组基因已转化至紫花苜蓿愈伤组织中并发挥生理功能,为研究缩合单宁合成与代谢的分子调控机制和培育具有抗除草剂和抗臌胀病的牧草新品种奠定基础。
甘肃红豆草;无色花青素还原酶;抗除草剂;绿色荧光蛋白;紫花苜蓿;转化
紫花苜蓿(Medicagosativa)叶片中不含有缩合单宁[1,2],反刍动物采食鲜嫩紫花苜蓿后会引起臌胀病。因此,含缩合单宁苜蓿新品种的培育和饲草组合利用被认为是解决采食紫花苜蓿引起牲畜臌胀病发生的两条途径。选育出遗传稳定的抗臌胀病苜蓿新品种无疑是牧草新品种培育者的首选途径。植物体内缩合单宁物质的积累受到自身遗传和调节因子的控制[3-6]。红豆草生长的各个时期叶片中均含有较高浓度的缩合单宁,反刍动物大量采食红豆草后不会引起臌胀病。有报道从红豆草(Onobrychisviciaefolia)中鉴定和分离控制缩合单宁积累的基因,利用基因工程技术将此基因导入紫花苜蓿中是实现遗传资源创新的途径之一[7-10]。既可解决牲畜鲜食紫花苜蓿引发的臌胀病问题,也利于降低牲畜瘤胃消化过程温室气体的排放,对草业和畜牧业的发展及缓解其对环境造成的压力都有重要的意义[11]。
缩合单宁(即花青素)属于类黄酮生物合成途径中的植物次生代谢产物。植物次生代谢物合成与积累量取决于其合成途径中的限速酶,其限速酶在植物次生代谢物生物合成途径中往往位于代谢支路分叉口或途径的下游[12]。无色花青素还原酶(LAR)位于缩合单宁合成途径的下游,直接将无色花青素转化成儿茶酚(2,3-反式黄烷-3-醇),即一类缩合单宁单体,最终聚合形成缩合单宁。LAR被认为是缩合单宁生物合成途径的限速酶[12]。因此,LAR在缩合单宁生物合成途径中尤为重要。除了拟南芥(Arabidopsisthaliala)中没有LAR基因,在多种植物中均发现LAR的活性,并且LAR的活性与缩合单宁的累积相关[13-14]。Bogs[15]发现LAR的表达决定葡萄中缩合单宁的累积和组成。Paolocci[16]报道LAR的稳定表达与百脉根叶中缩合单宁的累积一致。但是也有LAR活性与缩合单宁累积不符的报道,蒺藜苜蓿MtLAR的转录水平与缩合单宁的累积并不相符[17],也有发现柿中LAR基因的表达与缩合单宁累积不符。可见,LAR基因与缩合单宁合成受到种间差异的影响。可以推断利用种间的遗传差异和基因工程手段来调控植物缩合单宁含量是可行的。
研究拟采用广泛应用的绿色荧光蛋白GFP基因作为报告基因,结合兼具抗锄草剂特性和报告基因的双重功能的抗广谱除草剂草丁膦的bar基因;构建用于农杆菌转化的含双标记(bar和GFP基因)的LAR植物表达载体,遗传转化紫花苜蓿。这将为研究缩合单宁合成与代谢过程中的功能提供基础资料,也为利用无色花青素还原酶基因调控紫花苜蓿缩合单宁的含量奠定基础。
1 材料和方法
1.1 菌株与质粒
pMD-GFP质粒、pMD-LAR质粒、CPB质粒、农杆菌LBA4404由甘肃农业大学草业学院草业生态系统教育部重点实验室提供。
1.2 材料与试剂
红豆草品种为甘肃红豆草,苜蓿品种为和田苜蓿,由甘肃农业大学草业学院提供。SanPrep DNA胶回收试剂盒、Amp、Kan、Rif、Str购自上海生工生物工程公司,Taq酶、T4DNA连接酶、限制性内切酶(BamHⅠ、SmalⅠ、SacⅠ)、DNA Marker购自大连宝生物工程有限公司,其他药品、试剂为常规国产分析纯。
1.3 CPB-LAR-GFP表达载体的构建
pMD-GFP质粒用BamHⅠ和SmalⅠ双酶切,回收GFP片段(714 bp);pMD-LAR质粒用SmalⅠ和SacⅠ双酶切,回收LAR片段(1 089 bp);载体CPB(含bar基因)用BamHⅠ和SacⅠ双酶切,回收大片段。通过T4DNA连接酶,将GFP片段、LAR片段与载体大片段16℃连接6 h。连接产物转化大肠杆菌,经蓝白斑筛选,挑取阳性单菌落,通过质粒PCR和酶切鉴定筛选出重组克隆,送3个克隆样品到上海生工生物公司测序,将此含LAR和GFP基因的载体命名为:CPB-LAR-GFP(图1)。
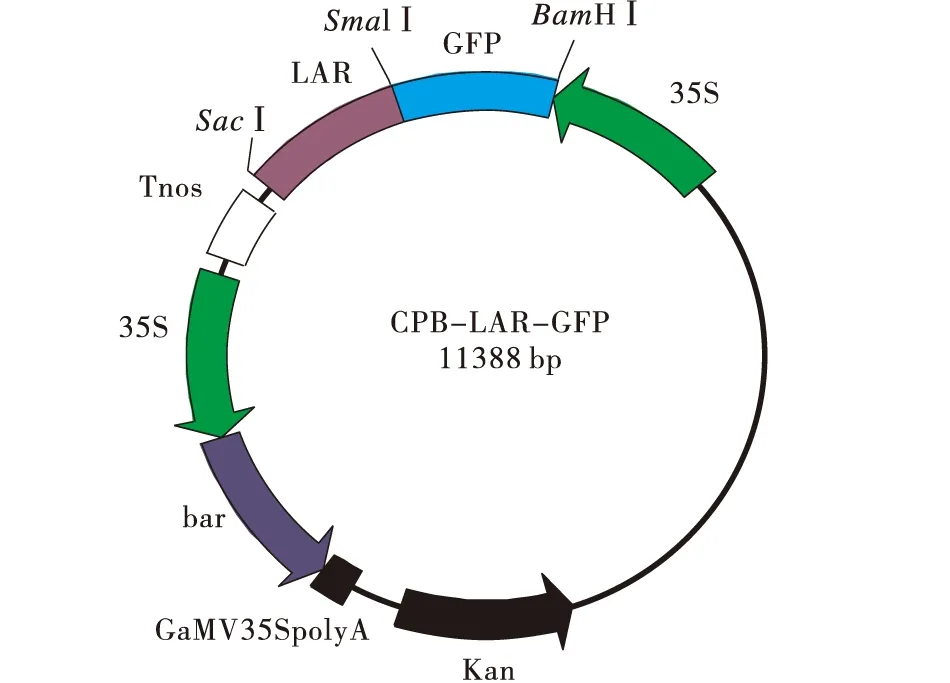
图1 CPB-LAR-GFP表达载体结构Fig.1 The structure of the eukaryotic expression vector CPB-LAR-GFP
1.4 紫花苜蓿遗传转化及检测
1.4.1 载体CPB-LAR-GFP转化农杆菌 采用文献[17]方法将植物表达载体CPB-LAR-GFP转化至农杆菌LBA4404。转化产物涂布于含50 μg/mL Kan、25 μg/mL Str、25 μg/mL Rif的YEB固体培养基上,28℃恒温培养2 d,挑取阳性单菌落,质粒PCR鉴定。
1.4.2 重组农杆菌转化紫花苜蓿 取含供试质粒CPB-LAR-GFP的农杆菌LBA4404,在含50 μg/mL Kan,25 μg/mL Str和25 μg/mL Rif的YEB平板培养基上划线,28℃培养2 d,挑取单菌落接入含相应抗生素的YEB液体培养基中,28℃振荡培养过夜。剪取紫花苜蓿无菌苗的下胚轴,用活化的农杆菌(D600 nm值为0.3~0.5)侵染10 min,用无菌水将组织材料清洗干净,用无菌滤纸吸干水分,放置在25℃共培养基(MS+2.0 mg/L 2,4-D)上暗培养3 d,转入诱导愈伤培养基(MS+2.0 mg/L 2,4-D+0.5 mg/L KT+50 mg/L Kan+300 mg/L Cef),25℃暗培养25 d,转入分化培养基(MS+2.0 mg/L 6-BA+0.5 mg/L NAA+50 mg/L Kan+300 mg/L Cef),进行分化再生培养。
1.5 转基因愈伤组织的检测
1.5.1 PCR检测 取愈伤组织0.10 g,按文献[18]方法提取基因组DNA,以此为模板,根据LAR基因设计特异引物P1:ATGGCGACTTCCCCAGCCAATATC,P2:TCAACAGGAAGCTGTTATTGGGACTG,扩增LAR基因。PCR反应体系(25 μL)包括DNA 1 μL,10×Buffer 2.5 μL,10 mmol/L dNTP 2 μL,引物P1和P2(10 pmol/μL)各1 μL,5 U/μLTaq酶0.5 μL。扩增参数为:94℃预变性4 min;94℃变性1 min,57℃退火1 min,72℃延伸1 min30 s,38个循环;72℃延伸10 min,最后于4℃保存。PCR产物于1%琼脂糖凝胶电泳检测。
1.5.2 抗除草剂抗性鉴定 将转基因愈伤组织接种到含不同浓度(1.0~5.0 mg/L)草丁膦(PPT)的分化培养基上,以组织培养获得的再生愈伤作抗性筛选对照,观察抗性愈伤对不同浓度PPT的抗性。
1.5.3 GFP荧光检测 取转基因愈伤组织进行压片,置于OLYPUSBX 51/BX 52型荧光显微镜下,用蓝光激发愈伤组织,观察并拍照。
1.5.4 缩合单宁含量检测 以未转基因愈伤为对照,采用正丁醇-盐酸法测定转基因愈伤缩合单宁含量[19-20]。
2 结果与分析
2.1 CPB-LAR-GFP植物表达载体的构建
用SmalⅠ+SacⅠ双酶切pMD-LAR质粒,回收LAR目的片段,用BamHⅠ和SmalⅠ双酶切pMD-GFP质粒,回收GFP目的片段,用BamHⅠ+SacⅠ双酶切载体CPB,回收大片段。将回收的LAR目的片段、GFP目的片段与载体大片段通过T4DNA连接酶连接后,连接产物转化E.coliDH5α感受态细胞,挑选阳性克隆子摇菌,PCR检测(图2)扩增出1 089 bp(LAR基因)和714 bp(GFP基因)的2条带;双酶切鉴定(图2)切下约为714 bp(GFP基因)、1 089 bp(LAR基因)、1 803 bp(LAR基因和GFP基因)的3条带,PCR与双酶切均得到预期大小的条带。说明成功构建了CPB-LAR-GFP植物表达载体。

图2 重组质粒CPB-LAR-GFP PCR及双酶切Fig.2 PCR and double digestion of the recombined CPB-LAR-GFP plasmid注:1,5.DL2000 Marker;2.BamHⅠ和SmalⅠ双酶切结果 (714 bp);3.SmalⅠ+SacⅠ双酶切结果 (1 089 bp);4.BamHⅠ+SacⅠ双酶切结果 (1 803 bp);6.PCR扩增产物 (1 089 bp);7.PCR扩增产物 (714b p);8.DL1000Marker
2.2 紫花苜蓿遗传转化及检测
2.2.1 植物表达载体CPB-LAR-GFP转化农杆菌 通过直接导入法将植物表达载体CPB-LAR-GFP转化至根癌农杆菌LBA4404的感受态细胞中,挑取阳性单菌落摇菌并提取质粒,进行PCR鉴定(图3),得到1 089 bp(LAR基因)和714 bp(GFP基因)的条带,与预期片段大小相符[17]。

图3 转LAR基因苜蓿愈伤的PCR检测Fig.3 PCR identification of Trans LAR gene alfalfa callus注:1,15.DL2000Marker;2.阴性对照;3.水;4.阳性对照;5~14:转基因苜蓿愈伤
2.2.2 苜蓿遗传转化及转基因愈伤的获得 苜蓿下胚轴外植体用制备好的菌液侵染10 min,吸干菌液,置于共培养基,25℃黑暗条件下共培养3 d,使农杆菌携带的基因转入苜蓿染色体中。之后转入愈伤组织诱导培养基,一周后开始形成愈伤组织,转基因愈伤仍能具有良好的细胞分裂和分化能力,25℃暗培养25 d后,转入分化培养基,进行分化再生培养。
2.2.3 转基因愈伤的PCR检测 经检测,筛选培养后获得的愈伤组织中大部分为转基因愈伤。选取的10株抗性愈伤中有7株获得了1 100 bp左右的LAR基因片段(图4)。说明转化的目的基因已整合到苜蓿基因组中。

图4 CPB-LAR-GFP导入农杆菌的PCR鉴定Fig.4 PCR analysis of CPB-LAR-GFP transformed Agrobacterium tumefaciens注:1,4.DL2000Marker;2,5.重组农杆菌PCR结果(1 089 bp);3,6.重组农杆菌PCR结果 (714 bp)
2.2.4 转基因愈伤组织抗除草剂抗性鉴定 在转化筛选培养基中加入适量的PPT利于筛选出转基因植株。转基因愈伤接种到含低浓度PPT(1.0 mg/L、2.0 mg/L)的MS培养基上,对愈伤组织影响比较弱。当PPT浓度为3.0 mg/L时,部分苜蓿愈伤受到抑制,发生褐化。当PPT浓度大于4.0 mg/L时,培养20 d以后的苜蓿愈伤组织生长受到明显抑制,随着培养时间的延长,褐化严重,愈伤组织生长受到严重抑制,甚至死亡。因此,PPT浓度选择3.0 mg/L。
2.2.5 转基因愈伤组织的GFP荧光检测 经检测含重组质粒的苜蓿愈伤组织在荧光显微镜下呈现绿光(图5),说明GFP基因在苜蓿愈伤组织中得到了高效表达。

图5 转基因愈伤GFP基因荧光表达Fig.5 Fluorescent expression of GFP gene of alfalfa transgenic callus
2.2.6 转基因愈伤组织缩合单宁含量检测 整合有LAR基因的苜蓿愈伤组织中缩合单宁的含量高于对照30.8%(图6),证明LAR基因的异源表达促进了紫花苜蓿原花青素的积累。进一步证明此次试验构建的LAR基因植物表达载体可以用于提高苜蓿CT含量的种质创新研究。

图6 转基因和未转基因紫花苜蓿愈伤组织缩合单宁的含量Fig.6 Condensed tannins content in the transgenic and non-transgenic callus in alfalfa注:CK为未转基因紫花苜蓿愈伤组织;HT1~HT6为转基因紫花苜蓿愈伤组织
3 讨论
3.1 CPB-LAR-GFP表达载体的特点
研究将无色花青素还原酶(LAR)基因和报告基因绿色荧光蛋白(GFP)基因同时连在已含有抗除草剂(bar)基因的载体CPB上,构建了植物表达载体CPB-LAR-GFP。GFP是被广泛应用的报告基因[21-22],连在目的基因启动子之后,在不破坏细胞和不进行化学染色的情况下直接成像,根据GFP的荧光强度可以检测目的基因的表达水平,而且能监测基因表达和蛋白质定位,检测方便且快速。抗广谱除草剂草丁膦的bar基因是目前广泛使用的具有抗锄草剂特性的报告基因,是一种能避免自身产物Bialaphos毒害的保护基因[23]。本研究构建的具有双标记bar和GFP基因的LAR基因植物表达载体CPB-LAR-GFP,既具有抗除草剂性质,又具有标记基因的功能。这样既可提高筛选转化细胞效率,同时使该载体转化的植株获得抗除草剂特性。研究也为进一步研究LAR基因的功能及其在缩合单宁合成中的作用奠定了基础,也为扩充了苜蓿育种的基因库资源,利用转基因技术提高苜蓿品质和性状提供支撑[8,10]。
3.2 紫花苜蓿转基因愈伤的筛选及LAR基因的功能分析
在研究匍匐剪股颖的转化中[24],利用卡那霉素作为选择压对转基因植物进行筛选,但筛选效果不佳,造成后期转基因植株的检测工作量过大。试验对转基因愈伤进行逐级筛选。首先利用卡那霉素作为选择压,在愈伤组织诱导培养基和分化培养基均加入适当浓度的卡那霉素;随后在分化培养基中添加一定浓度的PPT,部分愈伤发生褐化,生长受到抑制。这样筛选出抗性愈伤组织,将其放入荧光显微镜下照射蓝光,可以激发出绿色荧光的愈伤组织初步筛选成为转基因愈伤,方便、简化了后期转基因愈伤的检测工作,降低了工作难度。这样可以发挥bar基因在此次研究构建的载体中的双重功能,既作为抗除草剂基因,具有抗除草剂性质;又作为标记基因,便于筛选出转化体和非转化体。研究发现,将bar基因转入苜蓿中[25-26],转基因苜蓿对除草剂抗性明显。此次研究与其研究结果一致,转bar基因的紫花苜蓿愈伤组织具有抗除草剂特性,可以筛选出具有PPT抗性的愈伤组织。我们研究也发现,转LAR基因的紫花苜蓿愈伤的缩合单宁含量明显高于对照。由此推断LAR基因在缩合单宁合成途径中起着至关重要的作用,LAR基因直接影响了缩合单宁的合成,提高该基因的表达有利于合成缩合单宁,期望超量表达该基因以提高缩合单宁的含量。
4 结论
以LAR基因为靶序列,构建携带绿色荧光蛋白GFP和抗除草剂bar基因的双标记选择植物表达载体CPB-LAR-GFP,并导入农杆菌。遗传转化紫花苜蓿,提取转基因愈伤组织DNA,PCR扩增检测到1 089 bp的LAR片段。PPT抗性试验证明,构建的载体具有抗除草剂抗性,PPT临界筛选浓度为3.0 mg/L时。荧光显微镜照射转基因苜蓿愈伤组织呈现绿光。测定转基因紫花苜蓿愈伤组织缩合单宁的含量明显高于对照。初步证明转LAR基因的紫花苜蓿可以提高缩合单宁含量。这将为进一步研究LAR基因的表达与调控和培育具有抗除草剂和缩合单宁含量高的牧草新品种提供理论依据。
[1] Goplen B P,Howarth R E,Sarkar S K,etal.A Search for condensed tannis in annual and perennial species ofMedieago,Trigonella,andOnobrychis[J].Crop Science,1980,20:801-804.
[2] Koupai-Abyazani M R,McCallum J,Muir A D,etal.Purification and characterization of a proanthocyanidin polymer from seed of alfalfa (Medicagosativacv.Beaver)[J].Journal of Agricultural and Food Chemistry,1993,41:565-569.
[3] Paolocci F,Bovone T,Tosti N,etal.Light and an exogenous transcription factor qualitatively and quantitatively affect the biosynthetic pathway of condensed tannins in Lotus cornicuental latus leaves[J].Journal of Experim Botany,2005,56:1093-1103.
[4] Zhao J,Pang Y,Dixon R A.The mysteries of proanthocyanidin transport and polymerization[J].Plant Physiology,2010,153:437-443.
[5] Hichri I,Barrieu F,Bogs J,etal.Recent advances in the transcriptional regulation of the flavonoid biosynthetic pathway[J].Journal of Experimental Botany,2011,62:2465-2483.
[6] Verdier J,Zhao J,Torres-Jerez I,etal.MtPAR MYB transcription factor acts as an on switch for proanthocyanidin biosynthesis inMedicagotruncatula[J].Proceedings of the National Academy of Sciences USA,2012,109:1766-1771.
[7] 杨茁萌,陈颖,李林,等.红豆草浓缩单宁生物合成相关蛋白的研究[J].草原家畜(增刊),1996(9):47-54.
[8] 俞金蓉,玉永雄,陈丽梅.生物技术在紫花苜蓿中的应用[J].草原与草坪,2005(5):65-69.
[9] 王艳,李建龙,潘永年,等.草坪草转基因育种研究进展[J].草原与草坪,2007(6):13-17.
[10] 顾垒,毕玉芬.转基因苜蓿研究的现状和前景[J].草原与草坪,2004(1):17-21.
[11] Smith A K,Frank M,Phil M,etal.Reducing post-harvest losses of forage protein[J].Iger Innovationa,2004(8):30-33.
[12] 王旺田,张金文,王蒂,等.马铃薯块茎糖基转移酶基因的克隆及其RNAi载体的构建[J].作物学报,2011,37(11):1926-1934.
[13] 陈春艳,马晖玲,董文科.甘肃红豆草无色花青素还原酶LAR基因的克隆和表达分析[J].草业学报,2015,24(6):177-187.
[14] Tanner G J,Francki K T,Abrahams S,etal.Proanthocyanidin biosynthesis in plants:purification of legume leucoanthocyanidin reductase and molecular cloning of its cDNA[J].Journal of Biology Chemistry,2003,278:31647-31656.
[15] Bogs J,Downey M O,Harvey J S,etal.Proanthocyanidin synthesis and expression of genes encoding leucoanthocyanidin reductase and anthocyanidin reductase in developing grape berries and grapevine leaves[J].Plant Physiology,2005,139(2):652-663.
[16] Paolocci F,Robbins M P,Madeo L,etal.Ectopic expression of a basic helix-loop-helix gene transactivates parallel pathways of proanthocyanidin biosyn thesis:structure,expression analysis,and genetic control of leucoanthocyanidin 4-reductase and anthocyanidin reductase genes in Lotus corniculatus[J].Plant physiology,2007,143(1):504-516.
[17] 王关林,方宏筠.植物基因工程原理与技术[M].北京:科学出版社,1998:547-548.
[18] 王关林,方宏筠.植物基因工程(第二版)[M].北京:科学出版社,2002:742-744.
[19] 陈春艳,马晖玲,董文科.‘甘肃红豆草’肌动蛋白基因片段的克隆及序列分析[J].甘肃农业大学学报,2014,49(6):97-102.
[20] Terrill T H,Row An A M,Douglas G B,etal.Determination of extractable and bound condensed tannin concentrations in forage plans protein concentrate meals and cereal grains[J].Journal of the science of food and agriculture,1992,58:321-329.
[21] Chalfie M,Tu Y,Euskirchen G,etal.Green fluorescent protein as a maker for gene expression[J].Science,1994,263(5148):802-805.
[22] Jim H,Brad A.GFP in plant[J].Technical Focus,1995,8(11):10-11.
[23] 陈玉香,周道玮.转基因牧草研究进展[J].中国草地,2002,24(3):59-63.
[24] 安惠惠,马晖玲,李坚,等.农杆菌介导的Lyz-GFP基因对匍匐翦股颖Penn A-1转化和表达的研究[J].草业学报,2012,21(2):141-148.
[25] D′Halluin K,Boteerman J,de Greef W.Engineering of herbicide-resistant alfalfa and evaluation under field conditions[J].Crop Science,1990,30:866-871.
[26] 刘艳芝,王玉民,刘莉,等.Bar基因转化草原1号苜蓿的研究[J].草地学报,2004,12(4):273-280.
Construction of CPB-LAR-GFP expression vector and its transformation in callus of alfalfa
CHEN Chun-yan1,2,MA Hui-ling1,DONG Wen-ke1,YANG Jiang-wei3,LI Yu-zhu1
(1.CollegeofPrataculturalScience,GansuAgriculturalUniversity/KeyLaboratoryofGrasslandEcosystem,MinistryofEducation/PrataculturalEngineeringLaboratoryofGansuProvince/Sino-U.S.CenterforGrazinglandEcosystemSustainability,Lanzhou730070,China; 2.CollegeofAgronomy,HenanUniversityofScienceandTechnology,Luoyang471003,China; 3.CollegeofLifeSciences,GansuAgriculturalUniversity,Lanzhou730070,China)
Leucoanthocyanidin reductase is a key enzyme in plant condensed tannins synthesis.The target was Leucoanthocyanidin reductase encoded by LAR gene,the expression vector was constructed with the double-marker expressing green fluoresce protein GFP gene and herbicide resistance bar gene.Transgenic alfalfa callus were obtained byAgrobacteriumtumefaciensmediated transformation,and the resistant callus were screened by PPT.The condensed tannins content in transgenic alfalfa callus was 30.8% higher than that of control.The recombinant gene had been transformed to alfalfa callus and played a physiological function.These research work will provide the fundamental information and the method for studying the regulation mechanism of condensed tannins synthesis and further alfalfa breeding through transgenic technology with character of resistance to herbicide and bloat disease.
Onobrychisviciaefoliacv.Gansu;leucoanthocyanidin reductase;herbicide resistance;green fluoresce protein;alfalfa;transformation
2016-04-21;
2016-05-16
甘肃省科技厅科技支撑计划项目(1104NK CA087);国家自然科学基金项目(41261013)和国家自然科学基金项目(31502012)资助
陈春艳(1977-),女,甘肃兰州人,实验师,在读博士研究生。 E-mail:ccy0713@126.com 马晖玲为通讯作者。
Q 814.9;S 54
A
1009-5500(2017)01-0025-06
