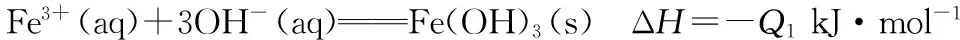水溶液中的离子平衡专题检测
2017-03-28北京李宏华
北京 李宏华
(作者单位:北京市顺义区第八中学)
水溶液中的离子平衡专题检测

一、选择题
1.(原创)下列事实不能证明HNO2是弱电解质的是
( )
A.HNO2和NaCl不能发生反应
B.0.1 mol·L-1HNO2溶液的pH=2.1
C.NaNO2和H3PO4反应,生成HNO2
D.0.1 mol·L-1HNO2溶液稀释至100倍,pH约为3.1
2.(原创)25℃时,现有0.10 mol/L Na2CO3溶液。下列观点不正确的是
( )
A.该溶液的pH>7
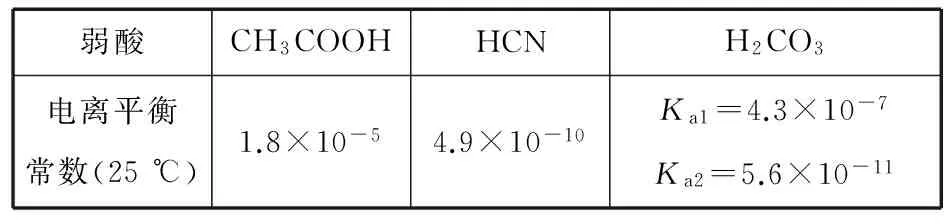
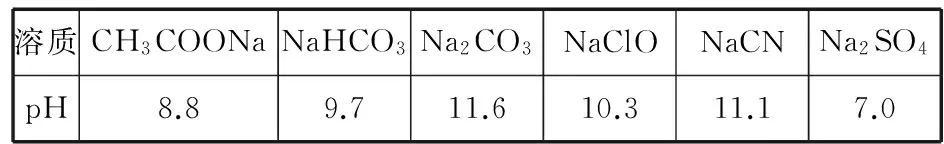
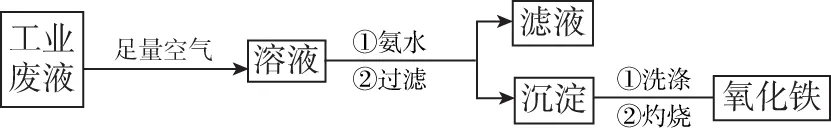
C.水垢中的CaSO4用Na2CO3溶液充分浸泡后可转化为CaCO3,说明溶解度CaSO4 3.(原创)某温度下,将相同pH的盐酸和醋酸分别加水稀释,溶液的pH随着溶液体积的变化曲线如图所示。据图判断正确的是 ( ) A.Ⅱ为稀释盐酸时的pH变化曲线 B.b点溶液的导电能力比c点溶液的导电能力强 C.a点Kw的数值比c点Kw的数值大 D.b点酸的总浓度大于a点酸的总浓度 ( ) B.Q点对应的溶液中c(Na+)>2c(Cl-)>c(OH-)>c(H+) D.如果M点表示开始滴加时的溶液,则N点表示反应结束时的溶液 5.(原创)下列判断不正确的是 ( ) A.①②⑥⑦⑧________________B.②③⑤⑦ C.①②③④⑤⑥⑧___________D.全部 ( ) A.MnS的Ksp小于CuS的Ksp B.达到平衡时c(Mn2+)=c(Cu2+) C.溶液中加入少量Na2S固体后,溶液中c(Cu2+)、c(Mn2+)保持不变 7.(原创)分析下表,下列选项中错误的是 ( ) B.将amol/L HCN溶液与amol/L NaOH溶液等体积混合,测得所得溶液呈碱性(pH>7),则c(OH-)>c(H+),c(CN-) C.相同物质的量浓度的Na2CO3和NaCN溶液,后者pH较大 D.等物质的量的各溶液pH大小关系为pH(Na2CO3)>pH(NaCN)>pH(CH3COONa) 二、非选择题 8.(改编题)(1)AlCl3溶液呈________(填“酸”“中”或“碱”)性,原因是________(用离子方程式表示)。把AlCl3溶液蒸干、灼烧,最后得到的主要固体产物是________(写化学式)。实验室在保存AlCl3溶液时,常在溶液中加少量的________,以________(填“促进”或“抑制”)其水解。 (2)将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈________(填“酸”“中”或“碱”)性,溶液中c(Na+)________(填“>”“=”或“<”)c(CH3COO-)。 (3)25 ℃时,pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈________(填“酸”“中”或“碱”)性,溶液中,c(Na+)________(填“>”“=”或“<”)c(CH3COO-)。 溶质CH3COONaNaHCO3Na2CO3NaClONaCNNa2SO4pH8.89.711.610.311.17.0 请回答下列问题: ①上述盐中的阴离子,结合质子能力最强的是________。 ②根据表中数据,下列浓度均为0.1 mol·L-1的五种溶液中,酸性最强的是________(填序号,下同);将各溶液分别稀释100倍,pH变化最小的是________。 A.HCN B.HClO C.H2SO4D.CH3COOH E.H2CO3 ③将CO2气体通入饱和碳酸钠溶液中,可以观察到的现象为________________,原因是________________________________ (用离子方程式表示)。 ④要增大氯水中HClO的浓度,可向氯水中加入少量的碳酸钠溶液,用离子方程式解释其原因:________。 9.(改编题)水的电离平衡曲线如图所示。 (1)购房者成本变动的影响与分析。购房者成本:购房者购买被动房时的增量成本费用为C3。下面是使用MATLAB仿真得出的图6,图像的纵轴是购房者选择购买普通房的概率,横轴是推广时间,因此曲线反映了概率水平随着推广过程进行产生的变化。 (1)若以A点表示25 ℃时水在电离平衡时的离子浓度,当温度升到100 ℃时,水的电离平衡状态到B点,则此时水的离子积从________增加到________。 (2)常温下,将pH=10的Ba(OH)2溶液与pH=5的稀盐酸混合,然后保持100 ℃的恒温,欲使混合溶液pH=7,则 Ba(OH)2溶液与盐酸的体积比为________。 (3)在某温度下,Ca(OH)2的溶解度为0.74 g,其饱和溶液密度设为1 g·mL-1,Ca(OH)2的离子积为________。 (4)25 ℃时,在等体积的①pH=0的H2SO4溶液,②0.05 mol·L-1的Ba(OH)2溶液,③pH=10的Na2S溶液,④pH=5的NH4NO3溶液中,发生电离的水的物质的量之比是________。 (5)等体积的下列溶液中,阴离子的总物质的量最大的是________(填序号)。 ①0.1 mol·L-1的CuSO4溶液 ②0.1 mol·L-1的Na2CO3 ③0.1 mol·L-1的KCl ④0.1 mol·L-1的NaHCO3 ①则Na2A溶液显________(填“酸性”“中性”或“碱性”);NaHA溶液显________(填“酸性”“中性”或“碱性”)。 ②若有0.1 mol·L-1Na2A的溶液,其中各种离子浓度由大到小的顺序是________(填字母)。 A.c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H+) B.c(Na+)>c(OH-)>c(HA-)>c(A2-)>c(H+) C.c(Na+)>c(H+)>c(A2-)>c(OH-)>c(HA-) D.c(A2-)>c(Na+)>c(OH-)>c(H+)>c(HA-) (7)一定温度下,向等体积纯水中分别加入等物质的量的下列物质:①NaOH、②CH3COOH、③NaClO,则水的电离程度最大的是________(填编号)。一定温度下,向等体积纯水中分别加入等物质的量的CH3COONa和NaCN,两溶液中阴离子的总物质的量分别为n1和n2,则n1和n2的关系为n1________(填“>”“<”或“=”)n2。 已知:常温下Ksp[Mg(OH)2]=1.2×10-11;Ksp[Fe(OH)2]=2.2×10-16;Ksp[Fe(OH)3]=3.5×10-38;Ksp[Al(OH)3]=1.0×10-33 (1)写出在该酸性废液中通入空气时发生反应的离子方程式:________,指出使用空气的优点是___________。 (3)常温下,根据已知条件计算在pH=5的溶液中,理论上下列微粒在该溶液中可存在的最大浓度c(Fe3+)=___________ 。 (4)有人用氨水调节溶液pH,在pH=5时将Fe(OH)3沉淀出来,此时可能混有的杂质是________(填化学式,下同),用________试剂可将其除去。 (5)FeCl2溶液蒸干灼烧得到的固体物质是________,原因是___________。 11.(改编题)三氯氧磷(化学式:POCl3)常用作半导体掺杂剂及光导纤维原料。氯化水解法生产三氯氧磷的流程如下: (1)氯化水解法生产三氯氧磷的化学方程式为___________。 (2)通过佛尔哈德法可以测定三氯氧磷产品中Cl元素含量,实验步骤如下: Ⅰ.取ag产品于锥形瓶中,加入足量NaOH溶液,待完全水解后加稀硝酸至酸性。 Ⅱ.向锥形瓶中加入0.100 0 mol·L-1的AgNO3溶液40.00 mL,使Cl-完全沉淀。 Ⅲ.向其中加入2 mL硝基苯,用力摇动,使沉淀表面被有机物覆盖。 Ⅳ.加入指示剂,用cmol·L-1NH4SCN溶液滴定过量Ag+至终点,记下所用体积。 已知:Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2×10-12 ①滴定选用的指示剂是___________ (填字母),滴定终点的现象为___________ 。 a.FeCl2___________b.NH4Fe(SO4)2 c.淀粉___________d.甲基橙 ②实验过程中加入硝基苯的目的是___________ ,如无此操作所测Cl元素含量将会________(填“偏大”“偏小”或“不变”)。 (3)氯化水解法生产三氯氧磷会产生含磷(主要为H3PO4、H3PO3等)废水。在废水中先加入适量漂白粉,再加入生石灰调节pH将磷元素转化为磷酸的钙盐沉淀并回收。 ①在沉淀前先加入适量漂白粉的作用是___________。 ②下图是不同条件对磷的沉淀回收率的影响图象。 处理该厂废水最合适的工艺条件为___________ (填字母)。 a.调节pH=9___________b.调节pH=10 c.反应时间30 min___________d.反应时间120 min (4)为了研究沉淀溶解平衡和沉淀转化,某同学查阅资料并设计如下实验。资料:AgSCN是白色沉淀,相同温度下,溶解度:AgSCN>AgI。 操作步骤现象步骤1:向2mL0.005mol·L-1AgNO3溶液中加入2mL0.005mol·L-1KSCN溶液,静置出现白色沉淀步骤2:取1mL上层清液于试管中,滴加1滴2mol·L-1Fe(NO3)3溶液溶液变红色步骤3:向步骤2的溶液中,继续加入5滴3mol·L-1AgNO3溶液,溶液红色变浅步骤4:向步骤1余下的浊液中加入5滴3mol·L-1KI溶液出现黄色沉淀 ①写出步骤2中溶液变红色的离子方程式:___________。 ②步骤3中现象a是___________。 ③用化学平衡原理解释步骤4的实验现象:___________。 参考答案及解析 1.A 【解析】A选项,HNO2和NaCl不能发生反应,只能说明不符合复分解反应的条件,但不能说明HNO3是弱酸,故A错误;B选项,常温下0.1 mol·L-1HNO2溶液的pH=2.1,说明亚硝酸不完全电离,溶液中存在电离平衡,所以能说明亚硝酸为弱酸,故B正确;C选项,强酸可以制取弱酸,NaNO2和H3PO4反应,生成HNO2,说明HNO2的酸性弱于H3PO4,所以能说明亚硝酸为弱酸,故C正确;D选项,常温下pH=1的HNO2溶液稀释至100倍,pH约为3.1说明亚硝酸中存在电离平衡,则亚硝酸为弱电解质,故D正确。 3.B 【解析】两种酸的起始pH相同,即c(H+)相同,说明起始时c(弱酸)远大于c(强酸);没有稀释前弱酸的c(H+) 已等于强酸的c(H+),而稀释导致弱酸的电离程度增大,所以在稀释的整个过程中,弱酸的c(H+)都大于强酸的c(H+),即pH:弱酸<强酸,所以曲线Ⅱ是醋酸、Ⅰ是盐酸,A项错误;溶液的导电能力的强弱取决于溶液中离子浓度的大小,对于酸而言,其pH越大,c(H+)越小,离子浓度越小,导电能力越弱,故B正确;Kw的大小只取决于温度,与溶液的浓度无关,C项错误;两溶液稀释相同的倍数时,醋酸的浓度始终大于强酸的浓度,故D项错误。 Al2O3HCl 抑制 9.(1)10-1410-12 (2)2∶9 (3)0.004 (4)1∶10∶1010∶109 (5)② (6)①碱性 酸性 ②A (7)③ > (2)-(Q2+Q1)kJ·mol-1 (3)3.5×10-11mol·L-1 (4)Al(OH)3NaOH (5)Fe2O3Fe2+水解生成Fe(OH)2和HCl,在加热蒸干过程中HCl挥发,Fe(OH)2逐渐被氧化生成Fe(OH)3,Fe(OH)3灼烧分解生成Fe2O3 (2)①b 溶液变为红色 ②防止在滴加NH4SCN时,将AgCl沉淀转化为AgSCN沉淀 偏小 (作者单位:北京市顺义区第八中学)