海洋红树林植物卤蕨内生真菌Cladosporium perangustumMA- 318中一个新的链烯酸酐衍生物methylate cordyanhydride A
2017-03-26李衍荷李晓明李洪雷王斌贵
李衍荷, 李晓明, 徐 蕊, 李洪雷, 王斌贵
海洋红树林植物卤蕨内生真菌MA- 318中一个新的链烯酸酐衍生物methylate cordyanhydride A
李衍荷1, 2, 李晓明1, 徐 蕊1, 2, 李洪雷1, 2, 王斌贵1
(1. 中国科学院 海洋研究所 实验海洋生物学重点实验室, 山东 青岛 266071; 2. 中国科学院大学, 北京 100049)
从采自海南东寨港的红树林卤蕨(Linn)中分离得到的一株内生真菌MA-318, 对其次级代谢产物进行了研究。利用反相硅胶柱层析、正相硅胶柱层析以及葡聚糖凝胶Sephadex LH-20柱层析等分离手段获得一个单体化合物。通过波谱数据分析(HRESIMS、1D NMR、2D NMR)鉴定该化合物为新的链烯酸酐, 其结构为methyl ()-3-(4-(2-((4-(but-1-en-1-yl)-2,5- dioxo-2,5-dihydrofuran-3-yl)methyl)butyl)-2,5-dioxo-2, 5-dihydrofuran-3-yl)propanoate, 命名为methylate cordyanhydride A。抗菌实验表明该化合物对藤黄微球菌()表现出一定的抑制作用。
红树林; 内生真菌; 化学成分; 结构鉴定; 抗菌活性
天然产物是药物研发先导化合物的重要来源[1]。其中, 来自特殊生态位的微生物, 例如海洋内生共生体, 为了适应海洋生态系统的特殊生活环境(高盐、高压、低氧、低光、营养限制等)[2], 在长期进化刚才中形成了独特的生物代谢途径, 能够产生许多结构新颖、具有良好生物活性的天然产物[3]。近年来我们系统开展了海洋生物天然产物研究, 发现、报道了一系列分子多样性丰富的海洋天然产物, 若干化合物具有显著的抗肿瘤、抗菌活性[4-6]。
本文报道从红树林植物卤蕨(Linn)中分离得到的一株内生真菌MA-318的化学成分研究。从该菌发酵产物中分离得到一个新的链烯酸酐类成分, 通过波谱数据分析鉴定其结构为methyl ()-3-(4-(2-((4-(but- 1-en-1-yl)-2,5-dioxo-2,5-dihydrofuran-3-yl)methyl)butyl)- 2,5-dioxo-2,5-dihydrofuran-3-yl)propanoate, 命名为methyate cordyanhydride A, 在其长直链上含有2个顺丁烯二酸酐结构单元(图1)。

图1 化合物1的结构
1 材料与方法
1.1 仪器与试剂
核磁共振图谱由Bruker Avance 500核磁共振仪测定, TMS为内标; 质谱数据由API QSTAR Pulsar 1质谱仪测定; 薄层色谱硅胶GF254和柱色谱硅胶(200~ 300目)为青岛海洋化工厂分厂产品; Lobar LiChroprep RP-18硅胶 (40~63 μm, Merck); 显色剂为茴香醛硫酸溶液; 所用有机溶剂为重蒸的工业级溶剂。
1.2 菌株发酵
(1) 菌株: 菌株MA-318分离自2015年3月采集自海南东寨港的卤蕨(Linn)。通过形态学观察与ITS序列系统发育分析[7], 将该菌株鉴定为。
(2) 菌株发酵: 菌种于–80℃以20% 甘油-水保存。发酵采用改良PDB培养基, 组成为: 蔗糖6.0 g, 甘露醇6.0 g, 蛋白胨1.5 g, 酵母浸粉0.9 g, 含20%土豆汁的纯海水300 mL。
采用1 L三角瓶发酵培养, 每瓶装液体培养基300 mL, 于116℃灭菌30 min后接种。共接种液体培养基18 L, 于28℃恒温、自然光条件下培养30 d, 分别收集菌丝体和发酵液。
1.3 提取分离
收集发酵液约18 L, 用乙酸乙酯萃取。菌丝体晾干、粉碎后用丙酮︰水(4︰1)浸泡。将丙酮蒸出, 水相用乙酸乙酯萃取, 萃取物经薄层层析检测发现与发酵液萃取物一致, 合并得粗提物39.7 g。
将上述粗提物进行硅胶柱层析, 以石油醚-乙酸乙酯、氯仿-甲醇体系梯度洗脱, 经TLC检测合并为9个组分(Fr.1-9)。其中组分Fr.5经反相硅胶柱层析(甲醇—水从10︰90到90︰10梯度洗脱)、Sephadex LH-20凝胶柱层析(甲醇)及正相硅胶柱层析(石油醚/乙酸乙酯20/1到5/1梯度洗脱)分离得到化合物1(20.9 mg)。
1.4 抑菌活性MIC测试
(1) 病原指示菌: 抗菌活性所使用的病原指示菌包括大肠杆菌(), 藤黄微球菌(), 铜绿假单胞菌(), 迟缓爱德华氏菌(), 副溶血性弧菌()和哈氏弧菌(), 以上所有供试菌株均来自于中国科学院海洋研究所。
(2) 指示菌菌悬液制备: 将接种于LB培养基表面的指示菌于37℃培养24 h后, 吸取2 mL无菌0.85% NaCl溶液洗涤培养物, 并用刮刀将菌刮下。吸取适量菌悬液于无菌试管中, 然后用0.85% NaCl溶液将菌悬液调至0.5麦氏浊度(相当于1.5×108CFU/mL),备用。
(3) 抑菌活性MIC测试: 采用微量肉汤稀释法[8], 测定化合物的抗菌活性。采用无菌操作, 以氯霉素为阳性对照, 将梯度稀释后不同浓度的样品溶液分别加到无菌的96孔聚苯乙烯板中(每孔5 μL)。然后取95 μL麦氏浊度为0.5的指示菌悬液, 依次加入到96孔板中。轻轻震荡后, 将96孔板置于37℃培养箱中, 培养24 h, 在600 nm波长下使用酶标仪测定每孔的吸光值, 以完全抑制指示菌生长的最低样品浓度为该化合物的MIC值。
2 化合物的结构鉴定
3 化合物的抗菌活性
化合物1是已知化合物cordyanhydride A的甲酯化产物[9], 迄今为止未见该类化合物的活性报道。我们对分离得到的化合物1进行了抗菌活性测试, 受试菌包括大肠杆菌(), 藤黄微球菌(), 铜绿假单胞菌(), 迟缓爱德华氏菌(), 副溶血性弧菌()和哈氏弧菌()。测试结果表明化合物1对藤黄微球菌表现出一定的抑制活性, 其MIC值为16 μg/mL(阳性对照氯霉素的MIC值为4 μg/mL)。
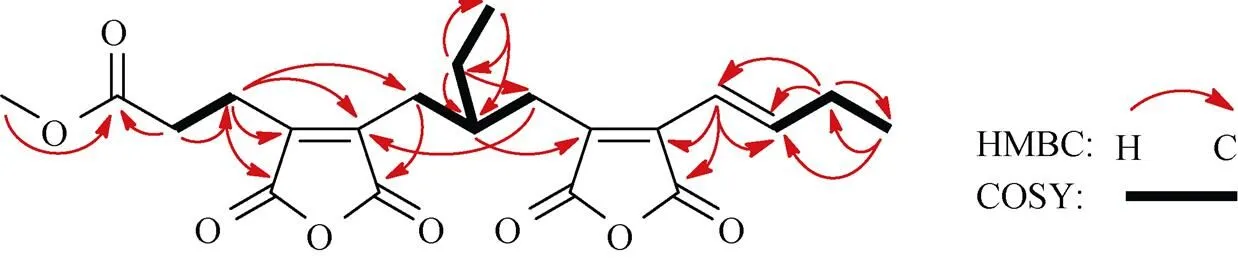
图2 化合物1的HMBC以及1H-1HCOSY相关
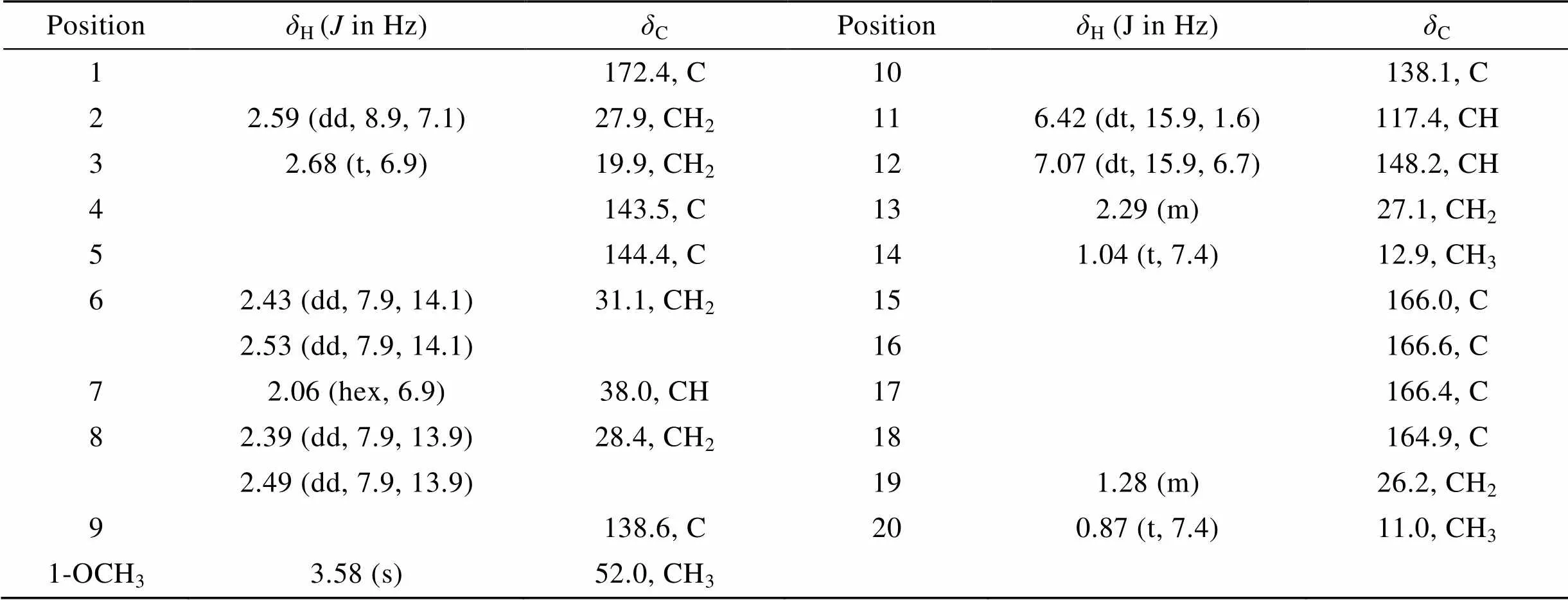
表1 化合物1的1H-(500 MHz)和13C-NMR(125 MHz)数据(DMSO-d6)
[1] Kaobayashi J. Search for new bioactive marine natural products and application to drug development[J]. Chem Pharm Bull, 2016, 64: 1079-1083.
[2] Song Y X, Qiao L T, Wang J J, et al. Two new meroterpenes from the mangrove endophytic fungussp. 085241B[J]. Helv Chim Acta, 2011, 94: 1875- 1880.
[3] Blunt J W, Copp B R, Keyzers R A, et al. Marine natural products[J]. Nat Prod Rep, 2015, 32: 116-211.
[4] Meng L H, Wang C Y, Mándi A, et al.Three diketopiperazine alkaloids with spirocyclic skeletons and one bisthiodiketopiperazine derivative from the mangrove-derived endophytic fungusMA-231[J]. Org Lett , 2016, 18: 5304-5307.
Liu H, Li X M, Liu Y, et al, Chermesins A−D: meroterpenoids with a drimane-type spirosesquiterpene skeleton from the marine algal-derived endophytic fungusEN-480[J]. J Nat Prod, 2016, 79: 806-811.
[5] Li X D, Li X M, Li X, et al. Aspewentins D−H, 20-nor- isopimarane derivatives from the deep sea sediment- derived fungusSD-310[J]. J Nat Prod,2016, 79: 1347-1353.
[6] Wang S, Li X M, Teuscher F, et al. Chaetopyranin, a benzaldehyde derivative and other related metabolites from, an endophytic fungus derived from marine red alga[J]. J Nat Prod, 2016, 69: 1622-1625.
[7] 孙好芬. 两株热带马尾藻内生真菌次生代谢产物研究[D]. 青岛: 中国科学院海洋研究所, 2010.Sun Haofen. Study on secondary metabolites of two endophytic fungal strains from tropicalspecies[D]. Qingdao: Institute of Oceanology, Chinese Academy of Sciences, 2010
[8] Isaka M, Tanticharoen M, Thebtaranonth Y. Cordyanhydrides A and B, two unique anhydrides from the insect pathogenic fungusBCC 1620[J]. Tetrahedron Lett, 2000, 41: 1657-1660.
(本文编辑: 康亦兼)
Methylate cordyanhydride A, a new alkenoic anhydride fromMA-318, an endophytic fungus derived from the marine mangrove plant
LI Yan-he1, 2, LI Xiao-ming1, XU Rui1, 2, LI Hong-lei1, 2, WANG Bin-gui1
(1. Key Laboratory of Experimental Marine Biology, Institute of Oceanology, Chinese Academy of Sciences, Qingdao 266071, China; 2. University of the Chinese Academy of Sciences, Beijing 100049, China)
The biochemical investigation ofMA-318, an endophytic fungus isolated from the mangrove plantLinn, resulted in the identification of a new alkenoic anhydride, methylate cordyanhydride A. Spectroscopic methods were used to elucidate the structure of this compound. Regarding the antimicrobial activity, this compound was found to possess moderate activity against, with an MIC value of 16 μg/mL.
Mangrove; endophytic fungus; chemical constituents; structure elucidation; antimicrobial activity
Mar. 7, 2017
李衍荷(1992-), 女, 山东青岛人, 硕士研究生, 主要从事天然产物化学研究; 王斌贵,
, 电话: 0532-82898553, E-mail: wangbg@ms.qdio.ac.cn
O629
A
1000-3096(2017)09-0110-04
10.11759/hykx20170307003
2017-03-07;
2017-04-24
国家自然科学基金项目(31570356)
[National Natural Science Foundation of China, No.31570356]
