1 883例住院药疹患者致敏药物分析
2017-03-22杨凡萍陈圣安朱沁媛吴晓瑾熊浩陈姿桦郜旭东骆肖群
杨凡萍陈圣安朱沁媛吴晓瑾熊 浩陈姿桦郜旭东骆肖群
(复旦大学附属华山医院皮肤科,上海200040)
皮肤药物不良反应 (cutaneous adverse drug reactions,cADRs)即药疹 (drug eruptions),是在疾病的预防、诊治或功能恢复期,药物通过注射、内服、吸入等途径进入人体后引起的皮肤、黏膜反应。药疹的发病率约1%~3%[1-2]。依据发病的严重程度,药疹可分为普通药疹 (ordinary drug eruptions)和重症药疹 (severe cutaneous adverse drug reactions,SCARs),前者包括斑丘疹型 (maculopapular exanthems,MPE)、荨麻疹型 (urticaria)、固定型 (fixed drug eruption,FDE)、红皮病型、紫癜型等,其中MPE主要包括麻疹型和猩红热型药疹。SCARs包括Stevens-Johnson综合征 (Stevens-Johnson syndrome,SJS)、中毒性表皮坏死松解症 (toxic epidermal necrolysis,TEN)、SJS-TEN重叠 (SJS-TEN overlap)、药物反应伴嗜酸性粒细胞增多和系统症状 (drug reactions with eosinophilia and systemic symptoms,DRESS)或称药物超敏反应综合征(drug induced hypersensitivity,DIHS)及急性泛发性发疹性脓疱病 (acute generalized exanthematous pustulosis,AGEP)[2-3]。
临床所见的药疹大多不可预测,部分类型预后较差。药疹的发生不仅使患者临床原发病的治疗受到影响,更给患者家庭及社会带来巨大身心伤害和经济损失。目前普遍认为早期识别及停用致敏药物是药疹治疗中最关键的一步[4]。临床上对药疹致敏药物的识别直接决定了能否有效停用药物,前者主要依靠病史分析、体外试验、体内试验和口服药物激发试验[5-7]。体外试验由于受到样本、药物、试验方案的影响,其诊断价值不能确定[6]。研究发现,体内试验 (主要包括皮肤试验和斑贴试验)的敏感度和特异度有限[5]。口服药物的体内激发试验为确定致敏药物的金标准,但由于其可导致严重的不良反应使得在临床上的应用受到限制[7]。本研究对大样本药疹患者病史进行回顾性统计分析,研究结果将为临床对药疹致敏药物的判断及药疹患者的诊断、治疗及后续用药指导提供参考。
对象与方法
研究对象
收集2007年1月1日至2016年12月31日因药疹于华山医院皮肤科住院且出院时明确诊断为药疹的患者。具体纳入标准: (1)入院初步诊断为药疹,入院后由主治医师和主任医师查房,实验室和临床检查 (包括病理、病毒血清学检查等)排除病毒疹等其他疾病;(2)在药疹的发病潜伏期内有可疑用药史。药疹不同疹型的诊断及分类标准依据文献[2-3]。本研究通过复旦大学伦理委员会批准。
患者符合上述药疹的诊断,则对其进行临床资料的收集及致敏药物和可疑致敏药物的判断:患者在发疹前潜伏期内仅使用过1种药物,则认为该药物为本次药疹的致敏药物,本次药疹为单药过敏 (其中如患者的致敏药物为1帖或1味中药或1种中成药 (traditional Chinesemedicine,TCM)亦将其归类为单药过敏);患者在发疹前潜伏期内使用2种及以上药物,则认为这些药物均为本次药疹的可疑致敏药物,本次药疹为混合药物过敏。药疹的潜伏期定义为患者发病前第一次接触致敏药物至发病的时间。
统计学处理
数据分析应用SPSS 16.0(SPSS Inc.,Chicago,IL,USA)统计软件及Microsoft Office EXCEL 2010进行处理。连续变量的描述使用均数±标准差 (±s)。两组之间的统计学分析使用t检验,两组以上的组间统计分析使用单因素方差分析 (ANOVA),两两比较使用Bonferroni校正。分类变量以百分比表示,组间统计学差异采用卡方检验。P<0.05为差异有统计学意义。
结 果
基本资料
本研究收集住院药疹患者共1 883例,其中男性652例 (34.63%),女性1 231例 (65.37%),男女比例为0.53∶1。各年住院药疹中,女性患者数均多于男性,女性患者数占相应年份总住院药疹的比例在58.46%~72.17%(表1)。药疹患者的平均年龄为(44.60±16.90)岁 (9~88岁)。重症药疹患者的平均年龄为 (47.51±18.70)岁 (15~88岁)。普通型药疹患者的平均年龄为 (43.78±16.26)岁 (9~84岁)。重症药疹患者的平均发病年龄大于普通型药疹(P<0.000 1)。根据年龄将所有药疹患者分为9~30岁组、31~50岁组、51~70岁组及≥71岁组:10年间51~70岁组的患者数最多,占药疹总数的33.46%(图1);前5年间 (2007至2011年),31~50岁的药疹患者数最多 (32.75%,283/864),51~70岁其次(32.06%,277/864);后5年间 (2012至2016年),51~70岁居多 (35.03%,357/1 019),31~50岁次之 (32.38%,330/1 019)。
药疹潜伏期
1 603例患者的患病潜伏期明确,平均为 (11.81±12.02)d(2 min至 90 d)。不同的药疹疹型中,DRESS潜伏期最长,之后依次为红皮病型、紫癜型、SJS/TEN、AGEP、多形红斑型、MPE、荨麻疹型及固定型 (表2);DRESS的潜伏期较其他疹型长 (均P<0.05)。荨麻疹型潜伏期较DRESS、红皮病型及SJS/TEN短 (均P<0.05)。不同药物所致药疹中,降尿酸药 (别嘌呤醇)所致药疹的潜伏期最长,之后依次为改善病情抗风湿药disease-modifying antirheumatic drugs,DMARDs) (以柳氮磺胺吡啶为主)、抗癫痫药、TCM、抗生素、解热镇痛药 (表3)。
药疹疹型构成
住院药疹中荨麻疹型药疹所占比例最高,之后依次为MPE、多形红斑型、SJS、DRESS、TEN、红皮病型、紫癜型 (图 2)。重症药疹占总药疹数的21.99%(414/1 883)。
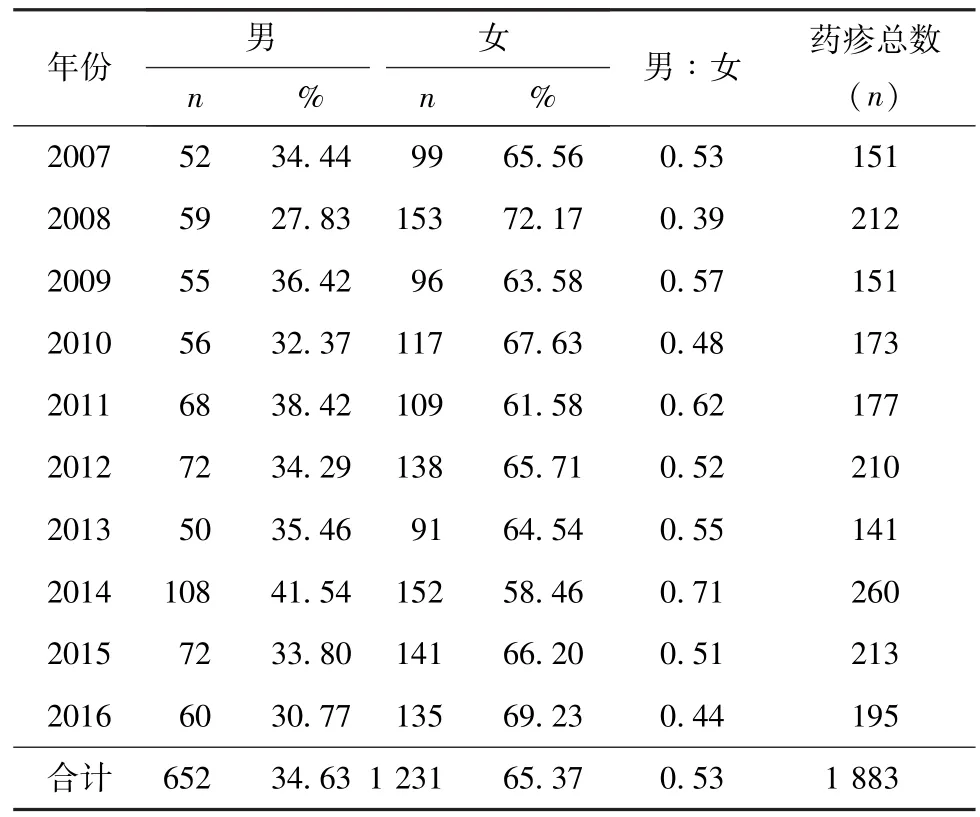
表1 2007至2016年1 883例药疹患者的性别构成Table 1 Gender composition of 1 883 patients with drug eruptions from 2007 to 2016

图1 2007至2016年1 883例药疹患者的年龄构成Fig 1 Age composition of 1 883 patients with drug eruptions from 2007 to 2016

表2 不同疹型药疹的潜伏期Table 2 Latency period of drug eruptions with different types(d)

表3 不同药物所致药疹的潜伏期Table 3 Latency period of drug eruptions with different causative drugs(d)

图2 2007至2016年1 883例住院药疹患者疹型构成Fig 2 Type of 1 883 drug eruptions from 2007 to 2016 MPE:斑丘疹型,包括猩红热型及麻疹型;EM:多形红斑;SJS:Stevens-Johnson综合征;DRESS:药物反应伴嗜酸性粒细胞增多和系统症状;TEN:中毒性表皮坏死松解症;AGEP:急性泛发性发疹性脓疱病
致敏药物谱
45.83% (863/1 883)为单药致敏,53.43%(1 006/1 883)为混合致敏;0.74%(14/1 883)致敏药物不详,即发疹前药疹潜伏期内患者有明确的服药史,但具体服药的种类不能回忆。
863例单药致敏中,331例为男性,占单药致敏的38.35%;重症药疹213例,占单药致敏的24.68%。单药致敏前5类最常见药物依次为抗生素、TCM、抗癫痫药、降尿酸药、解热镇痛药 (表4)。单药致敏重症药疹前5类最常见致敏药物依次为抗癫痫药、降尿酸药、抗生素、TCM、解热镇痛药 (表5)。单药致敏的650例普通药疹中前5类最常见药物依次为抗生素、TCM、解热镇痛药、破伤风抗毒素(TAT)、降尿酸药 (表6)。
抗生素为最常见的致敏药物种类。由抗生素所致的药疹以普通药疹为主 (93.17%,232/249)。最常引起药疹的抗生素依次为头孢菌素类 (10.08%,87/863)、青霉素类 (7.88%,68/863)、抗厌氧菌类 (3.13%,27/863)、喹诺酮类 (2.20%,19/863)、克林霉素及林可霉素类 (1.62%,14/863)、大环内酯类 (1.51%,13/863)等。引起重症药疹的抗生素以头孢菌素为主(76.47%,13/17)。
TCM(以丹参酮及血塞通为主)为药疹的第二常见致敏药物,由其所致的药疹以普通型为主(91.30%,126/138)。
抗癫痫药 (以卡马西平为主)为药疹的第三常见致敏药物。卡马西平也是重症药疹最为常见的致敏药物,由卡马西平所致的重症药疹占总重症药疹的31.46%(67/213),其中SJS最多 (80.60%,54/67),其次为TEN(16.42%,11/67)和DRESS(2.99%,2/67)。

表4 863例单药药疹致敏药物Table 4 The causative drug of 863 patientswith single drug induced drug eruptions

表5 单药所致重症药疹的致敏药物谱Table 5 The causative drug of single drug induced severe drug eruptions
降尿酸药 (别嘌呤醇)为重症药疹的第二大致敏药物 (31.46%,67/213)。由别嘌呤醇所致的药疹中,DRESS与SJS相当 (均为43.28%,29/67),其次为SJS-TEN重叠 (7.46%,5/67)和TEN(5.97%,4/67)。
单药所致药疹致敏药物谱变化
前5年间 (2007至2011年)华山医院住院单药所致药疹共396例,后5年间 (2012至2016年)共467例 (表7)。前5年间与后5年间的前7位常见单药致敏药物相同,依次为抗生素、TCM、抗癫痫药、降尿酸药、解热镇痛药、TAT及其他,其中除抗生素的致敏例数后5年间较前5年间有所下降外,其余药物所致药疹的例数均较前增加。另外,DMARDs(以柳氮磺胺吡啶为主)所致的药疹病例数在后5年间有所增加。
混合致敏的可疑致敏药物
67.59%(680/1 006)混合用药患者的可疑致敏药物包含抗生素,其中36.18%(364/1 006)包含1种抗生素,31.41% (316/1 006)包含≥2种抗生素。37.97%(382/1 006)可疑致敏药物包含1帖或1味中药或1种中成药。32.11%(323/1 006)可疑致敏药物同时含有中药或中成药和其他药物,其中16.50%(166/1 006)为中药或中成药与解热镇痛药合用,15.61%(157/1 006)为中药或中成药与抗生素合用。30.42%(306/1 006)可疑致敏药物包含解热镇痛药。

表6 单药所致普通药疹的致敏药物谱Table 6 The causative drug of single drug induced ordinary drug eruptions

表7 前5年间 (2007至2011年)与后5年间(2012至2016年)单药致敏药物谱变化Table 7 Comparison of causative drugs during 2007-2011 and 2012-2016
药疹常见疹型致敏药物
荨麻疹型药疹的常见致敏药物为抗生素、TAT、TCM、解热镇痛药等;MPE的常见致敏药物为抗生素、TCM、降尿酸药、解热镇痛药等;多形红斑型药疹的常见致敏药物为抗生素、TCM、抗癫痫药、解热镇痛药等;SJS的常见致敏药物为抗癫痫药、降尿酸药、解热镇痛药、抗生素等;TEN的常见致敏药物为抗癫痫药、降尿酸药、降眼压药、抗生素等;SJS-TEN的常见致敏药物为降尿酸药和抗癫痫药;DRESS的常见致敏药物为降尿酸药、DMARDs、抗癫痫药等 (表8)。
讨 论
本研究发现女性药疹患者较男性多,这与以往的研究[8-10]结果相似。造成这种差异的具体原因目前尚不清楚。有学者推测可能与男性与女性具有不同的药物代谢过程、免疫及性激素有关[8]。本研究中药疹的发病年龄 (44.60±16.90)岁,与2004至2008年本科及其他国家的研究结果接近;重症药疹的发病年龄大于普通药疹[11-13]。根据年龄将所有药疹患者分为9~30岁组、31~50岁组、51~70岁组及≥71岁组,可见在研究的10年间,药疹的发病年龄从前5年间的31~50岁青中年为主转换为后5年间的51~70岁中老年人为主。社会的老龄化使得老年人发病增多,病增多,使用药物多、药物代谢减慢、药物之间的相互作用复杂是药疹更易发生于中老年人的重要原因[14-16]。

表8 常见疹型药疹的致敏药物谱Table 8 The causative drug of some common drug eruption types
本研究结果发现抗生素为单一致敏药疹及单一致敏普通药疹中最常见的致敏药物种类,致敏抗生素以头孢菌素和青霉素为主,与既往研究结果[9,10,13]相符;抗生素也是混合致敏药物药疹中最常见的可疑致敏药物种类。抗生素药疹如此之多在很大程度上与其广泛使用相关:Yin等[17]对2000至2012年中国医院门诊处方进行系统分析得出,74.0%的处方中包含1种抗生素。青霉素和头孢菌素因化学结构中均含有β-内酰胺环而被归类于β-内酰胺类抗生素。由β-内酰胺类抗生素所致药疹的发病机制不清。有学者提出小分子β-内酰胺类抗生素作为半抗原与体内自身肽链结合形成新的完全抗原,后者可通过被体内抗原提呈细胞所识别后经处理激活特异性免疫应答或直接激活特异性免疫应答[18]。
TCM是我国传统药物的总称,凡是以中医传统理论为指导,进行采收、加工、炮制、制剂以利于临床应用的药物都称为TCM[19]。中成药为以中草药为原料,经制剂加工制成各种不同剂型的中药制品,包括丸、散、膏、丹等剂型[19]。据统计,2014年在中国有超过7亿人使用TCM,全世界有超过170个国家和地区在使用TCM[20]。本研究发现,TCM所致药疹的比例较以往研究[10,13]高;TCM所致药疹以普通型为主,但也有重症药疹 (12例);32.11%的混合用药药疹的致敏药物含有TCM。TCM所致药疹的发生有逐渐增多的趋势:Wang等[9]发现2003至2010年较1984至1994年TCM药疹发生率从10%增至26%;本研究发现2007至2011年较2012至2016华山医院TCM药疹发生率从14%增至17%。对TCM的不合理使用、药物原材料的生长环境改变等可能是TCM更易诱发药物不良反应的主要因素[21-22]。药疹的致敏中成药以丹参酮及血塞通为多,而丹参酮、血塞通所致药疹的报道仅限于中国[23-28]。TCM的成分较为复杂,引起药疹的具体成分难以确定,给药疹发病机制的研究造成了一定困难。
综上所述,本研究对华山医院住院药疹的临床资料进行回顾性分析发现:抗生素、TCM为药疹最多见的两类致敏药物。TCM的使用范围广、人数多,由其导致的药疹近年来有增多趋势,临床医师在使用时需警惕并预防其相关不良反应的发生。
[1]Lazarou J,Pomeranz BH,Corey PN.Incidence of adverse drug reactions in hospitalized patients:ameta-analysis of prospective studies[J].JAMA,1998,279:1200-1205.
[2]Roujeau JC.Clinical heterogeneity of drug hypersensitivity[J].Toxicology,2005,209:123-129.
[3]Bastuji-Garin S,Rzany B,Stern RS,et al.Clinical classification of cases of toxic epidermal necrolysis,Stevens-Johnson syndrome,and erythemamultiforme[J].Arch Dermatol,1993,129:92-96.
[4]Hoetzenecker W,Nägeli M,Mehra ET,et al.Adverse cutaneous drug eruptions:current understanding[J].Semin Immunopathol,2016,38:75-86.
[5]Viola M,Quaratino D,Gaeta F,etal.Allergic reactions to antibiotics,mainly betalactams:facts and controversies[J].Eur Ann Allergy Clin Immunol,2005,37:223-229.
[6]Polak ME,Belgi G,McGuire C,et al.In vitro diagnostic assays are effective during the acute phase of delayed-type drug hypersensitivity reactions[J].Br J Dermatol,2013,168:539-549.
[7]Davidovici BB,Wolf R.The challenge of drug-rechallenge:Facts and controversies[J].Clin Dermatol,2010,28:349-353.
[8]Chopra D,Sharma V,Kapoor R,etal.An observational study of cutaneous adverse drug reactions in a teaching hospital[J].Int JClin Pharm,2015,37:996-999.
[9]Wang F,Li Y,Mo Y,etal.Cutaneous adverse drug reactions:an 8-year retrospective study on hospitalized patients in Southern China[J].Indian J Dermatol Venereol Leprol,2012,78:488-490.
[10]Carneiro SC,Azevedo-e-Silva MC,Ramos-e-Silva M.Drug eruptions in the elderly[J].Clin Dermatol,2011,29:43-48.
[11]Rademaker M.Do women have more adverse drug reactions?[J].Am JClin Dermatol,2001,2:349-351.
[12]Turk BG,Gunaydin A,Ertam I,et al.Adverse cutaneous drug reactions among hospitalized patients:five year surveillance[J].Cutan Ocul Toxicol,2013,32:41-45.
[13]Choon SE,Lai NM.An epidemiological and clinical analysis of cutaneous adverse drug reactions seen in a tertiary hospital in Johor,Malaysia[J].Indian JDermatol Venereol Leprol,2012,78:734-739.
[14]Heng YK,Lim YL.Cutaneous adverse drug reactions in the elderly[J].Curr Opin Allergy Clin Immunol,2015,15:300-307.
[15]Martin RM,Biswas PN,Freemantle SN,et al.Age and sex distribution of suspected adverse drug reactions to newly marketed drugs in general practice in England:analysis of 48 cohort studies[J].Br JClin Pharmacol,1998,46:505-511.
[16]Huang HY,Luo XQ,Chan LS,et al.Cutaneous adverse drug reactions in a hospital-based Chinese population[J].Clin Exp Dermatol,2011,36:135-141.
[17]Yin X,Song F,Gong Y,et al.A systematic review of antibiotic utilization in China[J].J Antimicrob Chemother,2013,68:2445-2452.
[18]Hertl M,Geisel J,Boecker C,et al.Selective generation of CD8+T-cell clones from the peripheral blood of patients with cutaneous reactions to beta-lactam antibiotics[J].Br JDermatol,1993,128:619-626.
[19]Chan K.Chinesemedicinalmaterials and their interface with Western medical concepts[J].JEthnopharmacol,2005,96:1-18.
[20]Dang H,Wang Q,Wang H,et al.The Integration of Chinese Material Medica into the Chinese Health Care Delivery System,an Update[J].Phytother Res,2016,30:292-297.
[21]Shaw D,Graeme L,Pierre D,et al.Pharmacovigilance of herbalmedicine[J].JEthnopharmacol,2012,140:513-518.
[22]Zhang L,Yan J,Liu X,et al.Pharmacovigilance practice and risk control of Traditional Chinese Medicine drugs in China:current status and future perspective[J].JEthnopharmacol,2012,140:519-525.
[23]蔡翠君,陈倩,罗建华.血塞通注射液致麻疹样药疹2例 [J].临床医药杂志,2004,17:35.
[24]简华慧,韦秀玲.血塞通致药物性皮炎19例报告[J].右江民族医学院学报,2005,27:710.
[25]路庆丽,李文政,普雄明.血塞通致药疹8例临床分析 [J].甘肃医药,2013,32:694-695.
[26]吕香花,许经纶,蒋亦秀.丹参酮胶囊致多形红斑型药疹12例 [J].浙江中西医结合杂志,2014,24:169-170.
[27]袁定芬,白梅.丹参酮胶囊致多形红斑型药疹10例[J].实用医学杂志,2011,27:2689.
[28]张江霞.大疱性表皮坏死松解型药疹1例分析 [J].中国医药指南,2016,14:201.
