以帕金森综合征为主要表现的麻痹性痴呆1例并文献复习
2017-03-16付希英张耀文马倩倩
赵 兴, 付希英, 张耀文, 马倩倩, 李 鸣, 杨 薇
以帕金森综合征为主要表现的麻痹性痴呆1例并文献复习
赵 兴1, 付希英2, 张耀文1, 马倩倩1, 李 鸣1, 杨 薇1
麻痹性痴呆(general paresis of insane,GPI)是晚期神经梅毒最严重的类型之一,极易误诊及漏诊。其中以帕金森综合征为主要表现的病例少见,合并有癫痫发作的病例更加罕见。现将我科1例既往多次误诊为帕金森综合征,同时在入院治疗过程中伴有癫痫发作的GPI病例报道如下。
1 病例摘要
患者,男,59 y,司机。因“双手抖动伴言语笨拙渐重12 m,加重伴行为异常1 d”于2015年12月17日入院。患者于入院前12 m无明显诱因出现双手不自主抖动,以左侧为著。11 m前出现言语笨拙症状,就医后考虑“帕金森病”,药物治疗后上述症状渐进性加重。3 m前就诊于北京301医院,行头部MRI及PET/CT等相关辅助检查,结果示未见明显异常,给与口服“茴拉西坦”等药物治疗,言语笨拙症状较前略有好转,但开始出现行为异常。双手抖动症状较前未见明显好转。1 m前,右下肢活动不灵发作一次,给与改善循环等药物治疗,后未再发作。15 d前,出现无故发笑症状,出汗较前增多,伴步态异常,表现为躯干前倾、难以停止。同时出现睡眠变差。1 d前,上述精神行为异常症状突然加重,表现为无故使用电工刀刮手机,眼神散漫,不能认识家属,并全身屈曲跪于床上,患者发现家属后即藏于床下,持续时间约3 h好转,好转后不能回忆发病过程。入我院急诊后行头部核磁DWI检查过程中言语笨拙逐渐加重至言语不能,伴尿失禁,恶心、呕吐两次,呕吐物为胃内容物。病程中偶有饮水呛咳、吞咽困难,无发热,无特殊药物、毒物接触史。既往胃溃疡、糖尿病、乙型肝炎病史,否认冶游史。入院查体:意识朦胧,言语不能,查体欠配合。记忆力、计算力、定向力不能配合。双侧瞳孔等大等圆,直径约3.0 mm,对光反射迟钝,双眼向各方向活动灵活,无眼震,左侧口角可见不自主抽动,频率约1~2次/s,示齿口角略向左侧歪斜,左上肢肌张力呈“齿轮样强直”,左下肢肌张力增高,左手可见规律对指动作,约2~3 s/次,右上肢偶可见摸索动作,双下肢可支离床面,双侧病理征未引出。头部核磁检查DWI未见明显高信号。初步诊断:癫痫(待诊)、帕金森综合征。该患者病史复杂,病因不明。生化、凝血及其他血液检查未见明显异常。脑电图结果(见图2、图3);梅毒抗体检查(TP)11.631(参考值:0~1)。
入院后第2天出现抽搐范围较前增大,表现为左侧颜面部及口角抽动,左上肢抽动,根据脑电图检查结果考虑为癫痫发作,给与地西泮、苯巴比妥对症处理,并给予卡马西平0.1 g,TID口服预防发作。进一步查梅毒血清学试验(RPR+TP):梅毒抗体检查(TP)11.958(参考值:0~1),稀释32倍阳性,稀释64倍弱阳性。腰穿脑脊液初压120 mmH2O, RPR+TP:[TP:10.994(参考值:0~1),RPR原倍弱阳性];常规、生化回报均处于正常值范围之内。根据ICD-10神经梅毒的诊断标准,更改临床诊断为“神经梅毒、麻痹性痴呆、帕金森综合征、癫痫”。该患者青霉素G、头孢唑肟、哌拉西林他唑巴坦均试敏阳性,给与多西环素口服,150 mg,q12 h,症状好转后出院,共住院13 d。出院时查体:意识清楚,言语含糊,可交流,反应迟钝,近记忆减退,远记忆未见明显异常,概测定向力、计算力差,双侧瞳孔等大等圆,直径约3.0 mm,对光反射迟钝,无眼震,双眼向各方面活动灵活,伸舌居中,示齿口角略向左侧歪斜,左上肢肌张力呈“齿轮样强直”,左下肢肌张力增高,四肢肌力正常,双侧病理征未引出。
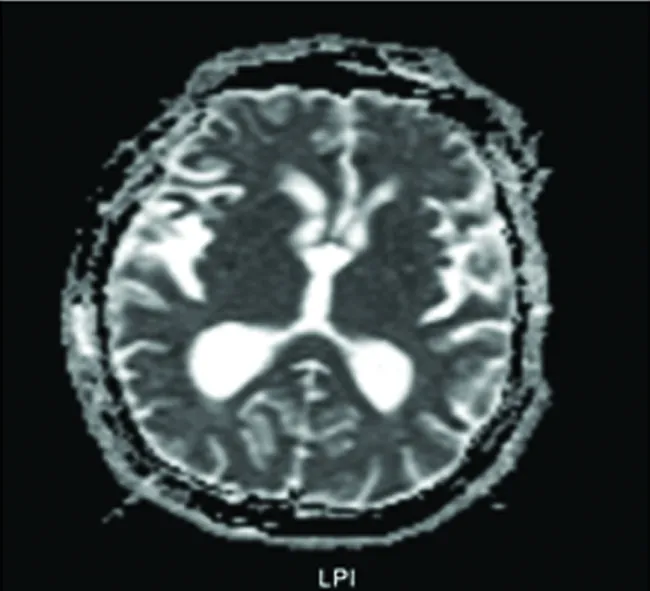
图1 侧脑室扩大,额叶、颞叶皮质萎缩明显

图2、图3 基本节律消失,各导联普遍呈中至高波幅3~4波/秒慢波活动,左侧高于右侧。快波:前部导联偶见低波幅20~24波/秒的β波(因患者不自主抖动,干扰波较多)
2 讨 论
GPI属实质性神经梅毒,是晚期梅毒全身性损害的重要表现,由梅毒螺旋体直接侵犯脑组织所致,痴呆是最常见的症状,常伴有精神行为异常。病理改变以脑实质损害为主,常累及额叶、颞叶、顶叶。早期症状以抑郁、失眠为主;中期表现为记忆力及智力障碍;晚期可出现癫痫发作、双下肢痉挛性瘫痪。目前GPI诊断尚无金标准,国内有学者统计其误诊率高达34.9%[1]。瞳孔变化是GPI患者较为常见的早期症状,但典型的Argyll-Robertson瞳孔(阿罗氏瞳孔)并不常见,约60%的患者表现阳性[2]。GPI的MRI检查与脑实质损害密切相关,主要表现为弥漫性脑萎缩、双侧脑室呈对称性扩大等[3],该患者头部MRI亦提示弥漫性脑萎缩(见图1),但在许多变性疾病如Alzheimer病、Pick病、Korsakoff综合征、血管性痴呆、HIV脑病等多种疾病中可出现此种病理改变,故影像学检查缺乏特异性。不过该患者提示我们,当发现青壮年出现与年龄不相符的颞叶、海马萎缩时,应考虑到麻痹性痴呆的可能[4]。GPI的脑电图主要表现为广泛的低、中幅慢波,对诊断GPI意义也不大[5]。目前唯一可以作为确诊手段为脑组织活检,如活检发现梅毒螺旋体伴有特征性的杆状小胶质细胞增生便可以明确诊断,但作为有创检查,在临床工作中受到很大的限制。梅毒因其复杂且不典型的临床表现被称为“杰出的模仿者”(The Great Imitator),神经梅毒表现更是如此[6]。这也为临床工作的鉴别诊断提出了严峻的挑战。至今为止,临床上表现为锥体外系症状的神经梅毒极为少见,继发于神经梅毒的帕金森综合征的文献报道及相关研究也不多。神经梅毒引起继发性帕金森综合征的机制尚不明确,推测其机制可能和脑炎一样引起基底节功能紊乱:(1)小动脉炎血管闭塞导致基底节区缺血性坏死,引起多巴胺神经元及多巴胺受体减少;(2)皮质-基底节区通路的多巴胺传递或代谢障碍[7]。帕金森综合征是指除原发性帕金森病以外的各种原因引起的类似帕金森病表现的运动障碍。一般情况下,帕金森病对美多芭试验反应良好,而帕金森综合征则反应不良,该患者口服抗帕金森药物无效,支持帕金森综合征的诊断。经驱梅治疗后,患者认知及精神障碍好转,因而该患者的帕金森症状考虑是由于梅毒感染中枢神经系统所致。有文献统计,在继发性帕金森综合征中,神经梅毒所致仅占0.3%[8]。
国外文献报道约20%的麻痹性痴呆可合并癫痫发作[9]。其发病机制可能为:(1)长期的慢性炎症刺激导致神经元细胞变性、坏死,炎性细胞浸润、脑组织缺血缺氧、酸中毒使膜电位兴奋性增高,导致痫性发作;(2)慢性炎症累及脑膜和小动脉导致血管闭塞,侵犯脑实质使得脑皮质结构受损、萎缩,可能形成致痫灶,导致癫痫发生。治疗上仍主张首先病因治疗,兼顾对症。该患者经多西环素驱梅治疗,并加用卡马西平后未再出现发作症状,证实有效。1 y后随访发现,经系统驱梅治疗后,该患者未再出现帕金森症状及癫痫发作,病情得到控制,3种疾病共存的可能性不大[10]。
自从青霉素发明以后,一直为治疗GPI最有效的药物。该患者多种常规抗生素均试敏阳性。曾考虑给与阿奇霉素驱梅,但阿奇霉素在国人体内耐药率高达95%[11]。与多西环素相比,四环素有较高的胃肠道反应,故改为口服多西环素治疗,取得了一定的疗效。这提示我们面对严重青霉素类过敏反应的患者,似乎有了替代药物的存在,但整体大样本数据分析还有待进一步研究。GPI治疗效果取决于脑损害程度,经治疗后痴呆可明显改善,但其预后与开始治疗的时间早晚明显相关,1 y后随访患者,发现仅残存部分性格改变,提示我们早期干预治疗,获益将会更大。
3 展 望
由于梅毒再度在我国流行已20余年,近年来发病率呈逐年上升趋势,神经梅毒必然会有一个新的发病高峰,可以推测GPI的发病率也会呈上升趋势,同时随着我国社会老龄化进程的发展,其他病因引起的痴呆发病率也逐年上升,因此加强对GPI的认识,提高鉴别诊断水平具有十分重要的现实意义。GPI是一种可治的痴呆,及早的诊断及治疗,对其预后较好,如不治疗,生存期一般不超过3 y。本例患者病程已有1 y,由于未给予正确对症治疗以至患者病情加重。所以对临床表现为认知障碍、精神症状、锥体外系症状的患者,如不能用常见疾病解释时,尤其当青壮年患者出现上述表现且合并其他非原发性疾病表现时,在鉴别诊断中要警惕神经梅毒,尽早行梅毒特异性血清学检查,争取早期诊断、早期治疗以改善预后。这就为广大医务工作者详询患者病史尤其是冶游史提出了迫切的要求。
[1]吴世韬,张 涛,颜 艳.麻痹性痴呆临床特征与防治(附126例分析)[J].航空航天医学杂志,2009,20(10):18-20.
[2]叶冬青.皮肤病流行病学[M].2001.328-332.
[3] Wang X,Yang Y,Wang X,et al.MRI findings and early diagnosis of general pares of the insane[J].Neurological Research,2014,36(2):137-142.
[4]靳 彪,赵康仁,张渭芳,等.麻痹性痴呆的临床特征与诊断(附2例报告)[J].临床神经病学杂志,2007,20(4):307-308.
[5]Sinha S,Harish T,Taly A B,et al.Symptomatic seizures in neurosyphilis:an experience from a university hospital in south India[J].Seizure,2008,17(8):711-716.
[6]Liis S,Mark B,Pille T.Neurosyphilis as a great imitator:a case report:[J].BMC Research Notes,2016,9(1):372.
[7]Chen Y F,Tseng Y L,Lan M Y,et al.The relationship of leukoaraiosis and the clinical severity of vascular Parkinsonism[J].Journal of the Neurological Sciences,2014,346(1~2):255-259.
[8]Pineda DA,Buritica O,Sanchez JL,et al.Parkinsonian syndromes in Medellin (Colombia)[J].Revista De Neurologia,2000,31(10):936-943.
[9]Yao Y,Huang E,Xie B,et al.Neurosyphilis presenting with psychotic symptoms and status epilepticus[J].Neurological Sciences Official Journal of the Italian Neurological Society & of the Italian Society of Clinical Neurophysiology,2011,33(1):99-102.
[10]Shah BB,Anthony E,Lang MD FRCPC.Acquired neurosyphilis presenting as movement disorders[J].Movement Disorders,2012,27(6):690-695.
[11]Martin I E,Gu W,Yang Y,et al.Macrolide resistance and molecular types of Treponema pallidum causing primary syphilis in Shanghai,China[J].Clinical Infectious Diseases,2009,49(4):515-521.
1003-2754(2017)02-0171-02
R742.5
2016-12-10;
2017-01-28
(1.吉林大学第二医院神经内科,吉林 长春 130041;2.吉林大学第二医院内分泌科,吉林 长春 130041)
杨 薇,E-mail:wei88linda@yahoo.com
