番木瓜泛素活化酶基因CpUBA1的表达模式分析
2017-03-10决登伟桑雪莲刘丽琴石胜友
决登伟,桑雪莲,舒 波,刘丽琴,石胜友
(中国热带农业科学院南亚热带作物研究所/农业部热带果树生物学重点实验室,广东 湛江 524091)
番木瓜(Carica papayaL.)是一种重要的经济型水果,广泛种植于热带和亚热带地区。番木瓜的果实不仅具有丰富的营养成分,还有一定的药用价值[1-2]。FAO数据显示,2016年世界番木瓜总产量排在香蕉、柑橘、芒果和菠萝之后,居当年热带水果的第五位[3]。果实成熟是一个重要且复杂的过程,有关该过程的调控机制研究报道很多。按成熟机制不同,果实分为呼吸跃变型和非呼吸跃变型。其中,呼吸跃变型果实主要包括香蕉、梨、番木瓜、芒果和番茄等,该类型果实成熟过程中会伴随着呼吸作用及乙烯含量的大幅上升;非呼吸跃变型果实主要包括凤梨、杨桃和西瓜等,该类型果实成熟过程中不会出现呼吸作用的大幅变化,乙烯含量也维持在一个很低水平[4]。
蛋白质作为细胞内最重要的生物大分子,其合成及降解受到精确的时间及空间调节,并具有高度选择性。泛素-蛋白酶体途径(Ubiquitin-proteasome pathway,UPP)是细胞内蛋白质选择性降解的重要途径。泛素分子主要通过泛素活化酶(E1)、泛素结合酶(E2)和泛素-蛋白连接酶(E3)与靶蛋白结合形成一条多泛素链,将底物蛋白泛素化,使靶蛋白被26S蛋白酶所识别和降解,从而实现对多种代谢过程的调节[5]。泛素系统广泛存在于真核生物中,并且在维持细胞功能以及细胞周期的运转、抵御环境胁迫、胚胎发育、激素响应和衰老等方面发挥着重要作用[6-8]。拟南芥基因组估计有超过1 400个基因(约占总蛋白质数量的5%)编码蛋白泛素化系统的组分。而这其中,编码E1基因只有两个,其突变体是致死的。已报道的编码E2基因有37个,还有8个编码E2-like基因。而编码E3的基因超过1 300个,并决定泛素化底物的特异性[9]。
目前对泛素-蛋白酶体途径关键酶的研究主要集中在E2和E3上,对于E1的研究报道很少,且多集中在模式生物中。在酵母(Saccharomyces cerevisiae)[10-11]和拟南芥(Arabidopsis thaliane)[12-13]中都含有 2 个UBA基因;小麦(Triticum aestivum)中有3个UBA基因,其中UBA1和UBA2的同源性很高[14];Li等[15]和张妮等[16]分别在龙须菜(Gracilaria lemaneiformis)和香蕉(musa acuminata)中发现UBA基因的存在。对UBA的功能研究表明,UBA除了具有激活泛素分子的作用外,可能还参与植株对逆境胁迫响应[17]及果实的采后成熟过程[16]。前期研究中[18],我们对番木瓜的泛素结合酶(Ubiquitin-conjugating enzymes,E2s)家族基因进行了研究,34个CpUBCs中有15个基因在番木瓜果实成熟过程中呈上调或下调表达,说明这些CpUBCs可能参与了果实成熟发育过程。而关于UBA基因在该进程中的作用目前仍未知。
本研究采用生物信息法从番木瓜基因组中分析得到1条UBA基因序列,对该基因进行序列分析及进化分析,并利用荧光定量PCR技术探讨了该基因在番木瓜不同组织及果实成熟进程中的表达模式。研究结果将有助于更好了解UBA基因在果实发育和成熟过程中的作用,也为丰富UBA在不同作物中的功能研究提供一定的理论依据。
1 材料与方法
1.1 试验材料
供试番木瓜材料品种为“日升”,组织表达分析试验以其成年树的根、茎、叶、穗、雌花、雄花和果实为材料,果实成熟过程表达分析以幼果(immature green,IG)、绿熟果(mature green,MG)、转色果(breaker,Br)和黄熟果(mature fruit,MF)为材料,由中国热带农业科学院南亚热带作物研究所国家热带果树种质资源圃保存。
1.2 CpUBA1基因的获得及分析
根据已有报道[10-13],以拟南芥及酵母的UBA氨基酸序列在C. papayaGenomics Database(CpGDB; http://www.plantgdb.org/CpGDB/)中搜索番木瓜的UBA同源序列。CpUBA1基因的基本信息,如ORF、氨基酸长度和染色体定位等从Phytozome数据库获得;CpUBA1基因的外显子、内含子结构通过在线软件Gene Structure Display Server (GSDS) (http://gsds.cbi.pku.edu.cn/)分析获得。分别利用软件SMART (http://smart.emblheidelberg.de/)和 Plant-mPLoc(http://www.csbio.sjtu.edu.cn/cgibin/ PlantmPLoc.cgi)预测CpUBA1蛋白的结构域等电点和分子量;利用ExPASy (http://expasy.org/tools/)分析CpUBA1蛋白的等电点和分子量;同时利用Clustal X对来自拟南芥、酵母、人类、小麦等物种的UBA氨基酸序列进行多重序列对比,然后通过MEGA 5软件进行氨基酸序列同源性分析及系统发育分析,构建Neighbor-Joining进化树,1 000 次重复,其他均为默认设置。
1.3 植物总RNA提取及Realtime PCR分析
使用CTAB[18]法从番木瓜的根、茎、叶、穗、雌花、雄花和不同发育阶段的果实中提取总RNA。cDNA第一链用TAKARA公司的PrimeScript RT试剂盒反转录合成,具体操作步骤参照说明书。根据番木瓜基因组中CpUBA1基因的CDS序列设计Realtime PCR引物,并以番木瓜的actin(FJ696416)基因作为内参基因,具体引物序列见表1。

表1 定量PCR所用引物序列
通过Roche的LightCycler480荧光定量PCR仪及TAKARA公司的SYBR Green Master Mix试剂进行定量PCR。反应体系为20 mL,其中模板cDNA 40 ng,上、下游引物各250 nmol/L,SYBR Green Master Mix 10 μL,其余用ddH2O 补齐。反应程序:94℃预变性5 min;94℃10 s、59℃ 20 s、72℃ 30 s,40个循环后作熔解曲线(95 → 65℃,0.1℃/s)。利用 2-ΔΔCt计算基因的相对表达量。所有样品进行3次重复,均设阴性对照。在分析CpUBA1基因的表达时,上调或者下调大于2倍时才认为存在差异。所有试验3次重复。
2 结果与分析
2.1 CpUBA1基因的获得及生物信息学分析
利用酵母和拟南芥U B A蛋白序列在PLAZA 3.0和CpGDB进行BLASTP搜索,我们获得1条番木瓜泛素活化酶基因序列,其在PLAZA 3.0数据库中的登录号为CP00002G03640。CpUBA1基因全长 5 560 bp,含有5个内含子。其中序列开放阅读框(ORF)为3 459 bp,编码的蛋白具有1 152个氨基酸,其分子量为128.93 ku,理论等电点为5.49,染色体定位信息为supercontig_2 :4307079- 4312638。预测表明CpUBA1定位于细胞核。将获得的CpUBA1与酵母(Saccharomyces cerevisiae)、人类(Homo sapiens)、拟南芥(Arabidopsis thaliane)、小麦(Triticum aestivum)、葡萄(Vitis vinifera)和可可(Theobroma cacao)中已知UBA的氨基酸序列进行对比,发现CpUBA1与 AtUBA1、AtUBA2、HsUBA1、ScUBA1、ScUBA2、TaUBA1、TaUBA3、VvUBA1、TcUBA1的同源性分别为76%、84%、41%、40%、13%、70%、68%、84%、83%。同时,番木瓜的CpUBA1含有UBA蛋白特有的保守氨基酸结构域(YRNTFANLALPLFSMAEPVPPKVIKHQDMR WTVWDRWILKNNPTLRELLRWLEDKGLNAYSIS CGSCLLYNSMFPRHRERMDKKLVDLAREVAKV DLPPYRRHLDVVVACEDEEDNDVDIPQI)、5个半胱氨酸残基及ATP结合位点(图1)。
2.2 CpUBA1基因的进化分析
采用MEGA 6软件将番木瓜的CpUBA1蛋白序列与酵母、人类、拟南芥、小麦、葡萄和可可中的UBA蛋白序列进行对比分析并构建进化树,结果(图2)显示,CpUBA1与可可的TcUBA1及葡萄的VvUBA1聚到同一分支上,亲缘关系最近,而与人类及酵母的亲缘关系最远。
2.3 CpUBA1基因在番木瓜不同组织中的表达分析
用Realtime PCR技术分析CpUBA1基因在番木瓜的根、茎、叶、穗、雌花、雄花和果实中的表达情况,结果(图3)显示,CpUBA1基因在番木瓜的不同组织中都检测到表达,但表达存在差异。其中,在雌花中检测到的表达量最低,叶片中的表达量最高,约为雌花的5.48倍。在雄花、果实、根及茎中的表达量约为叶片的3.82、3.18、2.76、1.71倍。该结果说明CpUBA1基因可能参与了番木瓜植株不同组织器官的发育,特别是叶片及花器官的发育过程。
2.3 CpUBA1基因在番木瓜果实成熟进程中的表达分析
分别提取幼果、绿熟果、转色果和黄熟果果肉的RNA,并以反转录后cDNA为模板进行表达分析。结果(图4)显示,CpUBA1基因的表达在绿熟果期没有出现变化,但在转色和成熟期分别上调为幼果期的2.43、2.66倍。该结果表明,CpUBA1基因可能参与了番木瓜实成熟进程。
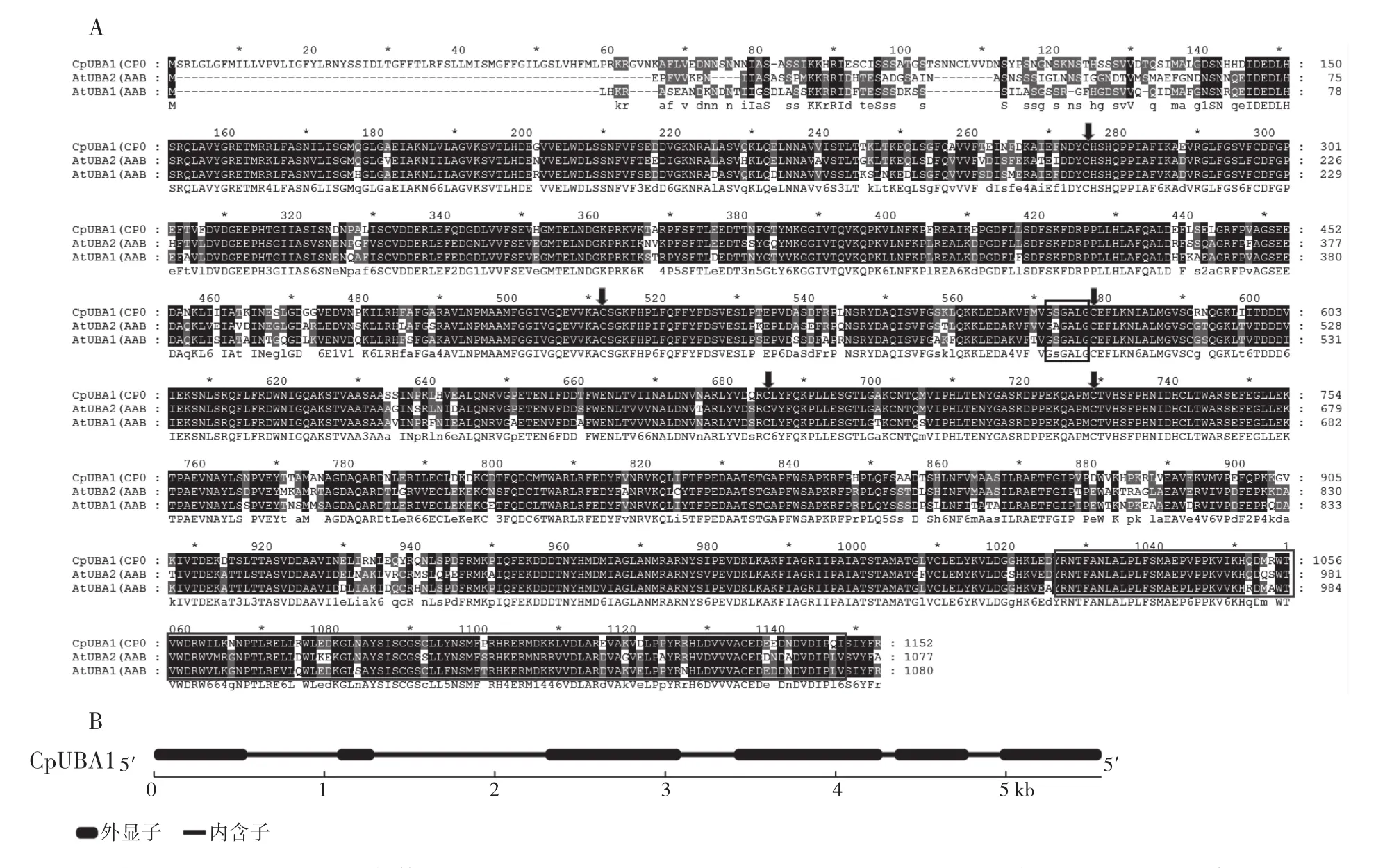
图1 CpUBA1氨基酸结构(A)及基因结构(B)

图2 番木瓜CpUBA1蛋白与其他物种UBA蛋白的进化关系

图3 CpUBA1基因在番木瓜不同组织中的表达水平

图4 果实果实进程中CpUBA1基因的表达
3 讨论
泛素化途径在很多生物途径中起重要作用,泛素活化酶作为泛素化途径的第一个参与酶,在识别靶蛋白泛素化过程中起关键作用[19]。目前关于植物UBA基因研究报道很少,多集中在拟南芥和小麦等模式植物或作物上。本研究首次从番木瓜基因组中得到1个UBA基因(CpUBA1),并对该基因的序列特征、进化关系及表达进行了分析。序列分析表明,CpUBA1含有C末端保守结构域、ATP结合位点及5个半胱氨酸残基,属于典型的UBA蛋白。这和拟南芥[12-13]、小麦[14]等植物的研究结果一致。Hatfield等[14]对小麦的5个半胱氨酸残基进行了点突变研究,大肠杆菌表达分析表明只有第626位的半胱氨酸参与形成硫酯键,对应于CpUBA1即为728位的半胱氨酸,但是否只有该位点半胱氨酸残基参与形成硫酯键,还需要进一步验证。进化分析结果显示,CpUBA1与拟南芥、小麦、葡萄和可可的UBA蛋白序列聚到同一分支,其中与可可的TcUBA1及葡萄的VvUBA1同源性最高,而与人类及酵母的UBA亲缘性较远。
目前关于植物E1的研究报道显示,E1参与了植物生长发育和逆境胁迫响应[16-17]。张妮等[16]采用酵母双杂交的方法得到了泛素活化酶E1的基因片段,命名为MuUBA。荧光实时定量PCR结果表明,MuUBA在茎中的表达量很低,在香蕉的花和子房发育第4个阶段的表达量最高。推测MuUBA在香蕉不同组织及果实的采后成熟过程中具有很重要作用。与该研究类似,本研究中,CpUBA1在番木瓜不同组织中的表达呈叶片>雄花>果实>根>茎>雌花的趋势。说明该基因可能在番木瓜植株不同组织器官的发育中发挥不同作用,特别是叶片及花器官的发育过程。同时CpUBA1基因的表达在转色期出现显著性上升,也就是番木瓜成熟的决定阶段,但在绿熟果期未出现变化。香蕉的UBA表达分别受外源乙烯和1-MCP的强烈诱导和抑制[16],与香蕉类似,番木瓜也是一种呼吸跃变型果实。虽然本研究结果表明CpUBA1可能参与了番木瓜果实成熟进程,但该基因具体是通过怎样的通路发挥该作用,还需要进一步试验分析。综上,本研究首次对番木瓜的泛素活化酶基因CpUBA1进行了系统性的生物信息学及表达分析,该结果将为进一步探讨泛素-蛋白酶体系在番木瓜果实成熟进程的作用奠定基础,同时也将丰富植物UBA基因的研究。
[1]Devitt L C,Fanning K,Dietzgen R G,et al.Isolation and functional characterization of a lycopene β-cyclase gene that controls fruit colour of papaya(Carica papayaL.)[J]. Journal of Experimental Botany,2010,61(1):33.
[2]Ming R,Hou S,Feng Y,et al. The draft genome of the transgenic tropical fruit tree papaya(Carica papayaLinnaeus)[J]. Nature,2008,452(7190):991-996.
[3]FAOSTAT. 2012a. Crop Production. http://www.fao.org/faostat/en/#data/QC
[4]White P J. Recent advances in fruit development and ripening:an overview[J]. Journal of Experimental Botany,2002,53(377):1995.
[5]Mukhopadhyay D,Riezman H. Proteasomeindependent functions of ubiquitin in endocytosis and signaling[J]. Science,2007,315:201-205.
[6]Moon J,Parry G,Estelle M. The ubiquitinproteasome pathway and plant development[J].Plant Cell,2004,16:3181-3195.
[7]Smalle J,Vierstra R D. The ubiquitin 26S proteasome proteolytic pathway.Annu[J]. Rev.Plant Biol,2004,55:555-590.
[8]Dreher K,Callis J. Ubiquitin,hormones and biotic stress in plants[J]. Ann.Bot,2007,99:787-822.
[9]Pickart C M,Eddins M J. Ubiquitin:structures,functions,mechanisms[J]. Biochim. Biophys.Acta,2004,1695:55-72.
[10]Mcgrath J P,Jentsch S,Varshavsky A. UBA 1:an essential yeast gene encoding ubiquitinactivating enzyme[J]. Embo Journal,1991,10(1):227-236.
[11]Dohmen R J,Stappen R,Mcgrath J P,et al.An essential yeast gene encoding a homolog of ubiquitin-activating enzyme[J]. Journal of Biological Chemistry,1995,270(30):18099-18109.
[12]Leyser H M,Lincoln C A,Timpte C,et al.Arabidopsis auxin-resistance gene AXR1 encodes a protein related to ubiquitin-activating enzyme E1[J]. Nature,1993,364(6433):161-164.
[13]Hatfield P M,Gosink M M,Carpenter T B,et al. The ubiquitin-activating enzyme(E1)gene family in Arabidopsis thaliana[J]. Plant Journal,1997,11(2):213-226.
[14]Hatfield P M,Vierstra R D. Multiple forms of ubiquitin-activating enzyme E1 from wheat.Identification of an essential cysteine by in vitro mutagenesis[J]. Journal of Biological Chemistry,1992,267(21):14799-14803.
[15]Li G Q,Zang X N,Zhang X C,et al. Cloning of ubiquitin-activating enzyme and ubiquitinconjugating enzyme genes from Gracilaria lemaneiformis,and their activity under heat shock[J]. Gene,2014,538(1):155-163.
[16]张妮,刘菊华,贾彩红,等. 香蕉MuMADS1与泛素激活酶(MuUBA)在采后果实中的相互作用[J]. 热带作物学报,2014,35(2):307-312.
[17]Li X,Zhang S S,Ma J X,et al. TaUBA,a UBA domain-containing protein in wheat (Triticum aestivumL.),is a negative regulator of salt and drought stress response in transgenic Arabidopsis.[J]. Plant Cell Reports,2015,34(5):755-766.
[18]Jue D,Sang X,Shu B,et al. Characterization and expression analysis of genes encoding ubiquitin conjugating domain-containing enzymes in Carica papaya[J]. PLOS ONE,2017,12(2):e0171357.
