青蒿素及其衍生物抗疟活性的密度泛函理论研究
2017-03-08刘靖丽
刘靖丽,郭 勇
(1.陕西中医药大学 药学院,陕西 咸阳 712046; 2.四川大学 化学学院,四川 成都 610064)
青蒿素及其衍生物抗疟活性的密度泛函理论研究
刘靖丽1*,郭 勇2
(1.陕西中医药大学 药学院,陕西 咸阳 712046; 2.四川大学 化学学院,四川 成都 610064)
为了深入研究青蒿素及其衍生物的抗疟活性和分子结构之间的关系,运用密度泛函理论B3LYP方法,以6-31G*为基组对青蒿素及其衍生物二氢青蒿素、蒿甲醚和青蒿琥酯进行了优化计算.从分子的几何构型、NBO电荷及前线轨道能等方面分析了青蒿素及其衍生物的抗疟活性与结构之间的关系.青蒿素及其衍生物结构中的过氧桥键是其抗疟作用的活性位,O17和O20带负电荷越多、ΔE(LUMO-HOMO)越低、EHOMO能级越高,分子的抗疟活性越强.结果表明,4种化合物的抗疟活性顺序为:青蒿素<二氢青蒿素<蒿甲醚<青蒿琥酯,与临床实验结果相吻合.
青蒿素;抗疟活性;密度泛函理论
青蒿为菊科艾属一年生草本植物黄花蒿,性寒,味苦、辛,归肝、胆经,具有清热解暑、除蒸、截疟之功效,青蒿自古以来就被用于发热和疟疾的治疗[1].上世纪70年代,屠呦呦等从青蒿中分离出一种具有抗疟活性的倍半萜内酯化合物,命名为青蒿素(artemisinin).通过化学反应、光谱数据和X射线单晶衍射方法证明青蒿素结构中含有独特的过氧桥键[2-3].后来人们对青蒿素化学结构进行了改造,以青蒿素母体为基础,在青蒿素的碳氧双键上加上不同基团,合成了二氢青蒿素(dihydroartemisinin)、蒿甲醚(artemether)和青蒿琥酯(artesunate)等衍生物[4-6].
实验表明[4],二氢青蒿素的活性比青蒿素高1倍,但不稳定,易分解.脂溶性的蒿甲醚也具有抗疟活性,其活性高于青蒿素,现已应用于临床.青蒿琥酯是目前唯一有效的青蒿素水溶性衍生物,是经我国卫生部批准上市用于抗疟的一类新药[6].近年来的相关研究表明[7-9],青蒿素除具有抗疟疾作用外,在心血管疾病、抗肿瘤、免疫调节等多方面具重要的药理作用和潜在的应用价值.但是有关其结构和活性关系的理论研究甚少,本文中我们利用密度泛函(DFT)方法对上述4个目标化合物进行研究,试图从微观层次上阐明其结构与活性之间的关系,为设计和合成抗疟活性更强的青蒿素类药物分子提供有用的理论信息.
1 计算方法
运用DFT(B3LYP)方法,以6-31G*为基组对4个目标化合物青蒿素(1)、二氢青蒿素(2)、蒿甲醚(3)和青蒿琥酯(4)的几何构型进行全优化,得到4个目标化合物的最优几何结构,并在此基础上进行频率计算.结果显示,优化得到的结构均无虚频,说明我们得到的是能量极小结构.最后进行NBO(Natural Bond Orbital)电荷和分子前线轨道分析,所有的计算均由Gaussian 03程序完成[10].
2 结果与讨论
2.1 分子的几何平衡构型
采用B3LYP/6-31G*方法对4个目标化合物的结构进行了几何全优化,获得了各个化合物的几何平衡构型,如图1所示.由此结构计算所得到的频率中没有虚频,说明理论计算几何结构为稳定结构,表1列出了计算所得的部分几何结构参数,并与青蒿素的晶体结构数据[3]进行了对比.

图1 青蒿素及其衍生物的结构和原子编号Fig.1 The geometry and atom numbering of artemisinin and its derivatives
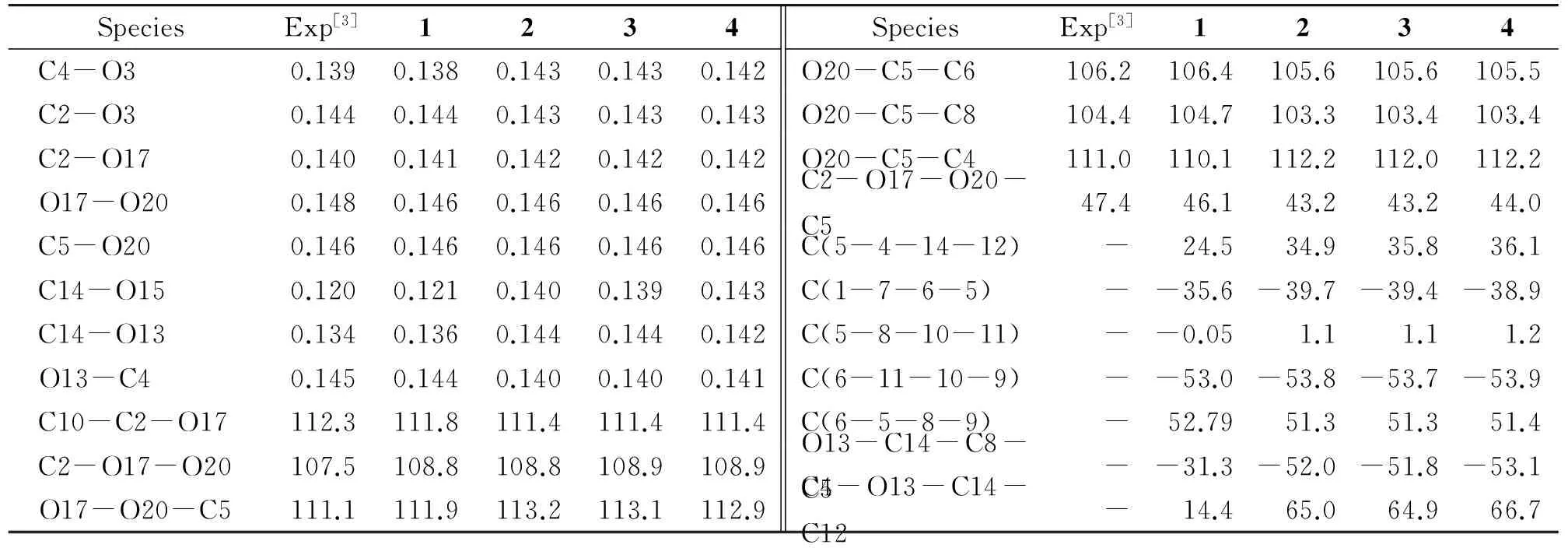
SpeciesExp[3]1234SpeciesExp[3]1234C4-O30.1390.1380.1430.1430.142O20-C5-C6106.2106.4105.6105.6105.5C2-O30.1440.1440.1430.1430.143O20-C5-C8104.4104.7103.3103.4103.4C2-O170.1400.1410.1420.1420.142O20-C5-C4111.0110.1112.2112.0112.2O17-O200.1480.1460.1460.1460.146C2-O17-O20-C547.446.143.243.244.0C5-O200.1460.1460.1460.1460.146C(5-4-14-12)-24.534.935.836.1C14-O150.1200.1210.1400.1390.143C(1-7-6-5)--35.6-39.7-39.4-38.9C14-O130.1340.1360.1440.1440.142C(5-8-10-11)--0.051.11.11.2O13-C40.1450.1440.1400.1400.141C(6-11-10-9)--53.0-53.8-53.7-53.9C10-C2-O17112.3111.8111.4111.4111.4C(6-5-8-9)-52.7951.351.351.4C2-O17-O20107.5108.8108.8108.9108.9O13-C14-C8-C5--31.3-52.0-51.8-53.1O17-O20-C5111.1111.9113.2113.1112.9C4-O13-C14-C12-14.465.064.966.7
从表1中可以看出,采用B3LYP/6-31G*方法计算所得4个目标化合物的结构参数与其母体化合物青蒿素的实验值[3]非常接近.由分子价键理论可知,键长越长,键能越小,键越容易断裂,反应活性越高.可见分子的键强度与键长有密切关系,所以我们可以通过判断键长来推断反应活性.正常的过氧键长为0.13 nm左右[11].4个目标化合物的过氧键长均大于0.13 nm,说明4个化合物中的过氧键比较容易断裂,从一定程度上反映出青蒿素及其衍生物的抗疟活性与过氧键有密切的关系.另外从二面角的数值可以看出,包括过氧键的七元环存在不同程度的扭曲,这种扭曲显然是由环与环之间不同程度的排斥所导致的.环己烷是一个椅式的稳定构象,六元环内酯是一个扭曲的椅式构象,理论计算结果与其母体青蒿素的晶体结构相吻合[3].
2.2 NBO电荷布局数
在药理学中,当药物分子与受体相互作用时,必须通过两者之间电子的相互作用来进行.因此,药物分子的电荷分布对药物活性有重要的影响.分析药物分子内电荷分布可以揭示其与受体的作用位点.表2列出了4个目标化合物中起主要作用的C和O原子的NBO电荷.
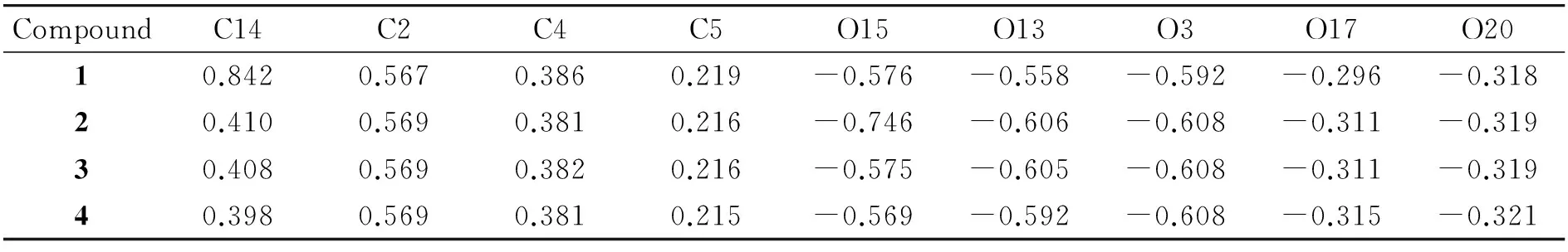
表2 C原子和O原子的NBO电荷Table 2 NBO charge on the carbon atoms and oxygen atoms
从表2中可以看出,4个目标化合物的电荷分布规律极为相似,除了青蒿琥酯.负电荷集中分布在5个O原子上,而正电荷则主要分布在与O原子相连的C上,由此分析O原子主要与受体的正电性区域相作用,而C14、C2、C4及C5则与受体的负电性区域相作用.对青蒿素分子结构与其抗疟活性的构效关系研究表明过氧键是分子中的关键活性部位[12],有活性的青蒿素类似物,如果把过氧基-O-O-变成-O-、-O-C-O-都将失去活性[13].随后进一步研究证实,青蒿素与疟原虫体内的血红素作用时,中心原子Fe2+的空轨道可结合富电子的原子和基团[14].SHUKLA等[15]利用分子模拟方法将青蒿素与血红素进行对接研究,结果提示青蒿素的分子内过氧桥结构紧靠于血红素的中心铁原子上.因此,青蒿素在发挥抗疟活性时,主要以供电子为主,过氧桥键是此类分子的主要供电子区,过氧桥键的给电子能力直接影响化合物的抗疟活性.这一结论与程永浩等[16]通过半经验的MNDO方法研究青蒿素的电子结构与生物活性关系的计算结果一致.由此可见,过氧原子O17和O20所带的负电荷越多,青蒿素与血红素的相互作用越强,分子的抗疟活性越强.根据表2中的电荷分布推测4个目标化合物的抗疟活性顺序可能为:青蒿素<二氢青蒿素≤蒿甲醚<青蒿琥酯.电荷分布分析不够充分,还需要考虑分子的前线轨道.
2.3 前线分子轨道及轨道能
根据前线分子轨道理论,最高的电子占据轨道(HOMO)和最低的电子未占轨道(LUMO)在化学反应中起着主要作用,前线轨道往往与分子的生物活性有着直接的联系.因此,研究前线轨道的性质可以为确定活性部分以及探讨作用机制等提供重要信息.HOMO具有优先提供电子的重要作用,HOMO能级越高,该物质越易失去电子参与反应;LUMO具有优先接受电子的重要作用,LUMO能级越低,该物质越易得到电子参与反应[17-19].图2给出了4个目标化合物的HOMO轨道和LUMO轨道图,由图2可以看出4个化合物的HOMO成份主要集中在过氧桥键O17和O20原子上,另外C5、C2、C4、O15、O13原子也有贡献.进一步说明,青蒿素及其衍生物二氢青蒿素、蒿甲醚和青蒿琥酯在发挥抗疟活性时,均以供电子为主,过氧桥键是决定其抗疟活性的关键几何结构.
表3分别列出了4个目标化合物的前线轨道能级数据,表中ΔE(LUMO-HOMO)为最高占据轨道能量EHOMO与最低未占据轨道能量ELUMO的能级差.ΔE(LUMO-HOMO)的大小反映了电子从最高占据轨道向最低空轨道跃迁需要的能量大小,能级差越小,电子越容易被激发,与电子得失相关的反应活性越强.对于4个目标化合物来说,ΔE(LUMO-HOMO)越小,过氧桥键的氧原子越容易给出电子,抗疟活性越强.由表3ΔE的大小可以得出4个化合物的抗疟活性顺序为:青蒿素<二氢青蒿素<蒿甲醚<青蒿琥酯,与前面电荷分布的分析结果一致.同时EHOMO能级越高,活性越高,由此得出的活性顺序为:青蒿素<二氢青蒿素<蒿甲醚<青蒿琥酯,与前面得到的活性顺序符合.无论是ΔE还是EHOMO,都表明4个目标化合物中,青蒿琥酯的活性是最强的,而二氢青蒿素与蒿甲醚的活性均高于青蒿素的抗疟活性.
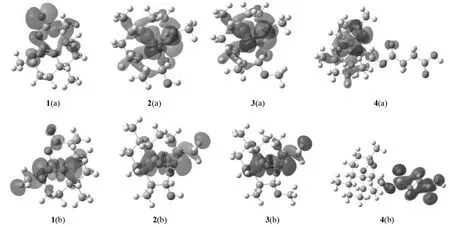
图2 4个化合物的HOMO(a)与LUMO(b)轨道图Fig.2 HOMO (a) and LUMO (b) orbitals of four compounds
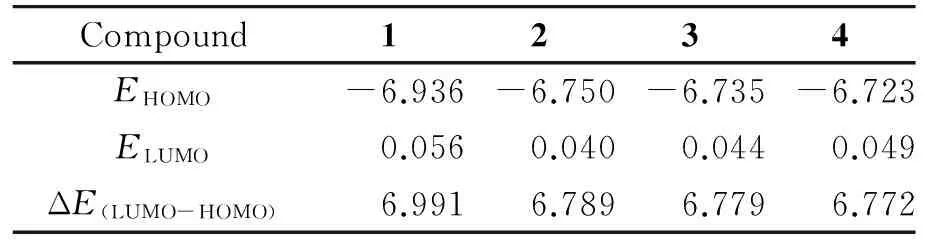
表3 4个化合物的最高占据轨道能和最低空轨道能以及两者之差(单位:eV)Table 3 Energies of HOMO and LUMO and the energy gap between HOMO and LUMO of four compounds (in eV)
3 结论
采用密度泛函理论B3LYP方法对青蒿素及其衍生物(二氢青蒿素、蒿甲醚和青蒿琥酯)分子进行了优化计算,得到了4个化合物的理论平衡几何结构,与其母体青蒿素的晶体结构吻合的较好.青蒿素及其衍生物的抗疟活性与其结构中的过氧键密切相关,从分子的几何结构、NBO电荷和前线轨道等方面分析了4个化合物的抗疟活性与结构的关系,结果表明,过氧桥键是其发挥抗疟活性的关键几何结构.从电子结构的角度对青蒿素及其衍生物抗疟活性的差异作出了合理的解释,为青蒿素及其衍生物的结构改造提供了理论指导.
[1] 屠呦呦.青蒿及青蒿素类药物[M].北京:化学工业出版社,2009:5.
TU Y Y.Artemisinin and artemisinin-based drugs [M].Beijing:Chemical Industry Press,2009:5.
[2] 青蒿结构研究协作组.一种新型的倍半萜内酯-青蒿素[J].科学通报,1977,22(3):123.
Research Group of Artemisinin Structure.A new kind of half terpene lactones-artemisinin [J].Chinese Science Bulletin,1977,22(3):123.
[3] 中国科学院生物物理研究所青蒿素协作组.青蒿素的晶体结构及其绝对构型[J].中国科学,1979,11:1114-1128.
Institute of Biophysics,Chinese Academy of Sciences,Artemisinin Group.The crystal structure of artemisinin and its absolute configuration [J].Science China,1979,11:1114-1128.
[4] 李英,虞佩琳,陈一心,等.青蒿素衍生物的合成[J].科学通报,1979,24(14):667-669.
LI Y,YU P L,CHEN Y X,et al.Synthesis of some derivatives of artemisinin [J].Chinese Science Bulletin,1979,24(14):667-669.
[5] 梁洁,李英.青蒿素芳香醚类衍生物的合成[J].中国药物化学杂志,1996,19:22-25.
LIANG J,LI Y.Synthesis of the arylether derivatives of artemisinin [J].Chinese Journal of Medicinal Chemistry,1996,19:22-25.
[6] 刘旭.青蒿素衍生物的研究[J].药学通报,1980,15(4):183.
LIU X.Research of artemisinin derivatives [J].Chinese Pharmaceutical Bulletin,1980,15(4):183.
[7] 郭燕,王俊,陈正堂.青蒿素类药物的药理作用新进展[J].中国临床药理学与治疗学,2006,11(6):615-620.
GUO Y,WANG J,CHEN Z T.Recent advancement in pharmacological effects of artemisinin and its derivatives [J].Chinese Journal of Clinical Pharmacology and Therapeutics,2006,11(6):615-620.
[8] 李琛琛,尹昆,闫歌.抗疟药青蒿素及其衍生物相关药理作用研究进展[J].中国病原生物杂志,2016,11(2):185-187.
LI C C,YIN K,YAN G.Advances in research on the pharmacological action of the antimalarial artemisinin and its derivatives [J].Journal of Pathogen Biology,2016,11(2):185-187.
[9] 张楠.青蒿素类药物的主要研究进展[J].中国药物评价,2013,30(1):13-16.
ZHANG N.Research progress of the artemisinin drugs [J].Chinese Journal of Drug Evaluation,2013,30(1):13-16.
[10] FRISCH M J,TRUCKS G W,SCHLEGEL H B,et al.Gaussian 03 [CP].Revision A.01,Wallingford CT:Gaussian,Inc.,2004.
[11] HNYK D,MACHACEK J,ARGUELLO G A,et al.Stucture and conformational properties of bis(trifluoromethyl) peroxydicarbonate,CF3OC(O)O-OC(O)OCF3[J].The Journal of Physical Chemistry A,2003,107(6):847-851.
[12] 陈扬,朱世民,陈洪渊.青蒿素类抗疟药研究进展[J].药学学报,1998,33(3):234-239.
CHEN Y,ZHU S M,CHEN H Y.The research progress of artemisinin-based antimalarial drugs [J].Acta Pharmaceutica Sinica,1998,33(3):234-239.
[13] BUTLER A R,WU Y L.Artemisinin (qinghaosu):a new type of antimalarial drug [J].Chemical Society Reviews,1992,21(2):85-90.
[14] GOLENSER J,WAKNINE J H,KRUGLIAK M,et al.Current perspectives on the mechanism of action of artemisinins [J].International Journal for Parasitology,2006,36(14):1427-1441.
[15] SHUKLA K L,GUND T M,MESHNICK S R.Molecular modeling studies of the artemisinin (qinghaosu)-hemin interaction:Docking between the antimalarial agent and its putative receptor [J].Journal of Molecular Graphics,1995,13(4):215-222.
[16] 程永浩,李晓艳,郑世均.青蒿素及其衍生物的量子化学及构效关系研究[J].计算机与应用化学,2000,17(21):21-22.
CHENG Y H,LI X Y,ZHENG S J.Quantum chemistry and structure-activity relationship studies of artemisinin and its derivatives [J].Computers and Applied Chemistry,2000,17(21):21-22.
[17] 张鑫,杨英杰,吕庆章.4种甘草黄酮类化合物抗氧化活性的密度泛函理论研究[J].计算机与应用化学,2012,29(6):656-660.
ZHANG X,YANG Y J,LÜ Q Z.Density functional theory calculations on antioxidation activity of four flavones from radix glycyrrhizae [J].Computers and Applied Chemistry,2012,29(6):656-660.
[18] 张鑫,杨英杰,吕庆章.黄芪异黄酮类化合物抗氧化活性的密度泛函理论研究[J].化学研究与应用,2012,24(11):1662-1669.
ZHANG X,YANG Y J,LÜ Q Z.Density functional theory calculations on antioxidation activity of the isoflavone compounds from astragalus [J].Chemical Research and Application,2012,24(11):1662-1669.
[19] 陈莹,徐抗震,宋纪蓉,等.酚酸抗氧化活性的理论计算[J].食品科学,2011,32(9):36-39.
CHEN Y,XU K Z,SONG J R,et al.Theoretical study on antioxidant activity of phenolic acids [J].Food Science,2011,32(9):36-39.
[责任编辑:吴文鹏]
Density functional theory studies on antimalarial activity of artemisinin and its derivatives
LIU Jingli1*,GUO Yong2
(1.CollegeofPharmacy,ShaanxiUnivserityofChineseMedicine,Xianyang712046,Shaanxi,China; 2.CollegeofChemistry,SichuanUniversity,Chengdu,610064,Sichuan,China)
In order to study the relationship between the structure and antimalarial activity of artemisinin and its derivatives,the density functional theory (DFT) B3LYP method with 6-31G*as a basis set was used to optimize the structure of artemisinin,dihydroartemisinin,artemether and artesunate.The properties of the artemisinin and its derivatives have been discussed in detail based on their molecular structures,NBO charges and the energies of the frontier molecular orbitals.The results showed that the endoperoxy bridge is likely the most active site and essential for antimalarial activity of artemisinin and its derivatives.The more negative charge of O17 and O20,the lower enengy of ΔE(LUMO-HOMO)and the higher energy ofEHOMOresulted in the stronger antimalarial activity of the compounds.It was revealed that the antimalarial activity of the compounds goes along with the order:artemisinin artemisinin; antimalarial activity; density functional theory (DFT) 2016-09-08. 陕西中医药大学重点培育项目(2015PY11). 刘靖丽(1984-),女,讲师,研究方向为量子化学.* ,E-mail:sculiujl@126.com. O641 A 1008-1011(2017)01-0087-05
