HPLC法同时测定软肝缩脾丸中芍药苷和丹酚酸B的含量
2017-03-03宋晓红汤长明王丽军张建邦解放军第一五三中心医院制剂室郑州450042
刘 栋,宋晓红,汤长明,王丽军,张建邦(解放军第一五三中心医院制剂室,郑州 450042)
HPLC法同时测定软肝缩脾丸中芍药苷和丹酚酸B的含量
刘 栋*,宋晓红,汤长明,王丽军,张建邦(解放军第一五三中心医院制剂室,郑州 450042)
目的:建立同时测定软肝缩脾丸中芍药苷和丹酚酸B含量的方法。方法:采用高效液相色谱法。色谱柱为Wondasil C18,流动相为乙腈-0.1%磷酸溶液(梯度洗脱),流速为1.0 mL/min,检测波长为230 nm(芍药苷)、286 nm(丹酚酸B),柱温为30℃,进样量为10 μL。结果:芍药苷和丹酚酸B检测质量浓度线性范围分别为9.79~195.80 μg/mL(r=0.999 9)、11.45~229.00 μg/mL(r=0.999 9);定量限分别为0.018 1、0.014 4 μg,检测限分别为0.005 4、0.004 3 μg;精密度、稳定性、重复性试验的RSD<2.0%;加样回收率分别为98.67%~102.22%(RSD=1.26%,n=9)、99.72%~103.28%(RSD=1.05%,n=9)。结论:该方法快速、灵敏、准确,可用于软肝缩脾丸中芍药苷和丹酚酸B含量的同时测定。
软肝缩脾丸;芍药苷;丹酚酸B;含量测定;高效液相色谱法
软肝缩脾丸[批准文号:济制字(2011)F12004]为解放军第一五三中心医院二十多年的临床经验方,由赤芍、丹参、黄芪、紫河车、大黄、三七等中药材组成,具有益气活血破瘀、软坚散结消痞之功效,适用于各种病因引起的慢性肝炎、肝硬化或无症状病毒携带者[1-4];该制剂临床疗效确切、口碑较好。但该制剂的质量标准不够全面,仅有鉴别检查和丸剂的常规检查,缺乏含量测定项目,不能全面控制该制剂的质量。依据“中国人民解放军总后勤部卫生部军队医疗机构制剂标准提高计划”要求,同时为了进一步控制该制剂的质量,本试验采用高效液相色谱法(HPLC)同时测定软肝缩脾丸中芍药苷和丹酚酸B的含量,以期为完善该制剂的质量标准提供参考。
1 材料
1.1 仪器
LC-10A型HPLC仪,包括SPD-10A型紫外检测器、手动进样器、LCsolutionLite型色谱工作站(日本Shimadzu公司);pHS-3C型酸度计(上海雷磁仪器厂);BT125D型十万分之一电子分析天平(德国Sartorius公司);AS3120A型超声波清洗仪(天津奥特赛恩斯仪器公司,功率:120 W,频率:40 kHz)。
1.2 药品与试剂
软肝缩脾丸(解放军第一五三中心医院自制,批号:150316、150419、150420,规格:48 g/瓶);芍药苷对照品(批号:110736-201136,纯度:96.0%)、丹酚酸B对照品(批号:111562-201313,纯度:97.0%)均购自中国食品药品检定研究院;乙腈为色谱纯,其余试剂均为分析纯,水为重蒸水。
2 方法与结果
2.1 色谱条件
色谱柱:Wondasil C18(250 mm×4.6 mm,5 μm);流动相:乙腈(A)-0.1%磷酸溶液(B),梯度洗脱(洗脱程序见表1);流速:1.0 mL/min;检测波长:230 nm(芍药苷)、286 nm(丹酚酸B);柱温:30℃;进样量:10 μL。
2.2 溶液的制备
2.2.1 混合对照品溶液 分别精密称取待测成分对照品适量,置于同一10 mL量瓶中,加稀乙醇(量取乙醇529 mL,加水稀释至1 000 mL,下同)溶解并定容,摇匀,即得芍药苷和丹酚酸B质量浓度分别为0.979、1.145 mg/mL的混合对照品贮备液。精密吸取上述混合对照品贮备液1 mL,置于10 mL量瓶中,加稀乙醇定容,摇匀,即得芍药苷和丹酚酸B质量浓度分别为97.90、114.50µg/mL的混合对照品溶液。

表1 梯度洗脱程序Tab 1 Gradient elution program
2.2.2 供试品溶液 取样品适量,除去包衣,研细,取约1 g,精密称定,置于100 mL具塞锥形瓶中,精密加入稀乙醇25 mL,密塞,称定质量,超声处理1 h,放冷;再次称定质量,用稀乙醇补足减失的质量,摇匀,滤过,取续滤液,即得。
2.2.3 阴性对照溶液 按样品的制备工艺和配方比例,分别制备缺赤芍和丹参的单一阴性样品,再按“2.2.2”项下方法制备单一阴性对照溶液。
2.3 系统适用性与专属性试验
分别精密吸取“2.2”项下混合对照品溶液、供试品溶液、阴性对照溶液各10 μL,按“2.1”项下色谱条件进样测定,记录色谱,详见图1。由图1可知,在该色谱条件下各成分均能达到基线分离(分离度>1.5);芍药苷和丹酚酸B的保留时间分别在10.2 min和25.6 min左右;供试品溶液在混合对照品溶液色谱相应的保留时间处有相同的吸收峰,而阴性对照溶液则没有相同的吸收峰。
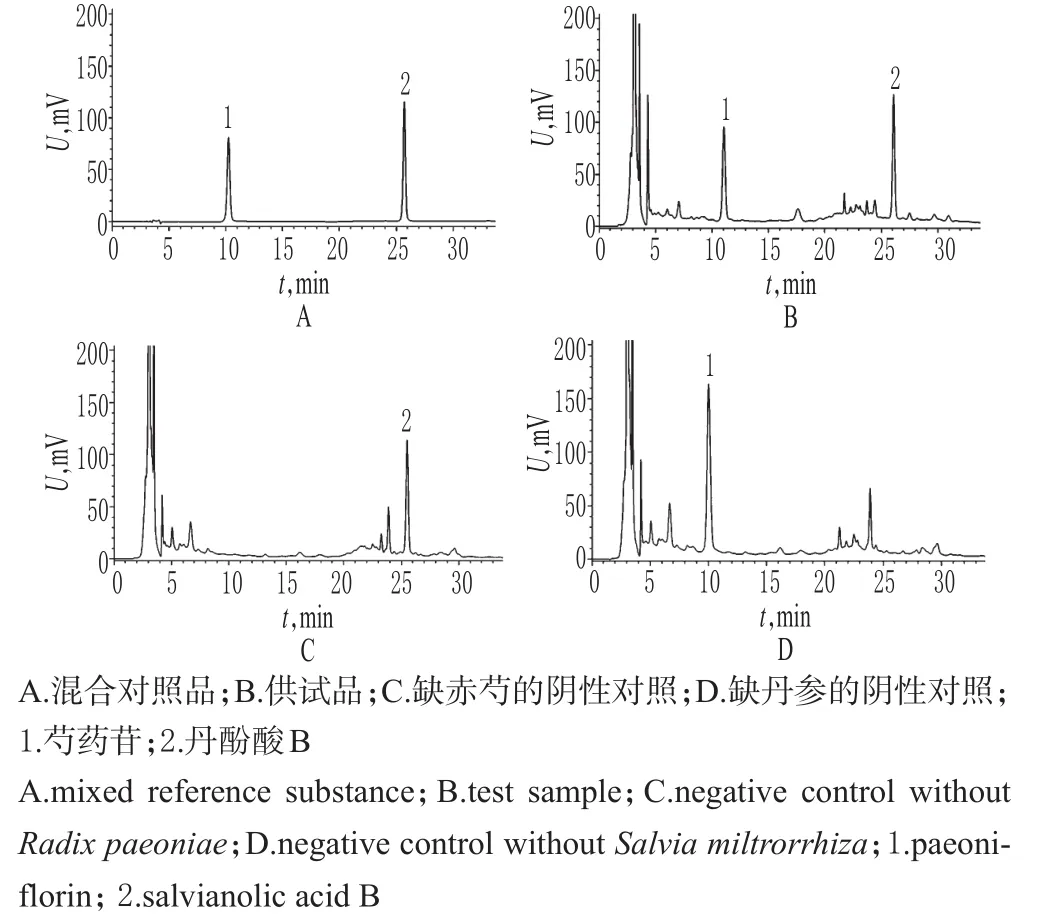
图1 高效液相色谱图Fig 1 HPLC chromatograms
2.4 线性关系考察
精密吸取“2.2.1”项下混合对照品贮备液适量,用稀乙醇逐步稀释制成芍药苷质量浓度分别为9.79、19.58、48.95、97.90、146.85、195.80 μg/mL,丹酚酸B质量浓度分别为11.45、22.90、57.25、114.50、171.75、229.00 μg/mL的系列混合对照品溶液。取上述系列混合对照品溶液适量,按“2.1”项下色谱条件进样测定,记录峰面积。以待测成分质量浓度(x,μg/mL)为横坐标、峰面积(y)为纵坐标进行线性回归,得芍药苷、丹酚酸B的回归方程为分别y=14 927x—5 914.1(r=0.999 9)、y=14 616x—1 282.6(r=0.999 9)。结果表明,芍药苷和丹酚酸B检测质量浓度线性范围分别为9.79~195.80、11.45~229.00 μg/mL。
2.5 定量限与检测限考察
取“2.2.1”项下混合对照品溶液适量,倍比稀释,按“2.1”项下色谱条件连续进样测定6次,记录峰面积。当信噪比为10∶1时,得芍药苷和丹酚酸B的定量限分别为0.018 1、0.014 4 μg;当信噪比为3∶1时,得芍药苷和丹酚酸B的检测限分别为0.005 4、0.004 3 μg。
2.6 精密度试验
精密量取“2.2.1”项下混合对照品溶液10 μL,按“2.1”项下色谱条件连续进样测定6次,记录峰面积。结果,芍药苷和丹酚酸B峰面积的RSD分别为0.26%、0.72%(n=6),表明仪器精密度良好。
2.7 稳定性试验
取“2.2.2”项下供试品溶液(批号:150316)适量,分别于室温下放置0、2、4、8、12、24 h时按“2.1”项下色谱条件进样测定,记录峰面积。结果,芍药苷和丹酚酸B峰面积的RSD分别为0.85%、0.80%(n=6),表明供试品溶液在室温放置24 h内稳定性良好。
2.8 重复性试验
取同一批样品(批号:150420)适量,按“2.2.2”项下方法平行制备6份供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并计算芍药苷和丹酚酸B的含量。结果,芍药苷和丹酚酸B的平均含量分别为2.882、2.985 mg/g,RSD分别为1.17%、1.14%(n=6),表明本方法重复性良好。
2.9 加样回收率试验
取样品(批号150420)适量,除去包衣,研细,精密称取9份粉末,每份约0.5 g,分别加入一定质量的芍药苷和丹酚酸B对照品,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并计算加样回收率,结果见表2。
2.10 样品含量测定
取3批样品各适量,分别按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并计算芍药苷和丹酚酸B的含量,结果见表3。
3 讨论

表2 加样回收率试验结果(n=9)Tab 2 Results of recovery tests(n=9)

表3 样品含量测定结果(n=3,mg/g)Tab 3 Results of contents determination of samples(n=3,mg/g)
3.1 供试品溶液制备方法的优化
笔者在试验过程中先后考察了提取溶剂、提取方式、提取时间、提取溶剂用量对样品所测指标成分提取效果的影响。提取溶剂分别选取75%甲醇、75%乙醇、50%甲醇、稀乙醇进行对比试验,结果稀乙醇的提取率优于前三者。提取方式考察了超声处理1 h、回流提取1 h和浸泡过夜(18 h),结果芍药苷采用3种方式的芍药苷提取率没有明显差异,但采用超声处理和回流提取的丹酚酸B含量要明显高于浸泡过夜(18 h)提取方式,考虑到超声处理简单、方便、安全,故采用超声处理。笔者将超声处理时间设置为0.5、1、1.5、2 h,结果芍药苷和丹酚酸B的含量在超声处理1、1.5、2 h时基本相同,并均明显高于超声处理0.5 h。笔者考察了稀乙醇用量(15、25、40、50 mL),发现提取溶剂用量为25、40、50 mL时,芍药苷和丹酚酸B的提取量基本相同,并均高于提取溶剂用量为15 mL时的提取量。为了节约时间、节约试剂,因此本试验最终确定制备供试品溶液的方式为25 mL稀乙醇,超声处理1 h。
3.2 流动相的考察
笔者先后考察了不同比例的乙腈-磷酸二氢钾溶液[5-6]、甲醇-磷酸溶液[7]、乙腈-甲醇-0.5%磷酸溶液[8-9]、乙腈-0.1%磷酸溶液[10-11]为流动相进行梯度洗脱。结果,有机相含有甲醇时丹酚酸B峰与相邻峰分离度差,水相含有磷酸二氢钾时芍药苷峰形有拖尾现象;而以乙腈-0.1%磷酸溶液为流动相进行梯度洗脱时,芍药苷和丹酚酸B峰与相邻色谱峰分离度良好,且峰形对称。因此,本试验选择乙腈-0.1%磷酸溶液为流动相。
3.3 检测波长的选择
取待测成分对照品适量,分别用稀乙醇溶解并稀释成每1 mL含药药苷和丹酚酸B各100µg的混合对照品溶液,在200~400 nm波长范围内扫描。结果显示,芍药苷和丹酚酸B最大吸收波长分别为230、286 nm。为减少测定误差,本试验在230 nm波长下测定芍药苷的含量,在286 nm波长下测定丹酚酸B的含量。
3.4 制剂制备及贮藏注意事项
试验过程中笔者发现,取生产日期较早(2年前的批次,已过期)的软肝缩脾丸测定时,丹酚酸B含量下降明显,且其色谱峰后出现一个半峰宽较大的未知峰,推测可能原因是丹酚酸B化学结构中含有多个酚羟基和酯基,易发生氧化降解和水解。故软肝缩脾丸制备过程中要严格控制水分含量,并包糖衣或薄膜衣,同时,建议其说明书的贮藏项下增加“密闭、防潮”字样。
综上所述,本方法快速、灵敏、准确,可用于软肝缩脾丸中芍药苷和丹酚酸B含量的同时测定。
[1] 申德林,张成道,王全楚,等.软肝缩脾丸治疗慢性肝纤维化的临床与实验研究[J].世界华人消化杂志,2000,8(10):1199-1200.
[2] 张成道,王全楚,申德林,等.拉米夫啶联合软肝缩脾丸对肝炎患者肝纤维化及肝细胞损伤的作用[J].实用医药杂志,2005,22(11):973-974.
[3] 杜慧芳,王全楚.软肝缩脾丸治疗慢性肝病120例[J].河南中医,2008,28(7):53-54.
[4] 王全楚,申德林,张燕,等.重型肝炎恢复期干扰素联合软肝缩脾丸抗肝纤维化的研究[J].胃肠病学和肝病学杂志,2008,17(9):741-742.
[5] 田润.HPLC法同时测定妇炎康片中丹酚酸B、隐丹参酮和芍药苷[J].中成药,2013,35(1):93-96.
[6] 黄鸣清,谢友良,王德杭,等.HPLC同时测定妇炎康片中芍药苷、丹酚酸B、小檗碱[J].中国实验方剂学杂志,2011,17(22):68-71.
[7] 谭生建,刘刚,张华,等.梯度洗脱HPLC法测定抗栓保心片中芍药苷和丹酚酸B的含量[J].药物分析杂志,2009,29(7):1104-1106.
[8] 姜晖,王绍志,张熙洁,等.HPLC法同时测定利脑心胶囊中6种成分的含量[J].中国药房,2015,26(3):374-376.
[9] 张熙洁,吴江,姜晖,等.多波长HPLC法同时测定心宁片中5种成分的含量[J].中国药房,2015,26(18):2535-2538.
[10] 喻录容,何先元,黄英如.HPLC同时测定冠心康颗粒中芍药苷、丹酚酸B和羟基红花黄色素A的含量[J].中国现代应用药学,2015,32(5):561-564.
[11] 刘静,谈瑄忠,陆兔林,等.HPLC法同时测定乌杞明目口服液中6种成分[J].中成药,2014,36(8):1652-1656.
(编辑:刘 柳)
Simultaneous Determination of Paeoniflorin and SalvianolicAcid B in Ruangan Suopi Pill by HPLC
LIU Dong,SONG Xiaohong,TANG Changming,WANG Lijun,ZHANG Jianbang(Dept.of Preparation,No.153 Central Hospital of PLA,Zhengzhou 450042,China)
OBJECTIVE:To establish a method for simultaneous determination of paeoniflorin and salvianolic acid B in Ruangan suopi pill.METHODS:HPLC was performed on the column of Wondasil C18with mobile phase of acetonitrile-0.1%phosphoric acid solution(gradient elution)at a flow rate of 1.0 mL/min,the detection wavelength was 230 nm for paeoniflorin and 286 nm for salvianolic acid B,the column temperature was 30℃,and the injection volume was 10 μL.RESULTS:The linear range was 9.79-195.80 μg/mL(r=0.999 9)for paeoniflorin,11.45-229.00 μg/mL(r=0.999 9)for salvianolic acid B;the limits of quantification were 0.018 1,0.014 4 μg,limits of detection were 0.005 4,0.004 3 μg;RSDs of precision,stability and reproducibility tests were lower than 2.0%;the recoveries were 98.67%-102.22%(RSD=1.26%,n=9)and 99.72%-103.28%(RSD=1.05%,n=9). CONCLUSIONS:The method is rapid,sensitive and accurate,and can be used for the simultaneous determination of paeoniflorin and salvianolic acid B in Ruangan suopi pill.
Ruangan suopi pill;Paeoniflorin;Salvianolic acid B;Content determination;HPLC
R917
A
1001-0408(2017)03-0416-03
2016-01-30
2016-07-16)
*主管药师,硕士。研究方向:医院制剂研发与质量控制。E-mail:liudong13673546650@163.com
DOI10.6039/j.issn.1001-0408.2017.03.36
