托瑞米芬对比他莫昔芬治疗乳腺癌安全性的系统评价Δ
2017-03-03成都市第三人民医院西药科成都610031
兰 瑛,胡 蝶,何 琴(成都市第三人民医院西药科,成都 610031)
托瑞米芬对比他莫昔芬治疗乳腺癌安全性的系统评价Δ
兰 瑛*,胡 蝶,何 琴(成都市第三人民医院西药科,成都 610031)
目的:系统评价托瑞米芬对比他莫昔芬治疗乳腺癌的安全性,为临床提供循证参考。方法:计算机检索Medline、PubMed、EMBase、Cochrane图书馆、中国期刊全文数据库、中国生物医学文献数据库、中文科技期刊数据库和万方库数据库,收集托瑞米芬对比他莫昔芬治疗乳腺癌安全性的随机对照研究(RCT)及队列研究,提取资料并评价质量后,采用Rev Man 5.0统计软件进行Meta分析。结果:共纳入10项RCT和9项回顾性队列研究,合计9 182例患者。Meta分析结果显示,托瑞米芬组患者总体药品不良反应发生率与他莫昔芬组比较差异无统计学意义[RR=0.88,95%CI(0.73,1.06),P=0.18];按托瑞米芬剂量进行亚组分析显示,常规剂量和高剂量托瑞米芬组患者与他莫昔芬组比较差异均无统计学意义。托瑞米芬组患者严重不良反应发生率与他莫昔芬组比较差异无统计学意义[OR=0.60,95%CI(0.23,1.52),P=0.28]。常规剂量托瑞米芬组患者血栓事件发生情况[OR=0.77,95%CI(0.60,0.98),P=0.03]、消化系统不良反应发生情况[OR=0.81,95%CI(0.70,0.94),P=0.006]、月经不规则的发生率[OR=0.61,95%CI(0.39,0.94),P=0.03]、出现发热伴/不伴寒战情况[OR=0.56,95%CI(0.34,0.92),P=0.02]等方面均优于他莫昔芬组,差异均有统计学意义。高剂量托瑞米芬组患者对比他莫昔芬的各类不良反应发生情况,差异均无统计学意义。结论:相较于他莫昔芬,常规剂量托瑞米芬治疗乳腺癌时在消化道不良反应、血栓事件、月经不规则、发热伴/不伴寒战等药品不良反应方面安全性较好。
托瑞米芬;他莫昔芬;乳腺癌;安全性;系统评价
乳腺癌是中国女性发病率最高的癌症。每年中国乳腺癌新发数量和死亡数量分别占全世界的12.2%和9.6%[1]。乳腺癌的治疗仍是以手术、放疗、化学药物治疗为主要方式。由于乳腺癌是一种由雌激素驱动的依赖性肿瘤,因此选择雌激素受体调节剂(SERMs)等内分泌治疗药物已成为乳腺癌综合治疗的重要手段,此类药物通过改变女性患者体内雌激素与孕激素水平,从而减弱肿瘤诱导性生长。国家食品药品监督管理总局批准他莫昔芬用于治疗女性复发转移性乳腺癌及用作乳腺癌手术后转移的辅助治疗、预防复发;托瑞米芬用于绝经后妇女雌激素受体阳性或不详的转移乳腺癌治疗。有研究显示,二者在乳腺癌治疗的有效性上无统计学差异[2]。近年来,有关文献报道长期使用他莫昔芬可引起子宫内膜癌、肺栓塞、深静脉血栓、脑卒中、肝脏毒性、视力损害等不良反应[3]。而托瑞米芬作为新一代SERMs在安全性上与他莫昔芬相比缺乏可靠证据。虽然,目前已有多个仅基于随机对照试验(RCT)的系统评价对二者的安全性差异进行研究,但纳入文献类型局限,纳入文献数量较少,部分文献发表时间较早,研究结果存在矛盾,因此本研究采用扩大纳入研究类型的方式对托瑞米芬对比他莫昔芬治疗乳腺癌的安全性进行系统评价,旨在为临床提供循证参考。
1 资料与方法
1.1 纳入与排除标准
1.1.1 研究类型 国内外公开发表的RCT,不论是否采用盲法或分配隐藏均纳入研究;国内外公开发表的队列研究,不论是前瞻性或回顾性均纳入研究。语种限定为中文和英文。
1.1.2 研究对象 根据我国乳腺癌诊疗规范[4]、美国国家综合癌症网乳腺癌临床实践指南等国内外权威指南[5-6]及病理检查诊断为乳腺癌且雌激素受体检测阳性或未知者。两组患者年龄、性别、国籍、种族、乳腺癌分期均不限。
1.1.3 干预措施 托瑞米芬组:给予托瑞米芬40~60 mg/次(常规剂量组),1日1次,口服或100~120 mg/次(高剂量组),1日2次,口服;他莫昔芬组:给予他莫昔芬10~20 mg/次,1日2次,口服。两组均进行常规对症支持治疗。治疗时间均≥28 d。
1.1.4 结局指标 主要结局指标:总体药品不良反应发生率、严重药品不良反应发生率;次要结局指标:各类不良反应发生率(如恶心呕吐、子宫内膜增生、肝功能异常、血脂异常等)。对药品不良反应、严重药品不良反应的认定按文献描述或我国《药品不良反应报告和监测管理办法》进行认定。
1.1.5 排除标准 ①排除存在混杂因素研究,如联合使用其他乳腺癌内分泌治疗药物、化疗药物的研究,受其他药物影响或疾病影响无法判断安全性或不良反应归属的研究,各组间基线存在显著性差异的研究等;②排除数据无法提取的研究;③排除体外实验、动物实验研究等;④排除未明确描述安全性或不良反应的研究。
1.2 检索策略
计算机检索Medline、PubMed、EMBase、Cochrane图书馆、中国期刊全文数据库、中国生物医学文献数据库、中文科技期刊数据库、万方数据库,检索时限均为各数据库建库起至2014年12月。采用主题词与自由词相结合的方式,并根据具体数据库调整,中文检索词包括“托瑞米芬”“他莫昔芬”“三苯氧胺”“乳腺癌”;英文检索词包括“Toremifene”“Acapodene”“Tamoxifen”“Breast cancer”“Breast tumor”“Breast neoplasms”等。同时,追溯纳入文献及相关综述的参考文献,以降低漏检的可能性。获得的文献导入文献管理软件Endnote X6进行管理。
1.3 文献筛选和资料提取
由两位研究者独立完成文献的筛选,对筛选后的文献进行资料提取,并进行交叉核对,对于任何有差异的资料通过查找研究文献后讨论解决。
1.4 质量评价
RCT根据Cochrane系统评价员手册5.0.1版的文献质量评价方法对纳入文献的偏倚风险进行评估,评估内容包括以下6个方面:1)随机方法是否正确;2)是否做到分配隐藏;3)是否实施盲法;4)结果数据是否完整;5)是否存在选择性报道偏倚;6)是否存在其他偏倚。
队列研究的质量评价采用文献质量评价量表(NOS)评估纳入文献的偏倚风险,包括研究人群选择(4个条目,4分)、组间可比性(1个条目,2分)、结果测量(3个条目,3分)三个部分,共8个条目,满分为9分,评价后分数越高则说明研究质量越高。7分及以上为高质量研究,5~7分为中等质量研究,4分及以下为低质量研究。
1.5 统计学方法
采用Rev Man 5.0统计软件进行Meta分析。计数资料采用相对危险度(RR)或比值比(OR)为效应分析统计量;计量资料采用均数差(MD)为效应分析统计量,区间估计采用95%置信区间(CI)表示。采用χ2检验分析各研究间的异质性。若各研究结果间无统计学异质性(P>0.10,I2≤50%),则采用固定效应模型进行分析;反之,采用随机效应模型进行Meta分析。此外,若异质性过大(I2≥75%),则只进行描述性分析,必要时采用敏感性分析检验结果的稳定性。P<0.05为差异有统计学意义。
2 结果
2.1 检索结果
初检出1 551篇中英文文献,排除重复文献,余下1 003篇文献;进一步根据纳入与排除标准,阅读题目、摘要后筛选出59篇,经过阅读全文,最终纳入19篇(项)研究[7-25]。
2.2 纳入研究基本信息
纳入的19项研究,合计9 182例患者,其中RCT 10项,回顾性队列研究9项;托瑞米芬常规剂量组累计3 851例患者,高剂量组累计369例患者;他莫昔芬组累计4 962例患者。样本量最大的两个研究分别纳入1 847[21]、1 813[15]例患者,样本量最小的研究纳入58例患者[17];研究时间最长的为5.5年[13,23],最短的为28 d[7]。
2.3 方法学质量评价结果
对10项RCT进行了方法学质量评价[7-13,15,23,25],结果见图1。由图1可知,1项研究为高质量研究[10],其余研究均存在不同程度偏倚风险;仅3项研究描述了随机序列按照计算机随机等方法产生[10-11,25],其余研究仅表示为RCT但未详细描述随机方法;8项研究为多中心研究,进行了随机序列分配隐藏[8-11,13,15,23,25];仅3项研究表示进行了盲法,但均未描述是何种盲法[7,10,12];1项研究由于失访率>20%[15],认为结果数据可能存在不完整性;1项研究仅报道了各组药品不良反应发生总例数,未具体描述不良反应类型[7]。

图1 纳入随机对照试验的偏倚风险评价Fig 1 The risk evaluation of bias of included RCT
9项回顾性队列研究根据NOS文献质量评价量表进行方法学质量评价[14,16-22,24]。9项研究均未实施盲法,1项研究观察终止时失访率超过40%[16],1项研究疗程描述不清[24];1项研究评为8分[16],1项研究为7分[24],其余7项研究评为9分[14,17-22],均为高质量队列研究。
3 Meta分析结果
3.1 总体药品不良反应发生率
4项研究报道了总体药品不良反应发生率[7,10,19,24]。各研究间无统计学异质性(P=0.39,I2=1%),采用固定效应模型进行分析,详见图2。Meta分析结果显示,托瑞米芬组患者总体药品不良反应发生率与他莫昔芬组比较差异无统计学意义[RR=0.88,95%CI(0.73,1.06),P=0.18]。按托瑞米芬剂量进行亚组分析显示,常规剂量托瑞米芬组患者与他莫昔芬组比较差异无统计学差异[RR=0.86,95%CI(0.71,1.03),P=0.11];高剂量托瑞米芬组患者与他莫昔芬组比较,差异亦无统计学差异[RR=1.60,95%CI(0.59,4.35),P=0.36]。
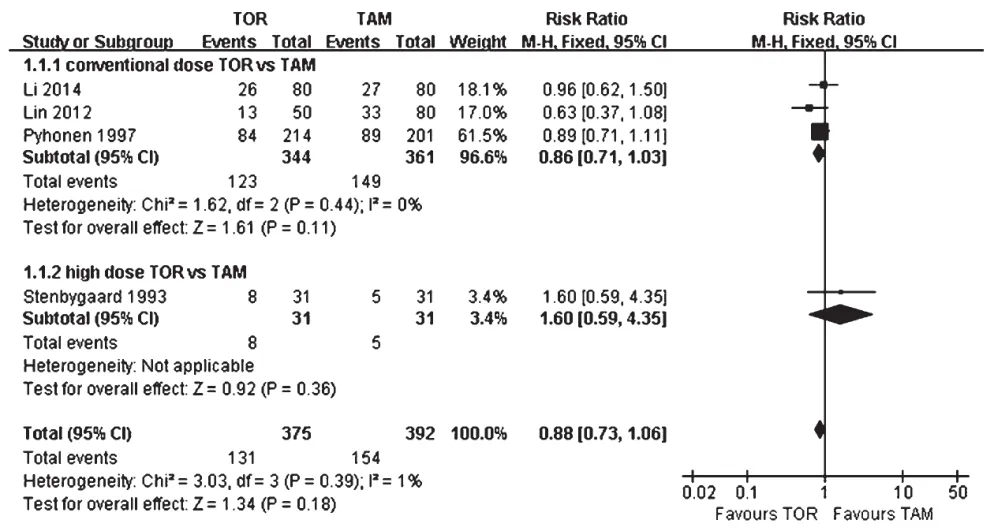
图2 两组患者总体药品不良反应发生率的Meta分析森林图Fig 2 Forest plot of Meta-analysis of the incidence of overall adverse reactions in 2 groups
3.2 严重药品不良反应发生率
2项研究报道了各组患者严重药品不良反应发生率[10,19]。托瑞米芬组剂量均为常规剂量。各研究间无统计学异质性(P=0.94,I2=0),采用固定效应模型进行分析,详见图3。Meta分析结果显示,托瑞米芬组患者严重不良反应发生率与他莫昔芬组比较差异无统计学意义[OR=0.60,95%CI(0.23,1.52),P=0.28]。
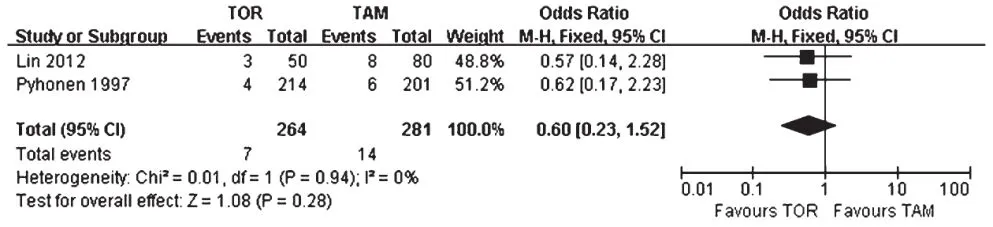
图3 两组患者严重药品不良反应发生率的Meta分析森林图Fig 3 Forest plot of Meta-analysis of the incidence of serious adverse reactions in 2 groups
3.3 各类不良反应发生情况
3.3.1 常规剂量托瑞米芬对比他莫昔芬 各类不良反应中,两组发生率均>10%的不良反应为抑郁、脂肪肝、恶心呕吐、腹泻、子宫内膜增生、子宫内膜息肉、阴道分泌物异常、白带增加、阴道干燥、绝经期症状、皮肤瘙痒、骨痛、发热/潮热、盗汗、肝功能损害等。把不良反应按照一定的事件和系统进行加下分类。
8项研究报道了血栓事件发生情况[8-13,15,21],各研究之间无统计学异质性(P>0.10,I2=0%),采用固定效应模型进行分析。Meta分析结果显示,常规剂量托瑞米芬组患者血栓事件发生情况显著少于他莫昔芬组,差异有统计学意义[OR=0.77,95%CI(0.60,0.98),P=0.03]。
共计11项研究报道了消化系统不良反应发生情况[8-12,14,18-19,21-23],各研究之间无统计学异质性(P>0.10,I2<20%),采用固定效应模型进行分析。Meta分析结果显示,常规剂量托瑞米芬组患者消化系统不良反应发生情况显著少于他莫昔芬组,差异有统计学意义[OR=0.81,95%CI(0.70,0.94),P=0.006]。
在神经系统、心脏、眼科、皮肤、骨骼关节、新发肿瘤、一般不良反应等不良反应发生率,以及引起实验室指标(转氨酶、碱性磷酸酶、胆红素、血脂指标等)改变等方面,两组比较差异均无统计学意义(P>0.05);但在出现发热伴/不伴寒战的事件方面,常规剂量托瑞米芬组患者显著低于他莫昔芬组,差异有统计学意义[OR=0.56,95%CI(0.34,0.92),P=0.02]。各类妇科不良反应中,在月经不规则的发生率方面常规剂量托瑞米芬组患者显著低于他莫昔芬组,差异有统计学意义[OR=0.61,95%CI(0.39,0.94),P=0.03];其余各类妇科不良反应发生率二者差异均无统计学意义(P>0.05)。
3.3.2 高剂量托瑞米芬对比他莫昔芬 仅2项研究报道了高剂量托瑞米芬与他莫昔芬的对比研究[8-9]。各类不良反应中,两组发生率均>5%的不良反应为头晕、白内障、眼干、恶心、阴道分泌物异常、潮热、水肿等,且两组在上述各不良反应发生情况方面差异均无统计学意义(P>0.05)。
4 讨论
托瑞米芬组患者总体药品不良反应发生率、严重不良反应发生率与他莫昔芬组比较差异无统计学意义;常规剂量托瑞米芬组患者血栓事件发生情况、消化系统不良反应发生情况、月经不规则的发生率、出现发热伴/不伴寒战情况等方面均优于他莫昔芬组,差异有统计学意义。高剂量托瑞米芬组患者对比他莫昔芬组的各类不良反应发生情况,差异均无统计学意义(P>0.05)。本研究对于临床关注较多的该类药品可引起子宫内膜癌、肺栓塞、深静脉血栓、脑卒中、肝脏毒性、视力损害等,并未发现托瑞米芬组患者与他莫昔芬组在上述不良反发生率上存在显著性差异。
本研究可能存在的一定局限性:(1)对于托瑞米芬目前较多应用于亚洲国家,特别是日本,但由于语言的限制,未纳入以日文发表的大量研究,因此结果可能存在发表偏倚风险。(2)本研究显示,托瑞米芬与他莫昔芬在引起月经不规则、发热伴/不伴寒战等不良反应存在显著性差异,各项下均只纳入了1篇样本量较大的研究。在血栓事件及消化系统不良反应中,各亚组药品不良反应(即各个分散的药品不良反应)上二者均无显著性差异,但总合并效应量存在显著性差异,可能由于单项不良反应项下纳入研究较少,样本量较小,在合并分析后,样本量扩大使检验效能增加引起。因此,笔者认为本研究结果可靠性仍需进一步考证。(3)本研究纳入的患者中仅1名为男性乳腺癌患者,对于雌激素受体调节剂治疗乳腺癌的安全性问题偏重于对女性的研究(比如妇科不良反应),对男性患者存在的特殊的安全性风险(比如生殖方面)还未见报道,也提示今后可对该领域进一步开展深入研究。
综上所述,相较于他莫昔芬,常规剂量托瑞米芬在治疗乳腺癌时在消化道不良反应、血栓事件、月经不规则、发热伴/不伴寒战等药品不良反应方面安全性较好,其余方面二者安全性相当;且高剂量托瑞米芬与他莫昔芬的安全性相当。由于纳入文献数量有限,结果仍需大量研究进行证明。
[1] Fan L,Strasser-Weippl K,Li JJ,et al.Breast cancer in China[J].Lancet Oncol,2014,15(7):279-289.
[2] Ye QL,Zhai ZM.Toremifene and tamoxifen have similar efficacy in the treatment of patients with breast cancer:a meta-analysis of randomized trials[J].Mol Biol Rep,2014,41(2):751-756.
[3] Osborne CK.Tamoxifen in the treatment of breast cancer [J].N Engl J Med,1998,339(22):1609-1618.
[4] National comprehensive cancer network.NCCN clinical practice guidelines in oncology:breast cancer(version 2.2016)[EB/OL].(2005-06-16)[2015-05-10].http:// www.nccn.org/.
[5] 国家卫生和计划生育委员会.关于印发胃癌等五种恶性肿瘤规范化诊疗指南的通知[EB/OL].(2013-04-23)[2015-06-10].http://www.nhfpc.gov.cn/.
[6] 中华医学会.临床治疗指南肿瘤分册[M].北京:人民卫生出版社,2005:139-179.
[7] Stenbygaard LE,Herrstedt J,Thomsen JF,et al.Toremifene and tamoxifen in advanced breast cancer-A doubleblind cross-over trial[J].Breast Cancer Res Treat,1993,25(1):57-63.
[8] Hayes DF,Zyl JAV,Hacking A,et al.Randomised comparison of tamoxifen and two separate doses of toremifene in postmenopausal patients with metastatic breast cancer [J].J Clin Oncol,1995,13(10):2556-2566.
[9] Gershanovich M,Garin A,Baltina D,et al.A phaseⅢcomparison of two toremifene doses to tamoxifen in postmenopausalwomen with advanced breastcancer[J]. Breast Cancer Res Treat,1997,45(3):251-262.
[10] Pyrhönen S,Valavaara R,Modig H,et al.Comparison of toremifene and tamoxifen in postmenopausal patients with advanced breast cancer:a randomized double-blind,the‘nordic’phaseⅢstudy[J].Br J Cancer,1997,76(2):270-277.
[11] Holli K,Valavaara R,Blanco G,et al.Safety and efficacy results of a randomized trial comparing adjuvant toremifene and tamoxifen in postmenopausal patients with node-positive breast cancer[J].J Clin Oncol,2000,18(20):3487-3494.
[12] Milla-Santos A,Milla L,Rallo L,et al.PhaseⅢrandomized trial of toremifene vs tamoxifen in hormonodependant advanced breast cancer[J].Breast Cancer Res Treat,2001,65(2):119-124.
[13] Pagani O,Gelber S,Price K,et al.Toremifene and tamoxifen are equally effective for early-stage breast cancer:first results of International Breast Cancer Study Group Trials 12-93 and 14-93[J].Ann Oncol,2004,15(12):1749-1759.
[14] 田丽军,徐兵河.托瑞米芬和他莫昔芬对血脂影响的对比研究[J].实用癌症杂志,2004,19(5):520-522.
[15] Lewis JD,Chagpar AB,Shaughnessy EA,et al.Excellent outcomes with adjuvant toremifene or tamoxifen in early stage breast cancer[J].Cancer,2010,116(10):2307-2314.
[16] 张琳,林红.早期乳腺癌患者术后应用托瑞米芬和他莫昔芬的对比研究[J].当代医学,2010,16(16):36-37.
[17] 卢强.他莫昔芬与托瑞米芬治疗复发或转移性乳腺癌的临床对比研究[J].当代医学,2011,17(26):128-129.
[18] Gu R,Jia W,Zeng Y,et al.A comparison of survival outcomes and side effects of toremifene or tamoxifen therapy in premenopausal estrogen and progesterone receptor positive breast cancer patients:a retrospective cohort study[J].BMC Cancer,2012,12(1):1-10.
[19] 林燕,陶红慧,严楚顺,等.他莫昔芬与托瑞米芬治疗乳腺癌的经济学分析[J].中国医院用药评价与分析,2012,12(4):330-332.
[20] 张琳.他莫昔芬和托瑞米芬在ER(+)乳癌患者中的疗效差异[J].当代医学,2012,18(3):20-21.
[21] Qin T,Yuan ZY,Peng RJ,et al.Efficacy and tolerabilityof toremifene and tamoxifen therapy in premenopausal patients with operable breast cancer:a retrospective analysis [J].Curr Oncol,2013,20(4):196-204.
[22] 伍楚蓉,唐武兵,杨文,等.乳腺癌患者化疗后内分泌治疗并发脂肪肝的发病因素分析[J].广东医学,2013,34(22):3411-3413.
[23] Kimura M,Tominaga T,Kimijima I,et al.PhaseⅢrandomized trial of toremifene versus tamoxifen for Japanese postmenopausalpatientswith early breastcancer[J]. Breast Cancer,2014,21(3):275-283.
[24] 李莉,王建军.枸橼酸托瑞米芬治疗管腔上皮型乳腺癌年轻患者的疗效与安全性研究[J].检验医学与临床,2014,11(18):2521-2522、2531.
[25] Parkkari M,Paakkala AM,Salminen L,et al.Ocular side-effects in breast cancer patients treated with tamoxifen and toremifene:a randomized follow-up study[J].Acta Ophthalmol Scand,2003,81(5):495-508.
Safety of Toremifene versus Tamoxifen in the Treatment of Breast Cancer:ASystematic Review
LAN Ying,HU Die,HE Qin(Dept.of Western Medicine Pharmacy,the Third People’s Hospital of Chengdu,Chengdu 610031,China)
OBJECTIVE:To systematically review the safety of toremifene versus tamoxifen in the treatment of breast cancer,and provide evidence-based reference for clinic.METHODS:Retrieved from Medline,PubMed,EMBase,Cochrane Library,CJFD,CBM,VIP and Wanfang Database,randomized controlled trails(RCT)and cohort study about toremifene versus tamoxifen in the treatment of breast cancer were collected.Meta-analysis was performed by using Rev Man 5.0 software after data extraction and quality evaluation.RESULTS:Totally 10 RCTs and 9 retrospective cohort studies were enrolled,involving 9 182 patients.Results of Metaanalysis showed,compared with tamoxifen group,there was no significant difference in the incidence of overall adverse reactions in toremifene group[RR=0.88,95%CI(0.73,1.06),P=0.18];the subgroup analysis based on the dose of toremifene showed,compared with tamoxifen group,there were no significant differences in conventional dose group and high-dose group.Compared with tamoxifen group,there was no significant difference in the incidence of serious adverse reactions in toremifene group[OR=0.60,95%CI(0.23,1.52),P=0.28].The incidences of thrombotic events[OR=0.77,95%CI(0.60,0.98),P=0.03],adverse reactions in the digestive system[OR=0.81,95%CI(0.70,0.94),P=0.006],irregular menstruation[OR=0.61,95%CI(0.39,0.94),P=0.03]and fever with or without chills[OR=0.56,95%CI(0.34,0.92),P=0.02]in toremifene conventional dose group were superior to tamoxifen group,with statistical significance.Compared with tamoxifen group,there were no significant difference in the incidence of various types of adverse reactions in toremifene high-dose group.CONCLUSIONS:Compared with tamoxifen,conventional dose of toremifene shows better safety in terms of adverse reactions in the digestive system,thrombotic events,irregular menstruation,fever with or without chills and other adverse reactions in the treatment of breast cancer.
Toremifene;Tamoxifen;Breast cancer;Safety;Systematic review
R737.9
A
1001-0408(2017)03-0360-05
2016-01-30
2016-09-11)
(编辑:刘 柳)
四川省预防医学会药物应用安全科研(孵化)项目(No.川预学〔2013〕70号)
*主管药师。研究方向:临床药学。电话:028-61318605。E-mail:lanying0212@126.com
DOI10.6039/j.issn.1001-0408.2017.03.21
