临床研究数据管理策略
2017-03-01综述审校
张 嵬(综述) 应 峻,2△(审校)
(1复旦大学图书馆 上海 200032; 2复旦大学循证医学中心 上海 200032)
临床研究数据管理策略
张 嵬1(综述) 应 峻1,2△(审校)
(1复旦大学图书馆 上海 200032;2复旦大学循证医学中心 上海 200032)
临床研究中产生的大量医学数据使临床科研人员逐渐认识到数据长期保存和共享的重要性,进而在实践中形成了研究数据管理的理念和方法。临床研究数据管理,可以促进临床研究的准确和高效进行,满足研究人员、机构、研究资助者的预期和要求。本文通过单个临床研究数据管理和机构临床研究数据管理两个层面,讨论了临床研究数据管理的关键事项及相关策略,帮助临床科研人员及科研管理人员了解临床研究数据管理流程,促进临床科研活动规范执行和机构数据管理的发展。
临床研究; 数据管理; 机构知识库; 数据仓储库
随着网络技术的不断进步、医学相关研究数量的不断增加,临床研究数据也呈现海量增长的态势,但伴随而来的研究低效率重复、研究数据质量缺陷、研究数据孤岛化等问题也不断显现,科研人员逐渐认识到:重要的研究数据必须能够长期保存并合理共享,这样不仅可以推进研究进展、促进研究知识更快的累积,同时还可以最大限度地提高科研经费的投资回报。鉴于此,研究数据管理(research data management,RDM)的理念和方法日益得到重视,并在实践中迅速发展。
研究数据管理,是指对研究数据进行获取、计划、组织、存档、共享、分析、利用、保护等与数据相关的所有管理活动的总称[1]。它属于研究进程的一部分,但又贯穿整个研究周期,它的主要目标是保证研究尽可能准确和高效,满足研究人员、机构、研究资助者的预期和要求。临床医学是科研最活跃的学科之一,也是最关注效率和精准的学科之一,因此对采用规范化的流程保证临床研究数据的完整性和准确性,具有更为迫切的需求。而临床研究数据管理,就是针对临床研究数据进行的数据管理活动。
本文通过单个临床研究的数据管理和机构临床研究数据管理两个层面,对临床研究数据管理的关键事项进行讨论,帮助临床科研人员及科研管理人员熟悉临床研究数据管理的流程,促进临床科研活动的规范执行,从而获得高质量的科研成果,并通过合理的分享,使成果更快地被本领域或其他领域相关人员所认知和利用。
单个临床研究的数据管理 单个临床研究的数据管理,是针对具体某个临床研究所采取的全部数据管理活动。国家食品药品监督管理总局为确保临床试验数据的真实、准确、完整和可靠,强化药物临床研究的自律性和规范性,于2016年7月发布了《临床试验数据管理工作技术指南》[2],可以作为临床研究数据管理工作的重要参考。单个临床研究数据管理的主要流程见图1,详述如下:
临床研究方案的制订 临床研究方案是临床科研项目的核心,一个科学完备的临床研究方案是整个临床研究高质量进行的基础和保证。它是整个研究数据管理流程的开始,其中涉及数据采集的内容和方式、数据质量的保证措施、数据分享和传播的方法等。在制订临床研究方案过程中,可以参照《药物临床试验质量管理规范》[3]或SPIRIT指南[4]中推荐的模块和架构。
临床研究注册 《世界医学协会赫尔辛基宣言》指出“在第一个主体募集前,每个临床试验都必须在可公开访问的数据库中注册”,这同时也是高质量临床研究发表的必须条件之一。接受临床注册的机构主要有美国NIH的ClinicalTrails.gov[5]和WHO的ICTRP(International Clinical Trials Registry Platform)[6],国内也可以通过WHO一级注册机构中国临床试验注册中心(Chinese Clinical Trials Registry,ChiCTR)[7]注册。注册时除了在线填写研究项目的基本信息外,通常还需要提供研究方案、伦理审查批件以及受试者知情同意书等相关文件。

图1 单个临床研究的数据管理流程图
Fig 1 Flow chart of data management in individual clinical research
制订数据管理计划 数据管理计划(data management plan,DMP)是在项目正式启动前制订的、描述整个项目周期内数据处理及相关质控的规范性文档,主要包括项目进展中以及在项目结题后数据收集、数据创建、数据组织、数据处理、数据存储、数据共享和数据复用的全过程[8],其主要目的是保证研究数据的准确性和完整性。在药物上市前的注册临床试验中,DMP早已成为必不可少的关键文档,但在临床研究中近年才得到重视。如美国国立医学卫生研究院(National Institute of Health,NIH)[9]、美国国家科学基金会(National Science Foundation,NSF)[10]等机构要求科研人员在提交项目申请时,必须提交研究数据管理计划。目前在国内临床研究项目申报过程中尚无此项规定,但随着国内临床研究数量及资助资金的飞速增长,对研究数据的质量要求将是必然的趋势,而DMP就是其中非常重要的环节。在制订数据管理计划时,可以参考两个现有的工具:加利福尼亚大学开发的DMPTool和英国DCC(Digital Curation Central)开发的DMPonline。
临床研究数据采集 多数临床研究从研究对象入组、随访直至研究结束,都需要较长的周期,从数月到数年。特别是在大数据背景下,临床科研人员更希望对大量试验对象进行长期、动态、实时的随访跟踪,从中发现和捕获影响疾病诊断、发生、发展、治疗和预后的关键因素。因此,快速准确地采集临床研究数据显得尤为重要。
临床研究方案中涉及的、与试验研究目的相关的所有临床信息,一般都会通过病例报告表(case report form,CRF)收集。因此CRF设计的科学性和规范性在很大程度上决定了研究的质量甚至成败。设计良好的CRF通常页面布局清晰易懂、随访流程条理顺畅、字段设计和编码符合相应标准,易于建立电子数据库并进行统计分析。传统依靠纸质CRF来收集临床数据的方式采集周期长,中间环节多,且无法保证数据的可靠性和安全性,CRF中的数据最终需数字化才能进行统计分析,但目前我国临床实践中CRF数字化的水平参差不齐。
电子数据采集(electronic data capture,EDC)系统,不论是基于本地的单机采集系统,还是基于网络的云存储系统,都是值得推荐的临床数据采集方式。本地单机采集系统,最常用的如免费版本的EpiData,简单易学且提供较完备的基础功能,包含数据双录入核对、数据逻辑检查、支持多种数据导出格式(EXCEL、STATA、SAS)等。但本地单机采集系统也存在一些诸如处理多中心研究数据时较为复杂、数据修改无法留痕、缺乏权限限定导致的安全问题等缺陷。对于多中心、较为复杂的临床研究,通常使用基于网络的云存储系统,数据库统一存储在服务器云端,各中心录入人员只需通过浏览器登陆即可录入数据。大多数云存储EDC系统,除了提供基础的录入功能,还会提供更为全面的权限控制、逻辑检查、数据溯源等功能,甚至可以提供整合随机化等其他专业功能。网络云存储EDC系统功能强大,但建库和维护的成本也较高,通常需要委托专门的公司或者学术机构进行管理。目前其种类较多,国内外均有不同的自主研发或商业类产品,国内多家公司或研究机构也使用不同的系统,选择时需考虑系统的稳定性和成熟性,是否经过多个项目的临床研究验证,以及相关技术人员的资质水平等因素。
临床研究数据核查 对于一个高质量、数据容错率较低的临床研究,即使是双录入后的研究数据,同样也需要系统全面的核查,核查的目的是确保数据的完整性、有效性和正确性。《临床试验数据管理工作技术指南》[2]规定,数据核查内容包括但不局限于:确定原始数据被正确且完整地录入到数据库、随机化核查、违背方案核查、时间窗核查、逻辑核查、范围核查、一致性核查等。
研究数据的统计分析以及文章发表 这部分通常不属于研究数据管理的范畴,但却是研究数据管理质量最好的体现和检验。规范的操作流程应在试验完成前由研究者和统计分析人员共同制订统计分析方案(statistical analysis plan,SAP),在试验结束后由统计分析人员完成统计分析报告(statistical analysis report,SAR),进而由研究者完成临床研究报告(clinical study report,CSR)或撰写文章发表。
研究数据的保存和共享 临床研究结束后,如果研究数据得到妥善保存并能够被重复利用,不但对于研究者本身,对于整个科研机构,甚至对于整个专业领域,都具有积极意义。而数据共享、开放存取更是目前大势所趋,其不但可以提高研究的效率和可信度,增强研究数据跨领域利用、引用与影响,更是研究者的义务和责任[11]。很多杂志在投稿时,需要投稿者提供原始数据仓储的位置和方式,甚至数据集的DOI。
机构临床研究数据管理 机构临床研究数据管理更加关注宏观层面,着力于系统全面存储整个临床科研机构的科研成果,并且能够为整个机构临床研究数据集提供保存与共享服务。机构临床研究数据管理便于研究者更好地管理自身已完成或正在进行中的科学研究项目、建立学者个性化档案、提高学术影响力,更是科研管理部门评价研究者、研究部门、研究机构学术水平和学科发展水平的重要工具,同时也有利于机构科研政策和科研发展方向的制订,推动整个机构科研水平的发展。机构临床研究数据管理主要通过机构临床研究知识系统实现,如图2所示,其包括临床科研机构知识库和临床研究数据仓储库两个子系统,子系统之间可以互相读取和链接。
临床科研机构知识库 机构知识库(institutional repository,IR)作为收集、存储与传播某个或多个学术机构(例如大学、研究所、图书馆、博物馆等)所创造的、可供机构内外用户共享的学术文献数据库,具有协助教育科研机构知识资产保存和知识管理的重要作用[12]。在科研机构知识库中,针对单一研究者而言,其所有的研究成果,包括期刊论文、图书、报告、视频、音频、教学参考书等,都将分类展示和保存。而针对同一机构中不同层级的部门,相应的科研成果可以逐级汇总展示,形成个人数据、项目数据、机构数据的层次化展示结构。通过科研机构知识库,整个科研机构的研究成果得到专业的组织管理和揭示,可以作为评价科研机构科研现状和水平的证据参考,同时也可避免图书期刊出版者设置的访问权限制约。虽然科研机构知识库的重要性已得到普遍认可,但由于起步较晚,我国科研机构知识库的发展尚处于初级阶段,虽然目前国内多家科研机构知识库已经投入使用,绝大多数科研机构知识库只提供基础的功能框架,需要用户自行上传数据,相应的学习成本和人力成本较高,主动上传率低;同时受语言和标准限制,尚不能很好地与国际进行接轨。
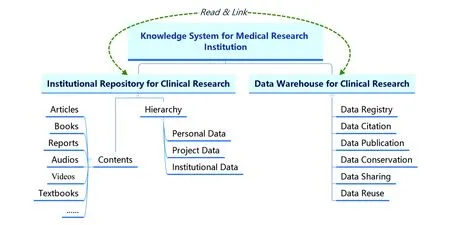
图2 机构临床研究知识系统架构
Fig 2 Infrastructure of knowledge system for medical research institution
未来机构知识库的发展,首先需要依托计算机科学技术的发展,综合人工智能、机器语言、数据库技术以及统计分析方法等数据挖掘技术,自动抓取和上传机构知识库中大部分数据内容,仅辅以人工干预;其次,机构知识库需要配合整个科研项目的运行流程,进行深度的嵌入和融合,内容架构灵活、扩展性强,可以在运行过程中不断完善和发展;第三,科研机构知识库需要考虑不同学科的特点,构建符合专业需求的科研机构知识库。如果以医学院系作为科研知识库的一级单位,并针对临床医学研究特点建设数据库的内容和架构,就可以构建相应的临床科研知识机构库;最后,机构库知识库应该具有多角度、多层级、多检索入口、多系统兼容的结果展示模块,以及功能强大的学科分析模块,不但能够客观全面地揭示整个机构的科研现状,而且可以为科研决策提供清晰有效的支持。
临床研究数据仓储库 当前各国基金组织、学术期刊、研究机构普遍采用的研究数据管理政策是鼓励研究人员将数据存储到所属学科的权威数据仓储库或公认的综合数据仓储库[13],如存储基因芯片数据的Array Express或GEO,存储生态学数据的Dryad。但考虑到某些公共数据仓储库需要按项目收费以及不同机构仓储的个性化需求,国外很多大学或研究机构开始着手建设机构科研数据仓储库,马建玲等[14]的研究显示U.S.News排名前50名的大学中有17所大学图书馆已经开展了与研究数据管理相关的服务。
建立临床研究数据仓储库,便于对临床机构的数据集的注册和引用。与临床研究注册类似,数据集通过注册被分配了唯一标识符,可以使科学数据成为独立的、可引用的、唯一的科学对象,便于科学数据的发现、引用和跟踪[15]。目前很多杂志在投稿时,需要投稿者提供原始数据仓储的位置和共享方式,Hrynaszkiewicz等[16]重点阐述了不同试验设计原始临床研究数据的出版指导原则,包括数据集内容的最小要求以及共享方式等。此外,建立临床研究数据仓储库,更加符合医学研究海量数据背景的特点,有利于将临床科研过程中产生的数据进行系统有序的保存和重新利用。
鉴于临床研究数据仓储库的特点,构建过程中需要无缝结合数据存储的软件技术和硬件技术。软件技术层面,在对数据进行结构化建模和建立相应元数据对象描述和标注的基础上,能够很好处理非结构、半结构化数据,具有灵活配置数据类型、标示、权限、仓储格式、属性等相关信息的能力,最大限度实现数据的完整性和可操作性;硬件层面,采用云端存储、分布访问的方式,应用性能强大、易于管理、灵活扩展、运行稳定的数据存储介质,保证仓储数据的高速访问和全时访问。
结语 临床医学由于与人类的健康息息相关,相应的研究极其活跃,因此对于数据的完整性和准确性具有更高的要求,同时对数据共享和重新利用的需求也极为迫切。对临床研究数据进行的科学管理不论是对临床研究者个人还是对临床研究机构都具有非常重要的积极意义,但临床研究数据管理在国内尚未得到足够重视,这对科研成果的传播、扩散、保存、发表和保护都将带来不利的影响。研究机构需要进行整体设计和规划,为研究者提供相应的政策指导和数据存储支持,引入相应的临床科研辅助人员,严格实施临床研究数据管理流程,这将有助于切实提高科研数据的真实性,减少无端重复研究所造成的资金浪费,促进机构临床科研的发展。在医学大数据时代更有助于科学驾驭临床研究大数据,为人类医学研究积累最佳证据。
[1] 刘桂锋,卢章平,阮炼.美国高校图书馆的研究数据管理服务体系构建及策略研究[J].大学图书馆学报,2016(03):16-22.
[2] 国家食品药品监督管理总局.临床试验数据管理工作技术指南[EB/OL].(2016-07-27)[2016-10-30] .http://www.sda.gov.cn/WS01/CL0087/160961.html.
[3] 国家食品药品监督管理总局.药物临床试验质量管理规范.(2003-08-06)[2016-10-30].http://www.sda.gov.cn/WS01/CL0053/24473.html.
[4] CHAN AW,TETZLAFF JM,GOTZSCHE PC,etal. SPIRIT 2013 explanation and elaboration:guidance for protocols of clinical trials[J].BMJ,2013,346:e7586.
[5] NIH.A service of the U.S.National Institutes of Health [DB/OL].[2016-10-30].https://clinicaltrials.gov/.
[6] WHO.International Clinical Trials Registry Platform [DB/OL].[2016-10-30].http://www.who.int/ictrp/en/.
[7] 中国临床试验注册中心.中国临床试验注册中心[DB/OL].[2016-10-30].http://www.chictr.org.cn/index.aspx.
[8] 陈秀娟,胡卉,吴鸣.英美数据管理计划与高校图书馆服务[J].图书情报工作,2015,59(14):51-58.
[9] NIH.NIH Data Sharing Policy and Implementation Guidance.(2003-03-05)[2016-10-30].http://grants.nih.gov/grants/policy/data_sharing/data_sharing_guidance.htm.
[10] NSF.Dissemination and sharing of research results[DB/OL].[2016-10-30].https://www.nsf.gov/bfa/dias/policy/dmp.jsp.
[11] 李农.研究数据共享时代图书馆的新职责——研究数据管理与数据综合处理[J].上海高校图书情报工作研究,2015(01):9-12.
[12] 韦成府,姚晓霞,聂华.我国教育科研机构知识库建设现状调查与分析[J].现代图书情报技术,2014(05):1-9.
[13] 曹月珍,马建玲.研究数据管理工具发展研究[J].图书馆学研究,2014(15):40-47.
[14] 马建玲,祝忠明,王楠,等.美国高校图书馆参与研究数据管理服务研究[J].图书情报工作,2012,56(21):77-82.
[15] 余文婷.开放科学数据仓储资源开发模式比较分析——以SRDA、eCrystals和Dryad为例[J].图书馆学研究,2014(11):58-62.
[16] HRYNASZKIEWICZ I,NORTON ML,VICKERS AJ,etal.Preparing raw clinical data for publication:guidance for journal editors,authors,and peer reviewers[J].BMJ,2010,340:c181.
Strategies for data management in clinical researches
ZHANG Wei1, YING Jun1,2△
(1FudanUniversityLibrary,Shanghai200032,China;2CenterofEvidence-basedMedicine,FudanUniversity,Shanghai200032,China)
Clinical researchers have begun to recognize the importance of long-term preservation and sharing of data because of the emergency of numerous medical data in clinical studies,so the concept and methods of research data management emerged.Data management in clinical researches can accelerate the accuracy and efficiency of clinical research and meet the expectations and requirements of researchers,institutions and research sponsors.This paper discussed the key points of clinical data management through two aspects,data management in individual clinical research and data management in organizational clinical researches.It will help clinical researchers and scientific research governors to understand the process of data management in clinical researches and promote standardized clinical research activities.
clinical research; data management; institutional repository; data warehouse
R-1
B
10.3969/j.issn.1672-8467.2017.01.021
2016-11-02;编辑:张秀峰)
中国高等教育文献保障系统全国医学文献信息中心科研基金(CALIS-2016-02-001)
△Corresponding author E-mail:jjunying@fudan.edu.cn
*This work was supported by the Scientific Research Fund Project of China Academic Library & Information System National Information Center in Medicine (CALIS-2016-02-001).
