生物基芳香平台化合物2,5-呋喃二甲酸的合成研究进展
2017-02-17王静刚刘小青朱锦
王静刚,刘小青,朱锦
(中国科学院宁波材料技术与工程研究所,浙江 宁波 315201)
生物基芳香平台化合物2,5-呋喃二甲酸的合成研究进展
王静刚,刘小青,朱锦
(中国科学院宁波材料技术与工程研究所,浙江 宁波 315201)
生物基芳香平台化合物2,5-呋喃二甲酸(2,5-FDCA)有望替代现有的石油基单体对苯二甲酸用于高性能高分子材料的合成。如何通过高效、廉价的路线制备2,5-FDCA已经成为近几十年的研究热点。本文系统地介绍了从5-羟甲基糠醛(HMF)、糠酸、呋喃、二甘醇酸或己糖二酸制备2,5-FDCA的各种方法,并重点介绍了HMF的直接氧化法、贵金属氧化法、非贵金属氧化法和生物酶氧化法合成2,5-FDCA。在比较了现有各种路线优缺点的基础上,认为HMF路线是2,5-FDCA规模化制备最有希望的路线,长远发展应朝着以纤维素为起始原料的方向,打通纤维素到糖的关键制备技术。
2,5-呋喃二甲酸;生物基;平台化合物;合成;进展
当前,随着经济的快速发展和石油储备量的下降,人们已经越来越重视可再生资源的开发和利用[1-4]。其中,以可再生资源为原料制备得到的生物基高分子材料被认为具有节约资源和保护环境的双重功效,业已成为当前高分子材料的一个重要发展方向。目前,广泛使用的生物基高分子材料主要有聚乳酸(PLA)[5]、聚羟基脂肪酸(PHA)[6]、聚羟基乙酸(PGA)[7]、聚丁二醇丁二酸酯(PBS)[8]等。它们都属于脂肪类聚合物,由于分子结构中缺乏刚性芳香环结构,其力学性能(如强度、模量、抗蠕变等)与耐热性能(如热机械性能、热变形温度等)均明显低于聚对苯二甲酸乙二醇酯(PET)、聚碳酸酯(PC)、芳香尼龙(PA)、双酚A型环氧树脂(Epoxy)等石油基高分子材料,严重限制了它们的应用范围。因此,生物基高分子材料要想部分取代和补充石油基高分子材料,迫切需要通过合成技术,在其分子结构中引入刚性环结构。2,5-呋喃二甲酸(2,5-FDCA)的分子结构中含有芳香环,用于合成生物基高分子材料可有效提高其耐热性能和机械性能,被认为是石油基单体对苯二甲酸(PTA)的理想替代品,也可以替代间苯二甲酸、己二酸、丁二酸、双酚A等应用于聚酯、聚酰胺、环氧树脂等生物基聚合物的合成。因此,它已被美国能源部评为12种最具潜力的生物基平台化合物之一,被杜邦和DSM公司认为是“沉睡的巨人”[9]。
目前,2,5-FDCA可以由5-羟甲基糠醛(HMF)、糠酸、呋喃、二甘醇酸和己糖二酸等不同起始原料制备得到。为了对比分析各种合成路线的优缺点,促进人们对本领域的深入认识,本文从合成路线、氧化催化剂、反应机理、合成工艺的局限性以及面临的挑战等方面论述了2,5-FDCA合成的研究进展。
根据原料来源的不同,目前2,5-FDCA主要有以下制备路线:①以HMF为原料,将HMF的醛基和羟甲基通过化学法或生物法氧化为羧基;②以糠酸为原料,在碱性、高温条件下,通过歧化反应合成;③以呋喃为原料,通过乙酰化反应得到2,5-二乙酰基呋喃(2,5-DAF),然后通过碘仿反应合成;④以己糖二酸为原料氧化合成;⑤以二甘醇酸为原料与甲醇和二氯亚砜反应得到二甘醇酸二甲酯,然后与二水合三聚乙二醛缩合合成;⑥2,5-二甲基呋喃等其他原料合成。本文将上述不同原料合成2,5-FDCA的方法分别简称为HMF路线、糠酸路线、呋喃路线、己糖二酸路线、二甘醇酸路线和其他路线。
1 HMF路线
1.1 直接氧化法
HMF主要由天然的纤维素、果糖、葡萄糖、海藻等转化得到,以HMF为原料制备2,5-FDCA主要是要将呋喃环侧位的醛基和羟甲基分别氧化为羧基。最初研究人员主要是采用传统的氧化剂进行氧化。如HAJJ等[10]早在1987年就使用硝酸氧化HMF制得了2,5-FDCA,但该方法容易产生副产物。后来,GRABOWSKI等[11]在碱性水溶液中采用镍氧化还原电极将HMF进行电化学氧化取得了较好效果,收率达到71%,但得到的是暗黄色晶体,需要进行重结晶纯化。为了降低HMF氧化为2,5-FDCA的成本,MIURA等[12]采用KMnO4为氧化剂,将1mmol HMF溶解于NaOH水溶液中,然后加入2.3mmolKMnO4,在室温下制备得到了纯度较高的2,5-FDCA。他们同时尝试了其它高锰酸金属盐,如高锰酸锂、高锰酸钠、高锰酸镁、高锰酸锌等,结果表明高锰酸钾的氧化效果最好,2,5-FDCA的收率可以达到89%。这种方法的优点是工艺简单,缺点是氧化剂KMnO4等使用量大。
1.2 贵金属催化剂
由于铂(Pt)、钯(Pd)、金(Au)、银(Ag)、铑(Rh)、钌(Ru)等贵金属的d电子轨道都未填满,表面易吸附反应物,且强度适中,利于形成中间“活性化合物”,具有较高的催化活性,同时还具有耐高温、抗氧化、耐腐蚀等特性。因此,采用上述贵金属作为催化剂来实现HMF的高效催化、氧化也得到了广泛研究。1991年荷兰代尔夫特科技大学的VINKE等[13]首先采用C/Al2O3负载Pd、Pt、Rh、Ru等在液相中氧化HMF,得到了中间体2,5-呋喃二甲醛(DFF)、5-羟甲基-2-呋喃甲酸(HMFCA)、5-甲醛基-2-呋喃甲酸(FFCA)和2,5-FDCA,如图1所示。

图1 HMF及其氧化衍生物
对比研究发现Pt、Pd都显示了优异的氧化稳定性和选择性,且金属催化剂的分散对反应速率影响较大。其中Pt对HMF氧化为FFCA显示了较好的选择性,而Pd催化时HFCA的收率更高,只有Al2O3负载Pt催化时得到2,5-FDCA。VERDEGUER等[14]采用C负载Pt与Pb氯化物、氧化物等为催化剂,在强碱性溶液中催化氧化HMF,反应不到2h,2,5-FDCA的纯度>99%,最高收率达到81%,但Pb作为高污染的重金属限制了此法的进一步应用。后来,研究人员采用在工业上大规模生产对苯二甲酸的高效催化剂金属溴化物(Co/Mn/Br)催化体系,将其用在HMF氧化为2,5-FDCA,取得了较好效果。有助催化剂时,在氧气压力70bar(1bar=0.1MPa)、125℃条件下反应3h可使2,5-FDCA的收率达到61%[15-16],但此过程采用的催化剂中含有HBr,容易对设备造成腐蚀。为了进一步提高催化效率和氧化选择性,研究人员将Pt、Ru、Au、Pd等制备成金属纳米颗粒直接催化或负载在C、金属氧化物、聚合物等载体上进行了大量而广泛的研究,来提高HMF的转化率和2,5-FDCA的收率。
1.2.1 Pt催化剂
Pt催化剂是贵金属催化剂中最重要的品种之一。2010年美国西北太平洋国家实验室的LILGA等[17-18]采用Pt纳米颗粒为催化剂,选择金属氧化物(ZrO2)为载体,纯氧做氧化剂,将HMF氧化为2,5-FDCA,收率达到98%。实验发现氧化路线如图2所示,DFF、HMFCA、FFCA和FDCA的收率和选择性取决于氧化剂、催化剂、pH以及反应温度等条件。
法国里昂催化研究所的RASS等[19]将Pt负载在C上,100℃、40bar空气压力下催化氧化HMF为2,5-FDCA。研究表明:HMF迅速氧化为HMFCA和DFF,进一步氧化为FFCA,最终羟基和醛基彻底氧化为羧基。若Bi/Pt的摩尔比为0.2,HMF/Pt=100,Na2CO3提供碱性环境,0.1mol的HMF在2h内可以99%转化为 2,5-FDCA。随后,他们又将Pt负载于TiO2、ZrO2、ZrO2-Y2O3等金属氧化物,在碱性水溶液中以空气为氧化剂将HMF氧化为2,5-FDCA,结果表明Pt/TiO2和Pt/ZrO2能够加速醛基的氧化,Y2O3和La2O3-ZrO2为载体的催化活性明显低于Pt/ZrO2[20]。SIANKEVICH等[21]将Pt纳米颗粒负载在PVP聚合物上,建立了HMF氧化为2,5-FDCA的反应动力学模型,通过聚合物载体控制金属纳米颗粒的催化比表面积,实现了HMF到2,5-FDCA在温和条件下转化。徐杰等[22-23]将Pt的平均尺寸降至1nm,负载在金属氧化物[TiO2、CeO2或Mg(OH)2]、ZSM-5及HY上催化HMF氧化为2,5-FDCA,在60℃水溶液中,0.3MPa O2压力条件下,以Au/Mg(OH)2、Au/TiO2、Au/CeO2、Au/HY为催化剂时,HMF的转化率都可以达到99%,在Au/HY体系中2,5-FDCA的收率也可以高达99%。HANG等[24]采用乙二胺(EDA)为N源,制备了N型C基载体Pt催化剂Pt/C-EDA-x,110℃,O2压力1.0MPa,反应12h,HMF氧化为FDCA的收率达到96.0%。进一步以Pt/C-O-Mg催化剂氧化HMF,FDCA的收率达到97%[25]。最近,ZHANG等[26]以Fe3O4为核,无定形炭为壳,最外层负载纳米Pt,形成核壳结构Fe3O4@C@Pt催化剂氧化HMF,在水相中,90℃反应4h,FDCA的收率接近100%,效果非常理想。
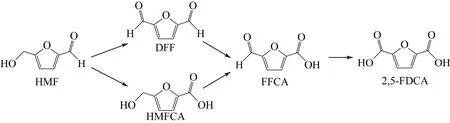
图2 HMF的氧化路线
1.2.2 Au催化剂
20世纪80年代,HARUTA实验室发现以Au为活性组分的催化剂对低温氧化具有催化活性,而且具有良好的抗水解性和稳定性,显示了良好的应用前景[27]。2008年,ROSSI等[28-29]发表了Au选择性催化氧化的综述文章,全面阐述了Au纳米颗粒在有机化合物选择性氧化方面具有的显著催化效果。同年TAARNING 等[30]报道了以甲醇为溶剂,在甲醇钠存在时,Au/TiO2催化氧化HMF制备2,5-呋喃二甲酸二甲酯的研究结果。2009年GORBANEV等[31]报道了室温条件下在水溶液中,Au/TiO2催化分子氧氧化HMF制备2,5-FDCA的研究,但此反应需要在较高的氧气压力和较高的碱液浓度条件下进行。除了选择TiO2作为载体外,CASANOVA等[32]进一步尝试了CeO2、活性炭、Fe2O3等作为载体,在水溶液中催化氧化HMF。与Au/TiO2相比,在相同条件下,Au/CeO2的活性和选择性更好,在130℃,10bar O2,NaOH/HMF(摩尔比)=4的条件下反应8h,2,5-FDCA的收率高达99%。后续研究发现纳米级的CeO2负载的金催化剂可以实现在醇溶剂中无碱催化氧化HMF到相应的酯[33]。2011年,PASINI等[34]报道了TiO2负载的双金属催化剂Au-Cu/TiO2催化氧化HMF,在优化条件下,2,5-FDCA的收率达到99%。相比于单金属催化剂Au/TiO2,由于Au-Cu合金的形成,双金属催化剂Au-Cu/TiO2的活性和稳定性得到了明显的提高。2012年,ALBONETTI等[35]同样选择TiO2为载体,采用Au-Cu合金制备成纳米颗粒作为催化剂,在温和的条件下实现了HMF的氧化,过程如图3所示。当Au/Cu的原子比率在3/1时,不但2,5-FDCA的收率较高,而且催化剂在重复多次使用后,质量和选择性没有明显下降。若Co(OAc)2/Zn(OAc)2/Br或者Au/TiO2和Au-CeO2的纳米颗粒为催化剂,乙酸为溶剂,1%的三氟乙酸为促进剂,90℃、1atm O2条件下,2,5-FDCA的收率仅为60%[36]。2013年,VILLA等[37]则用Pd改性C负载的Au催化剂氧化HMF,提高C/Au催化体系的转化率和选择性。2015年,ARDEMANI等[38]研究了羟基磷灰石负载Au催化剂氧化HMF为2,5-FDCA的过程和机理。
为了实现从果糖到2,5-FDCA的直接转化,YI等[39]设计了高效的分离提纯体系将果糖直接转化为2,5-FDCA,如图4(a)所示。在异丙醇中用HCl催化果糖脱水得到HMF,然后交换到水溶液中,采用Au/HT催化氧化HMF为2,5-FDCA,收率达到83%。为了使分离更加有效,他们进一步设计了四乙胺(TEAB)、水、甲基异丙酮(MIBK)三相体系将HMF转化为2,5-FDCA。首先在相Ⅰ(TEAB或水)中将糖转化为HMF,然后相Ⅱ(MIKB)将HMF提取和扩散到相Ⅲ(水)中,催化氧化为2,5-FDCA,果糖和葡萄糖转化为2,5-FDCA的收率分别为78%和50%[40],过程如图4(b)所示。YI等[41]的最新研究表明,在单一水相中Ru/C为催化剂,果糖转化为2,5-FDCA的收率可以达到53%。
1.2.3 Ru催化剂
贵金属Ru也是催化醇和醛基氧化的良好催化剂。ZHANG等[42]采用磷酸锆(ZrP)为载体负载Ru3+制备出ZrP-Ru催化剂,常压下可以将HMF全部转化,产物主要为FDCA和DFF的混合物,但FDCA的选择性较低。GORBANEV等[43]在水相、无碱体系,通过对不同载体负载Ru催化分子氧氧化HMF到2,5-FDCA的研究,结果表明:载体TiO2、A12O3、Fe3O4、ZrO2、CeO2、MgO、La2O3、Mg2A12O4、HT、羟基磷灰石(HAp)、MgO·La2O3中,碱性载体MgO·La2O3表现较佳,在140℃ 2.5bar 的O2压力下反应6h,2,5-FDCA的收率达到90%。并进一步研究了Ru(OH)x/MgO、Ru(OH)x/MgAl2O4和Ru(OH)x/HT体系[44],发现碱性载体在反应条件下会部分溶解,导致反应溶液呈碱性,促进HMF到2,5-FDCA的转化。
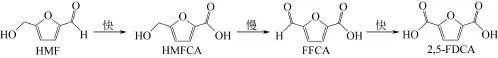
图3 Au-Cu纳米颗粒催化HMF氧化为2,5-FDCA的反应过程[35]
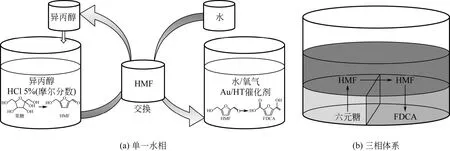
图4 糖转化为2,5-FDCA的体系设计
1.2.4 Pd催化剂
考虑到贵金属纳米颗粒催化剂的方便回收,2015年,中南民族大学的ZHANG等[45]研究了磁性Pd纳米颗粒催化剂[γ-Fe2O3@HAP-Pd(0)],制备方法为用Pd2+置换在γ-Fe2O3@HAP中的Ca2+,然后将Pd2+还原为Pd(0)价态,最优条件下, HMF转化率为97%,2,5-FDCA的收率为92.9%,优势在于反应完成后催化剂可以通过外加磁场进行完全回收,方便快捷,有利于重复利用。进一步将Fe3O4作为核,C层作为壳,制备出核壳结构的磁性微粒,然后将Pd纳米颗粒固定在PdC@Fe3O4上,这种催化剂清洁、简单、绿色、稳定性好,可以在水中高效将HMF转化为2,5-FDCA。通过对反应温度、溶剂等条件的优化,在80 ℃反应6h,HMF转化率为98.4%,2,5-FDCA收率为86.7%[46]。DAVIS等[47]则比较了活性炭负载的Pd、Pt与Au催化氧化HMF到2,5-FDCA的区别。22℃、0.69MPa O2压力、0.15mol HMF、0.3mol NaOH条件下,Pt/C、Pd/C、Au/C、Au/C、Au/TiO2的TOF值分别为0.08s–1、0.15s–1、5.0s–1、2.3s–1、1.6s–1。相同反应件下,Pt、Pd能催化氧化HMFCA到2,5-FDCA,而Au不能,Au催化氧化HMFCA到2,5-FDCA需要在更高的氧气压力和更高的碱浓度,相比于氧气压力对其转化的影响,碱浓度影响更大。
1.2.5 双金属催化剂
除了对单一贵金属及其纳米颗粒的催化活性和选择性研究以外,研究人员通过催化体系和载体的设计对金属合金的催化活性和选择性也进行了考察。2000年,ROGR等[48]报道了直接将果糖转化为2,5-FDCA的新方法。采用水和甲基异丙基酮(MIBK)用薄膜隔开作为两相体系,在水相中固体酸催化果糖转化为HMF,然后HMF通过薄膜进入MIBK有机相,将Pt-Bi负载C基上封装在硅树脂中,在MIBK中溶胀作为HMF的活性催化位点得到2,5-FDCA,如图5所示,收率达到25%,但存在水相中的HMF容易开环生成乙酰丙酸的缺点。2004年厦门大学WAN等[49]将Au-Pd合金的纳米颗粒负载在碳纳米管(CNT)上作为催化剂,水相中在CNT的表面将HMF氧化为2,5-FDCA。由于CNT表面含有大量羰基、醌、酚结构,有利于反应物和中间体的吸附,促进氧化。若采用Au单一催化,中间体主要为HMFCA,容易出现开环等副反应,但Au-Pd双金属催化协同效果使HMF迅速转化为DFF,Pd的存在促进了FFCA氧化为2,5-FDCA,最高转化率达到96%。
密歇根科技大学CHADDERDON等[50]以Au/C、Pd/C和Au-Pd/C纳米颗粒为催化剂,采用电化学氧化HMF。研究表明Au/C催化时醛基更容易氧化为羧基,HMF主要氧化为HMFCA,当电位提高后,羟基进一步氧化为羧基,得到2,5-FDCA;若Pd/C催化,低电位时醛基氧化更缓慢,提高电位可加速氧化;Au-Pd/C双金属催化剂则可以在低电位氧化HMF为FFCA或2,5-FDCA,Au/Pd比例不同时催化效果有所差异,2,5-FDCA最高收率为83%。ALBONETTI等[51]采用Au-Ce催化剂氧化HMF,将2,5-FDCA的收率提高到92%。
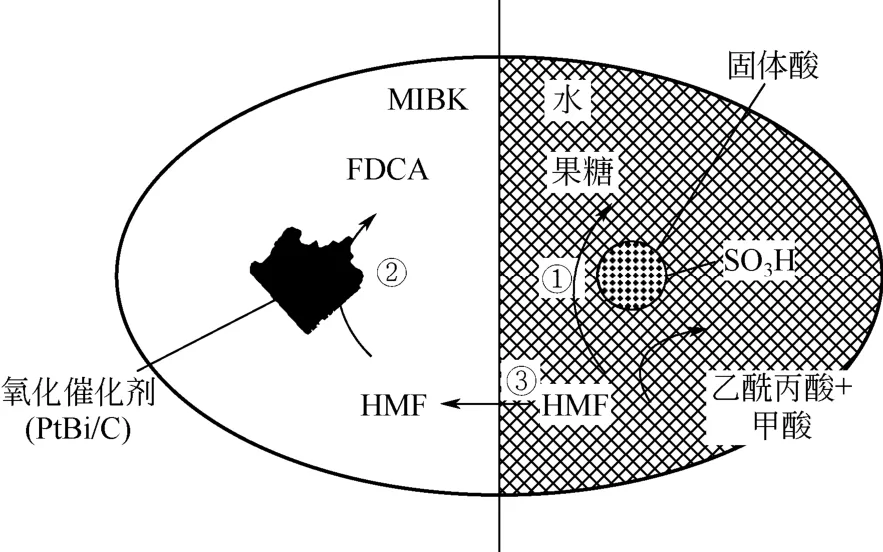
图5 果糖直接转化为2,5-FDCA的体系设计
1.3 Cu和Co金属催化剂
由于贵金属催化剂的价格相对昂贵,开发非贵金属催化剂催化HMF氧化为2,5-FDCA也具有重要意义。空气或t-BuOOH等为氧源,Cu做为催化剂氧化HMF为DFF或2,5-FDCA的研究表明:DFF的收率达到97%,而CuCl/t-BuOOH在MeCN溶液中2,5-FDCA的收率为50%,选择性和收率明显低于贵金属纳米颗粒的催化效果[52]。把Co乙酰丙酮化合物封装在硅胶中,同时进行酸催化和催化氧化两个过程,可以直接把果糖转化为2,5-FDCA,果糖的转化率为72%,2,5-FDCA的选择性为99%,分步反应的对比结果表明一锅法直接转化效果更好[53]。若将Co的氧化物制备成Fe3O4-CoOx纳米颗粒,t-BuOOH作氧化剂,2,5-FDCA的收率达到68.6%[54]。进一步将氯甲基聚苯乙烯树脂(Merrifield resin)负载Co-Py为催化剂,t-BuOOH为氧化剂,100℃反应24h,HMF转化率为95.6%,2,5-FDCA的收率提高到了90.4%,接近贵金属催化剂的催化效果[55]。ZUO等[56]以Co/Mn/Br为催化体系,180℃,二氧化碳和氧气混合气体为氧源,HMF转化为2,5-FDCA的最高收率达到90.0%。
以上将金属催化剂制备成纳米颗粒负载不同载体,在水相利用分子氧氧化HMF,避免了DMSO等非质子极性溶剂的大量使用,氧化选择性和转化率大幅度提高,部分催化体系将HMF催化氧化为2,5-FDCA的收率达到99%。虽然存在一些缺陷,如贵金属催化剂制备工艺复杂,价格相对昂贵,批量制备和回收活化需要进一步研究;氧化时需要大量金属碱性氢氧化物(如NaOH、KOH等)使2,5-FDCA形成羧酸盐溶于水相,才能避免二酸在金属催化剂表面吸附导致催化活性降低等问题,但催化剂用量少,工艺相对成熟,目前仍是合成2,5-FDCA的主要研究方向。
1.4 生物酶催化剂
化学催化将HMF转化为2,5-FDCA多数需要高温、高压、碱性环境以及有机溶剂的大量使用,容易对环境造成影响,而生物酶催化剂是一种符合环保要求的绿色催化剂,无毒无害,用量少,无污染。因此,利用生物酶催化剂将HMF转化为2,5-FDCA更加绿色。2014年荷兰格列宁根大学DIJKMAN等[57]发现一种新的酶在室温和常压下可以高效转化HMF为2,5-FDCA,收率达到99%。为了深入研究氧化路线和反应机理,分别采用2,5-二羟甲基呋喃和其氧化中间体为起始原料,研究了此种转化酶的催化转化效果,结果表明HMF氧化分为HMFCA(路径A)和DFF(路径B)两条路线,如图6所示,以路径A为主。
MCKENNA等[58]采用半乳糖氧化酶M3.5和醛氧化酶PaoABC串联氧化HMF,羟基和醛基可在温和的条件下高效转化为羧基得到2,5-FDCA,室温下,pH接近中性,2,5-FDCA收率为74%,氧化路线如图7所示。
QIN等[59]用酶工具箱可以选择性催化氧化HMF分别得到DFF、HMFCA、FFCA和FDCA。其中半乳糖氧化酶(GO)+过氧化氢酶+辣根过氧化物酶(HRP)可以有效氧化HMF为DFF,收率达到92%,进一步采用低共熔溶剂(DES)的方法可将DFF的分离纯度提高到97%,而GO酶和脂肪酶串联反应24h,2,5-FDCA最高收率88%。生物酶催化剂虽然制备规模尚在实验室阶段,但克服了贵金属催化剂的一些缺点,合成条件温和,经济环保,具有独特的优势。
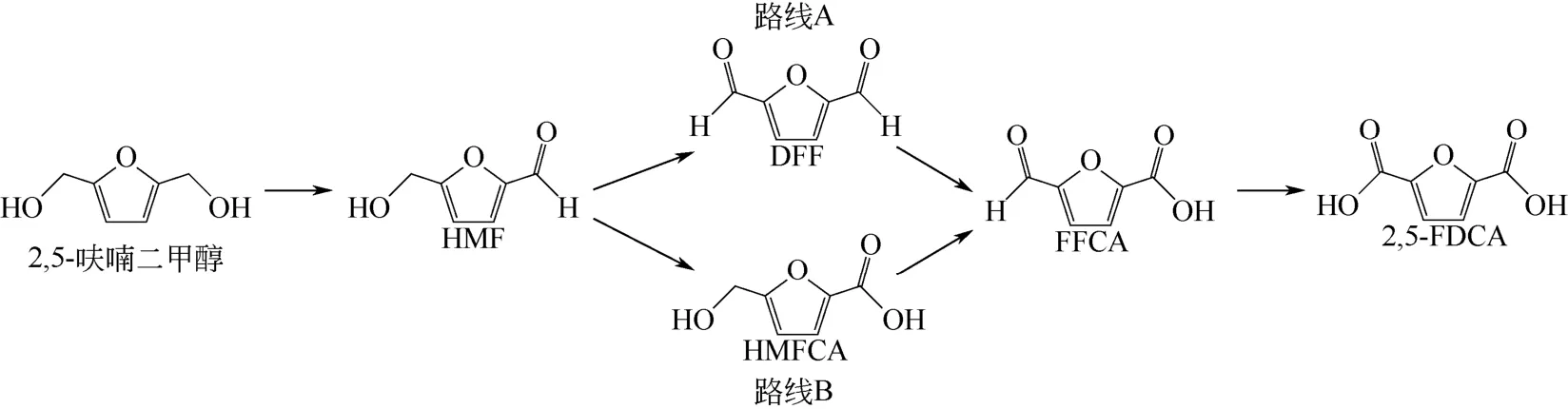
图6 2,5-呋喃二甲醇酶催化转化为2,5-FDCA

图7 HMF酶催化转化为2,5-FDCA
2 糠酸路线
糠酸制备2,5-FDCA的报道最早在1958年,德国的RAECKE[60]研究了芳环化合物(苯环、呋喃、吡啶、噻吩)的甲酸钾盐在高温下生成二取代的二甲酸钾盐,酸化得到芳环化合物的二甲酸,其中包括利用糠酸钾盐为原料,高温下,生成2,5-FDCA的钾盐和呋喃,进一步酸化可得到2,5-FDCA,如图8(a)所示。后来直到2013年,荷兰的THIYAGARAJAN等[61]详细研究了糠酸转化为2,5-FDCA的合成路线,如图8(b)所示。他们发现此路线可以有效地将糠酸的金属盐如糠酸钾盐转化为2,5-FDCA,总收率可以达到90%,但此路线存在异构化反应,制备得到的呋喃二酸包括2,4-FDCA和2,5-FDCA,尽管利用1H NMR、13C NMR和X射线详细表征2,4-FDCA,但两种异构体的物化性能极为接近,分离困难,限制了糠酸路线的进一步应用。中国科技大学的PAN等[62]利用糠酸金属盐为原料,通过对催化剂ZnCl2、CdCl2、CuCl2、LaCl2、NiCl2、SnCl2、ZnO、Zn(OAc)2的考察,发现ZnCl2的催化效果最好,通过对反应温度(220~280℃)和反应时间(30~240min)的考察,结果表明:在250℃反应180min,糠酸金属盐转化率为61%,2,5-FDCA的选择性为86%,但同样存在异构体分离问题。为了提高2,5-FDCA的选择性,解决糠酸路线的异构体分离问题,BANERJEE等[63]以二氧化碳为碳源,在反应体系中加入碳酸铯(Cs2CO3)辅助催化,最佳条件下2,5-FDCA的收率达到89%,糠酸的转化率为94%。此研究成功解决了糠酸法制2,5-FDCA选择性差的问题,但未反应原料2-糠酸的存在分离困难,若此法制备的2,5-FDCA用于聚酯的制备,由于单酸的存在,会影响到聚合物的分子量。
西南科技大学的刘浪等[64]以糠酸为原料,经过酯化、氯甲基化、水解、氧化得到2,5-FDCA,并对各步反应中的工艺参数进行了优化,酯化反应时间为10h,氯甲基化反应温度为35~40℃,水解反应原料摩尔比为n(氢氧化钠)∶n(5-氯甲基-2-呋喃甲酸甲酯) = 2.1∶1,氧化反应体系pH =7~8,2,5-FDCA的总收率为47.5%,合成路线如图9所示,虽然不存在异构体2,4-FDCA,但总收率较低。
3 呋喃路线
考虑到果糖属于紧缺食品,大量用于工业原料势必影响食物供应平衡,非食物来源的纤维素可能是2,5-FDCA更好的原料来源,中国科学院宁波材料所的生物基高分子材料课题组进行了2,5-FDCA新合成路线探索[65-67]。利用纤维素水解、环化制备的生物基大宗化学品呋喃为原料,与乙酸酐发生酰基化反应合成2,5-DAF,然后通过碘仿反应将乙酰基转化羧基得到2,5-FDCA,纯度>99%,呋喃到2,5-FDCA收率为40.2%,合成路线如图10所示。
此路线乙酰化反应条件温和,催化剂为常用的液体酸如浓硫酸、甲磺酸、苯甲磺酸等,副产物为乙酸,可直接回收脱水制备原料乙酸酐,碘仿反应在室温下进行,无需催化剂,反应速度快,副产物碘仿为重要的工业原料。因此,此路线条件温和、副产物少,若进一步提高收率,有望实现纤维素到2,5-FDCA的低成本、规模化制备。
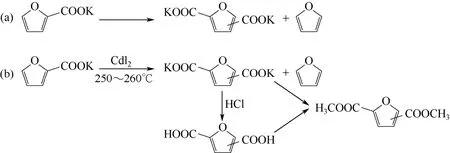
图8 糠酸金属盐路线制备2,5-FDCA
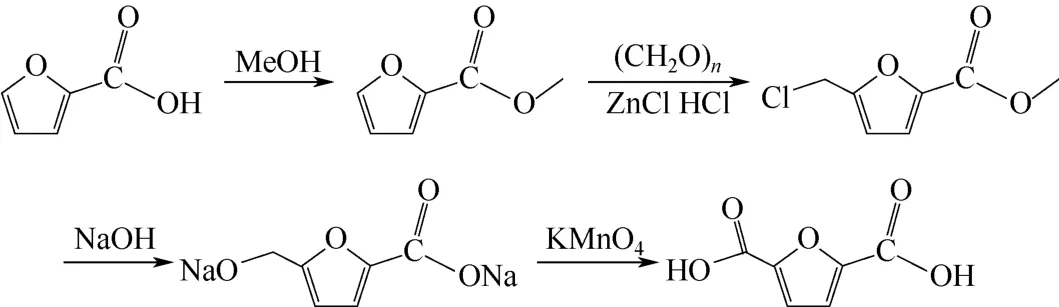
图9 糠酸制备2,5-FDCA
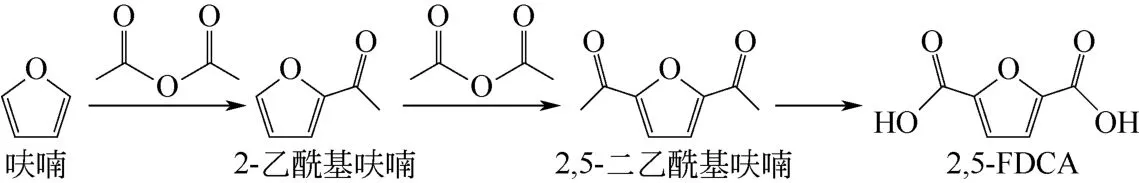
图10 呋喃路线制备2,5-FDCA
4 己糖二酸路线
葡萄糖和半乳糖氧化得到葡萄糖二酸和半乳糖二酸,在催化剂的作用下脱水环化得到2,5-FDCA。LEWKOWSK[68]以半乳糖二酸为起始原料,对甲苯磺酸为催化剂,140℃反应条件下脱水环化,采用氯化钙沉淀,盐酸酸化得到2,5-FDCA固体,烘干后收率为52%,如图11所示。BRǍTULESCU[69]则以葡萄糖二酸为起始原料,在微波反应器中,以苯磺酸为催化剂脱水得到2,5-FDCA,收率为58%。TAGUCHI等[70]通过采用正丁醇为溶剂,将半乳糖二酸在脱水环化的同时羧基酯化,得到2,5-呋喃二甲酸二正丁酯,收率提高到64%,但同时生成2,3-呋喃二甲酸二正丁酯,增加了异构体分离纯化步骤。葡萄糖二酸和半乳糖二酸通过脱水环化一步可以得到2,5-FDCA,方法简单,但原料在酸性条件下容易发生异构化和碳化副反应,导致收率较低。因此,需要开发温和、高效的己糖环化脱水催化剂进一步提高2,5-FDCA的收率。
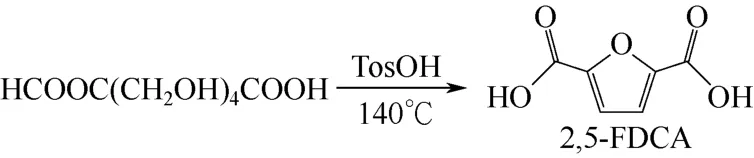
图11 半乳糖二酸路线制备2,5-FDCA
5 二甘醇酸路线
二甘醇酸的酯化产物与1,2-二羰基化合物缩合可以合成2,5-FDCA。李伟杰等[71]以二甘醇酸为原料,在甲醇和二氯亚砜中回流酯化得到二甘醇酸二甲酯,然后溶于环己烷,在固体KOH的作用下回流1h加入二水合三聚乙二醛继续回流6~8h,得到2,5-FDCA,收率为73.4%,合成路线如图12所示。对比作者用此法制备的3,4-二苯基-2,5-呋喃二甲酸的收率高达98.6%,2,5-FDCA收率低的主要原因在于所用的1,2-二羰基化合物二水合三聚乙二醛中含有水,在KOH-水体系中,乙二醛在缩合反应的前期发生了部分的重排反应。
6 其他路线
除了以上采用不同原料合成2,5-FDCA的路线之外,也有报道采用其他呋喃化合物合成2,5-FDCA。1876年,FITTING和HEINZELMAN[72]报道了黏酸(mucic acid)在浓氢溴酸的作用下脱除三分子H2O得到2,5-FDCA,收率48%。由于此法需要满足高浓度的酸、高温(120℃)和长时间(>20h),收率低于50%,并且黏酸的产量低,价格高。因此,此法并没有进一步深入研究。DIEGO等[73]以2,5-二甲基呋喃为原料,以空气为氧化剂,乙酸钴和乙酸锰、溴化钠为催化剂进行氧化,转化率为100%,但2,5-FDCA的选择性只有16%,其主要原因是原料2,5-二甲基呋喃的甲基为供电基团,在酸性条件下,容易导致呋喃环开环副反应,大幅度降低了2,5-FDCA的选择性。随后,他们将呋喃环5位的甲基改为乙酰基,通过2-甲基-5-乙酰基呋喃的氧化制备2,5-FDCA。同样以乙酸钴和乙酸锰、溴化钠为催化剂在空气中进行氧化,2,5-FDCA 的收率提高到64%[74]。美国伊斯曼化学公司的JANKA等[75]采用糠醛的衍生物如5-甲基-2-糠醛、5-乙基羟甲基-2-糠醛等为原料,在乙酸中,以空气为氧化剂,乙酰钴、乙酰锰和溴化氢为催化剂进行氧化得到2,5-FDCA,收率最高达到89%,但缺点是容易氧化不完全,且原料合成困难,并没有看到进一步深入研究。
7 结语与展望
源于石化资源的高分子材料是支撑人类社会快速进步与发展的重要材料,对推动和延续现代人类文明起到了至关重要的作用。然而,石油资源的大量使用已带来环境污染、废弃物处置、能源危机等一系列问题,发展绿色可再生资源是解决高分子材料可持续发展的重要研究方向之一。
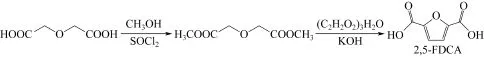
图12 二甘醇酸路线制备2,5-FDCA
2,5-FDCA作为生物基芳香单体,是石油基单体对苯二甲酸、间苯二甲酸、双酚A等理想替代品,在合成聚酯、聚酰胺、环氧树脂等生物基刚性高分子材料领异。通过对合成2,5-FDCA的HMF路线、糠酸路线、呋喃路线、己糖二酸路线和二甘醇酸路线的综述,认为二甘醇酸路线最为简单,但原料价格昂贵,不适合大规模的工业化生产;糠酸路线原料价格低廉,但得到的是2,4-FDCA和2,5-FDCA的混合物,异构体物性接近,分离困难,若直接用于高分子合成会破坏高分子链的规整排列,影响性能,虽然最近的研究表明FDCA的选择性大幅度提高,但存在原料大量残留的问题;己糖二酸路线的原料葡糖糖二酸和半乳糖二酸由葡萄糖和半乳糖氧化得到,HMF路线的原料由葡萄糖和果糖脱水得到,葡萄糖、果糖、半乳糖均是食品原料,价格相对低廉,若短期小规模制备2,5-FDCA,原料来源和价格均可满足需求,就制备方法而言,相比于己糖二酸路线存在异构化和碳化副反应,HMF路线得到学术界和工业界大量深入而广泛的研究,开发的新型Pt、Pd等贵金属催化剂和生物酶催化剂将HMF转化2,5-FDCA的收率提高到99%以上,虽然存在HMF原料容易开环、DMSO等大量溶剂使用、贵金属催化剂回收等问题,但制备技术相对成熟。生物酶催化剂的出现,克服了贵金属催化剂的一些缺点,合成条件温,经济环保,具有独特的优势。综合而言,HMF路线是2,5-FDCA规模化制备最有希望的路线之一。聚酯产业目前年产量已达到7000万吨以上,是2,5-FDCA的主要应用领域,可用于食品的葡萄糖和果糖若作为工业原料大规模用于2,5-FDCA的生产,容易造成食品短缺和打破全球范围食物供应链平衡。只有充分利用最为丰富和廉价的纤维素资源开发2,5-FDCA,才能长期实现2,5-FDCA的大规模生产和应用。呋喃路线利用了纤维素催化脱水得到的工业化学品呋喃为原料,方法虽然简单,但目前收率较低,需要开发温和、高效的酸性催化剂。因此,生物基2,5-FDCA的制备应朝着以纤维素为起始原料,打通纤维素到葡萄糖转化的关键环节,通过开发高效催化剂和高效催化体系,实现低成本、批量化生产的路线发展,最终实现高性能生物基高分子材料的可持续发展。
[1] SHELDON R A. Utilisation of biomass for sustainable fuels and chemicals:molecules,methods and metrics[J]. Catal. Today,2011,167:3-13.
[2] GALLEZOT P. ChemInform abstract:conversion of biomass to selected chemical products[J]. Chem. Soc. Rev.,2012,41:1538-1558.
[3] IWATA T. Biodegradable and bio-based polymers:future prospects of eco-friendly plastics[J]. Angew. Chem. Int. Ed.,2015,54:3210-3215. [4] BOND J Q,ALONSO D M,WANG D,et al. Integrated catalytic conversion of gamma-valerolactone to liquid alkenes for transportation fuels[J]. Science,2010,327:1110-1114.
[5] RHIM J W. Preparation and characterization of vacuum sputter silver coated PLA film[J]. LWT-Food Science and Technology,2013,54(2):477-484.
[6] HIROE A,USHIMARU K,TSUGE T. Characterization of polyhydroxyalkanoate (PHA) synthase derived from Delftia acidovorans DS-17 and the influence of PHA production in Escherichia coli[J]. Journal of Bioscience and Bioengineering,2013,115(6):633-638.
[7] TAKAHASHI K,KMURA L Y. Melt/solid polycondensation of glycolic acid to obtain high-molecular-weight poly(glycolic acid)[J]. Polymer,2000,41(24):8725-8731.
[8] YE H M,WANG R D,LIU J. Isomorphism in poly(butylene succinate-co-butylene fumarate) and its application as polymeric nucleating agent for poly(butylene succinate)[J]. Macromolecules,2012,45:5667-5675.
[9] BOZELL J J,PETERSEN G R. ChemInform abstract:technology development for the production of biobased products from biorefinery carbohydrates The US Department of Energy[J]. Green Chem.,2010,12(4):539-554.
[10] HAJJ E,MASROUA A,MARTIN J C,et al. Synthesis of 5-(hydroxymethyl)-furan-2-carboxaldehyde and its derivatives by acid treatment of sugars on ion-exchange resins[J]. Soc. Chim. Fr.,1987:855-860.
[11] GRABOWSKI G,LEWKOWSKI J,SKOWRONSK R. The electrochemical oxidation of 5-hydroxymethylfurfural with the nickel oxide/hydroxide electrode[J]. Electrochim. Acta.,1991,36(13):1995.
[12] MIURA T,HIROKAZU K,TAKENOBU K,et al. Method for producing furan-2,5-dicarboxylic acid:US20070232815[P]. 2007-10-04.
[13] VINKE P,POEL W V,BEKKUM H V. On the oxygen tolerance of noble metal catalysts in liquid phase alcohol oxidations the influence of the support on catalyst deactivation[J]. Heterogeneous Catalysis and Fine Chemicals Ⅱ,1991,59:385-394.
[14] VERDEGUER P,MERAT N,GASET A. Oxydation catalytique du HMF en acide 2,5-furane dicarboxylique[J]. Journal of Molecular Catalysis,1993,85(3):327-344.
[15] PARTENHEIMER W,GRUSHIN V V. Synthesis of 2,5-diformylfuran and furan-2,5-dicarboxylic acid by catalytic air-oxidation of 5-hydroxymethylfurfural[J]. Adv. Synth. Catal.,2001,343(1):102-111.
[16] PARTENHEIMER W. Methodology and scope of metal/bromide autoxidation of hydrocarbons[J]. Catalysis Today,1995,23(2):69-158.
[17] LILGA M A,HALLEN R T,Gray M. Production of oxidized derivatives of 5-hydroxymethylfurfural(HMF)[J]. Top. Catal.,2010,5:31264-1269.
[18] LILGA M A,HALLEN R T,HU J. Preparation of 2,5diformylduran from 5-HMF with a heterogeneous mesoporous silver containing manganese catalyst:US20080103318[P]. 2008-05-01.
[19] RASS H A,ESSAYEM N,BESSON M. Selective aqueous phase oxidation of 5-hydroxymethylfurfural to 2,5-furandicarboxylic acid over Pt/C catalysts:influence of the base and effect of bismuth promotion[J]. Green Chem.,2013,15:2240-2251.
[20] RASS H A,ESSAYEM N,BESSON M. Selective aerobic oxidation of 5-HMF into 2,5-furandicarboxylic acid with Pt catalysts supported on TiO2- and ZrO2-based supports[J]. Chemsuschem,2013,8(7):1206-1217.
[21] SIANKEVICH S,SAVOGLIDIS G,FEI Z F,et al. A novel platinum nanocatalyst for the oxidation of 5-hydroxymethylfurfural into 2,5-furandicarboxylic acid under mild conditions[J]. Journal of Catalysis,2014,315:67-74.
[22] CAI J Y,MA H,ZHANG J J,et al. Gold nanoclusters confined in a supercage of Y zeolite for aerobic oxidation of HMF under mild conditions[J]. Chem. Eur. J.,2013,19:14215-14223.
[23] LOLLI A,AMADORI R,LUCARELLI C,et al. Hard-template preparation of Au/CeO2mesostructured catalysts and their activity for the selective oxidation of 5-hydroxymethylfurfural to 2,5-furandicarboxlic acid[J]. Microporous and Mesoporous Materials,2016,226:466-475.
[24] HANG X W,LI C Q,GUO Y,et al. N-doped carbon supported Pt catalyst for base-free oxidation of 5-hydroxymethylfurfural to 2,5-furandicarboxylic acid[J]. Applied Catalysis A:General,2016,526:1-8.
[25] HANGa X W,GENG L,GUO Y,et al. Base-free aerobic oxidation of 5-hydroxymethylfurfural to 2,5-furandicarboxylic acid over a Pt/C-O-Mg catalyst[J]. Green Chem.,2016,18:1597-1604.
[26] ZHANG Y W,XUE Z M,WANG J F,et al. Controlled deposition of Pt nanoparticles on Fe3O4@carbon microspheres for efficient oxidation of 5-hydroxymethylfurfural[J]. RSC Adv.,2016,6:51229-51237.
[27] HARUTA M,KOBAYASHI T,SANO H,et al. Novel gold catalysts for the oxidation of carbon monoxide at a temperature far below 0℃[J]. Chemistry Letters,1987,16(2):405-408.
[28] PINA C D,FALLETTA E,PRATI L,et al. Selective oxidation using gold[J]. Chem. Soc. Rev.,2008,37:2077-2095.
[29] ZHENG N F,STUCKY G D. Promoting gold nanocatalysts in solvent-free selective aerobic oxidation of alcohols[J]. Chem. Commun.,2007,37:3862-3864.
[30] TAARNING E,NIELSEN I S,EGEBLAD K,et al. Chemicals from renewables:aerobic oxidation of furfural and hydroxymethylfurfural over gold catalysts[J]. ChemSusChem,2008,11:75-78.
[31] GORBANEV Y Y,KLITGAARD S K,WOODLEY J M,et al. Gold-catalyzed aerobic oxidation of 5-hydroxymethylfurfural in water at ambient temperature[J]. ChemSusChem,2009,2:672-675.
[32] CASANOVA O,IBORRA S,CORMA A. Biomass into chemicals:aerobic oxidation of 5-Hydroxymethyl-2-furfural into 2,5-furandicarboxylic acid with gold nanoparticle catalysts[J]. ChemSusChem,2009,2(12):1138-1144.
[33] CASANOVA O,IORRA S,CORMA A. Biomass into chemicals:One pot-base free oxidative esterification of 5-hydroxymethyl-2-furfural into 2,5-dimethylfuroate with gold on nanoparticulated ceria[J]. Journal of Catalysis,2009,265(1):109-116.
[34] PASINI T,PICCININI M,BLOSIl M,et al. Selective oxidation of 5-hydroxymethyl-2-furfural using supported gold–copper nanoparticles[J]. Green Chem.,2011,13(8):2091-2099.
[35] AALBONETTI S,PASINI T,LOLLI A,et al. Selective oxidation of 5-hydroxymethyl-2-furfural over TiO2-supported gold–copper catalysts prepared from preformed nanoparticles:effect of Au/Cu ratio[J]. Catalysis Today,2012,195(1):120-126.
[36] SAHA B,DUTTA S,ABU-OMAR M M. Aerobic oxidation of 5-hydroxylmethylfurfural with homogeneous and nanoparticulate catalysts[J]. Catal. Sci. Technol.,2012,2(1):79-81.
[37] VILLA D A,SCHIAVONI M,CAMPISI S,et al. Pd-modified Au on carbon as an effective and durable catalyst for the direct oxidation of HMF to 2,5-furandicarboxylic acid[J]. ChemSusChem,2013,6(4):609-612.
[38] ARDEMANI L,CIBIN C G,DENT A J,et al. Solid base catalysed 5-HMF oxidation to 2,5-FDCA over Au/hydrotalcites:fact or fiction?[J]. Chem. Sci.,2015,6:4940-4945.
[39] YI G S,TEONG S P,LI X C,et al. Purification of eiomass-derived 5-hydroxymethylfurfural and its catalytic conversion to 2,5-furandicarboxylic acid[J]. ChemSusChem,2014,7(8):2131-2135.
[40] YI G,TEONG S P,ZHANG Y G. The direct conversion of sugars into 2,5-furandicarboxylic acid in a triphasic system[J]. ChemSusChem,2015,8(7):1151-1155.
[41] YI G S,TEONG S P,ZHANG Y G. Base-free conversion of 5-hydroxymethylfurfural to 2,5-furandicarboxylic acid over a Ru/C catalyst[J]. Green Chem.,2016,18:979-983.
[42] WANG F,YUAN Z L,LIU B,et al. Catalytic oxidation of biomass derived 5-hydroxymethylfurfural (HMF) over RuIII-incorporated zirconium phosphate catalyst[J]. Journal of Industrial and Engineering Chemistry,2016,38:181-185.
[43] GORBANEV Y Y,KEGNAES S,RIISAAGER A. Effect of support in heterogeneous ruthenium catalysts used for the selective aerobic oxidation of HMF in water[J]. Topics in Catalysis,2011,54(16):1318-1324.
[44] GORBAN Y Y,KEGNAES S,RIISAGER A. Selective aerobic oxidation of 5-hydroxymethylfurfural in water over solid ruthenium hydroxide cwith magnesium-based supports[J]. Catal. Lett.,2011,141(12):1752-1760.
[45] ZHANG Z H,ZHEN J D,LIU B,et al. Selective aerobic oxidation of the biomass-derived precursor 5-hydroxymethylfurfural to 2,5-furandicarboxylic acid under mild conditions over a magnetic palladium nanocatalyst[J]. Green Chem.,2015,17:1308-1317.
[46] LIU B,REN Y S,ZHANG Z H. Aerobic oxidation of 5-hydroxymethylfurfural into 2,5-furandicarboxylic acid in water under mild conditions[J]. Catal. Green Chem.,2015,17:1610-1617.
[47] DAVIS S E,HOUK L R,TAMARGO E C,et al. Oxidation of 5-hydroxymethylfurfural over supported Pt,Pd and Au catalysts[J]. Catal. Today,2011,160(1):55-60.
[48] ROGR M,PRUBE U,VORLOP K D. A new approach for the production of 2,5-furandicarboxylic acid byin situoxidation of 5-hydroxymethylfurfural starting from fructose[J]. Topics in Catalysis,2012,13(3):237-242.
[49] WAN X Y,ZHU C M,CHEN J S,et al. Base-free aerobic oxidation of 5‑hydroxymethyl-furfural to 2,5-furandicarboxylic acid in water catalyzed by functionalized carbon nanotube-supported Au-Pd alloy nanoparticles[J]. ACS Catal.,2014,4:2175-2185.
[50] CHADDERDON D J,XIN L,QI J,et al. Electrocatalytic oxidation of 5-hydroxymethylfurfural to 2,5-furandicarboxylic acid on supported Au and Pd bimetallic nanoparticles[J]. Green Chem.,2014,16:3778-3786.
[51] ALBONETTI S,LOLLIA A,MORANDI V,et al. Conversion of 5-hydroxymethylfurfural to 2,5-furandicarboxylicacid over Au-basedcatalysts:optimization of active phaseand metal-support interaction[J]. Applied Catalysis B:Environmental,2015,163:520-530.
[52] HANSEN T S,SADABA I,GARCIA E J,et al. Cu catalyzed oxidation of 5-hydroxymethylfurfural to 2,5-diformylfuran and 2,5-furandicarboxylic acid under benign reaction conditions[J]. Applied Catalysis A:General,2013,456:44-50.
[53] RIBEIRO M L,SCHUCHARD U. Cooperative effect of cobalt acetylacetonate and silica in the catalytic cyclization and oxidation of fructose to 2,5-furandicarboxylic acid[J]. Catalysis Communications,2003,4(2):83-86.
[54] WANG S G,ZHANG Z H,LIU B. Catalytic conversion of fructose and 5-hydroxymethylfurfural into 2,5-furandicarboxylic acid over a recyclable Fe3O4-CoOxmagnetite nanocatalyst[J]. ACS Sustainable Chem. Eng.,2015,3:406-412.
[55] GAO L C,DENG K J,ZHENG J D,et al. Efficient oxidation of biomass derived 5-hydroxymethylfurfural into 2,5-furandicarboxylic acid catalyzed by Merrifield resin supported cobalt porphyrin[J]. Chemical Engineering Journal,2015,270:444-449.
[56] ZUO X B,VENKITASUBARAMANIAN P,BUSH D H,et al. Optimization of Co/Mn/Br-catalyzed oxidation of 5‑hydroxymethylfurfural to enhance 2,5-furandicarboxylic acid yield and minimize substrate burning [J]. ACS Sustainable Chem. Eng.,2016,4:3659-3668.
[57] DIJKMAN W P,GROOTHUIS D E,FRAAIJE M W. Enzyme-catalyzed oxidation of 5-hydroxymethylfurfural to furan-2,5-dicarboxylic acid[J]. Angew. Chem. Int. Ed.,2014,53(25):6515-6518.
[58] MCKENNA S M,LEIKKULER S,HERTER S,et al. Enzyme cascade reactions:synthesis of furandicarboxylic acid (FDCA) and carboxylic acids using oxidases in tandem[J]. Green Chem.,2015,17:3271-3275.
[59] QIN Y Z,LI Y M,ZONG M H,et al. Enzyme-catalyzed selective oxidation of 5-hydroxymethylfurfural (HMF) and separation of HMF and 2,5-diformylfuran using deep eutectic solvents[J]. Green Chem.,2015,17:3718-3722.
[60] RAECKE B. SynthesevonDiund Tricarbonsäuren aromatischer ringsysteme durch verschiebungvoncarboxyl-gruppen[J]. Angew. Chem. Int. Ed.,1958,70:1-5.
[61] THIYAGARAJAN S,PUKIN A,HAVEREN J V,et al. Concurrent formation of furan-2,5- and furan-2,4-dicarboxylic acid:unexpected aspects of the Henkel reaction[J]. RSC Adv.,2013,3:15678-15686.
[62] PAN T,DENG J,XU Q,et al. Catalytic conversion of furfural into a 2,5-furandicarboxylic acid-based polyester with total carbon utilization[J]. ChemSusChem,2013,6:47-50.
[63] BANERJEE A,DICK G R,et al. Carbon dioxide utilization via carbonate-promoted C–H carboxylation[J]. Nature,2016,531:215-219.
[64] 刘浪,杨顺利,李鸿波,等. 2,5-呋喃二甲酸的合成[J]. 精细化工,2011,28(4):410-412. LIU L,YANG S L,LI H B,et al. The synthesis of 2,5-furandicarboxylic acid[J]. Fine Chemicals,2011,28(4):410-412.
[65] 王静刚,刘小青,朱锦,等. 一种2,5-二酰基呋喃化合物的制备方法:201410763313.2[P]. 2014-12-11. WANG J G,LIU X Q,ZHU J,et al. One method for preparation of 2,5-diacetylfuran:201410763313.2[P]. 2014-12-11.
[66] 王静刚,刘小青,朱锦,等. 一种2,5-呋喃二甲酸的制备方法:201410787166.2[P]. 2014-12-17. WANG J G,LIU X Q,ZHU J,et al. One method for preparation of 2,5-dicarboxylic acid:201410787166.2[P]. 2014-12-17.
[67] WANG J G,LIU X Q,ZHU J,et al. Preparation method for 2,5-furandicarboxylic acid:WO2016095122[P]. 2016-07-23.
[68] LEWKOWSK J. Convenient synthesis of furan-2,5-dicarboxylic acid and its derivative[J]. Polish J. Chem.,2001,75(12):1943-1946.
[69] BRǍTULESCU G. Mass spectra of aromatic azoethers and azoxyethers[J]. Rev. Roum. Chim.,2000,45(9):883-885.
[70] TAGUCHI Y,OISSHI A,IIDA H. One-step synthesis of dibutyl furandicarboxylates from galactaric acid[J]. Chem. Lett.,2008,37(1):50-51.
[71] 李伟杰,陆豫. 合成3,4-二取代呋喃-2,5-二甲酸的简便方法[J]. 化学试剂,2006,28(5):309-310. LI W J,LU Y. Concise synthesis of 3,4-disubstitutedfuran-2,5-dicarboxylic acids[J]. Chemical Reagents,2006,28(5):309-310.
[72] FITTING R,HEINZELMAN H. Ueber neue derivate der schleimsaure[J]. Chem. Ber.,1876,9:1198-1201.
[73] DIEGO C M,DAM M A,GRUTER G J M. Method for the preparation of 2,5-furandicarboxylic acid and for the preparation of the dialkyl ester of 2,5-furandi- carboxylic acid[J:WO2011043661[P]. 2011.
[74] DIEGO C M,DAM M A,GRUTER G J M. Method for the preparation of furandicarboxylic acid and for the preparation of the dialkyl ester of 2,5-furandicaeboxylic acid:US8865921[P]. 2014-10-21.
[75] JANKA M J,PARKER K R,SHAIKH A S,et al. Oxidation process to produce a crude dry carboxylic acid product:US8772513[P]. 2014-07-08.
Research progress on the synthesis of bio-based aromatic platform chemical 2,5-furandicarboxylic acid
WANG Jinggang,LIU Xiaoqing,ZHU Jin
(Ningbo Institute of Materials Technology and Engineering,Chinese Academy of Sciences,Ningbo 315201,Zhejiang,China)
2,5-Furandicarboxylic acid(2,5-FDCA) is a promising bio-based aromatic platform chemical for the synthesis of high performance polymers and has been regarded as the most suitable alternative to the petroleum-derived terephthalic acid. The synthesis of 2,5-FDCA through efficient and low cost route has been a hot subject since last decade. In this review article,the popular starting materials,including 5-hydroxymethyl furfural(HMF),furoic acid,furan,diglycolic acid,and hexaric acid,for the fabrication of 2,5-FDCA,are introduced in detail. Perspectives are given based on the comparison of different synthetic routes. The most popular synthetic route is based on HMF by either directly oxidation,noble metal oxidation,non-noble metal oxidation or enzyme catalysis oxidation. This method is considered as the most promising one to achieve large scale preparation of 2,5-FDCA. More importantly,development of novel technology for the conversion of cellulose to glucose is critical to produce large amount of low cost HMF.
2,5-furandicarboxylic acid;bio-based;platform chemical;synthesis;progress
O63
:A
:1000–6613(2017)02–0672–11
10.16085/j.issn.1000-6613.2017.02.038
2016-03-01;修改稿日期:2016-09-28。
国家自然科学基金(51373194)及国家重点科技支撑项目(2015BAD15B08)。
王静刚(1982—),男,博士研究生,主要研究方向2,5-呋喃二甲酸及其聚合物的合成研究。联系人:刘小青,研究员,研究方向为生物基高分子材料。E-mail:liuxq@nimte.ac.cn。
