乙酰丙酮分光光度法测定土壤中甲醛
2017-02-16姚洁丹孙丹钟灿红方哲张瑶琴
姚洁丹,孙丹,钟灿红,方哲,张瑶琴
(1.宁波远大检测技术有限公司,浙江宁波 315105; 2.慈溪市环境保护监测站,浙江慈溪 315300)
乙酰丙酮分光光度法测定土壤中甲醛
姚洁丹1,孙丹2,钟灿红1,方哲1,张瑶琴1
(1.宁波远大检测技术有限公司,浙江宁波 315105; 2.慈溪市环境保护监测站,浙江慈溪 315300)
建立乙酰丙酮分光光度法测定土壤中甲醛含量的分析方法。在磷酸介质中,土壤中的甲醛经过加热蒸馏提取,与乙酰丙酮反应生成黄色的二乙酰基二氢二甲基吡啶,然后于412 nm波长处测定其吸光度。甲醛含量在0.0~25 μg范围内与吸光度呈良好的线性关系,线性相关系数r=0.999 6,加标回收率为76.2%~87.5%,方法检出限为0.03 mg/kg,定量限为0.12 mg/kg,测定结果的相对标准偏差为2.73%~3.68%(n=6)。该方法灵敏度高,分析速度快,适用于土壤中甲醛含量的测定。
土壤;甲醛;乙酰丙酮;分光光度法
甲醛是一种具有强还原性的原生质毒素物质[1],它对人体的皮肤和粘膜具有刺激和致敏作用,进入人体后易对人体的中枢神经及视网膜造成损害,并具有致畸、致癌作用。而当甲醛进入水体后,能消耗水中的溶解氧,影响水体的自净能力,造成水质恶化。在环境监测分析研究中,水环境中甲醛的测定多采用乙酰丙酮分光光度法、变色酸光度法[2–4];空气中甲醛的测定采用分光光度法(乙酰丙酮法、变色酸法、酚试剂法等)[5–6];食品中的甲醛采用定性筛选方法和定量测定方法,如分光光度法、高效液相法、催化动力学法、滴定法[1,7]。
目前土壤中甲醛含量的测定国家还未出台相关检测标准,文献报道的方法有衍生化–高效液相色谱法[8],但该方法反应过程复杂,操作繁琐,仪器要求高。乙酰丙酮分光光度法[9–12]已被纳入水质、空气以及食品领域中甲醛检测的国家标准中,该方法选择性好,灵敏度高,操作简单。笔者借鉴食品[7,13]、板材涂料中甲醛[14–15]的提取方法及土壤中甲醛测定方法研究[8],采用乙酰丙酮分光光度法测定土壤样品提取液中甲醛的含量,该方法测定结果准确可靠。
1 实验部分
1.1 主要仪器与试剂
722S分光光度计:上海菁华科技仪器有限公司;
数显恒温水浴锅:常州国华电器有限公司;
磷酸:优级纯;
石英砂:分析纯;
乙酸铵、乙酰丙酮:分析纯;
乙酰丙酮溶液:称取25 g乙酸铵,溶于100 mL蒸馏水中,加入3 mL冰乙酸和0.4 mL乙酰丙酮,摇匀,贮存于棕色瓶中,在2~8℃冰箱内可以保存1个月。
甲醛标准溶液:100 µg/mL,标准编号为GBW(E)082266;
甲醛标准使用液:5µg/mL,用蒸馏水对甲醛标准溶液稀释而成,现用现配;
实验用水为蒸馏水。
1.2 方法原理
土壤中的甲醛在磷酸介质中直接加热蒸馏,冷凝后经水溶液吸收,蒸馏液与乙酰丙酮在过量铵盐的存在下,生成黄色的二乙酰基二氢二甲基吡啶,用分光光度计于412 nm处比色定量[7,14]。
1.3 实验方法
1.3.1 样品处理
按HJ/T166规定采集土壤样品,充分混匀,取500 g备用,装入棕色采样瓶中。准确称取土壤样品10 g,置于500 mL圆底烧瓶中,加入250 mL蒸馏水,用玻璃棒搅拌均匀,浸泡30 min后加入10 mL磷酸溶液(1+9),立即加热蒸馏。接收管下口事先插入盛有20 mL的蒸馏水且置于冰浴的蒸馏液接收装置中。收集蒸馏液约225 mL后倒入250 mL的容量瓶中,用蒸馏水洗涤接收管并倒入容量瓶,然后容至标线,同时做空白对照试验(用石英砂代替土壤)。
1.3.2 标准曲线绘制
分别精密吸取甲醛标准使用溶液0.00,0.50,1.00,2.00,3.00,4.00,5.00 mL于20 mL比色管中,加水至10 mL。加入1 mL乙酰丙酮溶液,混合均匀,置于60℃水浴中加热15 min,取出,用水冷却至室温。以空白液为参比,于波长412 nm处,以1 cm比色皿测定吸光度,绘制标准曲线。
1.3.3 样品测定
根据样品蒸馏液中甲醛浓度的高低,吸取蒸馏液1.00~10.00 mL,补充蒸馏水至10 mL,加入1 mL乙酰丙酮溶液,混合均匀,置于60℃水浴中加热15 min,取出,用水冷却至室温,测定吸光度。
1.4 结果计算
土壤中甲醛含量按式(1)计算:
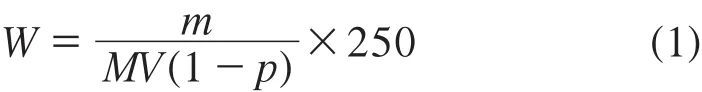
式中:W——土壤中甲醛的含量,mg/kg;
m——从工作曲线上查得的甲醛的量,µg;
M——样品质量,g;
V——样品测定时移取蒸馏液的体积,mL;
P——样品含水率,%;
250——蒸馏液总体积,mL。
2 结果与讨论
2.1 样品前处理方法的选择
取同一土壤样品10份(每份10 g),按以下4种不同的方法进行前处理,然后取样10 mL,加入1 mL乙酰丙酮溶液,于60℃水浴下加热15 min。
方法1:加入250 mL蒸馏水,混匀,浸泡15 h后直接过滤;
方法2:加入250 mL蒸馏水浸泡30 min,直接蒸馏,接收管下口事先插入盛有20 mL蒸馏水且置于冰浴的蒸馏液接收装置中,收集蒸馏液约225 mL后倒入250 mL容量瓶中,用蒸馏水洗涤接收管并倒入容量瓶,定容至标线;
方法3:加入250 mL蒸馏水浸泡30 min,然后加入10 mL磷酸溶液(1+9)后立即直接蒸馏,下同方法2。
方法4:加入20 mL蒸馏水浸泡30 min,加入10 mL磷酸溶液(1+9)后立即通入水蒸气蒸馏,下同方法2。
经以上方法处理后样品测定结果见表1。
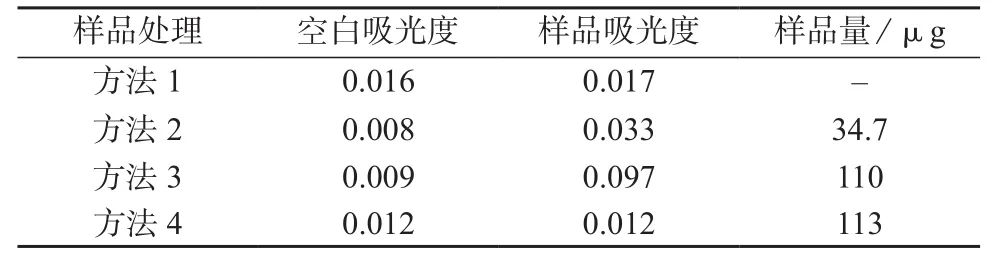
表1 不同前处理法所得样品质量
根据表1数据可知:(1)仅对土壤采取浸泡处理,无法将土壤中的甲醛提取出来;(2)通过比较方法2和方法3可知,磷酸介质的存在有利于甲醛的提取;(3)蒸馏加热方法和蒸汽加热方法对土壤甲醛的测定结果无显著性差异。综合考虑,本实验采用蒸馏加热的方法提取土壤中的甲醛。
2.2 反应温度和反应时间
用甲醛标准使用液配制44组平行样(移取甲醛标准使用液2.00 mL于20 mL比色管中,用蒸馏水定容至10 mL,甲醛的含量为10 µg)加入1 mL乙酰丙酮溶液,摇匀。于40,60,100℃的恒温水浴锅中加热,加热完毕后取出用冷水冷却至常温,用10 mm比色皿,于412 nm波长处以水为参比测定吸光度,测定结果见表2。不同水浴温度下,显色时间与吸光度的关系曲线见图1。通过比较表2中吸光度数据和图1中的曲线,选择在60℃恒温水浴条件下显色15 min。
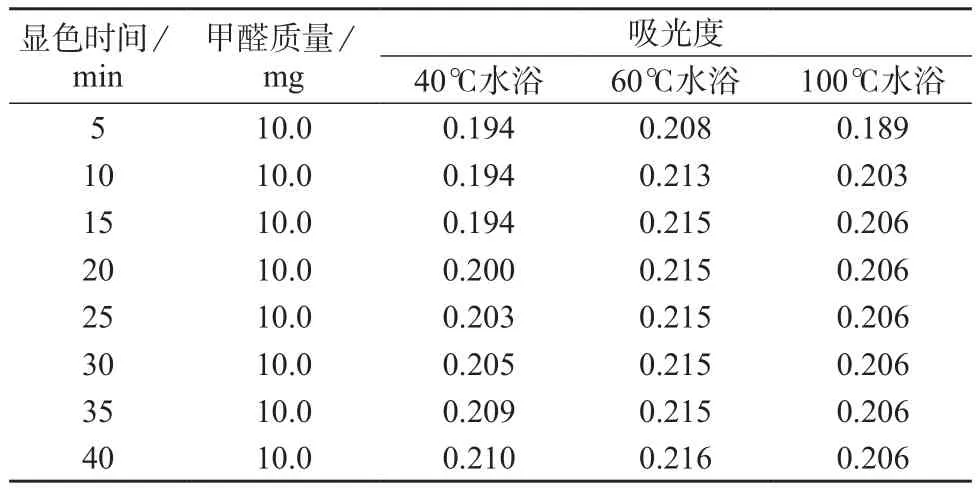
表2 水浴温度不同时甲醛使用液的吸光度
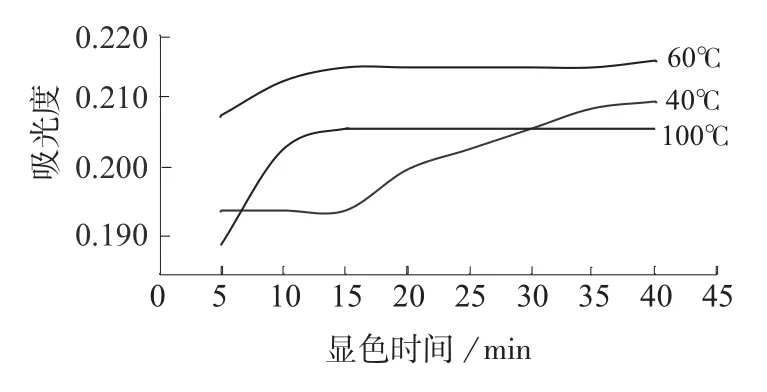
图1 不同水浴温度下显色时间与吸光度的关系
2.3 工作曲线方程及检出限
精密吸取甲醛标准使用液0.00,0.50,1.00,2.00,3.00,4.00,5.00 mL于20 mL比色管中,加水至10 mL。加入1 mL乙酰丙酮溶液,混合均匀,置于60℃水浴中加热15 min,取出,用水冷却至室温。以空白液为参比,于波长412 nm处,以1 cm比色皿测定吸光度,结果见表3。
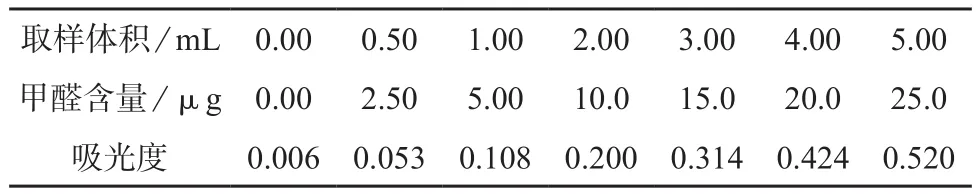
表3 系列标准溶液及吸光度测定结果
以甲醛的含量(X)为横坐标,对应的吸光度(Y)为纵坐标绘制标准曲线。甲醛的质量在0~25 µg范围内与吸光度呈良好的线性关系,线性回归方程为Y=0.0208X–0.003 9,相关系数r=0.999 6。以3倍标准偏差计算检出限,以4倍检出限计算定量限,得到该方法测定甲醛的检出限为0.03 mg/kg,定量限为0.12 mg/kg。
2.4 精密度与加标回收试验
按1.3实验方法,取6份土壤进行平行测定,结果样品本底值均小于检出限。另取18份土壤样品分为3组,每组分别加入0.5,1.0,2.0 mL甲醛标准溶液(100 µg/mL)。按1.3实验方法进行测定,结果见表4。由表4可知,甲醛的加标回收率为76.2%~87.5%,测定结果的相对标准偏差为2.73%~3.68%,说明该方法的精密度和准确度良好,满足检测要求。
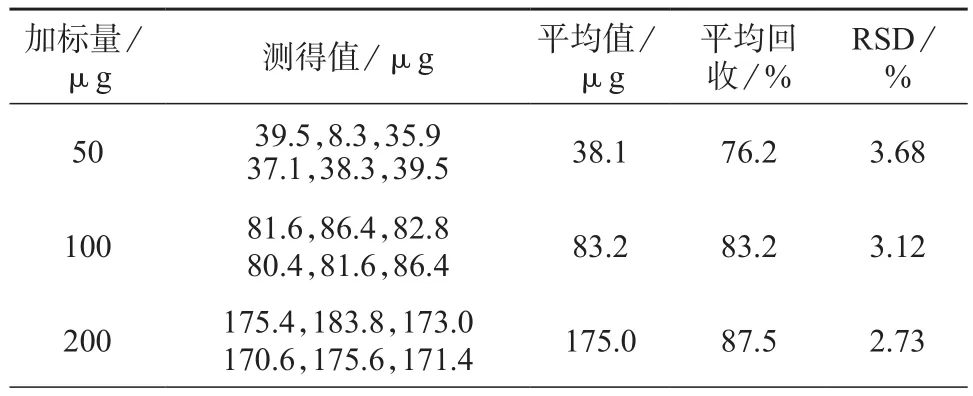
表4 回收率与精密度试验结果(n=6)
3 结语
采用乙酰丙酮分光光度法测定土壤中的甲醛含量,土壤样品中加入250 mL蒸馏水浸泡30 min后,在磷酸介质中直接加热蒸馏提取其中的甲醛,样品前处理方法简单,甲醛的测定结果准确可靠。该方法灵敏度高,操作简单,分析速度快,是一种易于推广的检测方法,适用于农业等领域甲醛的测定。
[1] 周群惠,彭琨,王洋.食品中甲醛测定新进展及各种方法的比较[J].食品科技,2004(10): 75–79.
[2] 魏复盛.水和废水监测分析方法[M].4版.北京:中国环境科学出版社,2002.
[3] GB 601–2011 水质甲醛的测定乙酰丙酮分光光度法[S].
[4] GB/T 5750.10–2006 生活饮用水标准检验方法 消毒副产物指标[S]
[5] 国家环境保护总局,空气和废气监测分析方法编委会.空气和废气监测分析方法[M].北京:中国环境科学出版社,2003.
[6] 李忠军,邹训重,黎彧,等.甲醛测定方法的进展概述[J].广东微量元素科学,2014,21(6): 28–31.
[7] SC/T 3025–2006 水产品中甲醛的测定[S].
[8] 杨俊衡.高效液相法测定土壤中甲醛的含量[J].湘潭师范学院学报:自然科学版,2008,30(1): 76–78.
[9] 韩宏伟.食品中甲醛的检测方法[J].国外医学:卫生学分册,2008,35(5): 318–332.
[10] 黄智勇,张剑.室内空气中甲醛测定方法研究现状[J].中国公共卫生.2006,22(2): 231–233.
[11] 黎瑞敏.室内空气中甲醛测定方法的比较[J].黑龙江环境通报,2012,36(4): 78–81.
[12] 金米聪.微量甲醛检测研究进展[J].中国公共卫生,2003,19(1): 101–102.
[13] 叶艺娟,周国慧,陈轶男.乙酰丙酮法测定食品中甲醛及前处理方法探讨[J].海峡预防医学杂志,2008,14(4): 50–51.
[14] GB 18583–2008 室内装饰装修材料粘合剂中有害物质限量[S].
[15] 魏晶晶,刘心同,薛秋红,等.水性涂料中甲醛测定方法研究现状[J].上海涂料,2010,48(8): 41–44.
Determination of Formaldehyde Content in Soil by Acetylacetone Spectrophotometry
Yao Jiedan1, Sun Dan2, Zhong Canhong1, Fang Zhe1, Zhang Yaoqin1
(1. Ningbo Yuanda Testing Technology Co., Ltd., Ningbo 315014, China; 2. Cixi Environmental Protection Bureau, Cixi 315300, China)
A method was established to determine formaldehyde content in soil by acetylacetone spectrophotometry. The formaldehyde in soil was heated by distillation in phosphoric acid medium,then reacted with acetylacetone to form yellow complex,absorbance of the complex was determined at 412 nm. The content of formaldehyde was linear with the absorbance in the range of 0.0–25µg, the correlation coeffcient was 0.999 6. The additon recovery was 76.2%–87.5%,the detection limit was 0.03 mg/kg. The relative standard deviation of determination results was 2.73%–3.68% (n=6). This method has advantages of high sensitivity,quick analysis,and it is suitable for the determination of formaldehyde content in soil.
soil; formaldehyde; acetylacetone; spectrophotometry
O657.3
:A
:1008–6145(2017)01–0085–03
10.3969/j.issn.1008–6145.2017.01.022
联系人:姚洁丹;E-mail: 786399316@qq.com
2016–11–09
