几种不锈钢和镍在高温碱液中的腐蚀行为
2017-02-10
(海军工程大学 理学院 材料科学与工程系,武汉 430033)
几种不锈钢和镍在高温碱液中的腐蚀行为
殷华敏,李国明,陈珊,刘亚强,孟令岽
(海军工程大学 理学院 材料科学与工程系,武汉 430033)
目的 为了减少制碱设备在碱液蒸发浓缩阶段发生的严重腐蚀。方法 采用静浸泡、电化学稳态极化测试技术、光学显微镜和扫描电镜(SEM)观察,以及XRD,XPS腐蚀产物分析等试验方法,研究几种材料(26-1,30-2,18-8Ti和Ni)在高温高浓碱液中的腐蚀行为。结果 在150 ℃、50%NaOH的碱液中,加入NaClO3会使18-8Ti的耐蚀性提高,却使镍的耐蚀性降低。只有碱液中NaClO3含量适量时(如0.15%NaClO3),才能使26-1和30-2和耐蚀性提高,NaClO3含量过多或过少,均使26-1和30-2耐蚀性降低。结论 Cl–的加入能够降低镍和18-8Ti和耐蚀性,而使30-2的耐蚀性提高,与18-8Ti相比,26-1和30-2的耐蚀性有着显著的提高。
不锈钢;镍;高温碱液;腐蚀
对制碱业影响很大的技术难题之一,就是生产过程中,设备及管道、阀门等的腐蚀问题。近年来,由于金属钛及非金属材料的使用,加之材料性能的改善,制造及防腐技术的提高,虽然在盐水制备、精制、输送生产系统中,问题已不很突出[1—8,15—17],但在碱加工过程,尤其是蒸发浓缩系统中,设备的腐蚀问题仍一直是厂家和科技工作者关注的焦点[11—15]。因为腐蚀不仅对产品的质量及生产安全带来问题,而且因停工检修或更换管道更会带来巨大的经济损失[9—10]。尽管早在苏联时代就已开始研究不锈钢等材料在强碱溶液中的耐蚀性问题[13],在理论上也有人做了一些相关的工作,但在隔膜法碱液中,NaClO3和 NaCl对腐蚀起什么作用等,仍缺乏深刻的理解[12—13,15]。由于浸泡时间短,温度相对较低,且试验前后介质环境变化很大,因而对这一问题并没有给出很令人信服的答案。对某些材料,如1Cr18Ni9Ti不锈钢(以下简称 18-8Ti)、镍、E-Brite-26-1不锈钢(以下简称 26-1)、SHOMAC钢(以下简称 30-2)等,在高温高浓碱液中的腐蚀行为进行深入的研究,将对这一问题的解决有很大的帮助。
1 试验
1.1 试验材料
试验所用的材料为26-1,30-2,18-8Ti和Ni200。各材料的化学成分见表1,其中18-8Ti和Ni为供货态,26-1经900 ℃固溶30 min后水冷。从几种材料的金相显微组织可以看出,18-8Ti晶粒细小,但明显可见轧制带状组织依然存在。26-1和30-2处理后晶粒粗大,取材方向均为沿轧制方向。

表1 试样材料的化学成分
1.2 电化学试验方法
电化学试验在高压釜中进行,试验温度为(150±1)℃。样品为Φ10 mm×10 mm的圆柱体,试样采用聚四氟乙烯紧配合方式封装,参比电极为 AgCl电极,参比电极在使用前后皆与甘汞电极进行校对,认为前后电位差不超过 10 mV为可靠。铂片作辅助电极,所有电极引线均由聚四氟乙烯管套装引出,动电位扫描速度为10 mV/min。试验所用仪器有HA-3.1型恒电位仪、HB104型函数发生器、HB-102型对数转换器和3080A4X-Y型记录仪。
1.3 静浸试验
静浸试验在高压釜中进行,试验温度为(150±1)℃。试样在试验前均精心去除边缘毛刺,用砂纸打磨至 400#,然后用清水冲洗,用酒精、丙酮除去表面油污、灰尘,置于干燥皿中备用。试验时间为200 h,试验后腐蚀产物用毛刷清洗,擦除,然后用脱脂棉擦拭干净,最后再用酒精、丙酮清洗,干燥后用分析天平称量。
1.4 腐蚀形貌观察与表面膜分析
腐蚀试验后用X-射线衍射(XRD)和X-射线光电子能谱(XPS)分析腐蚀产物和表面膜的成分以及结构,并在光学显微镜和扫描电镜(SEM)下对形貌进行观察。
2 结果与分析
2.1 电化学试验结果
对18-8Ti和26-1在NaOH中的极化研究(如图1—2所示)表明,18-8Ti在三种溶液中极化曲线形状大致相同,都存在一钝化区。随NaClO3含量增大,自腐蚀电位提高,维钝电流减小,钝化区间扩大,而且对含NaClO3和不含NaClO3的体系,二者的钝化区有着显箸的差别,加入NaClO3的体系中,18-8Ti明显提前钝化,且腐蚀电流也明显降低。从图2可看出,26-1在添加0.05%的NaClO3溶液中,钝化区减小,提前过钝化,而二次钝化范围也很狭窄,且维钝电流小于一次钝化。在50%NaOH溶液中有着很宽的钝化区,钝化区间在-1000~-500 mV之间,且维钝电流几乎为0,添加0.05%NaClO3使自腐蚀电位由-1144 mV降为-1240 mV。对照图1和2可以看出,26-1在所有环境下电流密度均比18-8约小一个数量级。
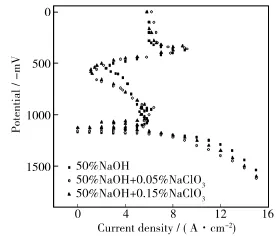
图1 18-8Ti在碱性溶液中的极化曲线

图2 26-1在碱性溶液中的极化曲线
2.2 浸泡试验结果
在50%NaOH加不同浓度NaClO3的溶液中的浸泡结果表明,随 NaClO3浓度的增加,18-8Ti腐蚀质量损失减少。当NaClO3的质量分数由0增加到0.05%时,腐蚀质量损失几乎成线性急剧减小,而后再增加NaClO3的含量,质量损失率减小得较少,如图 3所示。这说明随着 NaClO3含量的增加,18-8Ti表面形成的产物膜也逐渐变得致密,保护性增加,使材料显示出很好的耐蚀性。从图 4可以看出,26-1和 30-2的腐蚀质量损失率随NaClO3浓度的增加,变化规律大致相同。当NaClO3的质量分数由0增加到0.05%时,腐蚀质量损失剧增,随后,当NaClO3质量分数达 0.15%时,质量损失又减小。继续增加 NaClO3的质量分数到 0.8%,腐蚀质量损失又急剧增加。总的来看,溶液中NaClO3质量分数为0.15%时,耐蚀性最好。在50%NaOH含不同NaClO3杂质的环境下(图4)镍(Ni200)表现出良好的耐腐蚀性,随 NaClO3含量的升高,开始时,腐蚀率由0增大;当NaClO3质量分数增加到 0.05%后,腐蚀率又逐渐下降,NaClO3含量到0.8%时,腐蚀率降为0。
总的看来,当碱液中只含NaClO3杂质时,Ni具有最佳的耐蚀性,26-1的腐蚀率是Ni的10倍左右,甚至更高。当NaClO3的质量分数为0.8%时,18-8Ti与26-1,30-2的腐蚀率相差不大。当NaClO3含量较低时(质量分数为 0~0.15%),18-8Ti的腐蚀率急剧增大,为 26-1的几十倍乃至上百倍,相差两个数量级左右。另外,对比26-1和30-2的结果(如图4所示)还可以看出,NaClO3含量较低时(0~0.05%)26-1的耐蚀性比30-2好,而当含量较高时(0.15%~0.8%),30-2的耐蚀性比26-1好。这些都表明NaClO3杂质的含量对材料的耐蚀性有很大影响。

图3 18-8Ti在溶液中的腐蚀率与溶液中NaClO3含量的关系

图4 不同材料在溶液中的腐蚀率与溶液中NaClO3含量的关系(注:标有“ *”表示溶液中含5%NaCl)
2.3 表面腐蚀产物分析及观察
2.3.1 产物膜的XRD和XPS分析
表面腐蚀产物及表面膜的XRD和XPS分析结果见表2。
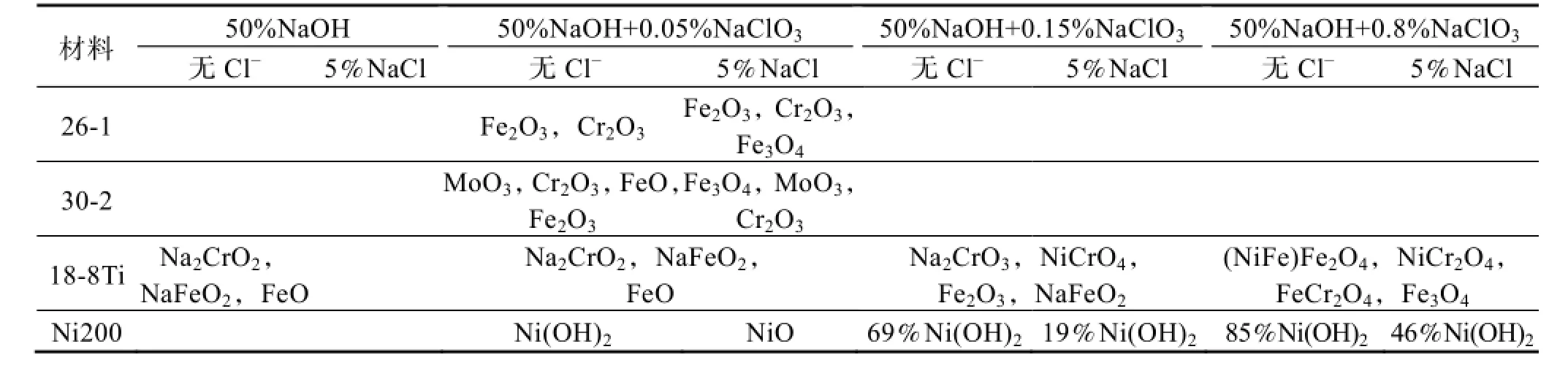
表2 表面产物和表面膜的XRD和XPS分析结果
2.2.2 表面腐蚀形貌观察
对浸泡试样进行表观检查,发现 18-8Ti在50%NaOH和50%NaOH+0.05%NaClO3以及其含Cl–的溶液中,腐蚀产物结构疏松,呈黑色,用棉球即可擦除。当 NaClO3浓度增大后,腐蚀产物逐渐变得致密,到0.8%NaClO3时,已完全形成一层致密的黑色保护膜(如图5a所示),而样品的边缘存在膜剥落的现象,且在含 Cl-的溶液中膜剥落情况更严重。随NaClO3浓度的增加,Ni表面腐蚀产物由零星淡黄色逐渐变成深灰色,颜色加深,产物膜加厚,致密性越来越好,且在含Cl–的介质中产物膜颜色均比不含Cl–的深,表面膜完整性也较差,为灰黑色(如图5b—5d所示)。26-1和30-2在碱液中,表面腐蚀产物膜颜色也随NaClO3浓度的增加而变深,由亮银色变为暗亮色到深棕黄色,含与不含Cl–区别不大。

图5 样品表面腐蚀产物的代表腐蚀形貌
对于18-8Ti来说,随溶液中氯酸钠浓度的增加,溶液的氧化性增强,试样表面的腐蚀产物由亚稳的氧化物逐渐过渡到稳定的氧化物,产物的致密性逐渐增强,耐蚀性也变好。18-8Ti在溶液中的极化试验也说明了这一点。氯离子使得其在氯酸钠浓度较高的高温碱液中耐蚀性变差。
26-1和30-2在碱液中的腐蚀很大程度上与氧化剂的含量有关,在不加Cl–的情况下,随NaClO3含量的增高出现几个转折点。在纯的50%NaOH溶液中,金属表面并没有形成很好的钝化膜,因此腐蚀率相对较高,加入NaClO3氧化剂后,在含量较少的情况下,生成的Fe2O3和Cr2O3膜的保护性并非很高,与此同时,加剧了晶间腐蚀的速度,从而使得耐蚀性进一步降低。当 NaClO3含量达到一定程度后,表面形成完整的钝化膜,因而腐蚀速率大大降低,继续提高NaClO3含量,氧化性增强,由于过钝化的发生,耐蚀性又会显著降低。
加入Cl离子后,30-2的耐蚀性普遍提高,从对30-2在50%NaOH+0.05%NaClO3+5%NaCl中表面的XPS分析结果中可以看出,此时的钝化膜由Fe3O4和Cr2O3组成。这样的膜层结构致密,保护性好,说明在这种情况下,Cl–对优良钝化膜的形成是有利的。另外,由于 Cl–的介入,使得晶间腐蚀受到抑制,这同样也使材料的耐蚀性提高。
26-1在加入Cl–后的一些特性与30-2稍有不同,在50%NaOH+0.05% NaClO3的情况下,其耐蚀性并不像30-2那样,比未加Cl-离子的好,其原因是26-1中的Mo含量比30-2低。Mo是抑制点蚀的有利元素,因此在这样的情况下,26-1虽然晶间腐蚀得到抑制,但由于点蚀加剧,从而使耐蚀性得不到提高。另外,二者钝化膜组成上的差异也是一个原因。从XPS的结果可以知道,30-2此时的膜由Fe3O4和Cr2O3组成,26-1的膜则由 Fe2O3,Fe3O4和 Cr2O3组成,主要是由于 26-1钝化膜中疏松 Fe2O3的掺入,使得保护性降低。
Ni(OH)2钝化膜的形成应该有一个形核和长大的过程,在金属的晶界、夹杂等缺陷处或溶解处将优先形核,按照能量最低原理,初期形成的细小晶核呈圆球形。依形核动力学,晶核在后期如能继续长大,必须达到临界尺寸。在溶液中NaClO3含量较低的情况下,由于未能形成连续的钝化膜,Ni(OH)2晶核将按球形继续长大。随NaClO3含量提高,形核和长大的速度增大,晶核的长大将遇到临近晶粒的阻碍,而长大成无定形。产物膜的这种形貌,使颗粒之间的结合更加紧密,钝化膜的保护作用也随之加强。
根据上面所述可以很好地解释镍在碱液中的腐蚀行为。当碱液中 NaClO3的含量不高时,一方面由于有利的形核位置较少,晶核的形核较困难;另一方面,此时Ni(OH)2的生成速度也较慢,能长大到临界尺寸的晶核数量也很少。因此此时晶核的形核速度很慢,镍在表观上表现为溶解而腐蚀。当碱液中NaClO3含量达到一定值时(如质量分数为 0.15%),镍的溶出相对较快,Ni(OH)2晶核的形核和长大速度均较快,金属表面将被钝化膜完全覆盖,在宏观上镍表现为因钝化膜的形成而使腐蚀减缓。同理,当 NaClO3含量很高时,钝化膜的形成也更快,此时形成的膜更致密,保护性更好,金属的腐蚀完全受到控制。当溶液中还含有Cl–时,由于Cl–对钝化膜的破坏作用,将使镍的耐蚀性大为降低。
3 结论
1)在高温碱液中,随氯酸钠浓度增加,18-8Ti耐蚀性增加;30-2和 26-1的耐蚀性则呈现周期性的变化;镍的耐蚀性先减小后增加。
2)在高温碱液中,随氯酸钠浓度增加,18-8 Ti的表面腐蚀产物膜越来越致密。
3)氯离子使镍和 18-8的耐蚀性变差,使 26-1和30-2的耐蚀性稍有增加。
[1] 郭强, 杨艳芹. 不锈钢在聚甲醛装置模拟介质中的腐蚀行为[J]. 装备环境工程, 2014, 11(4): 98—103.
[2] 丁国清, 杨海洋, 杨万国, 等. 两种不锈钢在冷却塔冷凝酸液中的耐蚀性能[J]. 装备环境工程, 2014, 11(2): 13—18.
[3] 江镇海. 氯碱工业设备的腐蚀与防腐材料的选用[J]. 清洗世界, 2005, 21(6): 29—33.
[4] HINDS G, WICKSTROM L, MINGARD K, et al. Impact of Surface Condition on Sulphide Stress Corrosion Ceraking of 316L Stainless Steel[J]. Corrosion Science, 2013, 71: 43—52.
[5] 苏驰, 吴丽娟. 氯碱生产中自控专业常见腐蚀问题与预防处理[J]. 中国氯碱, 2012(12): 34—46.
[6] 朱自勇, 魏翔云. 不同材料在高温碱液中的腐蚀行为[J].腐蚀科学与防护技术, 1993, 3(1): 1—12.
[7] 刘金华. 氯碱生产中的腐蚀与防护[J].中国氯碱, 2008(2): 35—38.
[8] SAKAKI T, SAKIYAMA K. Corrosion of Iron-Chromium Alloys in Hot Concentrated Caustic Soda Solution[J]. Journal of Japan Institute of Metals, 1979, 43(6): 1186—1190.
[9] 王玉荣, 乌日根. 制碱工业设备的腐蚀问题及防蚀措施[J]. 天津化工, 2012, 26(1): 46—48.
[10] SONG G, JOHANNESSON B, HAPUGODA S, et al. Galvanic Corrosion of Magnesium Alloy AZ91D in Contact with an Aluminum Alloy Steel and Zinc[J]. Corrosion Science, 2004, 46(4): 955—977.
[11] 李国明, 朱自勇, 陈学群, 等. 高温碱液中NaClO3杂质浓度对 1Cr18Ni9Ti耐蚀性的影响[J]. 材料保护, 2009, 42(6): 23—25.
[12] 张瑞珠, 赵元元, 严大考, 等. 1Cr18Ni9Ti不锈钢表面电火花熔覆WC涂层特性研究[J]. 表面技术, 2015, 44(4): 84—88.
[13] 齐敏. 国外氯碱工业的腐蚀及腐蚀控制[J]. 氯碱工业, 1992(2): 28—35.
[14] 陈燕鹏, 董振国. 氯碱生产中的腐蚀及常用防腐蚀措施[J]. 全面腐蚀控制, 2010, 11(3): 36—38.
[15] 陆世英. 不锈钢应力防蚀事故分析与耐应力腐蚀不锈钢[M]. 北京: 原子能出版社, 1985.
[16] 孙亮, 侯艳宏, 杨席, 等. 炼油加工过程中氯离子与硫离子对316L不锈钢和Monel合金腐蚀的影响[J]. 表面技术, 2015, 44(12): 41—45.
[17] 王世常. 隔膜烧碱蒸发设备和管道材料防蚀及其防护措施[J]. 氯碱工业, 1983(5): 52—62.
Corrosion Behaviors of Several Kinds of Stainless Steel and Nickel in High Temperature Alkali Solutions
YIN Hua-min,LI Guo-ming,CHEN Shan,LIU Ya-qiang,MENG Ling-dong
(Materials Science and Engineering, College of Science, Naval University of Engineering, Wuhan 430033, China)
Objective To reduce severe corrosion of alkali production equipment in evaporation and concentration of alkali solution. Methods Static immersion, electrochemical static polarization measurement technology, optical microscope and scanning electron microscope were used for observation. Test methods such as XRD, XPS corrosion product analysis, etc. were used to analyze corrosion behaviors of several kinds of materials (26-1, 30-2, 18-8Ti and Ni) in high temperature and high concentration alkali solution. Results The corrosion resistance of 18-8Ti would increase if NaClO3was added to 50%NaOH at 150 ℃ . But the corrosion resistance was nickel decreased. The corrosion resistance of 26-1 and 30-2 would increase only if NaClO3in alkali solution is proper (0.15%NaClO3for example); otherwise, the corrosion resistance of 26-1 and 30-2 would decrease. Conclusion Adding Cl–increases corrosion resistance of nickel and 18-8Ti, and thus increases the corrosion resistance of 30-2. Compared with 18-8Ti, the corrosion resistance of 26-1 and 30-2 increases more apparently.
stainless steel; nickel; high temperature alkali solution; corrosion
10.7643/ issn.1672-9242.2017.01.003
TJ07;TG172
A
1672-9242(2017)01-0009-05
2016-08-19;
2016-08-26
殷华敏(1993—),女,山东人,硕士生,主要研究方向为船用金属材料的腐蚀与防护。
