漆酶固定化磁性载体的研究进展
2017-02-09王珏玉范丽莉
王珏玉,范丽莉,王 炎,赵 敏*
(1.东北林业大学生命科学学院,黑龙江 哈尔滨 150040;2.中国科学院东北地理与农业生态研究所,黑龙江 哈尔滨 150081;3.哈尔滨工业大学化学工程与技术学院,黑龙江 哈尔滨 150001)
漆酶固定化磁性载体的研究进展
王珏玉1,范丽莉2,王 炎3,赵 敏1*
(1.东北林业大学生命科学学院,黑龙江 哈尔滨 150040;2.中国科学院东北地理与农业生态研究所,黑龙江 哈尔滨 150081;3.哈尔滨工业大学化学工程与技术学院,黑龙江 哈尔滨 150001)
漆酶是一种多铜氧化酶,催化效率高且催化反应的唯一副产物是水,是一种绿色环保的生物催化剂。漆酶催化底物范围广,在多个领域都有重要应用潜能。磁性载体固定漆酶可实现漆酶的磁性回收和重复使用、降低漆酶的使用成本、提高漆酶的稳定性,近年来已成为漆酶固定化研究的热点。对不同漆酶固定化磁性载体的制备方法、固定化漆酶的催化性能及应用进行了综述,比较分析了不同磁性载体的负载量和固定化漆酶的活性回复率,为漆酶固定化磁性载体的开发应用提供帮助。
漆酶;固定化;磁性载体;负载量;活性回复率

游离漆酶在反应体系中难以回收,因而使用成本较高。漆酶固定化是将漆酶分子固定于载体上,使漆酶分子更加稳定并能够被分离和重复利用的一种技术。固定化漆酶和游离漆酶相比往往具有更高的热稳定性,并对化学试剂具有更强的抵抗能力。将漆酶固定化,对降低漆酶使用成本、促进漆酶的实际应用具有重要意义[3-4]。
目前,文献报道的漆酶固定化载体主要有纳米材料、介孔材料、壳聚糖、硅胶和亲水性微滤膜等[5-7]。Fe3O4纳米粒子具有饱和磁化强度高和超顺磁性等优异的磁学性能,近年来常用其与其它材料结合用于漆酶的固定,固定化漆酶在磁场作用下可从反应体系中迅速分离,有利于漆酶的回收和重复再利用,同时也降低了漆酶的使用成本[7-8],具有重要的应用潜能。为寻找价廉且易于回收的磁性载体、提高固定化漆酶的实际应用能力,为磁性载体固定化漆酶的应用研究提供依据,作者在此对近年来报道的用于漆酶固定化的磁性载体的制备方法以及固定化漆酶的催化性能和应用进行了综述,并总结了不同磁性载体的特点,比较分析了不同磁性载体固定化漆酶的负载量和固定化漆酶的活性回复率,拟为漆酶固定化磁性载体的开发应用提供帮助。
1 磁性纳米粒子
尺寸为纳米级的磁性粒子可作为漆酶的固定化载体,与其它漆酶固定化载体相比,磁性纳米粒子比表面积更大,对漆酶的负载量较大,可与底物充分接触,具有良好的催化效果[9-10]。目前用于固定漆酶的磁性纳米粒子主要是Fe3O4,漆酶可通过共价结合、亲和吸附或交叉联合等方法固定于Fe3O4纳米粒子(Fe3O4-NPs)表面[11]。
Kumar等[12]利用戊二醛交联法将漆酶固定于经过3-氨丙基三乙氧基硅烷(APTES)修饰的Fe3O4-NPs表面。首先利用APTES修饰Fe3O4-NPs,使其表面带有氨基(Fe3O4-NPs-NH2),通过戊二醛(GA)将漆酶的交联酶聚集体(CLEA-Lac)固定在Fe3O4-NPs-NH2上,GA分子中的一个醛基与Fe3O4-NPs表面的氨基发生反应形成亚氨基(-N=CH-),另一个醛基与漆酶的氨基反应[13]。固定漆酶后的磁性纳米粒子的直径介于48~74nm之间,比表面积为552m2·g-1,负载量高达155mg·g-1,但漆酶活性回复率仅为32%,可能是由于交联的方式阻碍了漆酶和催化底物的结合。
酯酶和漆酶的分子大小、结构排列和组成有明显的差异,Alex等[14]利用共沉淀法合成了直径介于10~100nm之间的磁性Fe3O4-NPs,以同样的方式进行氨基化修饰用来固定酯酶,结果发现固定化酯酶的活性回复率为100%。由此可见,酶分子结构也是影响固定化效果的重要因素。
Xia等[15]提出了一种新的固定漆酶方法:利用螯合Cu2+的聚乙烯亚胺(PEI)将漆酶固定在Fe3O4-NPs-NH2上,利用漆酶对Cu2+的吸附作用固定漆酶,如图1所示。

图1 Fe3O4-NPs-NH2-PEI-Cu2+固定漆酶示意图Fig.1 The schematic diagram of laccase immobilizationby Fe3O4-NPs-NH2-PEI-Cu2+
由于PEI含有氨基丰富的支链结构,可以通过Cu2+螯合吸附更多的漆酶,通过PEI可以提高对漆酶的固定能力。Fe3O4-NPs-NH2-Cu2+和Fe3O4-NPs-NH2-PEI-Cu2+2种磁性纳米粒子在相同条件下对漆酶的负载量分别为85 mg·g-1和150 mg·g-1。
磁性纳米粒子的直径小且比表面积大,合成方法简单易行,是一种性价比很高的载体。磁性Fe3O4-NPs还具有优异的光催化降解性能,可用于有机染料(如亚甲基蓝和藏红T等[16-18])的光催化降解。由此可见,直接以磁性纳米粒子为载体的固定漆酶技术在染料去除中具有很大的发展空间。
2 磁性纳米粒子和有机材料(物)的复合材料
2.1 磁性壳聚糖
2.1.1 磁性壳聚糖微球
磁性高分子微球是一种多组分的功能型微球,由有机高分子材料和无机磁性物质复合而成,既具有有机高分子材料可以通过表面改性赋予功能性基团的优良特性,又兼具无机磁性物质的磁响应性,在外加磁场条件下很容易分离[19-20]。磁性高分子微球具有4种结构,如图2所示。
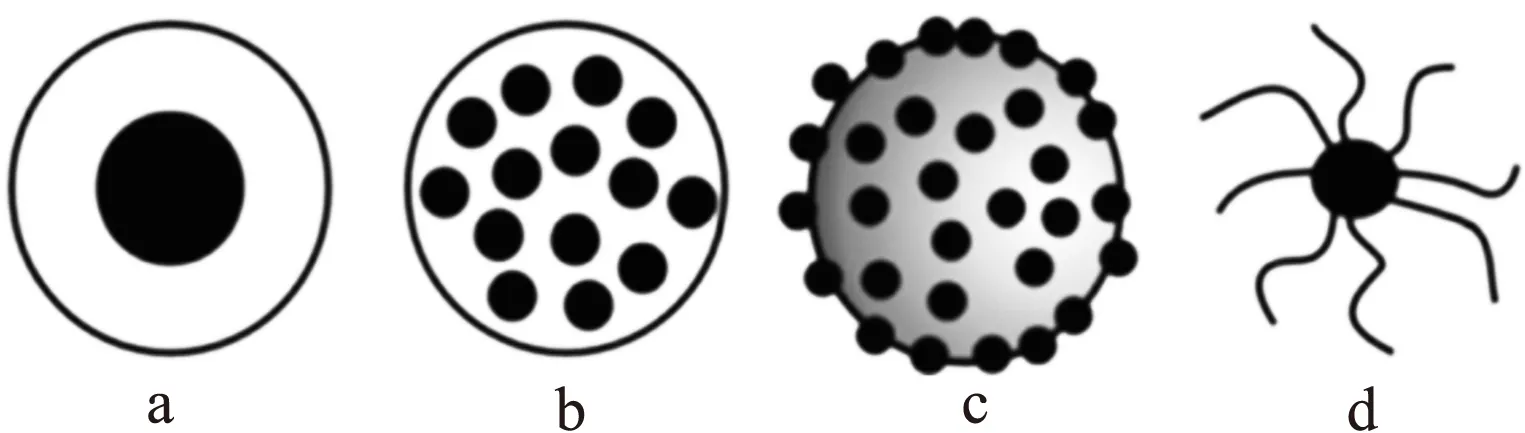
a.单个聚合物包裹单个磁性纳米粒子 b.单个聚合物中均匀 分布多个磁性纳米粒子 c.单个聚合物外部被多个磁性纳米 粒子均匀包裹 d.单个磁性纳米粒子表面连有多个聚合物配体[21]图2 磁性高分子微球的结构Fig.2 Structures of magnetic polymer microspheres
壳聚糖由于表面含有丰富的氨基和羟基[22],是制备磁性高分子微球的优良材料,近年来在固定化酶领域应用广泛。Jiang等[23]以Span-80为乳化剂、GA为交联剂,利用反相悬浮法将Fe3O4-NPs包裹在壳聚糖中制成磁性壳聚糖微球(呈图2中b型),表面呈网状结构。壳聚糖是否成球的重要因素是壳聚糖和GA的浓度,壳聚糖浓度过高形状不好,易粘连,过低不易成球;GA浓度过高微球间相互粘连不易分散,过低交联度低,微球机械性能差。当壳聚糖质量分数为2.5%、GA浓度为8%时,得到的微球具有较好的球形形貌,表面平滑,单分散性较好,粒径分布范围窄,平均粒径为0.9 μm,表面呈规则的网状结构,将血红密孔菌漆酶固定在该微球上,漆酶的活性回复率达100%。
Lin等[24]利用交联作用在Fe3O4上负载一层壳聚糖,然后将Cu2+和Mn2+螯合在Fe3O4磁性壳聚糖微球表面;通过调整溶液的pH值使漆酶带上负电荷;带负电荷的漆酶与Fe3O4磁性壳聚糖微球表面上的阳离子结合,使漆酶固定在磁性微球上。通过这种金属离子吸附作用固定漆酶的负载量可达到100 mg·g-1,固定化漆酶的活性回复率可达到100%。
当用GA为交联剂制备磁性壳聚糖微球固定漆酶时,GA自身易发生羟醛缩合反应形成不规则物质附着在微球表面,影响磁性壳聚糖微球固定漆酶的数量。Bayramoglu等[25]将壳聚糖溶液和磁性纳米粒子混合,利用相反转技术制备磁性壳聚糖微球(呈图2中b型);以环氧氯丙烷取代GA,在碱性条件下用环氧氯丙烷修饰磁性壳聚糖微球固定漆酶,虽然避免了交联剂自身反应,但漆酶负载量很低,仅为16.33 mg·g-1。固定过程如图3所示。
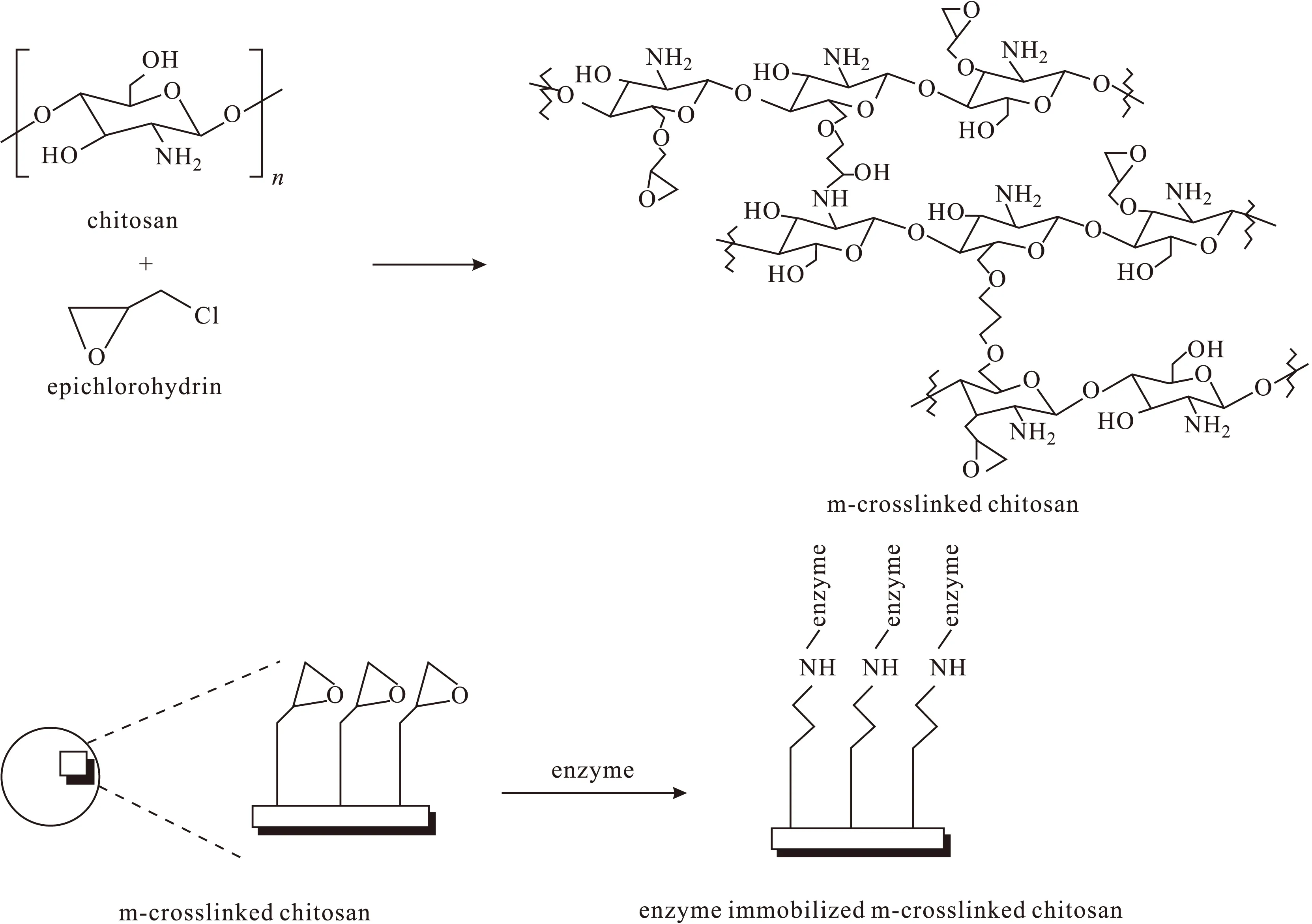
图3 磁性壳聚糖微球和漆酶的交联过程Fig.3 Cross-linking process of magnetic chitosan microsphere and laccase
2.1.2 磁性壳聚糖纳米粒子
Aksoy课题组[26]报道了壳聚糖包裹单个磁性纳米粒子形成磁性壳聚糖纳米粒子(呈图2中a型),并分别采用碳化二亚胺(EDAC)和氰脲酰氯(CC)为交联剂固定漆酶,与磁性壳聚糖纳米粒子固定漆酶进行比较。结果发现,3种方式固定的漆酶的催化效率和游离漆酶相当接近,3种方式固定的漆酶以2,2-联氮-二(3-乙基-苯并噻唑-6-磺酸)二铵盐(ABTS)为底物重复使用30次后的相对酶活仍然达到71%以上。由此可知,磁性壳聚糖纳米粒子可使固定化漆酶具有较高的重复利用率。
2.2 磁性海藻酸钠
海藻酸钠固定漆酶[27-30]是一种成熟的应用最普遍的漆酶固定方法,其原理是利用海藻酸钠与氯化钙乳化反应形成海藻酸钙凝胶包埋漆酶。该方法固定漆酶酶活力损失少且操作简单,但不易回收。
赵敏等[31]用海藻酸钠和磁性Fe3O4-NPs制备磁性海藻酸钠微粒,将其表面修饰生成酰氯基团,并通过化学共价法固定漆酶。结果表明,固定化漆酶与底物 ABTS亲和力降低,固定化漆酶反复使用10次后,仅保持 50%左右的活性,与其它磁性载体比较,重复利用率较低。
Le等[32]提出了一种新型固定漆酶技术,他们将漆酶封装在具有核壳结构的磁性海藻酸钠铜珠中,利用海藻酸钠的乳化作用,将Fe3O4-NPs、Cu2+和漆酶都封装形成微球,其中Fe3O4-NPs可实现固定化漆酶的磁性回收;Cu2+作为漆酶催化的辅助因子,有利于酶活力的保持。通过该技术固定漆酶的活性回复率达85%,并将其用于去除实际废水中的有机污染物。
3 磁性二氧化硅
用SiO2可较简单地制备孔径可调的介孔材料。在固定漆酶的过程中,SiO2孔径大小很重要,孔径过大不宜于酶分子固定在SiO2上;孔径过小易发生堵塞,影响酶和底物的结合[33-35]。
3.1 介孔磁性SiO2微球和管状介孔SiO2
孔径介于2~50 nm的材料称为介孔材料,介孔SiO2微球具有开放的孔道结构、合适的孔径分布、较大的比表面积及可调的孔径等特点,有利于酶分子进入孔道[36],但介孔SiO2微球尺寸较小,不利于回收。介孔磁性SiO2微球在磁场作用下可快速分离,实现固定化酶的回收再利用。
Deng等[37]和Zhang等[38]分别利用水热合成法和微乳液法制备了具备超顺磁性的核壳结构磁性介孔SiO2微球,但均存在颗粒均一性差、磁性粒子与介孔SiO2不易结合等缺点[39]。用介孔SiO2和Fe3O4纳米棒可以制备一种新型的磁性介孔SiO2/Fe3O4中空微球,具有独特的网状结构(图4)。制备方法如下:先将SiO2微球分散于含有Fe2+和F-的酸性溶液中进行预处理,以预处理的SiO2微球为核心,表面包覆β-FeOOH;然后利用NaOH溶液去除SiO2,得到中空的β-FeOOH微球,再利用正硅酸乙酯(TEOS)在碱性条件下水解,以十六烷基三甲基溴化铵(CTAB) 为结构模板对其进行包覆,最终得到中空的磁性介孔SiO2/Fe3O4微球[40-43]。该微球具有较大的比表面积(772 m2·g-1)和孔体积(0.83 cm3·g-1)、较好的磁性 (13.6 emu·g-1),对漆酶的负载量高达689 mg·g-1。这种由β-FeOOH纳米棒构建的中空微球,具有三维网络结构,漆酶分子可以通过β-FeOOH纳米棒间隙扩散进入中空核心,有利于漆酶的负载和储存。

图4 介孔SiO2/Fe3O4中空微球的SEM照片Fig.4 SEM images of mesoporous SiO2/Fe3O4hollow microspheres
介孔磁性SiO2作为载体一般呈球型[44-45]。席艳杰等[46]制备了管状介孔SiO2载体(图5),并用吸附和交联的方法进行漆酶固定化,制备的固定化漆酶可用于农药甲氧滴滴涕(MXC)的催化降解。这种管状磁性载体的形貌、尺寸大小都比较均一,但和SiO2微球相比管壁较薄、重复使用性差,固定化漆酶重复使用7次后,对MXC的降解率仅保持20%。

图5 管状介孔SiO2的SEM照片Fig.5 SEM image of tubular mesoporous SiO2
3.2 磁性SiO2纳米粒子
以磁性纳米粒子为核心、SiO2为外壳可制备核壳结构的磁性SiO2纳米粒子,对SiO2的表面进行修饰可用于固定漆酶。在碱性条件下,共沉淀法合成Fe3O4-NPs,以TEOS为硅源,磁性分离得到SiO2/ Fe3O4,用APTES修饰SiO2/ Fe3O4使其表面带有大量的氨基,通过GA的共价结合固定漆酶[47-48]。
Zheng等[47]合成了直径介于400~500 nm的磁性SiO2/ Fe3O4复合粒子固定漆酶,最大比活性为224 U,负载量为62.6 mg·g-1。Wang等[48]制备了直径介于25~30 nm的磁性SiO2/Fe3O4纳米粒子固定漆酶,负载量为85 mg·g-1。这是因为,直径小的磁性SiO2/Fe3O4纳米粒子的比表面积更大,有更多的连接位点可以固定漆酶,而且单分散性高增加了与漆酶分子的碰撞机会。Deng等[49]制备了磁性SiO2纳米粒子(Fe3O4@SiO2-NPs),利用多巴胺(DA)在溶解氧的作用下发生聚合反应形成黏附于固体表面的聚多巴胺(PDA)层[50],可将漆酶黏附在磁性SiO2表面,如图6b路线所示。与用APTES修饰Fe3O4@SiO2-NPs,通过GA固定漆酶方法(图6a)对比发现,4 ℃放置70 d,Fe3O4@SiO2-NPs-PDA-Lac(图6b)能保持最初活性的80%,而Fe3O4@SiO2-NPs-GA-Lac(图6a)只能保持35%。这是因为,PDA层可以将漆酶牢牢地包裹在磁性SiO2表面,防止漆酶受影响而失活。表明,DA的生物相容性好,反应条件温和,聚合速度快,反应可控,是一种较理想的聚合材料,在酶的固定化领域具有广阔的应用前景。
3.3 表面螯合Cu2+的磁性SiO2
贺芙蓉等[51]研究了磁性SiO2表面接枝的聚丙烯酰胺(PAM)络合Cu2+制备表面螯合Cu2+的磁性SiO2,通过配位作用固定漆酶,并用于水中2,4-二氯酚(2,4-DCP)的催化降解。Wang等[52-53]对磁性SiO2进行氨基修饰固定漆酶,固定化漆酶的酶活力为234 U·mg-1,但是固定化漆酶的活性和游离漆酶相比更易受pH值的影响,应用时受外界环境影响较大。孙丹丹等[54]在此基础上用Cu2+修饰磁性Fe3O4/SiO2固定漆酶并用于酚类染料的降解,结果表明,漆酶负载量虽低(26 mg·g-1),但Cu2+修饰后的固定化漆酶的酶活比未修饰的高54%,重复使用13次后降解率仍可达到92%。图7为Cu2+修饰固定化漆酶的SEM照片。
由图7可以看出,随着漆酶固定时间的延长,固定化漆酶从层片状逐渐变为花状。Ge等[55]研究发现,这种纳米花状的固定化漆酶比表面积大、吸附能力强、对底物脱色能力强。
将表面螯合Cu2+的磁性SiO2固定漆酶与其它工艺相结合可提高漆酶的催化效率。李丽芳等[56]将电化学工艺和表面螯合Cu2+的磁性SiO2固定漆酶结合,催化氧化水中的五氯酚。结果发现,漆酶酶活和重复利用率均比单独固定化漆酶高。这是因为,利用电化学预氧化五氯酚,降低了五氯酚的浓度,减少了固定化漆酶酶活的损失。在降解高毒性有机物质时电化学降解成本高,固定化漆酶酶活利用率低,通过两者的结合,不仅降低了使用成本,同时也减少了漆酶在催化过程中的损失,提高了固定化漆酶的效率,为降解高毒性有机污染物提供了一条新思路。

图7 Cu2+修饰固定化漆酶的 SEM照片Fig.7 SEM images of immobilized laccase modified by Cu2+
4 磁性碳材料
碳材料是一种比表面积大、孔隙体积大且孔径可调的多孔材料,和SiO2及其它材料相比具有高水热电阻,一直被认为是适合固定酶和分子的材料[57]。以介孔SiO2材料SBA-15[58]为模板、金属硝酸盐为合金来源、糠醇为碳源合成的FeNi/C磁性粒子固定的漆酶可用于酚类化合物的去除。FeNi/C磁性粒子为介孔材料,物理吸附漆酶,吸附量为491.7 mg·g-1,活性回复率为91%[59]。
石墨烯是一种二维碳材料,常用的合成方法有机械剥离法、氧化还原法、SiC外延生长法和化学气相沉积法(CVD)[60]。朱珣之等[61]利用氧化还原法制备了氧化石墨烯,通过水热共沉淀法制备了Fe3O4纳米磁性氧化石墨烯,利用GA为交联剂固定果胶酶,固定化酶稳定性明显增强。欧阳科等[35]采用Hummers法[62]和多羟基法[63]制备Fe3O4/石墨烯异质结固定漆酶,用于降解双酚A(BPA)。氧化石墨烯的比表面积大(726.34 m2·g-1),增强了漆酶和底物的亲和力。重复使用10次后的相对活性依然保持82%,具有良好的重复使用性。通过石墨烯固定的漆酶的耐酸性、耐热性、贮存稳定性都有所提高。
5 结语
漆酶固定化磁性载体的最大优势是可以利用磁性分离,使漆酶被快速回收利用。总体来看,磁性载体固定的漆酶的温度稳定性、pH值稳定性、贮存稳定性、重复使用性及操作性能都普遍提高,但固定化漆酶的比活力并不都令人满意。如何在保证稳定性和磁性的基础上提高固定化漆酶的活性是固定化磁性载体今后的研究方向。
[2] FAN L,WANG Y,ZHAO M,et al.MagneticGanodermalucidumspore microspheres:a novel material to immobilize CotA multicopper oxidase for dye decolorization[J].Journal of Hazardous Materials,2016,313:122-129.
[3] AYDEMIR T,GÜLER S.Characterization and immobilization ofTrametesversicolorlaccase on magnetic chitosan-clay composite beads for phenol removal[J].Artificial Cells Nanomedicine & Biotechnology,2015,43(6):1-8.
[4] DANDAYUDHAM R,RAMAN V K,VENKATESH R,et al.Magnetic nanoparticles as versatile carriers for immobilization of laccase[J].Research Journal of Engineering & Technology,2013,4(4):279-283.
[5] LEE K M,KALYANI D,TIWARI M K,et al.Enhanced enzymatic hydrolysis of rice straw by removal of phenolic compounds using a novel laccase from yeastYarrowialipolytica[J].Bioresource Technology,2012,123(4):636-645.
[6] LLORET L,HOLLMANN F,EIBES G,et al.Immobilisation of laccase on Eupergit supports and its application for the removal of endocrine disrupting chemicals in a packed-bed reactor[J].Biodegradation,2012,23(3):373-386.
[7] NICOLUCCI C,ROSSI S,MENALE C,et al.Biodegradation of bisphenols with immobilized laccase or tyrosinase on polyacrylonitrile beads[J].Biodegradation,2011,22(3):673-683.
[8] ROGALSKI J,DAWIDOWICZ A,JWIK E,et al.Immobilization of laccase fromCerrenaunicoloron controlled porosity glass[J].Journal of Molecular Catalysis B:Enzymatic,1999,6(1/2):29-39.
[9] 刘宇,郭晨,王锋,等.磁性 SiO2纳米粒子的制备及其用于漆酶固定化[J].过程工程学报,2008,8(3):583-588.
[10] ZHENG X,WANG Q,JIANG Y,et al.Biomimetic synthesis of magnetic composite particles for laccase immobilization[J].Industrial & Engineering Chemistry Research,2012,51(30):10140-10146.
[11] TANG T T,FAN H,AI S Y,et al.Hemoglobin(Hb) immobilized on amino-modified magnetic nanoparticles for the catalytic removal of bisphenol A[J].Chemosphere,2011,83(3):255-264.
[12] KUMAR V V,SIVANESAN S,CABANA H.Magnetic cross-linked laccase aggregates-bioremediation tool for decolorization of distinct classes of recalcitrant dyes[J].Science of the Total Environment,2014,487(1):830-839.
[13] FANG H,HUANG J,DING L Y,et al.Preparation of magnetic chitosan nanoparticles and immobilization of laccase[J].Journal of Wuhan University of Technology(Materials Science Edition),2009,24(1):42-47.
[14] ALEX D,MATHEW A,SUKUMARAN R K.Esterases immobilized on aminosilane modified magnetic nanoparticles as a catalyst for biotransformation reactions[J].Bioresource Technology,2014,167(3):547-550.
[15] XIA T T,LIU C Z,HU J H,et al.Improved performance of immobilized laccase on amine-functioned magnetic Fe3O4nanoparticles modified with polyethylenimine[J].Chemical Engineering Journal,2016,295:201-206.
[16] PATIL M R,SHRIVASTAVA V S.Adsorption removal of carcinogenic acid violet19 dye from aqueous solution by polyaniline-Fe2O3magnetic nano-composite[J].Journal of Materials & Environmental Science,2015,6(1):11-21.
[17] 刘淑玲,许青青.Fe3O4磁性材料的制备及其光催化降解性能[J].陕西科技大学学报(自然科学版),2015,35(2):103-107.
[18] WEI P C,HU B,ZHOU L,et al.New strategy to incorporate nano-particle sized water oxidation catalyst into dye-sensitized photoelectrochemical cell for water splitting[J].Journal of Energy Chemistry,2016,25(3):345-348.
[19] 谢钢,张秋禹,李铁虎.磁性高分子微球[J].高分子通报,2001(6):38-45.
[20] 张也,张会良,张会轩,等.聚合物基磁性复合微球的研究近况[J].高分子通报,2016(4):47-60.
[21] PENAMON P.Gold-coated magnetic polymer microsphere synthesis and characterization:applications in biological contexts[D].Vanderbilt University,2012.
[22] 王鹏.磁性壳聚糖基复合微粒的制备及对两种阴离子染料的吸附性能研究[D].哈尔滨:东北林业大学,2015.
[23] JIANG D S,LONG S Y,HUANG J,et al.Immobilization ofPycnoporussanguineuslaccase on magnetic chitosan microspheres[J].Biochemical Engineering Journal,2005,25(1):15-23.
[24] LIN J H,LIU Y J,SHI C,et al.Reversible immobilization of laccase onto metal-ion-chelated magnetic microspheres for bisphenol A removal[J].International Journal of Biological Macromolecules,2015,84:189-199.
[25] BAYRAMOGLU G,YILMAZ M,YAKUP A M Y.Preparation and characterization of epoxy-functionalized magnetic chitosan beads:laccase immobilized for degradation of reactive dyes[J].Bioprocess & Biosystems Engineering,2010,33(4):439-448.
[26] KALKAN N A,AKSOY S,AKSOY E A,et al.Preparation of chitosan-coated magnetite nanoparticles and application for immobilization of laccase[J].Journal of Applied Polymer Science,2012,123(2):707-716.
[27] ÜNAL A,KOLANKAYA N.Determination of optimum immobilization conditions ofTrametesversicolorlaccase with sodium alginate beads[J].IUFS Journal of Biology,2013,72(2):15-21.
[28] WANG J Y,YU H R,XIE R,et al.Alginate/protamine/silica hybrid capsules with ultrathin membranes for laccase immobilization[J].AIChE Journal,2013,59(2):380-389.
[29] GUZIK U,HUPERT-KOCUREK K,MARCHLEWICZ A,et al.Enhancement of biodegradation potential of catechol 1,2-dioxygenase through its immobilization in calcium alginate gel[J].Electronic Journal of Biotechnology,2014,17(2):83-88.
[30] BILAL M,ASGHER M.Dye decolorization and detoxification potential of Ca-alginate beads immobilized manganese peroxidase[J].BMC Biotechnology,2015,15(1):1-14.
[31] 赵敏,王玮,李昕芯,等.海藻酸钠磁性微粒的制备及对漆酶的固定化[J].中国造纸学报,2008,23(4):94-99.
[32] LE T T,MURUGESAN K,LEE C S,et al.Degradation of synthetic pollutants in real wastewater using laccase encapsulated in core-shell magnetic copper alginate beads[J].Bioresource Technology,2016,216:203-210.
[33] SEYEDEH-SHAGHAYEGH M,SEYED-MOSTAFA K,SHA-HLA R,et al.Decolorization of two synthetic dyes using the purified laccase ofParaconiothyriumvariabile,immobilized on porous silica beads[J].Journal of Environmental Health Science & Engineering,2014,12(1):1-9.
[34] PANDYA P H,JASRA R V,NEWALKAR B L,et al.Studies on the activity and stability of immobilizedα-amylase in ordered mesoporous silicas[J].Microporous & Mesoporous Materials,2005,77(1):67-77.
[35] 欧阳科,谢珊,赵雅,等.磁性Fe3O4/石墨烯异质结固定漆酶特性及其对水中双酚A的降解研究[J].生态环境学报,2015(1):106-112.
[36] ISPAS C,SOKOLOV I,ANDREESCU S.Enzyme-functionalized mesoporous silica for bioanalytical applications[J].Analytical and Bioanalytical Chemistry,2009,393(2):543-554.
[37] DENG Y,QI D,DENG C,et al.Superparamagnetic high-magnetization microspheres with an Fe3O4@SiO2core and perpendicularly aligned mesoporous SiO2shell for removal of microcystins[J].Journal of the American Chemical Society,2008,130(1):28-29.
[38] ZHANG L,QIAO S Z,JIN Y G,et al.Magnetic hollow spheres of periodic mesoporous organosilica and Fe3O4nanocrystals:fabrication and structure control[J].Advanced Materials,2008,20(4):805-809.
[39] 李笑涵,李群艳,朱庆强,等.介孔SiO2/Fe3O4中空微球孔径调控以及漆酶固定性能研究[J].人工晶体学报,2014,43(11):2957-2965.
[40] WANG P Y,LI Q Y,ZHOU Y L,et al.Immobilization of laccase in glycidoxypropyl-functionalized magnetic mesoporous SiO2/Fe3O4hollow microspheres[J].Key Engineering Materials,2016,697:749-755.
[41] 王苗苗,李群艳,韦奇,等.介孔SiO2/Fe3O4中空磁性微球的漆酶固定化[J].高等学校化学学报,2013,34(2):299-305.
[42] TAVARES A P M,RODRGUEZ O,FERNNDEZ-FERN-NDEZ M,et al.Immobilization of laccase on modified silica:stabilization,thermal inactivation and kinetic behaviour in 1-ethyl-3-methylimidazolium ethylsulfate ionic liquid[J].Bioresource Tec-hnology,2013,131:405-412.
[43] LI Q Y,WANG P Y,ZHOU Y L,et al.A magnetic mesoporous SiO2/Fe3O4hollow microsphere with a novel network-like composite shell:synthesis and application on laccase immobilization[J].Journal of Sol-Gel Science and Technology,2016,78(3):1-8.
[44] DAI J,WANG H,CHI H,et al.Immobilization of laccase fromPleurotusostreatuson magnetic separable SiO2support and excellent activity towards azo dye decolorization[J].Journal of Environmental Chemical Engineering,2016,4(2):2585-2591.
[45] LI Y T,ZHANG L,LI M,et al.A disposable biosensor based on immobilization of laccase with silica spheres on the MWCNTs-doped screen-printed electrode[J].Chemistry Central Journal,2012,6(1):1-8.
[46] 席艳杰.管状介孔材料固定化漆酶及水相降解MXC的研究[D].上海:华东理工大学,2014.
[47] ZHENG F,CUI B K,WU X J,et al.Immobilization of laccase onto chitosan beads to enhance its capability to degrade synthetic dyes[J].International Biodeterioration & Biodegradation,2016,110:69-78.
[48] WANG H X,ZHANG W,ZHAO J X,et al.Rapid decolorization of phenolic azo dyes by immobilized laccase with Fe3O4/SiO2nanoparticles as support[J].Industrial & Engineering Chemistry Research,2013,52(12):4401-4407.
[49] DENG M F,ZHAO H,ZHANG S P,et al.High catalytic activity of immobilized laccase on core-shell magnetic nanoparticles by dopamine self-polymerization[J].Journal of Molecular Catalysis B:Enzymatic,2015,112:15-24.
[50] 张笛,邓满凤,赵赫,等.多巴胺包埋磁性 SiO2固定化漆酶催化去除 4-氯酚[J].化工学报,2015,66(9):3705-3711.
[51] 贺芙蓉,王颖,陈晓春,等.表面铜螯合磁性二氧化硅固定化漆酶及其催化降解水中2,4-二氯酚[J].环境工程学报,2011,5(12):2651-2657.
[52] WANG Y,ZHANG D,HE F R,et al.Immobilization of laccase by Cu2+chelate affinity interaction on surface modified magnetic silica particles and its use for the removal of pentachlorophenol[J].Chinese Chemical Letters,2012,23(2):197-200.
[53] 王新,刘丽,陆佳靓,等.固定化漆酶载体研究进展[J].生态学杂志,2013,32(10):2823-2829.
[54] 孙丹丹,宋守欣,王红霞.Cu2+修饰低固载量固定化漆酶的活性研究[J].化学工程师,2015,29(3):14-17.
[55] GE J,LEI J D,ZARE R N.Protein-inorganic hybrid nanoflowers[J].Nature Nanotechnology,2012,7(7):428-432.
[56] 李丽芳,于光认,陈晓春,等.电化学-表面铜螯合水溶液中磁性二氧化硅固定化漆酶联合催化降解水中五氯酚[J].环境工程,2014(6):24-28.
[57] ZHAO D Y,HUO Q S,FENG J L,et al.Nonionic triblock and star diblock copolymer and oligomeric surfactant syntheses of highly ordered,hydrothermally stable,mesoporous silica structures[J].Journal of the American Chemical Society,1998,120(24):6024-6036.
[58] WANG Z L,LIU X T,LV M F,et al.Simple synthesis of magnetic mesoporous FeNi/carbon composites with a large capacity for the immobilization of biomolecules[J].Carbon,2010,48(11):3182-3189.
[59] LIU Y Y,ZENG Z T,ZENG G M,et al.Immobilization of laccase on magnetic bimodal mesoporous carbon and the application in the removal of phenolic compounds[J].Bioresource Technology,2012,115:21-26.
[60] LIU Y,LI Q,FENG Y Y,et al.Immobilisation of acid pectinase on graphene oxide nanosheets[J].Chemical Papers:Slovak Academy of Sciences,2014,68(6):732-738.
[61] 朱珣之,李强,华楠,等.磁性氧化石墨烯固定化果胶酶[J].化工进展,2014,33(12):3324-3328.
[62] HUMMERS W S,OFFEMAN R E.Preparation of graphitic oxide[J].Journal of the American Chemical Society,1958,80(6):1339.
[63] LI X H,YI H B,ZHANG J W,et al.Fe3O4-graphene hybrids:nanoscale characterization and their enhanced electromagnetic wave absorption in gigahertz range[J].Journal of Nanoparticle Research,2013,15(3):1-11.
Research Progress on Magnetic Carrier for Laccase Immobilization
WANG Jue-yu1,FAN Li-li2,WANG Yan3,ZHAO Min1*
(1.CollegeofLifeSciences,NortheastForestryUniversity,Harbin150040,China;2.NortheastInstituteofGeographyandAgroecology,ChineseAcademyofSciences,Harbin150081,China;3.SchoolofChemicalEngineeringandTechnology,HarbinInstituteofTechnology,Harbin150001,China)
Asakindofmulticopperoxidases,laccasehashighcatalyticefficiencyandtheonlyby-productiswater,soitisagreenbiocatalyst.Basedonawidesubstraterange,laccasehasimportantapplicationpotentialinvariousfields.Theimmobilizationoflaccasebymagneticcarriercanachievemagneticrecyclingandreuseoflaccase,reducethecostoflaccase,andincreasethestabilityoflaccase.Inrecentyears,immobilizationoflaccasebymagneticcarrierhasattractedincreasingattention.Thepreparationmethodsofdifferentmagneticcarriers,catalyticpropertiesandapplicationsofimmobilizedlaccasearesummarized.Theloadingcapacityofdifferentmagneticcarriersandactivityrecoveryofimmobilizedlaccasearecompared.Thisstudyprovidesahelpforthedevelopmentandutilizationofmagneticcarrierforlaccaseimmobilization.
laccase;immobilization;magneticcarrier;loadingcapacity;activityrecovery
2016-08-31
Q 814.2
A
1672-5425(2017)01-0015-08
王珏玉,范丽莉,王炎,等.漆酶固定化磁性载体的研究进展[J].化学与生物工程,2017,34(1):15-22.
