革命性的基因编辑技术
2017-01-20叶水送
叶水送
革命性的基因编辑技术
叶水送
2016年3月24日,美国《科学》杂志发表了合成生物学领域一项里程碑式的重要研究,人类基因组研究先驱克雷格·文特尔(Craig Venter)及其团队耗费20年时间,设计并制造出了一种最简单的人工合成生命体,该生命体仅有维持生命所需的473个基因,是目前已知最小的生命体基因组。据介绍,研究者利用一种叫做规律成簇间隔短回文重复序列(CRISPR/Cas9)的技术实现对特定基因的筛选。该研究有望帮助科学家更好地了解细胞中每个必需基因的功能。
CRISPR/Cas9技术再次发挥重要作用。2015年年底,《科学》杂志“年度十大科学发现”将基因编辑技术CRISPR/Cas9列为年度科学发现榜首。早在2012年和2013年,《科学》杂志就已将CRISPR纳入到年度10大科学发现的榜单中,不过彼时它属于陪跑的“角色”。如今这种革命性的基因编辑技术已经走入全球各地科学家的分子生物实验室中,成为科研工作者探索生命奥秘以及临床科研人员攻克疾病的有力工具。
革命性的分子生物学技术
CRISPR/Cas9技术从一开始被发现到现在被分子生物学家广泛应用,并没有经历很长的时间。20世纪80年代,日本科学家在细菌中就已经发现这种简单重复的特殊序列。2007年,丹麦哥本哈根一家酸奶公司研究者鲁道夫·巴冉古(Rodolphe Barrangou)发现细菌中拥有抵御病毒的特殊防御机制,随后细菌的防御机制与这种特殊序列即CRISPR序列之间的关联被阐述清楚。近年来,利用CRISPR/Cas9基因编辑技术进行的研究快速增长。由于其能高效地对基因特定位点进行编辑,而且简单易行,因此CRISPR/Cas9技术的发现被视为分子生物学的一个奇迹。
随着近些年来科学家利用CRISPR/Cas9技术发现一系列的重要科学问题,该技术备受瞩目。其中最重要的两项研究是修饰不同物种的基因序列以及编辑人类胚胎细胞的基因组,它们的出现都给现有科学伦理规范提出巨大的挑战。2015年年初,中山大学学者黄军就利用CRISPR/Cas9技术对一组不能正常发育的受精卵进行基因编辑,随即这项研究引起国际社会的强烈议论。该研究亦成为2015年12月份在华盛顿召开的国际人类基因编辑峰会(International Summiton Human Gene Editing)的一个重要导火索。大会达成共识:当前利用CRISPR技术对人类胚胎细胞基因进行修饰的临床应用,是“不负责任”(irresponsible)的举动。2016年4月,由广州医科大学附属第三医院范勇领导的研究团队,完成全球第二例人类胚胎基因编辑,该研究同样引起国际同行的高度关注。
CRISPR系统拥有如此强大的能力,以至于科学家很容易地创造出基因型完全不同的生命体。《自然》杂志主编菲利普·坎贝尔(Philip Campbell)博士曾表示:“业余科学家在自家车库中就可利用它来实现基因编辑。”这些地方往往是科学伦理不能约束的空白区域,因此加强CRISPR/Cas9技术的伦理规范显然很重要。
事实上,基因编辑技术并不很新鲜,此前还有锌指核糖核酸酶(ZFN)和转录激活因子样效应物核酸酶(TALENs)等技术。相比前面两项技术,CRISPR/Cas9技术要简单很多,以至于“每个分子生物实验室都可用CRISPR技术编辑基因”。CRISPR/Cas9技术的原理大体如下:当病毒如噬菌体的DNA序列进入细菌中时,细菌的前导序列(leader sequence)会启动CRISPR序列,开始合成两种R N A:CRISPR RNA(crRNA)与反式激活crRNA(tracrRNA),二者结合形成RNA复合体,即sgRNA(singleguide RNA),然后再与Cas9核酸酶形成RNA-蛋白复合体。如果是人为设计,由特定序列组成的sgRNA,可指引RNA-蛋白复合体中的Cas9核酸酶对病毒或外源性DNA序列的特定位点进行编辑,从而实现基因序列的精准剪辑(图1)。CRISPR系统的最早发现者之一、加州伯克利分校的分子生物学家詹妮弗·杜德纳(Jennifer Doudna)表示:“它就像PCR技术,一个潜藏在工具箱里的工具”。
CRISPR/Cas9技术也有短板,其效率以及脱靶问题备受关注。例如,最近文特尔就表示:“如果只是对基因序列进行简单地编辑,CRISPR/Cas9技术可以胜任,但是如果想利用它来设计新生命体,CRISPR/Cas9还远满足不了需求。”
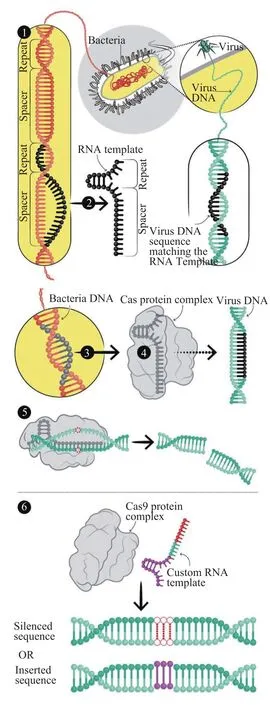
图1 CRISPR/Cas9技术原理简图。CRISPR序列广泛存在于细菌以及古生菌中,是细菌用来抵御病毒的防御机制。步骤1、2:当细菌发现有病毒入侵时,细菌的CRISPR系列会启动合成RNA;步骤3、4:新合成的RNA与Cas9核酸酶形成复合体;步骤5、6:复合体中的Cas9核酸酶能够敲除或敲入特定序列的基因片段(图片来自theglobeandmail.com)
基因编辑技术的专利纠纷
有关CRISPR技术的专利纠纷,似乎早已让这一领域的数位先驱科学家——博德研究所(Broad Institute)的张锋、加州大学伯克利分校的杜德纳以及德国亥姆霍兹传染研究中心的埃马纽埃尔·卡彭蒂耶(Emmanuelle Charpentier)之间的关系降到冰点。最近一则获奖消息,或许可以弥合他们之间长久以来的嫌隙。2016年3月23日,素有“小诺贝尔奖”之美誉的加拿大盖尔德纳奖(Canada Gairdner Awards)公布,张锋、杜德纳以及卡彭蒂耶“因将基因编辑技术CRISPR-CAS应用于真核细胞所作出的努力”(“for development of CRISPR-CAS as a genome editing tool for eukaryotic cells”)而获得盖尔德纳国际奖(Canada Gairdner International Awards)(图2)。值得注意的是,盖尔德纳基金会谨慎地使用了“development”(发展),而不是“finding”(发现),也许这样避免了三人长期以来因谁最早发明CRISPR基因编辑技术而引起的纠纷。截止到2012年,曾获得盖尔德纳奖的300多名获奖者中,已有72名获奖者同时也获得诺贝尔奖,因此该奖项有“小诺贝尔奖”之称。
自2014年CRISPR技术首次获得科学突破奖(Breakthrough Prize)的认可后,杜德纳和卡彭蒂耶连连获得包括科学突破奖以及阿尔珀特奖在内的数个国际科学大奖,张锋则与之失之交臂。此次获得盖尔德纳奖,无疑增加了他的信心。他表示:“荣获盖尔德纳奖是对我整个团队的高度认可,我也因能够与CRISPR领域的其他几位先锋学者一同获奖感到非常荣幸。”在基因编辑技术CRISPR早期开发上,另一位科学家哈佛大学乔治·彻奇(George Church)教授的贡献可圈可点,但他仍与诸多国际大奖无缘。
张锋与杜德纳和卡彭蒂三人共同获奖,是否意味着未来有关CRISPR专利的纠纷会到此为止?实际的情况并不妙,而且颇有愈演愈烈之势。原本张锋或在CRISPR专利上占据有利位置,现在可能会被削弱。张锋在申请过程中,被竞争对手认为采取了“非正当竞争手段”的快速通道:晚申请专利,却率先获得CRISPR专利。目前,杜德纳仍在积极地争取CRISPR专利权,美国专利与商标局已于2016年3月10日启动对CRISPR专利归属的干涉程序。除非是两家机构自己达成妥协,CRISPR专利之争在短时间内不会结束。

图2 2016年盖尔德纳奖获得者张锋(左)、杜德纳(中)和卡彭蒂耶(右)(张锋照片来自MIT大学网站,杜德纳照片来自WIKI,卡彭蒂耶照片来自podcastscience)
CRISPR技术在科学以及商业上潜力无限
CRISPR专利之争之所以难以解决,不仅在于这种革命性技术已经成为研究者的科研利器,同时它也能源源不断地带来商业上的利益,任何人都希望将CRISPR专利拽在手中。由张锋、杜德纳以及彻奇创立的生物技术公司Editas Medicine在Google等公司的投资下,最终登陆美国纳斯达克上市。缘于专利纠纷,杜德纳中途选择离开Editas Medicine公司,重新创立另一基因编辑公司Caribou Biosciences。
目前基于CRISPR技术的基因编辑公司,不仅能够建立不同需求的实验动物模型,同时也有可能在数个领域实现对人类相关疾病进行治疗的突破。因为在动物实验中,研究者已经利用该技术修复了部分小鼠所患的遗传疾病。例如研究者对患遗传性白内障小鼠的基因突变进行修复,消除了小鼠的白内障症状。尽管未来这一技术在人类生殖细胞上的应用红线仍不可能被跨越,但终有一天,该技术很有可能会突破现有的伦理禁忌,使用于人类体细胞的基因缺陷修复上,从而造福于人类。
注:本文部分内容来自作者写在《知识分子》微信公众号的文章中。
(2016年4月7日收稿)■
(编辑:段艳芳)
CRISPR/Cas 9 gene editing technology: Will it revolutionize molecular biology
YE Shuisong
10.3969/j.issn.0253-9608.2016.02.013
†通信作者,E-mail: yeshuisong@gmail.com
