基于三(2-氨基乙基)胺和6-羧基荧光素的双模式核磁共振成像造影剂
2017-01-18钱伟桥胡爱国
潘 斐, 朱 勤, 钱伟桥, 胡爱国
(华东理工大学材料科学与工程学院,上海市先进聚合物材料重点实验室,上海 200237)
基于三(2-氨基乙基)胺和6-羧基荧光素的双模式核磁共振成像造影剂
潘 斐, 朱 勤, 钱伟桥, 胡爱国
(华东理工大学材料科学与工程学院,上海市先进聚合物材料重点实验室,上海 200237)
通过将三(2-氨基乙基)胺(TREN)、6-羧基荧光素与溴乙酸苄酯结合而合成出多胺多羧型配体,并赋予化合物荧光成像的功能。进一步与顺磁性的六水合氯化钆(Ⅲ)反应获得兼具核磁共振成像(Magnetic Resonance Imaging,MRI)和光学成像功能的双模式核磁共振成像造影剂。通过核磁氢谱、碳谱、高分辨质谱和ICP-AES表征了配体和金属配合物的结构。研究结果表明,该配合物的纵向弛豫率(r1)为3.46 mM-1·s-1,与小分子型商用造影剂如马根维显®(Gd-DTPA)接近。该配合物同时拥有66%的荧光量子产率,在紫外光照射下显示明亮的绿色荧光,为以后进行生物体内研究打下坚实基础。
核磁共振成像; 造影剂; 三(2-氨基乙基)胺; 荧光成像; 量子产率
Lauterbur和Mansfield因在核磁共振成像(Magnetic Resonance Imaging,MRI)领域[1-2]作出开拓性贡献而荣获2003年诺贝尔生理医学奖。MRI具有高的空间分辨率、较深的组织穿透力以及对人体检测无创伤性等特点,成为当前最有效的医学诊断手段之一[3-6]。在很多核磁共振成像(MRI)检测中,比如肠胃管和脑部区域,由于软组织间的区分度不够高而使得诊断信息不够充分。在这些情形下,需要用到造影剂(Contrast agent)以提高诊断影像的质量。含有顺磁性金属离子可以通过改变人体组织中水质子的弛豫速率,增强正常组织和病变组织的对比度,从而提高MRI的成像效果。临床实践中有将近一半的MRI需要用到造影剂,而这些造影剂大多为钆(III)配合物[7-8]。钆(III)造影剂的灵敏度可以用单位浓度造影剂对水分子弛豫速率的影响,即弛豫率(r1)来表征。根据SBM (Solomon-Bloembergen-Morgan)理论[9],影响造影剂弛豫率的因素主要有以下3个:水合常数q、配位水分子的停留时间τm和造影剂的旋转相关时间τR。其中缩短τm或者延长τR是目前提高造影剂弛豫率研究的主流方法。虽然造影剂的加入能有效地提高组织分辨率,但是却无法解决MRI本质上存在的一个缺点:较低的灵敏度。与之相反,光学成像(Optical imaging)的组织穿透性很差,却具有很高的灵敏性。为此,许多研究者们开展了将这两种成像手段结合的双模式成像研究以获得更好的诊断效果。
小分子有机荧光团、金属配合物发光体、碳量子点等都可以通过共价键或者非共价键的方式与钆配合物链接起来而成为符合这种要求的双模式造影剂。Rivas等[10]通过酰胺键将基于DO3A的钆配合物与荧光基团罗丹明链接起来获得双模式造影剂。Jang等[11]以二乙三胺(DTTA)作为核磁共振探针,以萘亚胺作为荧光基团,均赋予了造影剂光学成像的功能。我们研究组通过细乳液聚合方式将钆配合物接枝在5-丙烯酰氨基荧光素和苯乙烯共聚形成的聚合物纳米粒子上,获得双模式造影剂[12]。Livramento等[13]以4,4'-双(溴甲基)-2,2'-联吡啶作为结构核心,一端修饰为多氨多羧型配体与钆配位形成核磁共振成像探针,原吡啶环上的氮原子则进一步与Fe2+配位自组装。Verwilst等[14]在1,10-邻二氮杂菲-5-苯胺的胺基端接上DOTA类钆配合物,原邻二氮菲上的氮原子与Ru3+配位,Dehaen等[15]在通过酰胺反应将DTPA类钆造影剂接于3,4-(二苄氧基)苯乙胺上的胺基端以及苄氧基脱保护后直接与Ti4+配位,均得到双模式造影剂。Gong[16]、Bourlinos[17]等以碳量子点作为荧光部分,同样获得了双模式造影剂。本课题组最近将碳量子点与含有双季铵盐基团的配合物通过静电自组装方式获得了生物相容性良好的双模式造影剂[18]。当前多数双模式造影剂都是基于DOTA或DTPA及其衍生物的钆配合物作为核磁共振成像探针,且所得到的造影剂的荧光量子产率不高,在提高造影剂灵敏性方面提升较小,在后续的生物体内研究中仍然有所限制。
针对以上情况,本文以6-羧基荧光素作为荧光探针,以三(2-氨基乙基)胺(TREN)作为新的钆配体应用于双模式造影剂的制备,合成出多胺多羧型配体,再与六水合氯化钆配位得到相应的顺磁性钆(Ⅲ)配合物,将核磁共振成像和光学成像有效结合成一种双模式核磁共振成像造影剂,使其既具有MRI的高空间分辨率和深层组织穿透力,又具有很高的荧光量子产率,以应用于高灵敏度光学成像。
1 实验部分
1.1 主要试剂和仪器
1,4-二氧六环、间苯二酚、氢氧化钠、乙腈、碳酸钾、N,N-二甲基甲酰胺(DMF),上海凌峰化学试剂有限公司,分析纯;1,2,4-偏苯三甲酸酐,Alfa Aesar公司,分析纯;三(2-氨基乙基)胺,Alfa Aesar公司,纯度97%;甲基磺酸、盐酸、硅胶、乙醚,国药集团化学试剂有限公司,分析纯;N,N-二异丙基乙胺、二环己基碳二亚胺(DCC),上海达瑞精细化学品有限公司,分析纯;二碳酸二叔丁酯((Boc)2O)、溴乙酸苄酯、三氟乙酸、1-羟基苯并三唑(HOBt),安耐吉化学,纯度98%;二氯甲烷、甲醇、正己烷,苏州晶协高新电子材料有限公司,分析纯;氢化钙,上海天莲精细化工有限公司,纯度≥96%;氘代氯仿(CDCl3)、氘代二甲基亚砜(DMSO-d6)、重水(D2O)、氘氧化钠(NaOD),J&K化学有限公司,分析纯。6-羧基荧光素合成参考文献[19]。
核磁共振氢谱(1H-NMR)、碳谱(13C-NMR):美国Bruker公司Ultra Shield 400 spectrometer核磁共振仪;质谱(MS):英国质谱公司Micromass LCTTM液相色谱/飞行时间质谱联用仪,电喷雾电离(ESI)方式;等离子吸收光谱(ICP-AES):采用等离子体发射光谱(IRIS 1000,Varian 710ES)测定Gd(III)含量;核磁共振成像T1测试:通过1.5T的GE核磁共振成像仪(GE Signa Excite 1.5T,GE Medical Systems,USA)进行测定;紫外可见(UV-Vis)荧光波谱:采用Fluorolog-3-p 分光光谱仪,激发和发射光谱的狭缝都是3 nm。样品制备:配置一定浓度的溶液样品,置于石英比色皿用于测试。
1.2 钆(III)配合物的合成
图1示出了双模式照影剂钆(III)配合物7的合成路线。
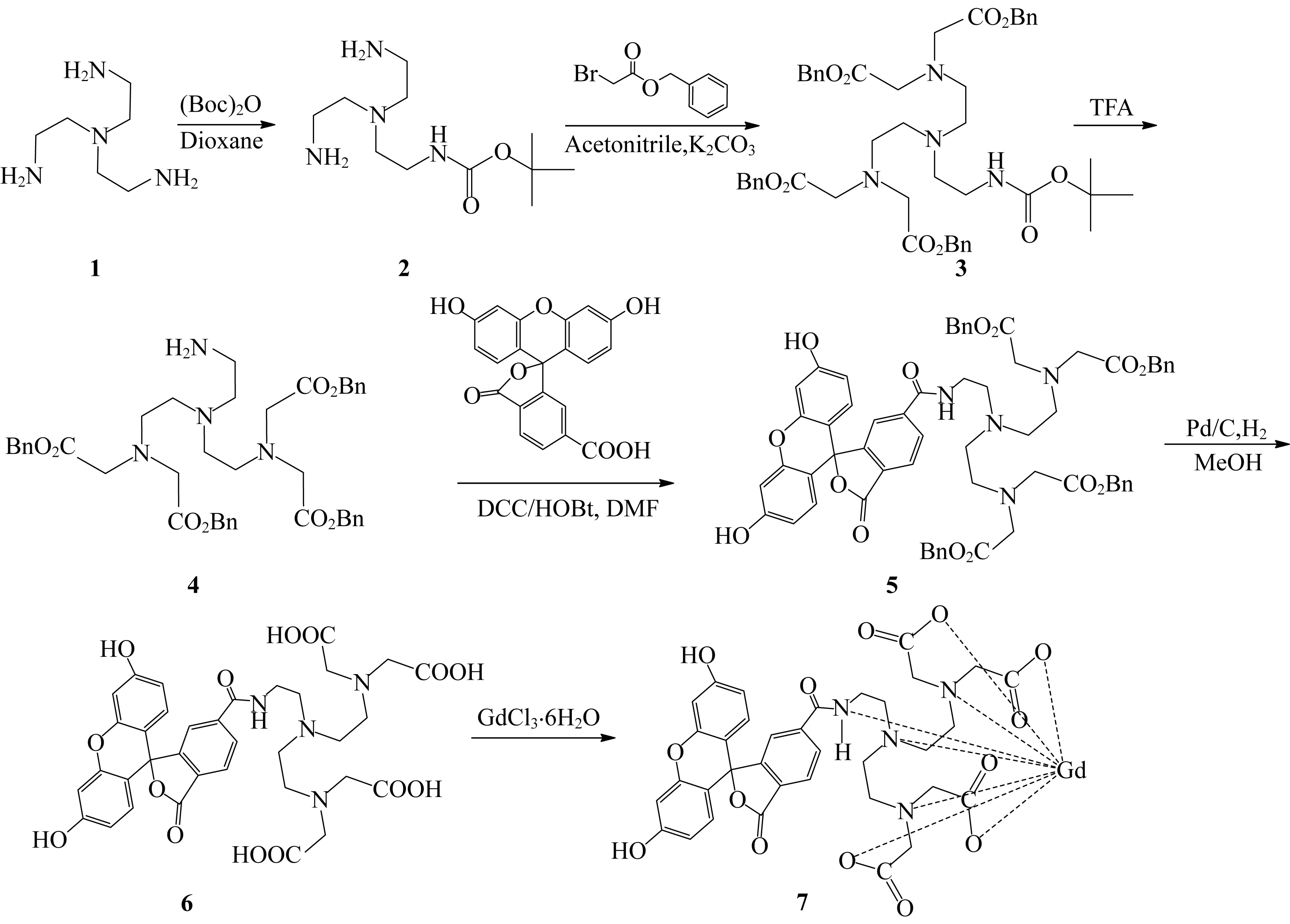
图1 双模式造影剂钆(III)配合物7的合成路线Fig.1 Synthesis of dual modal contrast agent Gd (III) complexes 7
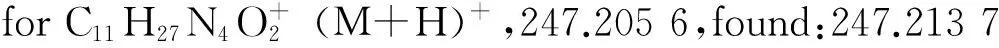
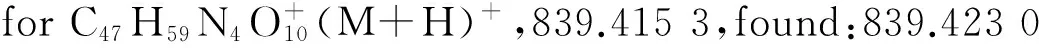
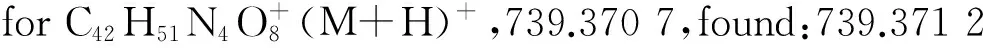

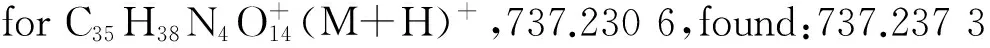
配合物7的合成:取配体6(120 mg,0.16 mmol)溶于超纯水(100 mL),溶液呈黄绿色,于三颈烧瓶内50 ℃下回流搅拌,并用0.5 mol/L NaOH调节反应体系的pH至6.5左右。另外将六水合氯化钆(75 mg,0.20 mmol)溶于超纯水(5 mL),用注射器缓慢加入该反应体系,共计2 d。期间用0.5 mol/L NaOH溶液不断调pH,保持体系的pH在6.5左右,注射完后搅拌反应3 d。反应完毕,用4 mol/L NaOH溶液调节pH至9,过滤除去不溶物,滤液旋干得到钆配合物7(0.134 g,产率92%)。
2 结果与讨论
2.1 钆配合物的合成
图2显示了化合物2,3和4的核磁氢谱图。三(2-氨基乙基)胺(TREN)中的伯胺通过碳酸二叔丁酯单保护后得到化合物2,在化学位移1.36处可以清楚地看到叔丁基的信号峰,2.30~3.20间的多重峰为乙基胺上氢的信号峰。在此反应的后处理中,用二氯甲烷/水体系分液萃取能除去TREN和副产物,从而使得提纯过程大幅度简化而得纯净的化合物2。此外,利用蠕动泵恒速微量滴加碳酸二叔丁酯至TREN中,也有助于提高目标产物的产率。接下来,采用乙腈为溶剂,碳酸钾为缚酸剂,将另外两个伯胺与过量的溴乙酸苄酯发生亲核取代反应后得到化合物3。在化学位移为7.33处显示了苄基上苯环的峰,5.11处为苄基上亚甲基的信号峰,3.59处为叔胺旁边的亚甲基的信号峰。最后,经过三氟乙酸对叔丁基氧羰基脱保护后获得化合物4。在核磁氢谱中,位于1.41处的叔丁基的峰完全消失,证明脱保护的成功。对化合物4的高分辨质谱(ESI-MS)分析进一步证明了化合物的结构。
6-羧基荧光素与化合物4的酰胺化反应是整个合成路线中重要的一步,该反应赋予配体荧光成像的功能。在本实验中,分别尝试过以1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(EDCI)/4-二甲氨基吡啶(DMAP),N-羟基丁二酰亚胺(NHS)的NHS/DMAP,EDCI/NHS等组合来活化羧基,但是反应均无法顺利进行。最后以DCC/HOBt来活化6-羧基荧光素,制成活性酯后再加入化合物4,成功得到目标化合物。随后以钯/碳作为催化剂,在氢气鼓泡的情况下常压氢解脱去苄基,通过无水乙醚反沉淀法去除杂质,得到纯净的配体6。
在配体6与六水合氯化钆的配位反应中,随着反应程度的深入,体系中会出现副产物盐酸,导致配体上氮原子被质子化进而影响配位效果。为此,需要在配位过程中不断地用氢氧化钠中和所产生的盐酸,同时需要保证体系的pH不能超过7。如果pH过高的话,钆离子会迅速转变为氢氧化钆沉淀而影响到其与配体6的配位效果。等配位反应完毕后,提高pH,将多余的氯化钆沉淀后即获得所需的双模式造影剂配合物7。该配合物具有良好的水溶性,在室温下10 mL去离子水中可以溶解0.89 g配合物,对应于约0.05 mol/L的溶解度。
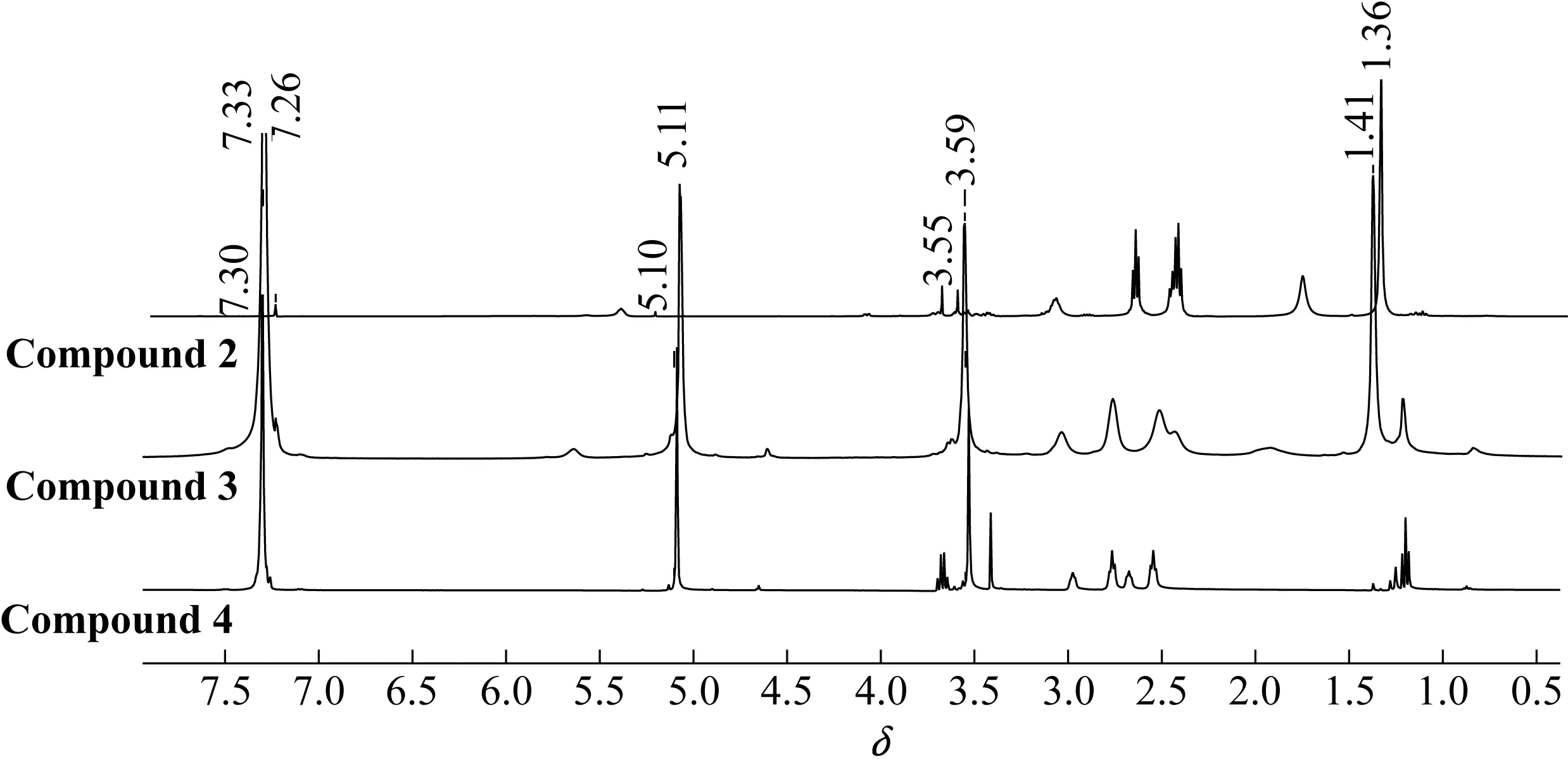
图2 化合物2,3,4的核磁共振氢谱的对比Fig.2 Comparison of 1H-NMR spectra of compound 2,3,4
2.2 钆配合物弛豫率的分析
钆配合物水溶液的纵向弛豫时间(T1)通过1.5T的GE核磁共振成像仪进行测定。将不同浓度的钆配合物溶液置于1.5 mL的塑料离心管,对这些样品进行核磁共振成像后得到图像。分析其像素与信号的指数关系,计算出样品中心的平均像素值,并得出相应的T1值。再根据1/T1与钆(Ⅲ)的浓度(c)的线性关系得到一次函数关系图,拟合直线的斜率即为弛豫率r1。
c与1/T1的线性关系如图3所示。由此得到钆配合物的弛豫率r1为3.46 mM-1·s-1,与商用造影剂马根维显[23](Gd-DTPA)的弛豫率(3.2 mM-1·s-1)接近。当核磁共振成像造影剂的水合常数为1时,其弛豫率通常在3~4 mM-1·s-1之间,因此配合物7的弛豫率符合这类造影剂的预期。另外,核磁共振成像结果显示随着钆浓度的增加,成像效果会越来越亮,如图4所示。
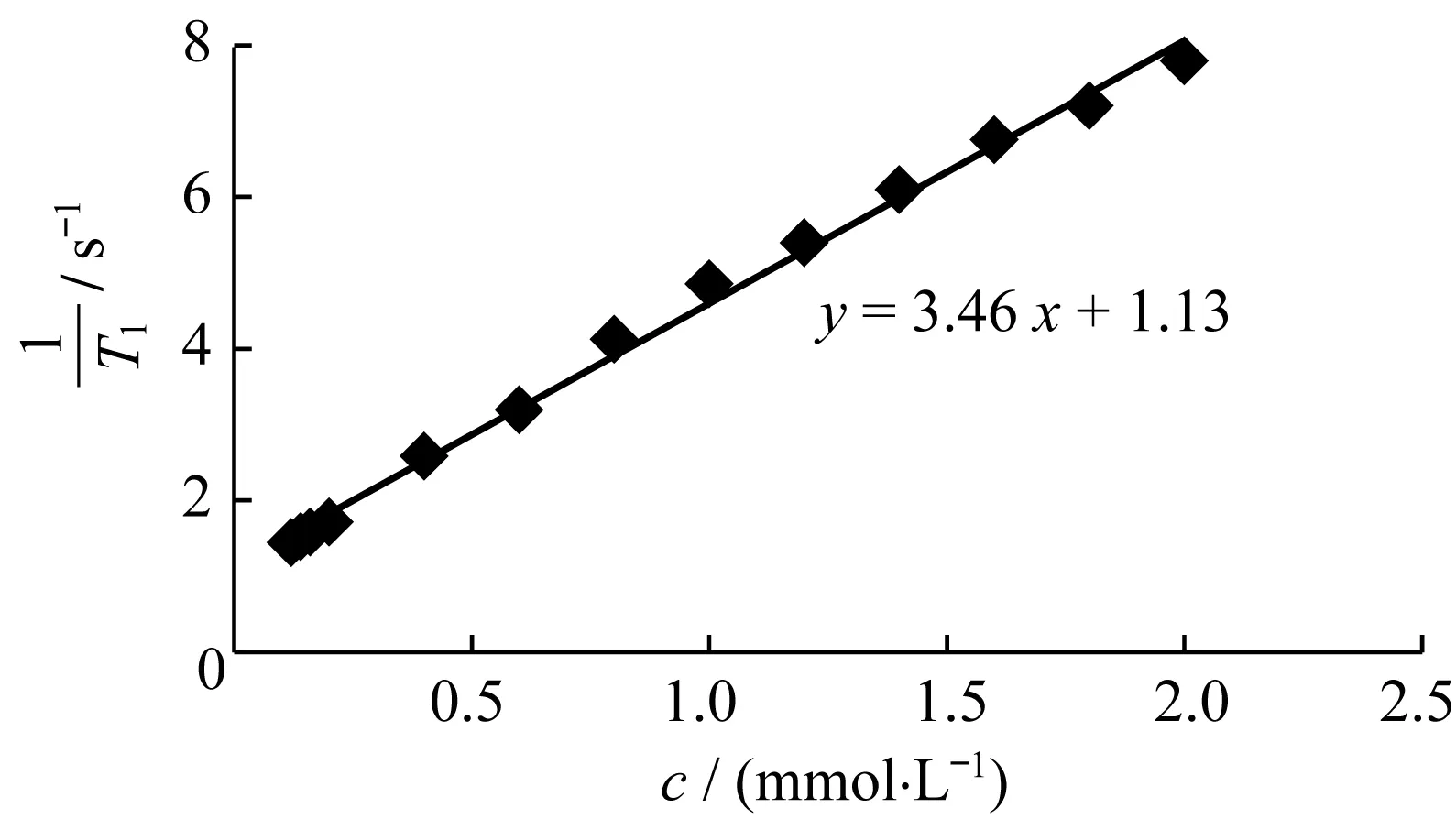
图3 双模式造影剂的r1曲线Fig.3 r1 curve of the bimodal contrast agent

图4 双模式造影剂的核磁共振成像Fig.4 MR image of the bimodal contrast agent
2.3 钆配合物荧光测试
图5显示了配合物7的紫外可见吸收光谱和荧光光谱。在紫外可见光谱中,配合物于490 nm处显示吸收峰,该吸收峰与6-羧基荧光素的吸收峰相近。选择460 nm作为激发波长,对配合物7进行荧光光谱扫描,发现其发射峰出现在522 nm,与6-羧基荧光素及化合物5,6的荧光发射峰均很接近,说明配合物7的颜色及荧光主要由荧光素单元贡献。如图5内插图所示,在自然光下,钆配合物7的水溶液呈现黄色荧光,当其受到365 nm紫外光的激发时,发出很强烈的黄绿色荧光。通过与荧光标准化合物(荧光素,79%)对比,配合物7的荧光量子产率的计算值为66%,其荧光灵敏度超过前述多种双模式造影剂。
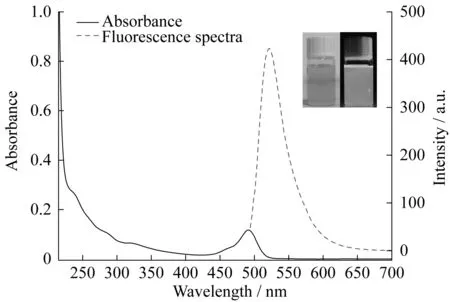
图5 双模式造影剂的紫外可见吸收光谱和荧光光谱Fig.5 UV-vis absorption and fluorescence spectra of the bimodal contrast agent
3 结 论
本文以三(2-氨基乙基)胺(TREN)与6-羧基荧光素为原料设计合成出一种新的双模式核磁共振成像造影剂,将核磁共振成像与光学成像有效结合。该造影剂弛豫率为3.46 mM-1·s-1,与商用造影剂马根维显(Gd-DTPA)的弛豫率相接近。荧光光谱显示该配合物的荧光发射峰出现在522 nm处。在紫外光的激发下,配合物发出强的黄绿色荧光。即使将造影剂稀释数倍,其仍保留了较高的荧光亮度,为今后在生物体内的应用打下良好基础。
[1] LAUTERBUR P C.Image formation by induced local interactions:Examples employing nuclear magnetic resonance [J].Nature,1973,242 (5394):190-191.
[2] LIANG Z P,LAUTERBUR P C.Principles of Magnetic Resonance Imaging:A Signal Processing Perspective [M].[s.l.]:Wiley-IEEE Press,2000.
[3] CARAVAN P,ELLISON J J,MCMURRY T J,etal.Gadolinium(III) chelates as MRI contrast agents:Structure,dynamics and applications [J].Chemical Reviews,1999,99(9):2293-2352.
[4] WERNER E J,DATTA A,JOCHER C J,etal.High-relaxivity MRI contrast agents:Where coordination chemistry meets medical imaging [J].Angewandte Chemie International Edition,2008,47(45):8568-8580.
[5] VISWANATHAN S,KOVACS Z,GREEN K N,etal.Alternatives to gadolinium-based metal chelates for magnetic resonance imaging [J].Chemical Reviews,2010,110(5):2960-3018.
[6] CARAVAN P.Strategies for increasing the sensitivity of gadolinium based MRI contrast agents [J].Chemical Society Reviews,2006,35(6):512-523.
[7] BOTTA M,TEI L.Relaxivity enhancement in macro molecular and nanosized gdIII-based MRI contrast agents [J].European Journal of Inorganic Chemistry,2012(12):1945-1960.
[8] DATTA A,RAYMOND K N.Gd-hydroxypyridinone (HOPO)-based high-relaxivity magnetic resonance imaging (MRI) contrast agents [J].Accounts of Chemical Research,2009,42(7):938-947.
[9] LAUFFER R B.Paramagnetic metal complexes as water proton relaxation agents for NMR imaging:Theory and design [J].Chemical Reviews,1987,87 (5):901-927.
[10] RIVAS C,STASIUK G J,GALLO J,etal.Lanthanide(III) complexes of rhodamine-DO3A conjugates as agents for dual-modal imaging [J].Inorganic Chemistry,2013,52(24):14284-14293.
[11] JANG J H,BHUNIYA S,KANG J,etal.Cu2+-Responsive bimodal (optical/MRI) contrast agent for cellular imaging [J].Organic Letters,2013,15(18):4702-4705.
[12] GONG P,CHEN Z,CHEN Y,etal.High-relaxivity MRI contrast agents prepared from miniemulsion polymerization using gadolinium(III)-based metallosurfactants [J].Chemical Communications,2011,47(14):4240-4242.
[13] LIVRAMENTO J B,TOTH E,SOUR A,etal.High relaxivity confined to a small molecular space:A metallostar-based,potential MRI contrast agent [J].Angewandte Chemie International Edition,2005,44(10):1480-1484.
[14] VERWILST P,ELISEEVA S V,VANDER ELST L,etal.A tripodal ruthenium-gadolinium metallostar as a potential alpha(v)beta(3) integrin specific bimodal imaging contrast agent [J].Inorganic Chemistry,2012,51(11):6405-6411.
[15] DEHAEN G,ELISEEVAS V,KIMPE K,etal.A self-assembled complex with a titanium (IV) catecholate core as a potential bimodal contrast agent[J].Chemistry:A European Journal,2012,18(1):293-302.
[16] GONG N,WANG H,LI S,etal.Microwave-assisted polyol synthesis of gadolinium-doped green luminescent carbon dots as a bimodal nanoprobe [J].Langmuir,2014,30(36):10933-10942.
[17] BOURLINOS A B,BAKANDRITSOS A,KOULOUMPIS A,etal.Gd (III)-doped carbon dots as a dual fluorescent-MRI probe [J].Journal of Materials Chemistry,2012,22(44):23327-23330.
[18] ZHU Q,PAN F,TIAN Y,etal.Facile synthesis of Gd(III) metallosurfactant-functionalized carbon nanodots with high relaxivity as bimodal imaging probes [J].RSC Advances,2016,35(6):29441-29447.
[19] UENO Y,JIAO G S,BURGESS K.Preparation of 5,6-carboxyfluorescein [J].Synthesis-Stuttgart,2004(15):2591-2593.
[20] DIVITTORIO K M,HOFMANN F T,JOHNSON J R,etal.Facilitated phospholipid translocation in vesicles and nucleated cells using synthetic small molecule scramblases [J].Bioorganic & Medicinal Chemistry,2009,17(1):141-148.
[21] CHONG H S,SONG H A,BIRCH N,etal.Efficient synthesis and evaluation of bimodal ligand NETA [J].Bioorganic & Medicinal Chemistry Letters,2008,18(11):3436-3439.
[22] BRELLIER M,BARLAAM B,MIOSKOWSKI C,etal.Insight into the complexation mode of bis (nitrilotriacetic acid) (NTA) ligands with Ni2+involved in the labeling of histidine-tagged proteins [J].Chemistry:A European Journal,2009,15(46):12689-12701.
[23] VILLARAZA AJ L,BUMB A,BRECHBIEL M W.Macro molecules,dendrimers,and nanomaterials in magnetic resonance imaging:The interplay between size,function,and pharmacokinetics [J].Chemical Reviews,2010,110(5):2921-2959.
Synthesis of Bimodal Magnetic Resonance Imaging Contrast Agent from Tris(2-aminoethyl)amine and 6-Carboxy-Fluorescein
PAN Fei, ZHU Qin, QIAN Wei-qiao, HU Ai-guo
(Shanghai Key Laboratory of Advanced Polymeric Materials,School of Materials Science and Engineering,East China University of Science and Technology,Shanghai 200237,China)
A fluorescent ligand with polydentate amino carboxylate moieties was synthesized from tris(2-aminoethyl)amine and benzyl 2-bromoacetate,followed by the introduction of fluorescent functionality through an amidation reaction between the primary amine group and 6-carboxy-fluorescein.After coordination with paramagnetic GdC13·6H2O,a bimodal contrast agent combing the ability for magnetic resonance imaging (MRI) and optical imaging was formed.The structures of the ligands and the complexes were confirmed by both H- and C-NMR、high resolution mass spectrometry,and ICP-AES.This new MRI contrast agent showed ar1value (longitudinal relaxivity) of 3.46 mM-1·s-1,comparable to commercial small molecular contrast agent like Magevist®(Gd-DTPA).This complex also showed bright green fluorescence when shined with UV light,showing a high quantum yield of 66%,which is essential for clinical bimodal imaging.
magnetic resonance imaging; contrast agent; TREN; fluorescence imaging; quantum yield
1006-3080(2016)06-0758-06
10.14135/j.cnki.1006-3080.2016.06.003
2016-04-01
国家自然科学基金(21274042)
潘 斐 (1991-),男,江苏常州人,硕士生,主要从事高分子合成研究。E-mail:irving00@126.com
胡爱国,E-mail:hagmhsn@ecust.edu.cn
O621.3
A
