酰基硅烷的合成方法研究进展*
2017-01-17王晓娟
唐 贝,王晓娟
(1 河南应用技术职业学院,河南 开封 475001;2 商丘师范学院化学系, 河南 商丘 476000)
酰基硅烷的合成方法研究进展*
唐 贝1,王晓娟2
(1 河南应用技术职业学院,河南 开封 475001;2 商丘师范学院化学系, 河南 商丘 476000)
酰基硅烷是一类令人着迷的有机化合物,显示出许多独特的化学和物理性质。其结构中所含的酰基硅烷官能团[R-C(O)Si]持有的独特反应模式,使它们成为现代有机合成中越来越吸引人的一部分。本文简要的概述了近十五年来酰基硅烷在有机化学中的合成方法的最新进展。由于酰基硅烷化合物中官能团[R-C(O)Si]所具有的独特反应模式,近十五六年来, 酰基硅烷化合物的合成方法备受关注,大大推动了这一领域的发展。
酰基硅烷;有机合成;研究进展
1 有机硅试剂:酰基硅烷的合成方法
1.1 利用二噻烷或苯并三唑类化合物
2000年,Moran等[1]将N-溴代丁二酰亚胺(NBS)用于2-甲基硅基-1,3-二噻烷的氧化水解。实验结果显示:生成的芳香族酰基硅烷易被进一步氧化成羧酸。后来,通过加入碱和降低反应温度有效地阻止了酰基硅烷氧化为羧酸。

图1 由2-二甲基硅基-1,3-二噻烷合成双酰基硅烷
2000-2002年,Portella等[2-3]采用Brook-Corey法,成功制备出一些更有趣的酰基硅烷衍生物,如:碳水化合物衍生的酰基硅烷[4]和双(酰基硅烷)。

图2 由2-烷基或2-苯基-1,3-二噻烷和双(氯代)二硅烷或二硅氧烷反应合成双酰基硅烷
除了硅烷基1,3-二噻烷,还有一些α-硅烷基酰基阴离子等价物也被用于合成酰基硅烷化合物。
1996年,Katritzky[5]开发出另外一种通用合成方法,经以下几步:1-(苯并三唑-1-基)-1-乙氧基烷烃1经锂化、硅烷基化形成酰基硅烷前体2,随后将化合物2在酸性条件下水解,形成各种芳酰基、杂芳酰基、α, β-不饱和烯酰基和炔酰基硅烷3。
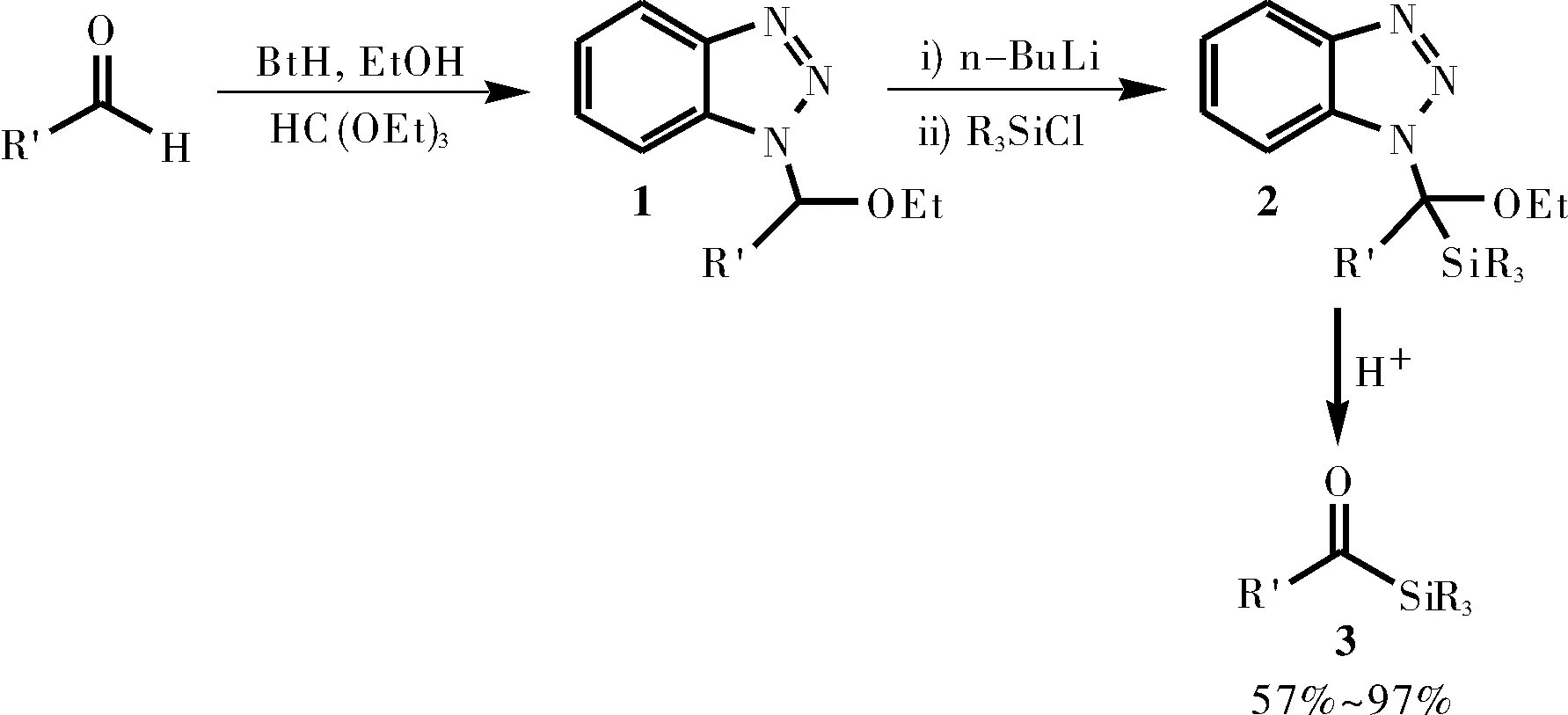
图3 由N, O-缩醛化合物合成酰基硅烷
1.2 羧酸衍生物的硅烷基化
2000年,Ricci小组[6]通过酰基咪唑4与多金属试剂(PhMe2Si)2CuCNLi2反应,顺利制得N-叔丁氧羰基保护的α-氨基酰基硅烷5。

图4 利用有机铜锂制备酰基硅烷
2004年,Scheidt等[7]使用吗啉酰胺6与硅烷基锂试剂7反应成功合成出各种酰基硅烷,并得到良好的产率。

图5 由吗啉酰胺合成酰基硅烷
2011年,Okano等[8]通过硫酯8与硅烷基锌氯化物9的钯催化偶联反应,具有多种官能团的S-苯基硫酯转化成为相应的酰基硅烷。

图6 硫酯的钯催化反应合成酰基硅烷
基于Beller小组[9]对卤代芳烃的钯催化羰基化反应的持续关注,2012年,他们报道了一种用于合成酰基硅烷的新型的钯催化羰基化反应。
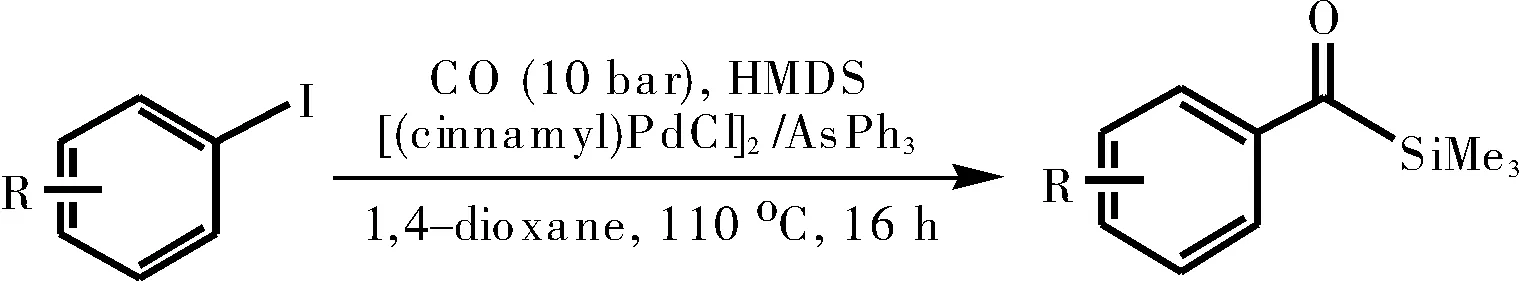
图7 钯催化羰基化反应合成酰基硅烷
2012年,Murakami小组[10]报道了一些更不寻常的取代酰基硅烷的合成方法,即通过碳碳和硅硅键之间的分子内σ-键复分解反应。

图8 二硅烷与环丁酮的分子内反应形成酰基硅烷
1.3 酰基硅烷合成的替代方法
最早报道的酰基硅烷的合成方法中,有些是采用苄基和烯丙基硅烷与NBS反应形成相应的gem-二溴化物11[11-13],随后经醋酸银氧化得到一系列酰基硅烷12。这种方法被证明是合成芳香族酰基硅烷的一种特别有效的方法。

图9 由gem-二溴化物形成酰基硅烷
2006年,Oshima课题组[14-15]报道了一种制备各种酰基硅烷的简单方法,他们以二氯双(甲基二苯基硅基)甲烷13a或硼基二氯甲基硅烷13b为原料。利用一锅煮方法,化合物13先与正丁基锂反应、在CuCN2·LiCl存在下再与格氏试剂反应形成gem-二硅基烷基铜酸盐或gem-硼基硅基烷基铜酸盐14。

图10 由gem-二氯硅烷合成酰基硅烷
2013年,Grée等[16]报道了一个镍-催化的合成方法,以α-羟基烯丙基硅烷15为原料分别制备出脂肪族取代酰基硅烷16和17。在超氢化物(三乙基硼氢化锂)、催化剂NiCl2·dppe的存在下,形成烷基取代的酰基基硅烷16,收率良好。在催化量的NiCl2·BINAP、超氢化物和溴化镁作用下,一个类似的异构化-缩醛反应促使α-羟基烯丙基硅烷和醛反应形成高度取代的酰基硅烷17。
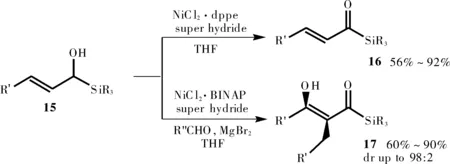
图11 镍催化合成酰基硅烷
α-烷氧基硅烷通过烷基锂介导的[1,4]-魏悌锡重排反应也可制备酰基硅烷[17]。由于[1,2]-魏悌锡重排反应的竞争和其他相关异构体的产生,导致反应收率较低。

图12 利用α-烷氧基硅烷的[1,4]-魏悌锡重排反应提供酰基硅烷
1.4 α, β-不饱和酰基硅烷的合成
2003年,Akiyama小组[18]开发出一种高效的不对称合成方法。在铜(Ⅰ)催化下,他们将1-甲氧基联烯基硅烷与α-亚氨酸酯进行对映选择性的[2+2]环加成反应,并以良好的收率得到3-亚甲基氮杂环丁烷-2-羧酸酯。随后经酸介导的水解,得到手性的氨基酯酰基不饱和硅烷衍生物18。
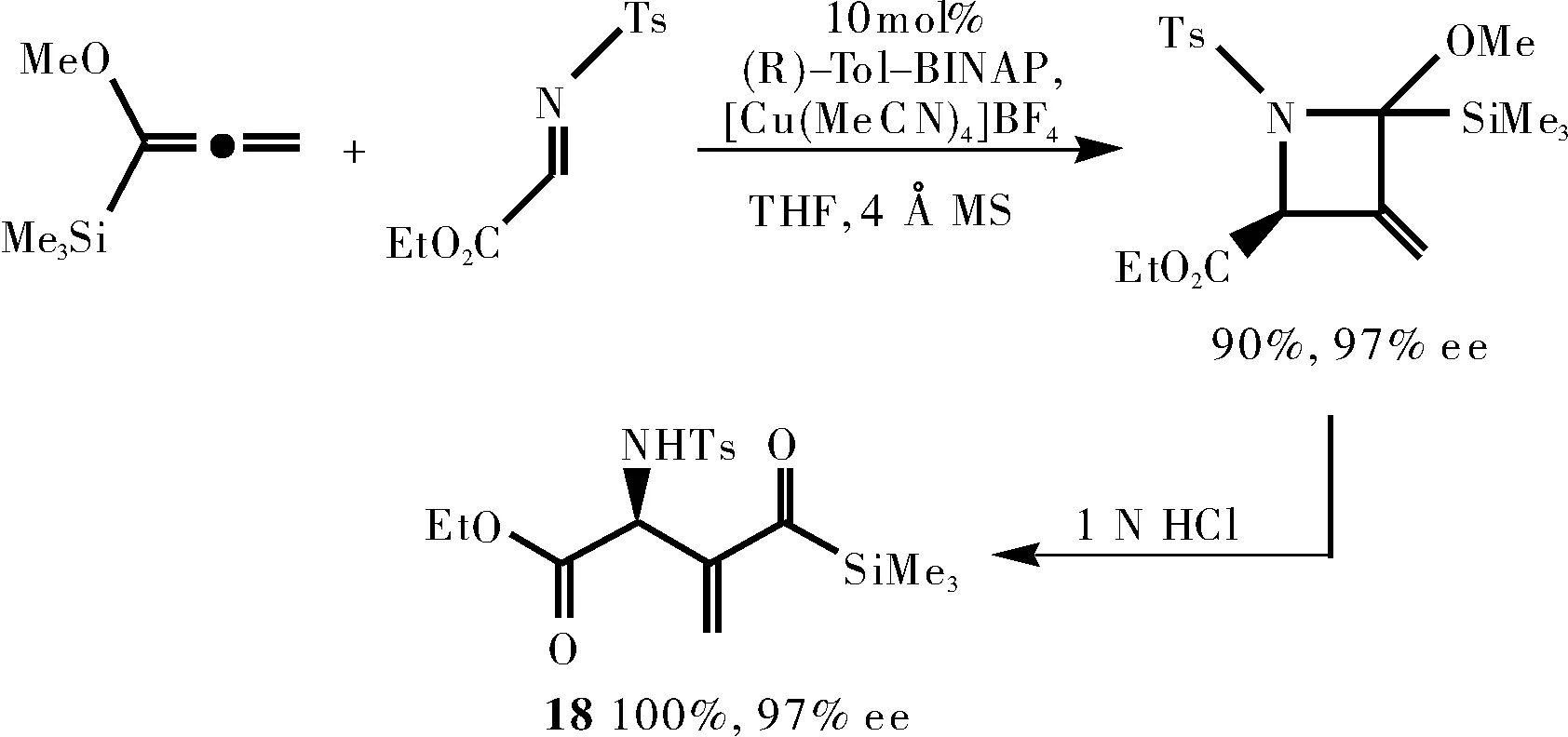
图13 手性α,β-不饱和酰基硅烷的合成
2007年,Denmark[19]报道了在路易斯酸作用下,1-三甲基硅基二烯醇硅醚与硝基烯经γ-选择性共轭加成反应生成α,β-不饱和酰基硅烷19,该α,β-不饱和酰基硅烷可进一步合成为氮杂环庚烷。

图14 利用Mukaiyamatype vinylogous型羟醛缩合反应制备α,β-不饱和酰基硅烷
1.5 氟取代酰基硅烷的合成
2001年,Percy等[20]以几种烯丙基三氟乙基醚为原料,先经脱氟化氢/金属化形成二氟烯醇硅烷20,再经克莱森重排得到α,α-二氟酰基硅烷21。

图15 α,α-酰基硅烷的合成
同时,Welch等[21]报道了化合物22及相关氟化酰基硅烷23~25的合成方法。
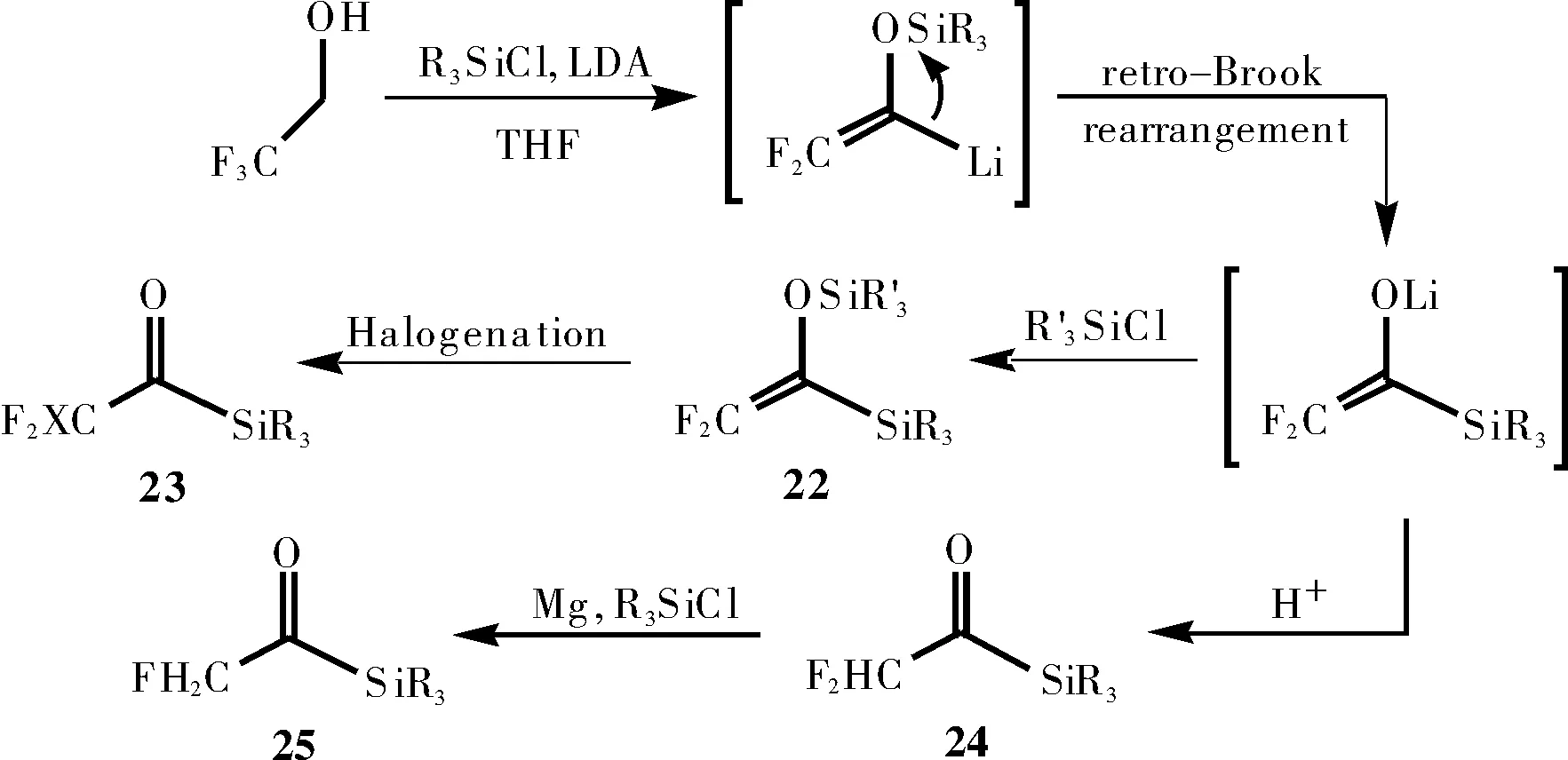
图16 由2,2,2-三氟乙醇合成α-氟代酰基硅烷
随后,他们还报道了化合物26和磺酰亚胺27经Mannich反应产生相应的α,α-二氟酰基硅烷28,且化合物28很容易转变成相应的α,α-二氟-β-氨基酸酯[22]。

图17 曼尼希反应合成α-氟代酰基硅烷
2003年,Bordeau研究小组[23]开发了一种有效的电化学方法,该方法从三氟乙酸乙酯开始,成功合成出三氟乙酰基三甲基硅烷。
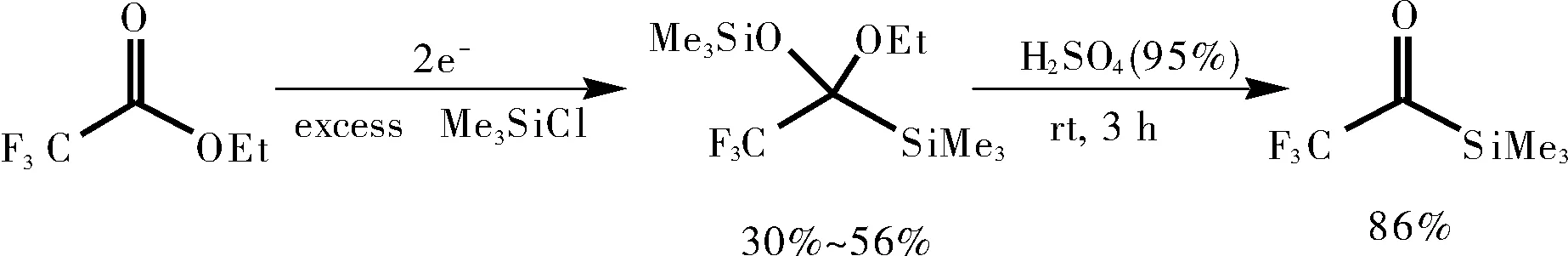
图18 制备三氟乙酰基三甲基硅烷的一种电化学方法
2009年,卿凤翎等[24]开发了一种有效的方法用于制备β-氨基-α,α-二氟酮衍生物,其中包括α,α-二氟酰基硅烷29。

图19 叔胺的氧化二氟甲基化制备酰基硅烷衍生物
2 结论与展望
自50年前被发现,酰基硅烷的合成已受到广泛的研究。它们在有机合成的众多反应过程中显示出很大的价值,然而,与其他官能团相比,酰基硅烷的合成方法仍然有限。更加有效、更加通用的合成方法还有待开发,特别是对那些官能化酰基硅烷的合成方法的研究。
[1] Patrocínio A F, Moran P J S. Synthesis of acylsilanes via oxidative hydrolysis of 2-silyl-1,3-dithianes mediated by N-bromosuccinimide [J]. Journal of Organometallic Chemistry, 2000, 603(2): 220-224.
[2] Saleur D, Bouillon J P, Portella C. First Synthesis of 1,4-Bis(acylsilanes)[J]. Tetrahedron Letters, 2000, 41(3):321-324.
[3] Bouillon J P, Huguenot F, Portella C. Synthesis of a new type of bis(acylsilanes) starting from 2-alkyl-or 2-phenyl-1,3-dithiane and bis(chlorinated) disilane or disiloxane [J]. Synthesis, 2002, 2002(04):552-556.
[4] Gérard S, Richard P R, Portella C. Synthesis of 3-trialkylsilyl pyrazoles from β-oxo acylsilanes [J]. Tetrahedron Lett., 2000, 41(50):9791-9795.
[5] Katritzky A R, Lang H, Wang Z, et al. Convenient Syntheses of Functionalized Dialkyl Ketones and Alkanoylsilanes: 1-(Benzotriazol-1-yl)-1-phenoxyalkanes as Alkanoyl Anion Equivalents.[J]. ChemInform, 1997, 61(8):7551-7557.
[6] Bonini B F, Comes-Franchini M, Fochi M, et al. Silylcupration of acylimidazolides: a new synthesis of α-aminoacylsilanes and their synthetic applications[J]. Polyhedron, 2000, 19(5):529-531.
[7] Clark C T, Milgram B C, Scheidt K A.Efficient synthesis of acylsilanes using morpholine amides [J]. Org. Lett., 2004, 6(22):3977-3980.
[8] Azuma H, Okano K, Tokuyama H.Synthesis of acylsilanes by palladium-catalyzed cross-coupling reaction of thiol esters and silylzinc chlorides [J]. Chem. Lett., 2011, 40(9):959-961.
[9] Wu X F, Neumann H, Beller M.Palladium-catalyzed carbonylative coupling re-actions of aryl iodides with hexamethyldisilane (HMDS) to benzoyl silanes [J]. Tetrahedron Letters, 2012, 53(5):582-584.
[10]Ishida N, Ikemoto W, Murakami M. Intramolecular σ-bond metathesis between carbon-carbon and silicon-silicon bonds [J]. Org. Lett., 2012, 14(12):3230-3232.
[11]Brook A G. Triphenylsilyl phenyl ketone [J]. J. Am. Chem. Soc., 1957, 79(16):4373-4375.
[12]Brook A G, Peddle G J D. Dibenzoylsilanes and substiyuted benzoylsilanes [J]. Can. J. Chem., 1963, 41(9):2351-2356.
[13]Cossrow J, Rychnovsky S D. Optically pure α-(trimethylsilyl)benzyl alcohol: a practical chiral auxiliary for oxocarbenium ion reactions [J]. Org. Lett., 2002, 4(1):147-150.
[14]Inoue A, Kondo J, Hiroshi Shinokubo A, et al. Facile synthesis of acylsilanes via aerobic oxidation ofgem-disilylalkylcopper compounds [J]. J. Am. Chem. Soc., 2001, 123(44):11109-11110.
[15]Kondo J, Shinokubo H, Oshima K. Oxidation ofgem-borylsilylalkyl coppers to acyl-silanes with Air [J]. Org. Lett., 2006, 8(6):1185-1187.[16]Reddy GP, Reddy JS, Das S, et al. Synthesis of acylsilanes via nickel-catalyzed reactions of α-hydroxyallylsilanes.[J]. ChemInform, 2013, 44(33):1524-1527.
[17]Onyeozili N, Mori-Quiroz L M, Maleczka-JR R E.[1,2]-and [1,4]-Wittig re-arrangements of α-alkoxysilanes: effect of substitutions at both the migrating benzylic carbon and the terminal sp2carbon of the allyl moiety [J]. Tetrahedron, 2013, 69(2):849-860.
[18]Akiyama T, Daidouji K, Fuchibe K.Cu(Ⅰ)-catalyzed enantioselective [2+2] cyclo-addition of 1-methoxyallenylsilane with α-imino ester: chiral synthesis of α, β-unsaturated acyl-silanes [J]. Org. Lett., 2003, 5(20):3691-3693.
[19]Denmark S E, Xie M. Lewis acid-promoted conjugate addition of dienol silyl ethers to nitroalkenes:Synthesis of 3-substituted azepanes [J]. J. Org. Chem., 2007, 72(18):7050-7053.
[20]Garayt M R, Percy J M. A direct and useful route to difluoroacylsilanes and difluoro-acylstannanes and their potential for the generation of structurally diverse difluoroketones [J]. Tetrahedron Lett., 2001, 42(36):6377-6380.
[21]Higashiya S, Chung W J, Welch J T. Synthesis of mono-and difluoroacetyltri alkyl-silanes and the corresponding enol silyl ethers [J]. J. Org. Chem., 2004, 69(19):6323-6328.
[22]Chung W J, Omote M, Welch J T. The catalytic Mannich reaction of 1,1-difluoro-2-trialkyl(aryl)silyl-2-trimethyl-silyloxyethenes: preparation of β-amino acid derivatives [J]. J. Org. Chem., 2005, 70(19): 7784-7787.
[23]Bordeau M, Clavel P, Barba A. Non-defluorinative electrochemical silylation of ethyl trifluoroacetate: a practical synthesis of trifluoroacetyltrimethylsilane via its ethyltrimethyl-silyl ketal [J]. Tetrahedron Lett., 2003, 44(19):3741-3744.
[24]Chu L L, Zhang X G, Qing E L. CuBr-catalyzed oxidative difluoro-methylation of tertiary amines with difluoroenol silyl ethers [J]. Org. Lett., 2009, 11(10):2197-2200.
Research Progress on Synthetic Methods of Acylsilanes*
TANGBei1,WANGXiao-juan2
(1 Henan Vocational College of Applied Technology, Henan Kaifeng 475001;2 Department of Chemistry, Shangqiu Normal University, Henan Shangqiu 476000, China)
The acyl silane is a class of organic compounds, fascinating shows many unique chemical and physical properties. Contained in the structure, acyl silane functional groups [R-C(O)Si] holds unique reaction mode, makes them become a part of the more and more attractive in modern organic synthesis. A brief overview of the acyl silane nearly fifteen years of the progress of the synthesis in organic chemistry was introduced.Functional groups in the acyl silane compounds [R-C(O)Si] had unique reaction mode, nearly in 15~16 years, much attention was paid to synthetic methods of the silane compounds which greatly promoted the development of this field.
acylsilanes; organic synthesis; research progress
国家自然科学基金资助项目(No. U1504207);河南省科技攻关项目(No. 162102310486)。
唐贝(1984-),女,硕士,助讲,主要从事不对称合成及催化的研究。
O62
A
1001-9677(2016)024-0006-04
