S-N-乙基-2-氨甲基吡咯烷的合成研究进展
2017-01-09侯俊波陈志卫
张 权,侯俊波,陈志卫
(浙江工业大学药学院,浙江杭州310014)
医药化工
S-N-乙基-2-氨甲基吡咯烷的合成研究进展
张 权,侯俊波,陈志卫*
(浙江工业大学药学院,浙江杭州310014)
(S)-N-乙基-2-氨甲基吡咯烷作为左旋舒必利与舒托必利合成的必要起始原料,具有潜在的广阔市场。综述了(S)-N-乙基-2-氨甲基吡咯烷的几种具有代表性的合成方法,并对其进行了分析评价。
(S)-N-乙基-2-氨甲基吡咯烷;化学合成;舒必利;手性
0 前言
舒必利(Sulpiride)是一种新型抗精神病药,1967年由法国Delagrange首先合成,与传统抗精神病药物不同,舒必利只选择性地阻断D2受体[1]。椎体系副反应轻微是其突出的优点。该药副作用小,治疗范围广,有“关系调节药物”、“情感赋活剂”和“抗孤独剂”等名称。左旋舒必利可通过舒必利拆分获得,但因其收率低,分离纯化困难[2],目前工业上通常以左旋N-乙基-2-氨甲基吡咯烷与2-甲氧基-5-氨磺酰苯甲酸甲酯为原料制备得到[3]。抗精神病新药舒托必利通常也使用S-N-乙基-2-氨甲基吡咯烷与2-甲氧基-5-乙磺酰基苯甲酸甲酯反应制得[4]。
由此可见,S-N-乙基-2-氨甲基吡咯烷是制备左旋舒必利与舒托必利的关键中间体,其制备方法在国内外引起众多药物化学工作者的关注。本文主要综述了不同的合成路线并简评了其优缺点。
1 合成路线
S-N-乙基-2-氨甲基吡咯烷制备方法可分为化学拆分法和经手性源不对称合成两大类。
1.1 化学拆分法
化学拆分法是先合成其相应外消旋体N-乙基-2-氨甲基吡咯烷2,然后进行手性拆分,目前常用的拆分剂为D-酒石酸。
1.1.1 以N-乙基吡咯烷酮为原料制备S-N-乙基-2-氨甲基吡咯烷
Kamiya T等人[5]报道了以N-乙基吡咯烷酮为原料,经Henry反应、加氢还原、手性拆分[6-8]三步得到目标产物1,总收率为8.2%。如Scheme 1所示。
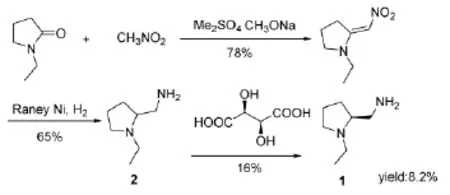
Scheme 1
该路线的优点在于以价格低廉的N-乙基吡咯烷酮为起始原料,使路线成本较低,该工艺操作简便,不足之处在于手性拆分收率较低。
1.1.2 以四氢糠醇为原料制备S-N-乙基-2-氨甲基吡咯烷
邱国祥等人[9]以四氢糠醇为原料,氯代后与邻苯二甲酰亚胺缩合,经开环-溴代反应、氨化-水解反应、手性拆分[6-8],得目标产物1,总收率为4.8%,如Scheme 2所示。

Scheme 2
该工艺的不足之处在于合成过程中需要消耗大量二甲基甲酰胺及价格昂贵的溴化钠,总收率低,导致路线成本较高。
吴廷照等[10]对上述路线进行了改进,以四氢糠醇为原料,经氯代、氨化、苯甲酰氯保护,氯化亚砜开环,与乙胺环合后水解,最后手性拆分[6-8]得到目标产物1,总收率为6.6%。如Scheme 3所示。
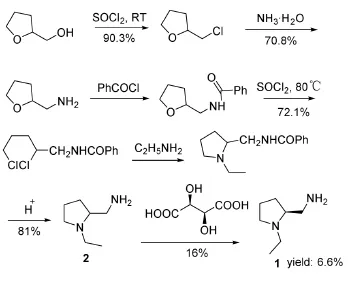
Scheme 3
该工艺的优点是用价廉的氯化亚砜替代了价格昂贵的溴化钠,本工艺不足之处在于反应步骤较多,收率低,路线的成本较高。
1.2 经手性源不对称合成
由手性源不对称合成主要有以下两种类型:(1)以S-2-羟甲基吡咯烷为手性源;(2)以L-脯氨酸为手性源。
1.2.1 以S-2-羟甲基吡咯烷为手性源制备SN-乙基-2-氨甲基吡咯烷
John E B等[11]报道了以S-2-羟甲基吡咯烷为原料,经N-乙酰化、氯代、叠氮化和还原制备目标产物1,总收率为49%,如Scheme 4所示。
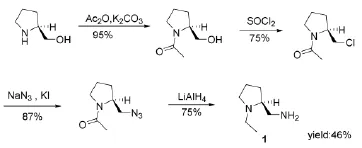
Scheme 4
该反应中所用到的氯化亚砜,会产生有毒气体二氧化硫;氢化锂铝,使该路线成本高;叠氮化钠操作不当,容易发生爆炸。
1.2.2 以L-脯氨酸为手性源制备S-N-乙基-2-氨甲基吡咯烷
邱国祥等人[12]报道以L-脯氨酸为原料,经N-乙酰化、酰氯化、氨解、KBH4-CH3COOH体系还原合成目标产物1,如Scheme 5所示。

Scheme 5
该路线不足之处在于需要将两个羰基还原成亚甲基,还原剂KBH4用量大,使路线成本高。
Lannoye G S[13]以L-脯氨酰胺为原料,经N-乙基化,氢化锂铝还原得目标产物1,总产率为48%,如Scheme 6所示。

Scheme 6
该方法优点在于经N-乙基化制备中间产物3,从而只需要还原一个羰基,降低了还原剂的用量,但氢化锂铝价格较贵,导致路线成本较高。
任来阳[14]以L-脯氨酸为原料,经N-乙基化、氨解、NaBH4-TiCl4还原得到目标产物1,总收率为73%,如Scheme 7所示。
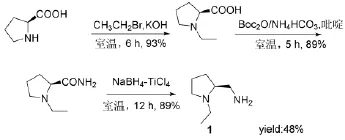
Scheme 7
该路线的优点在于总收率在所有路线中最高,作者用NaBH4-TiCl4代替LiAlH4为还原剂,降低了原料成本,因起始原料L-脯氨酸价格较贵,工业上大规模应用受到限制。
梁江辉等人[15]在前人的基础上,结合硼氢化钠在使用时,加入碘可大大提高其还原能力[16-17]的特性,以L-脯氨酸为原料,经N,O-双乙基化、氨解、NaBH4-I2还原三步反应合成目标产物1,总收率为30.7%,如Scheme 8所示。
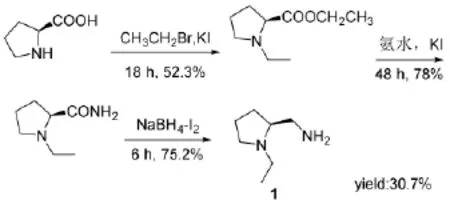
Scheme 8
该路线的优点在于还原过程中实现了以NaBH4-I2的还原体系替代LiAlH4,降低了成本,不足之处在于反应耗时长,整个反应需要72 h,反应过程使用了碘单质,对人体危害大,起始原料L-脯氨酸价格较贵,限制了工业上大规模应用。
2 小结
S-N-乙基-2-氨甲基吡咯烷作为一种重要的手性药物中间体,尽管文献报道了很多关于它的制备方法,但是其制备方法还有待进一步改进和完善。
化学拆分法中,以价廉的N-乙基吡咯烷酮为起始原料,路线成本较低,然而手性拆分收率低,相当于有一半以上的原料被浪费;而以L-脯氨酸为手性源制备目标产物可以避免这一浪费现象,但还原剂和L-脯氨酸价格较贵限制了该路线工业上大规模应用。
目前主流工业化生产路线是化学拆分法,随着对手性拆分的深入研究,开发出手性拆分效率更高的拆分试剂势必给以S-N-乙基-2-氨甲基吡咯烷为中间体的医药化工行业带来巨大的经济效益。
[1]唐济生,李星宝,宋振铎,等.舒必利的抗抑郁作用[J].山东精神医学,1995,(4):61-64.
[2]姚文豪,陈斌.多巴胺受体阻断剂左旋舒必利[J].国外药学——合成药生化药制剂分册,1988,9:299-302.
[3]王福兰,李桂玲,唐登峰.舒必利的合成[J].中国医药工业杂志,1996,27(11):487-489.
[4]朱占元,丁爱忠,牟玲.盐酸舒必利的合成[J].北京工商大学学报,2003,21(3):21-22.
[5]Kamiya T,Hashimoto M.2-Aminomethy l-1-alkylpyrrolidines:DE,1941536 A[P].1970-03-05.
[6]蒋忠良,栾家国,施宪法,等.左舒必利的合成[J].中国医药工业杂志,1996,27(11):485-486.
[7]吴廷照,陈同明,韩炳荣.N-乙基-2-氨甲基吡咯烷的拆分[J].浙江化工,2001,32(3):28.
[8]张恺,薛娜,杜玉民,等.(S)-(-)-氨磺必利-D-(-)-酒石酸盐的合成[J].中国现代应用药学,2009,26(8):635-637.
[9]邱国祥.1-乙基-2-氨甲基四氢吡咯及其生产工艺:CN,1174191A[P].1998-02-25.
[10]吴廷照,朱占元.N-乙基-2-氨甲基吡咯烷的合成[J].应用化工,2001,30(4):33-34.
[11]John E B,Chester A M,John M,et al.Synthesis and in vitro evaluation of 2,3-dimethoxy-5-(fluoroalkyl)-substituted benzamides:high-affinity ligands for CNSdopamine D2receptors[J].J.Med.Chem.,1991,34(5):1612-1624.
[12]邱国祥.左旋1-乙基-2-氨甲基吡咯烷及其制备方法:CN,1380286 A[P].2002-11-20.
[13]Lannoye G S,Moerlein S M,Parkinson D,et al.N-fluoroalkylatedandN-alkylatedanaloguesofthe dopaminergic D-2 receptor antagonist raclopride[J].J. Med.Chem.,1990,33(9):2430-2437.
[14]任来阳,冯文化.S-1-乙基-2-氨甲基吡咯烷合成新方法[J].化学试剂,2010,32(10):928-929.
[15]梁江辉,张明杰.(S)-1-乙基-2-氨甲基吡咯烷的合成[J].化学与生物工程,2012,29(12):54-55.
[16]Kanth J V B,Periasamy M.Selective reduction of carboxylic acids into alcohols using sodium borohydride and iodine[J].J.Org.Chem.,1991,56(20):5964-5965.
[17]McKennon M J,Meyers A I,Drauz K,et al.A convenient reduction of amino acids and their derivatives[J].J.Org. Chem.,1993,58(13):3568-3571.
The Synthesis Development of(S)-(1-Ethylpyrrolidin-2-yl)methanamine
ZHANG Quan,HOU Jun-bo,CHEN Zhi-wei
(College of Pharmaceutical Sciences,Zhejiang University of Technology,Hangzhou,Zhejiang 310014,China)
(S)-(1-ethylpyrrolidin-2-yl)methanamine is an important synthetic intermediate of Levosulpiride and Sultopride,so that it has a broad market prospects.This article summarizes some representative synthetic methods of(S)-(1-ethylpyrrolidin-2-yl)methanamine and reviewes the advantages and disadvantages of these methods.
(S)-(1-ethylpyrrolidin-2-yl)methanamine;chemical synthesis;sulpiride;chirality
1006-4184(2016)12-0017-04
2016-04-26
张权(1999-),男,本科生。研究方向:药物中间体合成。
*通讯作者:陈志卫,E-mail:chenzhiwei@zjut.edu.cn。
