高效液相色谱法同时测定小儿咳喘灵口服液中绿原酸与甘草苷的含量
2017-01-06张婷
张婷
(淮北市食品药品检验中心,安徽 淮北 235000)
高效液相色谱法同时测定小儿咳喘灵口服液中绿原酸与甘草苷的含量
张婷
(淮北市食品药品检验中心,安徽 淮北 235000)
目的 建立采用高效液相色谱法(HPLC)同时测定小儿咳喘灵口服液中绿原酸与甘草苷含量的方法。方法 采用Agilent Eclipse Plus C18(150 mm×4.6 mm,5 μm)色谱柱;流动相为乙腈-0.1%磷酸溶液,梯度洗脱,流速为1.0 mL·min-1;波长切换检测,检测波长为327 nm(0~16 min,测定绿原酸)和217 nm(16~64 min,测定甘草苷);进样量为10 μL;柱温为30℃。结果 绿原酸在0.081 3~0.812 8 μg范围内呈良好的线性关系(r=0.999 8),平均加样回收率为97.5%(n=9),RSD=2.8%;甘草苷在0.038 6~0.386 1 μg范围内呈良好的线性关系(r=0.999 8),平均加样回收率为103.6%(n=9),RSD=1.9%。结论 该方法操作简便、灵敏度高、重现性好,适用于小儿咳喘灵口服液中绿原酸与甘草苷的含量测定。
小儿咳喘灵口服液;高效液相色谱法;绿原酸;甘草苷
小儿咳喘灵口服液收载于中华人民共和国卫生部药品标准中药成方制剂第四册,由麻黄、金银花、苦杏仁、板蓝根、石膏、甘草、瓜蒌等七味中药制备而成,具有宣肺清热,止咳、祛痰、平喘的功效,用于治疗上呼吸道感染,气管炎、肺炎、咳嗽等症[1]。金银花和甘草是该制剂中的重要成分,金银花性寒,味甘,具有清热解毒的功效,甘草性平,味甘,具有和中缓急、化痰止咳平喘的功效[2-3]。鉴于绿原酸和甘草苷分别是金银花和甘草的主要有效成分,本文采用高效液相色谱法同时测定该制剂中绿原酸和甘草苷的含量,该方法操作简便、灵敏度高、重现性好,适用于小儿咳喘灵口服液的质量控制。
1 仪器与试药
1.1 仪器 Agilent1200液相色谱仪:G1310A四元泵、G1316A柱温箱、G1315D二极管阵列检测器(美国Agilent科技有限公司),SY-800超声提取器(上海宁商超声仪器有限公司),XS105电子分析天平(0.01 mg,METTLER TOLEDO)。
1.2 试药 绿原酸(批号:110753-201314,来源:中国食品药品检定研究院,供含量测定用,含量以96.6%计,使用前无需干燥处理);甘草苷(批号:111610-201106,来源:中国食品药品检定研究院,供含量测定用,含量以93.7%计,使用前无需干燥处理);小儿咳喘灵口服液(安徽辉克药业有限责任公司,批号:14052001、14060101、14101001);乙腈为色谱纯;甲醇、磷酸为分析纯;水为重蒸馏水。
2 方法与结果
2.1 色谱条件 Agilent Eclipse Plus C18(150 mm×4.6 mm,5 μm)色谱柱,柱温为30 ℃;流动相:以乙腈为流动相A,以0.1%磷酸溶液为流动相B,按表1梯度洗脱条件进行梯度洗脱;流速为1.0 mL·min-1;检测波长:0~16 min为327 nm(测定绿原酸),16~64 min为217 nm(测定甘草苷);进样量为10 μL。

表1 流动相梯度洗脱条件
2.2 溶液的制备
2.2.1 混合对照品储备液的制备 分别精密称取绿原酸对照品10.52 mg、甘草苷对照品5.15 mg,置100 mL量瓶中,加甲醇使溶解并稀释至刻度,摇匀,作为混合对照品储备液。
2.2.2 供试品溶液的制备 精密量取本品5 mL置25 mL量瓶中,加入甲醇10 mL,超声处理30 min,放冷至室温,加甲醇定容至刻度,摇匀,滤过,取续滤液,作为供试品溶液。
2.2.3 阴性样品溶液的制备 按小儿咳喘灵口服液处方比例及制备工艺分别制备不含金银花、甘草的阴性样品,按供试品溶液制备方法制成阴性对照溶液。
2.3 专属性考察 分别取混合对照品溶液、供试品溶液、缺金银花阴性样品溶液、缺绿原酸阴性样品溶液,按照“2.1”项色谱条件进样测定,色谱图见图1。结果阴性样品色谱图在与绿原酸、甘草苷对照品色谱峰相同保留时间处未见明显色谱峰,表明该方法专属性良好。
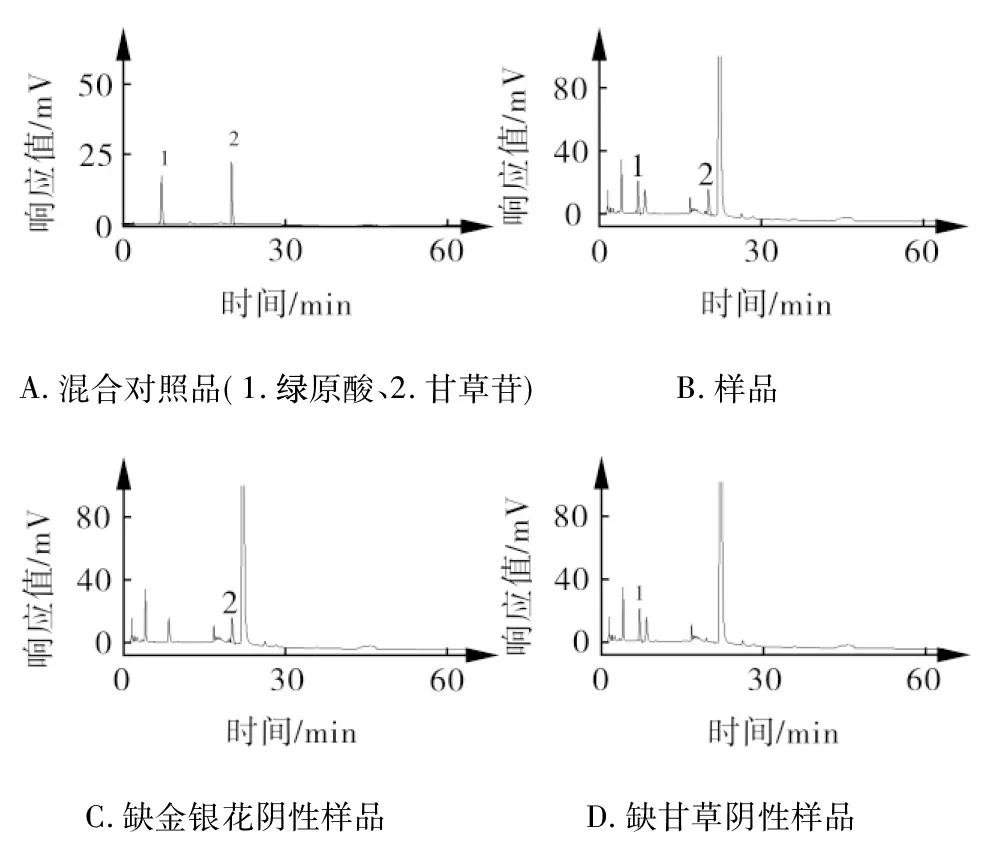
图1 HPLC图
2.4 线性关系考察 分别精密吸取混合对照品储备液0.8、1.0、2.0、4.0、6.0、8.0 mL,置10 mL量瓶中,加甲醇稀释并定容至刻度,摇匀,制成系列浓度混合对照品溶液。分别精密吸取10 μL进样测定,记录峰面积,以进样量(μg)为横坐标,峰面积为纵坐标,进行线性回归。回归方程:绿原酸为Y=1 628.828 7X-12.213 8(r=0.999 8),甘草苷为Y=3 188.569 9X-5.652 4(r=0.999 8),结果表明绿原酸和甘草苷分别在0.081 3~0.812 8、0.038 6~0.386 1 μg范围内具有良好的线性关系。
2.5 精密度试验 精密吸取同一混合对照品溶液,在“2.1”项色谱条件下重复进样6次,记录峰面积。结果绿原酸对照品峰面积的RSD为1.3%,甘草苷对照品峰面积的RSD为0.84%,表明精密度良好。
2.6 重复性试验 取同一批次样品(批号为14052001)按“2.2.2”项方法制成供试品溶液6份,在“2.1”项色谱条件下测定含量。结果样品中绿原酸的平均含量为0.100 g·L-1,RSD=0.43%;甘草苷的平均含量为0.047 g·L-1,RSD=0.50%;表明本法重复性良好。
2.7 稳定性试验 取同一供试品溶液(批号为14052001),在“2.1”项色谱条件下,分别于配置后0、2、4、8、12、24 h进样测定,记录峰面积。结果绿原酸峰面积的RSD为0.19%,甘草苷峰面积的RSD为0.72%,表明供试品溶液在24 h内稳定性良好。
2.8 加样回收率试验 分别精密量取已知含量的样品(批号为14052001)2.5 mL,共9份,每3份1组,每组一个质量浓度。分别精密加入“2.2.1”项下的混合对照品储备液1.2、2.5、5 mL,按供试品溶液制备方法制备,在“2.1”项色谱条件下测定,绿原酸和甘草苷的平均回收率分别为97.5%和103.6%,RSD分别为2.8%和1.9%,结果见表2、表3,表明本方法结果准确可靠。
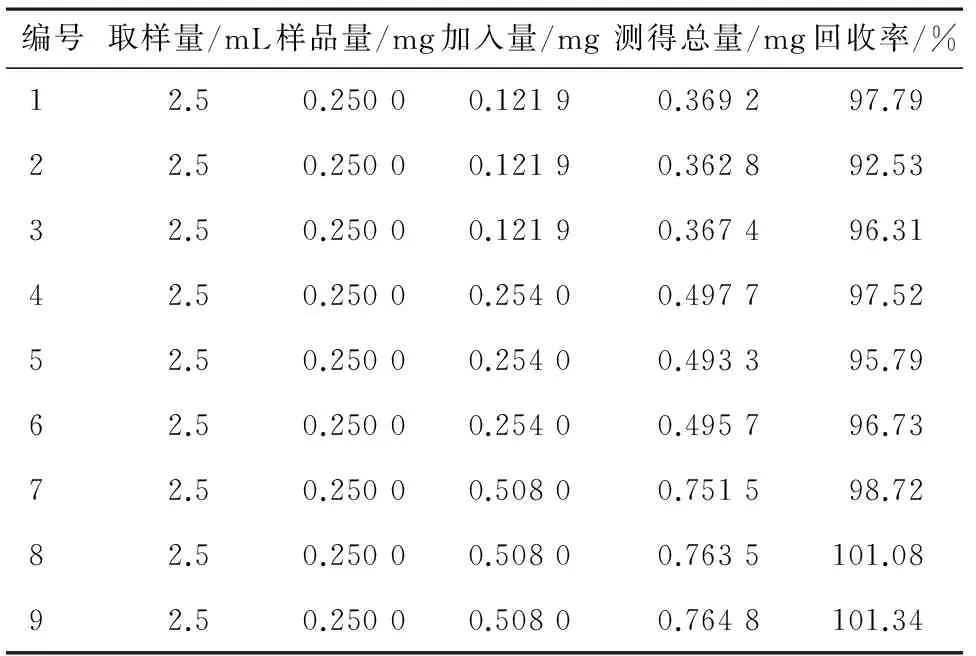
表2 绿原酸加样回收率
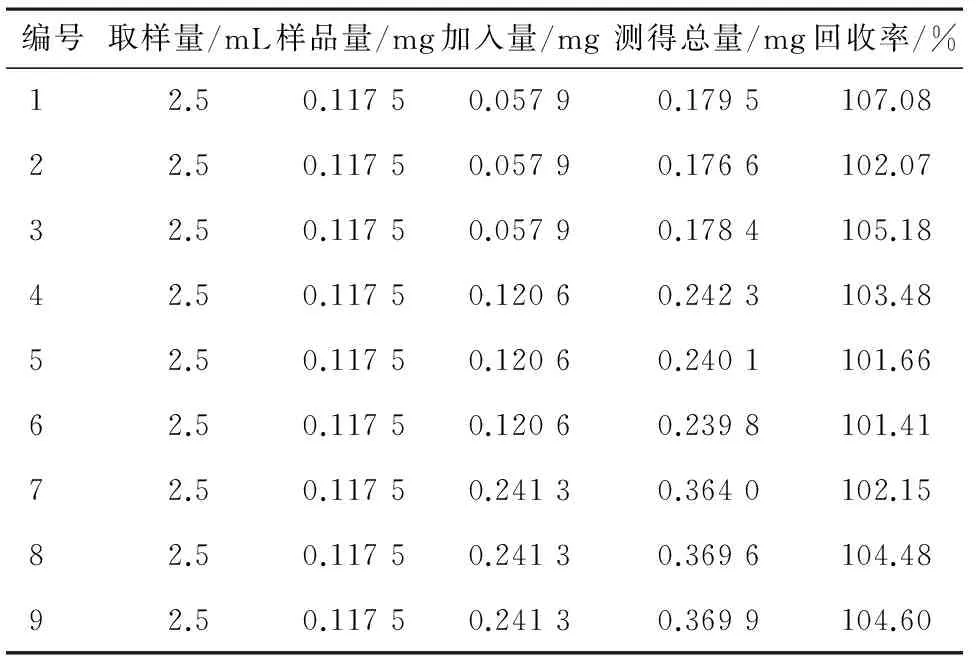
表3 甘草苷加样回收率
2.9 样品含量测定 取3批样品(批号分别为14052001、14060101、14101001),每批2份,按供试品溶液制备方法制备,在“2.1”项色谱条件下进样测定,计算3批样品中绿原酸和甘草苷的含量,结果见表4。
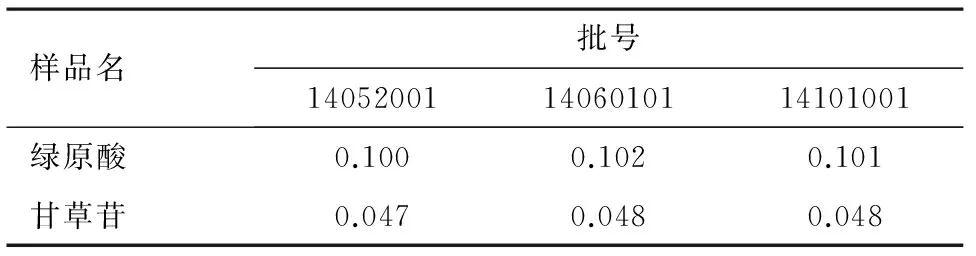
表4 绿原酸和甘草苷样品测定结果/g·L-1
3 讨论
小儿咳喘灵口服液收载于中华人民共和国卫生部药品标准中药成方制剂第四册,现行标准比较简单,仅有性状、鉴别、检查项,无含量测定项。有文献报道采用高效液相色谱法测定该制剂中盐酸麻黄碱、盐酸伪麻黄碱、绿原酸等成分的含量[4-5],但无同时测定绿原酸和甘草苷含量的相关报道。本文采用高效液相色谱法,利用二极管阵列检测器波长转换方式同时测定绿原酸和甘草苷的含量,该方法操作简便、准确、稳定,达到一测多评的效果,为该制剂中绿原酸和甘草苷的质量控制及制定新的检验方法提供可靠依据。
根据有关文献报道[6-8],绿原酸在327 nm处有最大吸收,甘草苷在217 nm处有较大吸收,经试验,0~16 min检测波长设为327 nm以测定供试品溶液中绿原酸的含量,16~64 min检测波长设为217 nm以测定供试品溶液中甘草苷的含量,结果稳定,无杂质峰干扰。
供试品溶液的制备,参考相关文献[9-11],比较了以70%甲醇、甲醇为不同的提取溶剂进行超声和加热回流提取。结果以70%甲醇提取的供试品溶液杂质干扰较多,且超声与加热回流提取无明显差别,故本实验选用甲醇为提取溶剂,进行超声提取,提取完全,杂质干扰较少。试验中曾取同一批样品,比较了分别超声提取15、30、45 min对测定结果的影响,结果超声提取30 min后测定结果不再增加,故确定超声提取时间为30 min。
小儿咳喘灵口服液是由多种药味制备而成的复方制剂,按照供试品溶液制备方法制备的样品溶液中除含有绿原酸和甘草苷外,尚含有其他多种化学成分,采用等度洗脱的方式待测组分无法与杂质峰有效分离。参照有关文献[12-15],经试验,采用乙腈-0.1%磷酸溶液为流动相梯度洗脱,供试品溶液中绿原酸和甘草苷与相邻组分分离完全,且出峰时间适宜,阴性溶液无干扰。
[1] 中华人民共和国卫生部药品标准.中药成方制剂[S].第4册.北京:中国医药科技出版社,1991:20.
[2] 陈继明,洪超群.金银花药理作用分析[J].亚太传统医药,2015,11(5):43-44.
[3] 张利.甘草的药理作用及现代研究进展[J].中医临床研究,2014,6(10):147-148.
[4] 毕福均,林彤.HPLC法测定小儿咳喘灵口服液中盐酸麻黄碱和盐酸伪麻黄碱含量[J].中药新药与临床药理,2014,25(4):490-493.
[5] 刘杰,孙娇,秦莉,等.复配絮凝剂用于小儿咳喘灵原药水提液絮凝效果研究[J].中草药,2013,44(16):2246-2251.
[6] 郑娟,茅纯.HPLC波长转换法同时测定小儿咳喘灵颗粒中(R,S)-告依春、绿原酸和甘草苷的含量[J].中国现代应用药学,2015,32(6):727-731.
[7] 陈建琴.川贝清肺糖浆中苦杏仁苷、甘草苷和甘草酸的双波长UPLC法测定[J].中国医药工业杂志,2015,46(8):889-891.
[8] 俞永梅,牟娜,张平.HPLC-DAD法同时测定小儿肺热咳喘口服液中9个成分[J].中成药,2013,35(4):709-713.
[9] 郝乘仪,郭淑英,冯波,等.RP-HPLC法同时测定芎菊上清丸中绿原酸、盐酸小檗碱和黄芩苷的含量[J].药物分析杂志,2014,34(1):193-197.
[10] 张宏梅,崔佰吉,姚鑫,等.HPLC同时测定茵山莲颗粒中5个有效成分的含量[J].中国实验方剂学杂志,2015,21(24):57-60.
[11] 王丽萍,曹英杰,段晓颖.HPLC同步测定润肠通丸中9种成分的含量[J].中国实验方剂学杂志,2015,21(23):50-54.
[12] 姜丽,李惠兰,张启云,等.HPLC法同时测定麻杏石甘汤中5种成分的含量[J].中华中医药杂志,2015,30(2):537-540.
[13] 李莉,孙夏荣.RP-HPLC法测定杜仲颗粒中绿原酸的含量[J].中国医药指南,2013,11(26):341-344.
[14] 张慧,闫磊,林龙飞,等.HPLC法测定小柴胡颗粒中7种指标成分[J].现代药物与临床,2014,29(2):162-165.
[15] 谢清萍,彭文明,刘萍绿.RP-HPLC法同时测定小儿咽扁颗粒中5个成分的含量[J].药物分析杂志,2015,35(12):2163-2167.
Determination of chlorogenic acid and liquiritin in xiao’er kechuanling oral liquid by HPLC
ZHANG Ting
(HuaibeiFoodandDrugInspectionCenter,Huaibei,Anhui235000,China)
Objective To develop an HPLC method for the determination of chlorogenic acid and liquiritin in xiao’er kechuanling oral liquid.Methods The samples were analyzed by Agilent Eclipse Plus C18(150 mm×4.6 mm,5 μm)with acetonitrile-0.1% phosphoric acid as mobile phase in gradient elution at the flow rate of 1.0 mL·min-1.The detection wavelength was set at 327 nm for the determination of chlorogenic acid(0~16 min)and 217nm for the determination of liquiritin(16~64 min).The injection volume was 10 μL and the column temperature was 30 ℃.Results The linear range of chlorogenic acid was within 0.081 3~0.812 8 μg(r=0.999 8)with an average recovery of 97.5%(n=9,RSD=2.8%).The linear range of liquiritin was within 0.038 6~0.386 1 μg(r=0.999 8)with an average recovery of 103.6%(n=9,RSD=1.9%).Conclusion The method is convenient,highly sensitive and reproducible for the quantitative analysis of xiao’er kechuanling oral liquid.
Xiao’er kechuanling oral liquid;HPLC;Chlorogenic acid;Liquiritin
10.3969/j.issn.1009-6469.2016.11.013
2016-06-28,
2016-09-10)
