离子色谱法与滴定法测定甜菜碱含量的不确定度评估
2017-01-05索德成肖志明
■索德成 肖志明 田 静
(中国农业科学院农业质量标准与检测技术研究所,北京 100081)
甜菜碱(betaine)是一种天然的类维生素物质,19世纪发现于欧洲,存在于动植物和微生物体内。其功效直到20世纪70年代才渐被认可。近年来,在畜禽生产和水产养殖中进行了大量的研究:甜菜碱作为高效甲基供体,可以部分替代蛋氨酸;甜菜碱具有抗脂肪肝功能,增强脂肪代谢,改善肉质,提高瘦肉率;对水生物摄饵有特殊的刺激和促进作用,可以提高采食率,降低饵料系数,是畜禽水产动物的新型饲料生长促进剂[1-2]。因此,准确检测甜菜碱的实际含量,对保障产品质量意义重大。目前饲料添加剂甜菜碱含量的检测方法主要有雷氏盐法、非水滴定法、离子色谱法等[3-4]。目前的农业行业标准NY 399—2000使用非水滴定法检测甜菜碱盐酸盐,但是无法对一些掺假物质进行鉴别。为此,国家标准GB∕T 23710—2009制定了用离子色谱法检测甜菜碱的方法。在实际工作中,发现两种检测方法对产品检测结果具有一定差异,因此需要了解两种方法误差产生的原因。
测量不确定度是指表征合理地赋予被测量之值的分散性,与测量结果相联系的参数测量。测量不确定度分析已经作为国际认可的实验结果评价指标,已代替传统的测量误差理论,用以衡量测量结果的可靠性实验[5-6]。随着人们对检测结果的可靠性要求不断提高,对测量不确定度的评价日益关注和重视。为此我们参考JJF 1059、CNAS-GL06和文献报道[5-14],对两种检测方法的不确定度进行了评定,基本阐明了两种方法误差产生主要来源。
1 仪器与方法
1.1 仪器及试剂
戴安2500型离子色谱仪,1、5、10、25 ml A级刻度吸管;50、100 ml A级容量瓶,50 ml酸性滴定管,超声波清洗器,电子天平(感量0.000 1 g)。甜菜碱纯度标准物质,定值于中国医学科学院药物研究所,标准编号为GBW09540,标准值为99.7%,相对不确定度为0.6%。邻苯二甲酸氢钾纯度标准物质定值于中国计量科学研究院,标准编号为GBW(E)060019k,标准值为99.97%,扩展不确定度为0.02%。其他试剂及相关化学品均为分析纯。
1.2 测试方法
1.2.1 滴定法测定
按NY 399—2000所提供的方法测定,试样预先在105℃烘箱干燥至恒重,称取干燥试样0.4 g(精确至0.000 1 g),加50 ml冰乙酸,加热至溶解,加25 ml乙酸汞溶液,冷却,加2滴结晶紫指示剂,用高氯酸标准液(0.1 mol∕l)滴定至溶液呈绿色,并将滴定结果用空白试验校正。高氯酸标准溶液按GB∕T 601—2002提供方法标定。称取105℃干燥恒重的工作基准试剂邻苯二甲酸氢钾0.75 g(精确至0.000 1 g),置于干燥锥形瓶中,加50 ml冰乙酸,温热溶解。加3滴结晶紫指示液,用配制好的高氯酸溶液滴定至溶液由紫色变为蓝色(微带紫色)。
1.2.2 离子色谱法测定
按GB∕T 23710—2009所提供的方法测定。称取干燥试样0.1 g(精确至0.000 1 g),置于100 ml容量瓶中,加入大约80 ml水,混合后,超声提取30 min。静止10 min,用水定容。离心,过0.45 μm滤膜,上机测定。采用外标法测定。
2 讨论
2.1 滴定法的不确定评价
2.1.1 数学模型
甜菜碱盐酸盐的质量百分数计算∶
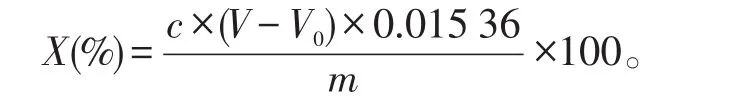
式中:X——试样中甜菜碱盐酸盐含量(%);
c——高氯酸标准滴定溶液的浓度(mol∕l);
V——滴定试样时消耗高氯酸标准液的体积(ml);
V0——滴定空白时消耗高氯酸标准液的体积(ml);
m——试样的质量(g);
0.015 36——与1.00 ml高氯酸标准滴定溶液[c(HC1O4)=0.1 mol∕l]相当的、以克表示的甜菜碱盐酸盐的质量。
高氯酸标准溶液标定的计算公式为:

式中:c——高氯酸标准滴定溶液的浓度(mol∕l);
m——邻苯二甲酸氢钾基准物质量(g);
P——邻苯二甲酸氢钾基准物的纯度(99.97%);
V——高氯酸标准滴定溶液的体积(ml);
M——邻苯二甲酸氢钾的摩尔质量(g∕mol)。
2.1.2 滴定法测量不确定度的来源分析
根据含量计算公式,滴定法测定甜菜碱盐酸盐不确定度的来源主要有标定高氯酸标准溶液浓度c的不确定度、称量样品质量m的不确定度、用高氯酸标准溶液滴定样品所消耗体积V与空白体积V0的不确定度。其中标定高氯酸标准溶液的不确定度涉及因素较多,应单独讨论。由于实验室温度基本保持一致,并且温度的不确定度对实验结果影响较小,可以忽略不计,本次不确定度评估过程忽略温度的影响。
2.1.3 高氯酸标准滴定溶液标定过程及测量不确定度的评估
标准溶液标定过程的不确定度与基准试剂的称量m、纯度P、标定时消耗溶液的体积V、邻苯二甲酸氢钾的摩尔质量M等影响因素有关。以某次标定为例:称样0.706 1 g,标定体积为34.12 ml,代入公式可得:

2.1.3.1 基准试剂的称量不确定度
干燥器与天平称量器内均放置同质硅胶,视为相同湿度,称量时无吸潮。电子天平检定证书给出最大允差为0.000 1 g,按均匀分布,取包含因子k=,故称量的标准不确定度为0.000 1 g∕3=0.000 058 g;因为称量采用的是减量法,故称量的标准不确定度u(m)为:u(m)=×0.000 058=0.000 082 g。
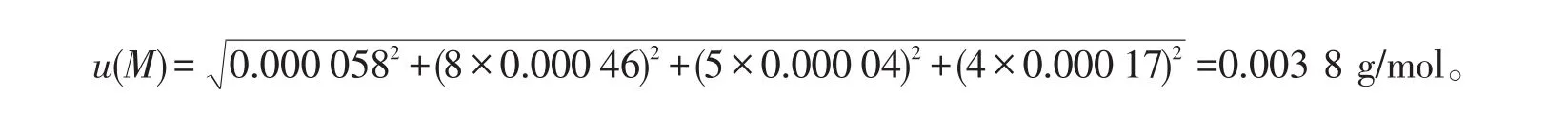
2.1.3.2 邻苯二甲酸氢钾基准物的摩尔质量(M)的不确定度
邻苯二甲酸氢钾(KHP)的分子式为C8H5O4K。该分子的摩尔质量的不确定度可以通过合成各组成元素原子量的不确定度得到。计算公式为:
2.1.3.3 纯度P
采用基准邻苯二甲酸氢钾,其标准物质证书所给的纯度为99.97%,扩展不确定度(k=2)为0.02%,则其纯度的不确定度为:u(P)=0.02%∕2=0.01%=0.000 1。
2.1.3.4 滴定体积含量的不确定度
滴定过程借助于50 ml的酸式滴定管来完成,高氯酸标准溶液滴定的体积有三个同样的不确定度来源:滴定体积终点的判断、体积校准时的不确定度以及由实验室温度与酸式滴定管校准时温度不一致而带来的不确定度。
滴定使用50 ml酸式滴定管(A级),按照检定证书给出的最大允许误差为±0.05 ml,假定为三角形分布,取包含因子k=,则量具本身引入的标准不确定度为0.05∕6=0.020 4 ml;由于使用结晶紫指示剂肉眼判断终点,根据CNAS—GL06:2006所述,肉眼判断的标准不确定度大约为0.03 ml;则滴定管标定引入的标准不确定度为u(V)==0.036 3 ml。
2.1.3.5 标定标准溶液的合成不确定度评定
按下式计算合成不确定度:

2.1.4 用高氯酸标准滴定溶液测定样品中甜菜碱含量的测量不确定度的评估
2.1.4.1 称量样品质量引起的标准不确定度
如前所述,样品称量引起的不确定度主要是分析天平校准不确定度,称量的标准不确定度u(m)为:u(m)=0.000 082 g。
2.1.4.2 用高氯酸标准溶液滴定甜菜碱样品所消耗体积的不确定度
用高氯酸标准溶液滴定样品所消耗体积的不确定度,包括滴定样品引起的不确定度和滴定空白引起的不确定度。根据本实验的实际滴定情况,滴定空白时所消耗的高氯酸标准滴定溶液的体积几乎为零,因此可以认为滴定样品时所消耗的高氯酸标准滴定溶液的体积与滴定空白时所消耗的高氯酸标准滴定溶液的体积之差的不确定度(V-V0)与滴定样品引起的不确定度V相同。则滴定管的不确定度为u(V-V0)=0.036 3 ml。
2.1.4.3 高氯酸标准滴定溶液浓度引起的不确定度
高氯酸标准滴定溶液浓度如上文所述,其不确定度为 uc(c)=0.000 16 mol∕l。
2.1.4.4 滴定法测定甜菜碱盐酸盐样品的不确定度
以某次标定为例:称样0.401 6 g,标定体积为25.72 ml,代入公式可得:
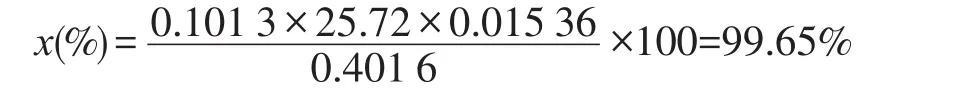

因最终计算是取重复测量的两个结果的算术平均值,根据JJF 1059-2012中合并样品的标准不确定度的规定:最终测量结果表示为0.157∕=0.11。
2.1.4.5 扩展不确定度
在有效自由度不确定的情况下,一般情况下扩展因子是k=-2,因此甜菜碱盐酸盐含量测定结果的扩展不确定度为:u(x)=uc(x)×2=0.22%,含量测定结果可表示为(99.65±0.22)%。
2.2 离子色谱法不确定度评价
2.2.1 数学模型
根据 GB∕T 23710—2009,离子色谱法检测甜菜碱盐酸盐含量,测定结果和有关参数有以下函数关系:

式中:c——由标准曲线查得的试样测试液中甜菜碱的浓度(mg∕ml);
V——定容体积(ml);
m——试样的质量(g)。
以某次测定为例:称样0.101 6 g,定容至100 ml,测定溶液中甜菜碱的浓度为0.750 9 mg∕ml,代入公式可得:
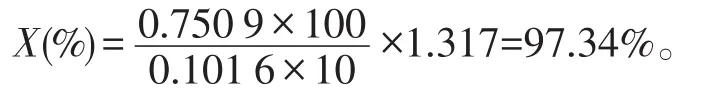
2.2.2 甜菜碱含量测量不确定度的来源分析
根据本项目检测方法及数学模型,影响甜菜碱含量检测的不确定度分量为3种:样品质量m不确定度、样品稀释体积V的不确定度、标准曲线查找浓度c的不确定度。其中标准曲线查找浓度c的不确定度与标准储备液配制过程、标准工作液的稀释、采用最小二乘法拟合标准工作曲线求得试样浓度有关。
2.2.3 测量不确定度评定
2.2.3.1 样品质量的不确定度
如上文所述称量的标准不确定度u(m)为:u(m)=0.000 082 g。
2.2.3.2 样品稀释引起的不确定度
在测量过程中,将称量好的样品溶液于100 ml容量瓶中,加水定容。100 ml容量瓶的允许误差分别为±0.2 ml、按三角分布计;稀释过程中引起的不确定度u(V)=0.2=0.081 6 ml。
2.2.3.3 标准储备液配制过程产生的不确定度(见表1)
标准储备液配制过程时产生的不确定度主要来自于标准物质固体称量、定容等过程,它的准确称量直接关系到稀释的各个浓度标准溶液的准确性。根据标准物质证书,甜菜碱纯度标准品的纯度为99.7%,相对不确定度为0.6%。在配制标准储备液过程中,标准品、天平称量与100 ml容量瓶定容所产生的不确定度分别为 u(P)∕P=0.006,u(m)∕m=0.000 818 g和u(V)∕V=0.000 816 ml。标准储备液浓度为:

2.2.3.4 稀释标准工作曲线时产生的不确定度u(V)
使用标准储备液稀释标准工作曲线进行了4次稀释,分别使用了1、5、25 ml的分度吸量管和50 ml的容量瓶。根据JJC 196要求,1、5、25 ml的分度吸量管和50 ml的容量瓶的最大允许误差分别为±0.10 ml、±0.025 ml、±0.008 ml和±0.05 ml,假定为三角形分布(1),取包含因子k=,分别得不确定度为0.040 8、0.010 2、0.003 26、0.020 4。

表1 标准储备液稀释标准工作曲线的不确定度的计算

2.2.3.5 采用最小二乘法拟合标准工作曲线求得试样浓度过程中引入的不确定度
使用手工绘制的校准曲线计算甜菜碱的量。用1 mg∕ml甜菜碱标准溶液中配制五个标准溶液,其浓度分别为0.01、0.05、0.1、0.5、1 mg∕ml。并对其峰面积进行测定,测定数据见表2。

表2 标准溶液与检测样品测定的峰面积及拟合曲线值
由表2得到的标准溶液的工作曲线方程:y=7.258 6x-0.017 5(r=0.999 8),取待测样品溶液,平行测定2次、由标准工作曲线求的平均浓度c0=0.750 9 mg∕ml,参照文献和JJC 2159,c0的相对标准不确定度:

2.2.3.6 离子色谱仪器自身的不确定度
因仪器所处状态不同、噪音水平不同,同一试样在离子色谱上的响应值存在一定的差异。离子色谱仪自身的不确定度因各自仪器的不同而有所差距。根据离子色谱检定证书的检定数据,检测所使用的离子色谱仪在k=2的情况下,离子色谱的扩展不确定度为1.5%,根据数据结果离子色谱仪器自身的不确定度为u(y)=0.75%=0.007 5。
2.2.4 合成不确定度
根据以上对各不确定度分量的评定结果,结合甜菜碱盐酸盐中甜菜碱盐酸盐含量的相对不确度数学模型,甜菜碱样品中甜菜碱含量测定结果的相对合成不确定度计算结果如下:
因最终计算是取重复测量的两个结果的算术平均值,根据JJF 1059—2012中合并样品的标准不确定度的规定:最终测量结果表示为2.07∕=1.46。
2.2.5 扩展不确定度
在有效自由度不确定的情况下,一般情况下扩展因子是k=2,因此离子色谱法含量测定结果的扩展不确定度u(x)=uc(x)×2=2.92%,含量测定结果可表示为(97.34±2.92)%。
3 总结
采用非水滴定法测定甜菜碱的含量,其测量不确定度来源于高氯酸标准溶液重复性的标定、滴定液消耗的体积和电子天平的不确定度。而影响其测量不确定度的最主要因素为标定高氯酸标准溶液浓度c的不确定度。因此,对高氯酸标准溶液标定是检测甜菜碱的关键控制点,在实验过程应加以重视,此外滴定液消耗的体积也是一个值得注意的控制点。
从计算结果可以看出,在离子色谱法测定甜菜碱含量的过程中,影响其测量不确定度的最主要因素为采用最小二乘法拟合标准工作曲线求得试样浓度过程中引入的不确定度、稀释标准工作曲线的时产生的不确定度、离子色谱仪器自身的不确定度。因此使用离子色谱法检测过程中,离子色谱自身状态和标准工作曲线配置是检测的关键控制点。
从两种方法的不确定度数据上来看:离子色谱法测定甜菜碱含量的不确定度为2.92%。远远高于非水滴定法测定甜菜碱含量的不确定度0.22%。虽然离子色谱法可准确鉴别的甜菜碱的真假,并准确的测定饲料及复合预混料中甜菜碱的测定。但是离子色谱法能够有效地测定甜菜碱的检测误差与非水滴定法高的多。因此,如果是对真正的饲料添加剂甜菜碱盐酸盐纯品,建议可以使用离子色谱法来鉴别甜菜碱的真假;如果测得含量大于90%,可以使用非水滴定法准确确定甜菜碱的含量。

