阿米福汀对苯并[a]芘诱导腹主动脉瘤形成的作用*
2017-01-03陶潞渊吴少泽王娇妮王国强薛杨静徐志强唐疾飞季亢挺
陶潞渊, 吴少泽, 王娇妮, 王国强, 薛杨静, 徐志强, 汪 洁, 唐疾飞, 季亢挺
(温州医科大学附属第二医院心血管内科,浙江 温州 325027)
阿米福汀对苯并[a]芘诱导腹主动脉瘤形成的作用*
陶潞渊, 吴少泽, 王娇妮, 王国强, 薛杨静, 徐志强, 汪 洁, 唐疾飞, 季亢挺△
(温州医科大学附属第二医院心血管内科,浙江 温州 325027)
目的: 研究阿米福汀对苯并[a]芘(BaP)诱导C57BL/6J小鼠腹主动脉瘤(AAA)形成的作用,并探讨相关机制。方法:体外培养RAW264.7单核巨噬细胞,分为正常对照组,溶剂对照组(即DMSO组),BaP组,低剂量(1 μmol/L)阿米福汀组,中剂量(5 μmol/L)阿米福汀组及高剂量(25 μmol/L)阿米福汀组,应用Western blot法检测体外培养的RAW264.7单核巨噬细胞基质金属蛋白酶(MMP)-9、MMP-12、TNF-α、NF-κB表达。48只C57BL/6J小鼠(8月龄,雄性)随机分为对照组、模型组(AngⅡ+BaP组)、低剂量(50 mg/kg)阿米福汀组、高剂量(100 mg/kg)阿米福汀组。6周后取腹主动脉察看标本形态;行HE、 Masson染色观察血管形态结构;测定腹主动脉的血管周长。Western blot、免疫组化法评价腹主动脉组织中的巨噬细胞浸润情况及MMP-9、MMP-12、TNF-α、NF-κB的表达。结果:Western blot发现 BaP刺激使巨噬细胞MMP-9、MMP-12、TNF-α、NF-κB的表达升高,而阿米福汀对此有显著抑制作用,且呈剂量依赖性(P<0.05)。动物实验可见对照组成瘤率为0,高剂量阿米福汀组成瘤率为16.67%,与模型组(58.33%)和低剂量阿米福汀组(33.33%)相比显著降低(P<0.05)。免疫组化结果显示高剂量阿米福汀组腹主动脉壁的巨噬细胞浸润程度及TNF-α、MMP-9、MMP-12、NF-κB的表达较模型组和低剂量阿米福汀组相比显著下降(P<0.05)。Western blot实验结果证实高剂量阿米福汀组腹主动脉壁TNF-α、MMP-9、MMP-12、NF-κB的表达较模型组和低剂量阿米福汀组相比显著下降(P<0.05)。结论:阿米福汀可以抑制BaP诱导的巨噬细胞的活化,同时可以抑制BaP诱导的小鼠腹主动脉瘤发生、发展,其机制可能跟抑制NF-κB途径、巨噬细胞浸润及MMPs、TNF-α的表达有关。
阿米福汀; 腹主动脉瘤; 苯并[a]芘; 巨噬细胞; 基质金属蛋白酶
腹主动脉瘤(abdominal aortic aneurysm,AAA)是各致病因素下,腹主动脉中层弹性纤维退化断裂,血管壁变薄,在长期血压压力冲击下局部向外扩张,形成的瘤体,其破裂后死亡率高达90%。目前针对AAA的治疗主要为手术和介入治疗,但费用高并发症多,因此对腹主动脉的药物治疗需求日益迫切。
AAA的主要病理特征是腹主动脉壁炎症反应、巨噬细胞浸润、弹性纤维及胶原蛋白的降解和血管平滑肌细胞的凋亡[1]。目前的观点认为是动脉壁上的炎症反应启动AAA的整个病理过程[2],而巨噬细胞在此过程中起关键作用[3],炎症发生后,随之而来的是弹性纤维和胶原蛋白的降解[4],主要原因是血管壁中基质金属蛋白酶(matrix metalloproteinases,MMPs)活性增加。
吸烟是腹主动脉瘤的高危因素[5]。吸烟者患AAA的风险比不吸烟者高8倍,戒烟后患AAA的风险降低4倍[6]。苯并[a]芘(benzo[a]pyrene,BaP)是香烟烟雾的重要组成部分[7]。研究表明,BaP可使正常血管发生病理改变[8],使巨噬细胞浸润增加、MMPs的表达升高、核因子-κB (nuclear factor-κB,NF-κB) 活化[9-10]。BaP诱导的病理学改变与AAA发展中的病理改变极其相似。我们的前期实验发现[11],在BaP协同血管紧张素II(angiotensin II,Ang II)作用下,C57BL/6J小鼠AAA的发生率显著高于单独AngII处理的小鼠。
阿米福汀(amifostine)是一种放化疗辅助用药,能够减轻放、化疗对正常组织的损伤,在碱性磷酸酶作用下,阿米福汀转化为WR-1065,能够抑制过氧化从而使得细胞氧化损伤减轻。 Chok等[12]在肾脏的缺血再灌注模型中发现阿米福汀可以通过清除氧自由基、抗炎、减少细胞凋亡来减轻再灌注损伤。我们的前期实验发现阿米福汀抑制BaP诱导的巨噬细胞的活化和炎症因子的表达。故设计此实验研究阿米福汀对腹主动脉瘤形成的作用及其相关机制,为腹主动脉瘤的药物治疗提供新的策略。
材 料 和 方 法
1 研究对象
1.1 实验细胞 RAW264.7细胞为小鼠白血病单核细胞,购自上海中科院细胞库。
1.2 实验动物 无特定病原体(specific pathogen free, SPF)级C57BL/6J雄性小鼠(购自于北京维通利华实验动物技术有限公司),8月龄,体重28~32 g。放置于温州医科大学附属第二医院科研中心SPF级动物房中饲料喂养。饮用无菌纯净水,无菌饲料喂养,自由饮食。昼夜变化规律,室内恒温、恒湿。
2 主要材料、药物和试剂
药物微量渗透泵(0.15 μL/h)购自Alzet;阿米福汀注射液购自大连美罗大药厂;DMEM培养液、胎牛血清(fetal bovine serum,FBS)、血管紧张素Ⅱ和苯并[a]芘均购自Sigma;中链甘油三酯购自GATTEFOSSE;抗MMP-12、MMP-9、CD68、肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)和NF-κB p65抗体购自Abcam;苏木素伊红染色(hematoxylin and eosin staining,HE staining)试剂盒和马松染色(Masson staining)试剂盒购自北京索莱宝科技有限公司。
3 主要方法
3.1 细胞实验 (1)细胞培养: RAW264.7细胞经复苏后培养于10% DMEM培养液中并在倒置显微镜下观察细胞生长情况。当细胞生长达培养瓶底面积的80%时,使用吸管吹下。待90%以上细胞脱落时,将细胞悬液转移至15 mL离心管中,1 000 r/min离心5 min,弃去上清液。吸取9 mL 10% DMEM完全培养液至上述含有细胞沉淀的离心管中,吹打成细胞悬液。分别吸取3 mL细胞悬液至预先装好1 mL 10% DMEM完全培养液的25 cm3的培养瓶中,轻轻摇晃混匀。将培养瓶重新置于饱和湿度培养箱中孵育。(2)实验分组:正常对照(control)组不做任何处理;溶剂对照组(即DMSO组)的DMSO终浓度为0.01%;BaP组的BaP终浓度为20 μmol/L,BaP先溶于DMSO;低(1 μmol/L)、中(5 μmol/L)、高(25 μmol/L)剂量阿米福汀组:先分别将1 、5、25 μmol/L的阿米福汀作用细胞2 h后,再用20 μmol/L的BaP作用细胞24 h。(3)取材:将各组RAW264.7巨噬细胞培养24 h后提取总蛋白,各组实验重复5次。
3.2 动物实验分组和模型建立 C57BL/6J小鼠共分为对照(control)组、模型组(即Ang II+BaP组)、低剂量阿米福汀组、高剂量阿米福汀组,每组12只。对照组的动物接受腹腔注射中链甘油三酯5 mL/kg,每周1次,给药6周。Ang II+BaP组:戊巴比妥钠(2%,40 mg/kg)腹腔注射麻醉,在背部切一长约1 cm的切口,将灌注Ang II溶液的ALZET泵通过切口埋入皮下(Ang Ⅱ溶于生理盐水,每只泵注入168 μL的Ang II溶液,微量缓释泵持续释放Ang II 0.9 mg·kg-1·d-1,释放速度为0.15 μL/h,持续6周,植入前,先将药物缓释泵放置于37 ℃水浴箱中12 h,腹腔注射BaP(10 mg/kg),将BaP溶解于中链甘油三酯中,制成浓度为2 g/L的溶液,以5 mL/kg腹腔注射,每周1次,共给药6周。低剂量阿米福汀组:植入Ang II微量渗透泵,腹腔注射阿米福汀注射液(50 mg/kg),30 min后腹腔注射BaP,每周1次。高剂量阿米福汀组:植入Ang II微量渗透泵,腹腔注射阿米福汀注射液(100 mg/kg),30 min后腹腔注射BaP,每周1次。
3.3 腹主动脉标本制备 各组小鼠处理6周后,用戊巴比妥钠(80 mg/kg)腹腔注射麻醉致死,取腹主动脉,部分存于液氮中行Western blot检测,部分存于4%多聚甲醛中行HE染色、Masson染色和免疫组化检测。
3.4 组织包埋、切片 取小鼠腹主动脉标本,常规二甲苯透明、浸蜡、脱水、包埋,以4 μm为厚度切片。
3.5 HE染色 常规烤片、脱蜡。染色:苏木素染色液滴于玻片组织上2 min,自来水冲洗,PBS溶液浸泡5 s返蓝,清水冲洗,伊红染色液滴于玻片组织上5 min,清水冲洗。再脱水、透明、封片、镜下观察。
3.6 Masson染色 常规烤片、脱蜡、染色(具体步骤按照试剂盒说明书进行);再脱水、透明、封片、镜下观察。
3.7 免疫组织化学染色 常规烤片、脱蜡、水合。用MMP-12、MMP-9、CD68、TNF-α和NF-κB p65各抗体行免疫组化染色,采用SP法,具体操作步骤按照试剂盒说明书进行。
3.8 Western blot测定目的蛋白 检测各组TNF-α、NF-κB、MMP-9、MMP-12和GAPDH蛋白的表达情况。上样总蛋白量为40 μg, 室温下SDS-PAGE分离蛋白,湿转法转目的蛋白到PVDF膜上,常规洗膜封闭,分别孵育Ⅰ抗(TNF-α抗体1∶1 000稀释,NF-κB抗体1∶1 000稀释,MMP-9抗体1∶1 000稀释,MMP-12抗体1∶1 000稀释,GAPDH抗体1∶10 000稀释)和Ⅱ抗(1∶10 000),然后化学发光,Bio-Rad凝胶成像仪曝光。图像处理软件 AlphaEaseFC对Western blot图像进行分析。
3.9 动脉瘤形成的判定 首先肉眼判定瘤体形成情况,再取染色切片,在显微镜下,每张切片均以相同的设置拍照。观察血管切片染色情况(细胞核呈蓝色,细胞质呈粉红色,弹力蛋白纤维呈亮粉红色)。在每只小鼠腹主动脉取不同位置的12张切片,运用ImageJ图像分析软件检测每张切片腹主动脉周长,继而算出各组小鼠腹主动脉的平均周长;只要小鼠的腹主动脉的最大周长大于对照组小鼠平均周长的50%,就可以认为此只小鼠腹主动脉瘤形成。
4 统计学处理
所有统计资料采用SPSS 21.0软件处理。经处理后得到实验数据均以均数±标准差(mean±SD)描述。使用单因素方差分析、SNK-q法检验各组资料。实验中成瘤率的比较采用卡方检验。以P<0.05为差异有统计学意义。
结 果
1 阿米福汀抑制BaP诱导的巨噬细胞TNF-α、MMP-9、MMP-12和NF-κB的表达
各实验组单核巨噬细胞Western blot检测结果显示,BaP组TNF-α、MMP-9、MMP-12和NF-κB的表达较正常对照组显著升高(P<0.05);阿米福汀组上述蛋白表达受到显著抑制;高剂量阿米福汀组巨噬细胞TNF-α、MMP-9、MMP-12和NF-κB的表达较BaP组、低剂量阿米福汀组和中剂量阿米福汀组有显著的下降(P<0.05),见图1。
2 阿米福汀抑制BaP诱导的小鼠腹主动脉瘤形成
各组小鼠处理6周后解剖,分离腹主动脉观察形态,见模型组腹主动脉局部有瘤样突出,视为肉眼瘤体形成。行HE染色,运用ImageJ图像分析软件检测各组小鼠的腹主动脉平均周长,腹主动脉瘤形成标准为血管最大周长大于对照组动脉平均周长的50%。对照组的腹主动脉平均周长为(954±103)μm,各实验组小鼠腹主动脉的最大周长只要大于1 431 μm,即可视为动脉瘤的形成。结果显示模型组的AAA形成率为58.33%,动脉平均血管周长为(1 401±230)μm;低剂量阿米福汀组的AAA形成率为33.33%,平均血管周长为(1 322±211)μm;高剂量阿米福汀组的AAA形成率为16.67%,腹主动脉平均血管周长为(1 023±102)μm。高剂量阿米福汀组的AAA形成率与模型组和低剂量阿米福汀组相比显著降低(P<0.05),见图2。

Figure 1.Amifostine attenuated BaP-induced expression of TNF-α, MMP-9, MMP-12 and NF-κB in the RAW246.7 macrophages. Mean±SD.n=5.*P<0.05vscontrol group;#P<0.05vsBaP group;$P<0.05vsamifostine (1 μmol/L) group;&P<0.05vsamifostine (5 μmol/L) group.
图1 阿米福汀抑制BaP诱导的巨噬细胞TNF-α、MMP-9、MMP-12和NF-κB 表达
3 腹主动脉组织学的改变
HE染色和Masson染色切片可见模型组腹主动脉壁中膜弹力纤维有显著降解、断裂;胶原蛋白溶解、丢失,血管中膜弹力层断裂,血管正常结构破坏,符合典型的动脉瘤组织病理学特征,高剂量阿米福汀组血管结构破坏程度较模型组、低剂量阿米福汀组有显著改善,见图3。
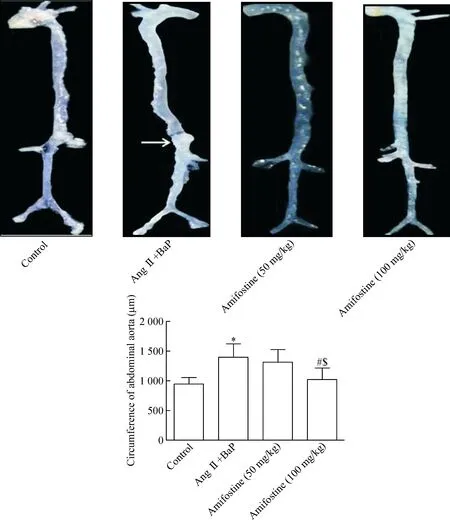
Figure 2.Amifostine reduced BaP-induced abdominal aortic circumference in mice. Mean±SD.n=12.*P<0.05vscontrol group;#P<0.05vsAng Ⅱ+BaP group;$P<0.05vsamifostine (50 mg/kg) group.
图2 阿米福汀降低BaP刺激小鼠的腹主动脉周长

Figure 3.Amifostine inhibited BaP-induced abdominal aortic damage in mice (×400).
图3 阿米福汀抑制BaP诱导的小鼠腹主动脉壁结构的破坏
4 阿米福汀减轻BaP诱导的腹主动脉血管壁巨噬细胞的浸润
运用羊抗鼠CD68抗体对各组血管切片进行免疫组化染色,观察血管壁巨噬细胞的浸润情况(图4)。与对照组相比,模型组腹主动脉血管壁巨噬细胞的浸润显著增加(P<0.05),阿米福汀呈剂量依赖性减轻BaP诱导的血管壁巨噬细胞的浸润程度(P<0.05),见图4、表1。

Figure 4.Amifostine inhibited BaP-induced abdominal aortic augment on CD68, TNF-α, MMP-9, MMP-12 and NF-κB expression in abdominal aorta wall of each group (×400).
图4 阿米福汀抑制BaP诱导的小鼠腹主动脉壁CD68、TNF-α、MMP-9、MMP-12和NF-κB的表达
5 阿米福汀抑制BaP诱导的血管壁NF-κB、TNF-α、MMP-9和MMP-12的表达
我们对小鼠腹主动脉切片进行NF-κB、MMP-9、MMP-12和TNF-α免疫组化染色(图4),同时对各组腹主动脉组织行Western blot检测。免疫组化染色可见,与对照组相比,模型组腹主动脉壁NF-κB、TNF-α、MMP-9和MMP-12的表达显著增加(P<0.05),而阿米福汀对腹主动脉壁NF-κB、TNF-α、MMP-9和MMP-12的表达有显著抑制作用,并呈剂量依赖性(P<0.05),见表1。Western blot检测结果与免疫组化结果一致,高剂量阿米福汀组腹主动脉壁NF-κB、TNF-α、MMP-9和MMP-12的表达较低剂量阿米福汀组和模型组均显著减少(P<0.05),见图5。
表1 各组小鼠腹主动脉壁MMPs、TNF-α和NF-κB表达的免疫组化结果
Table 1.The expression of MMPs, TNF-α and NF-κB in abdominal aorta of each group detected by immunohistochemisty (Mean±SD.n=12)
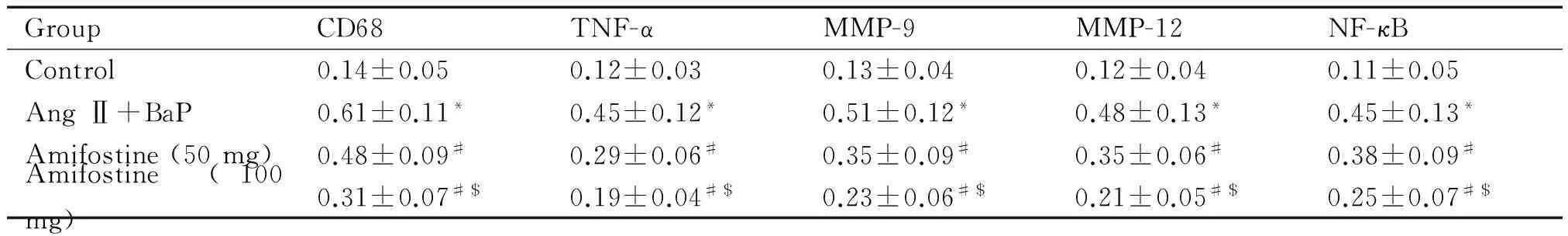
GroupCD68TNF-αMMP-9MMP-12NF-κBControl0.14±0.050.12±0.030.13±0.040.12±0.040.11±0.05AngⅡ+BaP0.61±0.11*0.45±0.12*0.51±0.12*0.48±0.13*0.45±0.13*Amifostine(50mg)0.48±0.09#0.29±0.06#0.35±0.09#0.35±0.06#0.38±0.09#Amifostine(100mg)0.31±0.07#$0.19±0.04#$0.23±0.06#$0.21±0.05#$0.25±0.07#$
*P<0.05vscontrol group;#P<0.05vsAng Ⅱ+BaP group;$P<0.05vsamifostine (50 mg/kg) group.

Figure 5.The results of Western blot showed that amifostine attenuated BaP-induced TNF-α, MMP-9, MMP-12 and NF-κB expression of mice abdominal aorta. Mean±SD.n=12.*P<0.05vscontrol group;#P<0.05vsAng Ⅱ+BaP group;$P<0.05vsamifostine (50 mg/kg) group.
图5 阿米福汀抑制BaP诱导的小鼠腹主动脉壁TNF-α、MMP-9、MMP-12和NF-κB 表达
讨 论
腹主动脉瘤目前有效的主流治疗方法包括外科手术治疗和血管介入治疗,两者的围术期并发症和手术死亡率均较高。在腹主动脉瘤瘤体较小的时候,早期应用药物抑制腹主动脉瘤体的增大可以避免手术和介入治疗,对于腹主动脉瘤患者有重要的临床意义。
腹主动脉瘤的早期病理特征为炎症反应[13-15],局部巨噬细胞浸润增加,弹性纤维降解断裂,弹力蛋白和胶原退变[16-19]等。主动脉壁上血管平滑肌细胞减少,腹主动脉壁炎症反应是腹主动脉瘤病理过程关键因素。大量的流行病学调查显示吸烟是腹主动脉瘤的高危因素,而BaP是吸烟烟雾中重要成分,炎症细胞尤其是巨噬细胞的活化在吸烟诱发AAA中起重要作用,我们前期实验[11]也发现BaP促进Ang Ⅱ诱导的AAA发展 。抑制炎症反应可显著抑制瘤体的生长速度,Lawrenece等[20]报道雷帕霉素可显著降低瘤体的直径。阿米福汀是一种细胞保护剂,广泛用于放化疗的辅助治疗,减轻正常组织细胞的损伤,相关研究[12]表明阿米福汀能够抑制炎症反应、清除氧自由基。在本次实验研究阿米福汀对BaP诱导的腹主动脉瘤的作用中显示:低剂量、高剂量阿米福汀组AAA的形成分别为33.33%、16.67%,都小于模型组AAA的形成率(58.33%),高剂量阿米福汀组AAA的形成率更低。各组小鼠HE、Masson染色示:高剂量阿米福汀组小鼠腹主动脉壁弹性纤维断裂,胶原蛋白的缺失情况较模型组和低剂量阿米福汀组显著改善。
本实验证实阿米福汀显著抑制BaP诱导巨噬细胞NF-κB和TNF-α细胞因子的表达。NF-κB和TNF-α细胞因子在AAA的血管壁的炎症反应中起重要作用,Ren等[21]在穿心莲内酯抑制AAA作用的实验中,发现穿心莲内酯能够抑制AAA的发生、发展,且伴随着TNF-α表达下调和NF-κB活化的抑制。核转录因子NF-κB与免疫应答,炎症反应,细胞增生、凋亡等多种病理生理过程密切相关,在许多疾病中发挥着着重要作用。血管壁细胞外基质弹性纤维和胶原蛋白退化降解的过程中,MMPs的激活和表达增加被认为是主要因素。在人类腹主动脉瘤标本中检测到MMP-1、MMP-2、MMP-9、MMP-12和 MMP-13的表达均增加[16-19]。有研究显示在AAA的病理过程中,NF-κB是巨噬细胞迁移和MMPs表达重要的调节介质。吡咯烷二巯基氨甲酸具有抑制NF-κB活力的作用,在其作用下,AAA发生率降低,表明NF-κB途径与AAA显著相关[13]。有研究设计用嵌合体诱导寡核苷酸来阻止NF-κB发挥作用,腹主动脉瘤的发展受到抑制,同时观察到巨噬细胞浸润减少和MMPs表达下降[22]。Chase等[23]通过体外培养人单核细胞源性巨噬细胞,以重组腺病毒介导相关基因表达,抑制NF-κB活性能使MMP-9及MMP-1的表达下降,这进一步说明NF-κB对巨噬细胞及MMPs的表达起着调控作用。在我们前期实验中[11],我们也观测到在腹主动脉瘤发生、发展的过程中,NF-κB活化的同时,巨噬细胞浸润及MMP表达均增加。相关研究表明对血管壁炎症反应的控制可减少MMP-2、MMP-9、MMP-12的表达并抑制AAA的发生、发展[24]。巨噬细胞可以分泌NF-κB、TNF-α,作为炎症反应的关键因子,两者可以相互作用,增加血管壁巨噬细胞浸润及血管壁MMP-9、MMP-12的表达,加强炎症反应,促进细胞外基质的退化降解,促进腹主动脉的形成。
在细胞实验中我们发现:应用阿米福汀预保护后可以显著减轻BaP刺激引起的巨噬细胞NF-κB、TNF-α、MMP-9、MMP-12的表达。同时在动物实验中我们发现相比于对照组,NF-κB的表达在模型组显著增加,同时伴随巨噬细胞浸润、MMP-9/-12及TNF-α表达增加,高剂量阿米福汀可显著逆转上述作用。由此,我们推测阿米福汀可能通过抑制NF-κB途径,从而抑制巨噬细胞浸润、MMP、TNF-α的表达,最终抑制腹主动脉瘤的发生。
本次实验中,我们证实阿米福汀可以抑制BaP诱导的巨噬细胞的活化,并且可以抑制BaP诱导的小鼠腹主动脉瘤发生发展,其机制可能跟抑制NF-κB途径、巨噬细胞浸润、MMPs及TNF-α的表达有关。
[1] Crawford CM, Hurtgen-Grace K, Talarico E, et al. Abdominal aortic aneurysm: an illustrated narrative review[J]. J Manipulative Physiol Ther, 2003, 26(3): 184-195.
[2] Paravastu SC, Murray D, Ghosh J, et al. Inflammatory abdominal aortic aneurysms (IAAA): past and present[J]. Vasc Endovasc Surg, 2009, 43(4): 360-363.
[3] Turner GH, Olzinski AR, Bernard RE, et al. Assessment of macrophage infiltration in a murine model of abdominal aortic aneurysm[J]. J Magn Reson Imaging, 2009, 30(2):455-460.
[4] Tsuruda T, Kato J, Hatakeyama K, et al. Adventitial mast cells contribute to pathogenesis in the progression of abdominal aortic aneurysm[J]. Circ Res, 2008, 102(11):1368-1377.
[5] Forsdahl SH, Singh K, Solberg S, et al. Risk factors for abdominal aortic aneurysms: a 7-year prospective study: the Tromso Study, 1994-2001[J]. Circulation, 2009, 119(16): 2202-2208.
[6] Sauerbeck LR, Hornung R, Moomaw CJ, et al. The effects of study participation in the Familial Intracranial Aneurysm Study on cigarette smoking[J]. J Stroke Cerebrovasc Dis, 2008, 17(6):370-372.
[7] Guo X, Luo L, Ma Y, et al. Sorption of polycyclic aromatic hydrocarbons on particulate organic matters[J]. J Hazardous Materials, 2010, 173(1-3):130-136.
[8] Curfs DM, Lutgens E, Gijbels MJ, et al. Chronic exposure to the carcinogenic compound benzo[a]pyrene induces larger and phenotypically different atherosclerotic plaques in ApoE-knockout mice[J]. Am J Pathol, 2004, 164(1): 101-108.
[9] Sharma A, Neekhra A, Gramajo AL, et al. Effects of Benzo(e)Pyrene, a toxic component of cigarette smoke, on human retinal pigment epithelial cellsinvitro[J]. Invest Ophthalmol Visual Sci, 2008, 49(11):5111-5117.
[10]Weng MW, Hsiao YM, Chen CJ, et al. Benzo[a]pyrene diol epoxide up-regulates COX-2 expression through NF-kappa B in rat astrocytes[J]. Toxicol Lett, 2004, 151(2):345-355.
[11]Ji K, Zhang Y, Jiang F, et al. Exploration of the mechanisms by which 3,4-benzopyrene promotes angiotensin II-induced abdominal aortic aneurysm formation in mice[J]. J Vasc Surg, 2014, 59(2):492-499.
[12]Chok MK, Conti M, Almolki A, et al. Renoprotective potency of amifostine in rat renal ischaemia-reperfusion[J]. Nephrol Dialysis Transplantation, 2010, 25(12): 3845-3851.
[13]Dalainas I, Nano G, Ranucci M, et al. Inflammatory abdominal aortic aneurysms. A 20-year experience[J]. J Cardiovasc Surg, 2007, 48(3):305-308.
[14]Forester ND, Cruickshank SM, Scott DJ, et al. Functional characterization of T cells in abdominal aortic aneurysms[J]. Immunol, 2005, 115(2):262-270.
[15]Lawrence DM, Singh RS, Franklin DP, et al. Rapamycin suppresses experimental aortic aneurysm growth[J]. J Vasc Surg, 2004, 40(2):334-338.
[16]Nishimura K, Ikebuchi M, Kanaoka Y, et al. Relationships between matrix metalloproteinases and tissue inhibitor of metalloproteinases in the wall of abdominal aortic aneurysms[J]. Int Angiol, 2003, 22(3):229-238.
[17]Daugherty A, Cassis LA. Mechanisms of abdominal aortic aneurysm formation[J]. Current atherosclerosis reports, 2002, 4(3): 222-227.
[18]Halloran BG, Baxter BT. Pathogenesis of aneurysms[J]. Semin Vasc Surg, 1995, 8(2):85-92.
[19]吴建秋, 景在平.基质金属蛋白酶及其抑制剂在腹主动脉瘤发病中的作用[J].中国病理生理杂志,2001, 17(6):580-583
[20]Lawrenece DM , Singh RS, Franklin DP, et al. Rapamycin suppresses experimental aortic aneurysm growth[J]. J Cardiovasc Surg, 2004, 40(2): 334-338.
[21]Ren J, Liu Z, Wang Q, et al. Andrographolide ameliorates abdominal aortic aneurysm progression by inhibiting inflammatory cell infiltration through downregulation of cytokine and integrin expression[J]. J Pharmacol Exp Ther, 2016, 356(1):137-147.
[22]Nakashima H, Aoki M, Miyake T, et al. Inhibition of experimental abdominal aortic aneurysm in the rat by use of decoy oligodeoxynucleotides suppressing activity of nuclear factor kappa B and ets transcription factors[J] .Circulation, 2004, 109(1): 132-138.
[23]Chase AJ, Bond M, Crook MF, et al. Role of nuclear factor-kappa B activation in metalloproteinase-1, -3, and -9 secretion by human macrophagesinvitroand rabbit foam cells producedinvivo[J]. Arteriosclerosis Thrombosis Vasc Biol, 2002, 22(5):765-771.
[24]Holmes DR, Petrinec D, Wester W, et al. Indomethacin prevents elastase-induced abdominal aortic aneurysms in the rat[J]. J Surg Res, 1996, 63(1):305-309.
(责任编辑: 陈妙玲, 余小慧)
Effects of amifostine on formation of abdominal aortic aneurysm in mice induced by benzo[a]pyrene
TAO Lu-yuan, WU Shao-ze, WANG Jiao-ni, WANG Guo-qiang, XUE Yang-jing, XU Zhi-qiang, WANG Jie, TANG Ji-fei, JI Kang-ting
(DepartmentofGardiology,TheSecondHospitalAffiliatedtoWenzhouMedicalUniversity,Wenzhou325027,China.E-mail:jikt@wzmc.edu.cn)
AIM: To study the role of amifostine on the formation of benzo[a]pyrene (BaP)-induced abdominal aortic aneurysm (AAA) in C57BL/6J mice and the underlying mechanism. METHODS: RAW246.7 mononuclear macrophageinvitrowere divided into control group, DMSO group, BaP group, low dose (1 μmol/L) amfostine treated group, middle dose (5 μmol/L) amfostine treated group and high dose (25μmol/L) amfostine treated group. The influence of BaP on the expression of matrix metalloproteinase (MMP)-9, MMP-12, TNF-α, NF-κB in the RAW246.7 mononuclear macrophagesinvitrowas determined by Western blot. Male C57BL/6J mice (8 months old) were divided into control group, model group (AngII+BaP group), low dose (50 mg/kg) amfostine treated group and high dose (100 mg/kg) amfostine treated group. After 6 weeks, the abdominal aorta were isolated. The aortic tissues were subjected to HE and Masson staining. The vascular wall structure, infiltration of macrophage, the expression of MMP-9, MMP-12, TNF-α, NF-κB were evaluated by Western blot and immunochemistry staining. RESULTS: Amifostine attenuated BaP-induced expression of TNF-α, MMP-9, MMP-12, NF-κB in the RAW246.7 mononuclear macrophages (P<0.05). The results of animal experiments showed that the incidence of AAA in high dose amifostine treated group were significantly lower than that in low dose amifostine treated group and model group (P<0.05). Immunohistochemistry staining observation showed that amifostine inhibited the aortic macrophage infiltration more obviously in high amifostine treated group compared with model group and low dose amifostine treated group (P<0.05). Compared with model group and low dose amifostine treated group, the MMP-9, MMP-12, TNF-α and NF-κB expression of abdominal aorta in high amifostine treated group was reduced significantly (P<0.05).CONCLUSION: Amifostine inhibits BaP-induced activation of macrophages, and also prevents the formation of abdominal aortic aneurysm in C57BL/6J mice induced by BaP by inhibition of the NF-κB pathway, macrophage infiltration and the expression of TNF-α and MMPs.
Amifostine; Abdominal aortic aneurysm; Benzo[a]pyrene; Macrophage; Matrix metalloproteinases
1000- 4718(2016)12- 2168- 09
2016- 06- 20
2016- 10- 21
国家自然科学基金资助项目(No. 81573185);浙江省科技厅项目(No. 2014C33163);温州科技局项目(No. Y20140678)
R363; R543.1+6
A
10.3969/j.issn.1000- 4718.2016.12.008
杂志网址: http://www.cjpp.net
△通讯作者 Tel: 0577-88002214; E-mail: jikt@wzmc.edu.cn
