重组人源性凝血因子Ⅶa治疗产后出血13例疗效分析
2016-12-25,,
, ,
(1.南华大学附属第二医院重症医学科,湖南衡阳,421001;2.衡阳市妇幼保健院重症医学科)
·临床经验·
重组人源性凝血因子Ⅶa治疗产后出血13例疗效分析
吴鹏1,2,桂培根1,黄菊芳2
(1.南华大学附属第二医院重症医学科,湖南衡阳,421001;2.衡阳市妇幼保健院重症医学科)
目的探讨重组人源性凝血因子Ⅶa(rFⅦa)对产后出血患者的治疗效果。方法对13例产后出血常规止血治疗效果欠佳的患者,在输血的同时,加以rFⅦa 90 μg/kg静脉滴注辅助治疗,视止血效果,最多再加rFⅦa两次,每次45 μg/kg,若止血效果仍欠佳,行外科手术治疗。结果13例产后出血常规止血治疗效果欠佳的患者,经rFⅦa治疗,有8例得到有效控制,有效率达61.54%(8/13),其凝血时间(PT)及凝血活酶时间(APTT)缩短,血红蛋白(Hb)、血小板数量(PLT)及纤维蛋白原(FIB)升高。结论rFⅦa可有效治疗常规止血治疗无效的产后出血。
产后出血; 凝血因子Ⅶa; 辅助治疗
产后出血是全世界孕产妇最重要的死亡原因之一,据统计,全世界每年约有12~14万妇女死于产后出血[1]。目前,治疗产后出血的常用方法有:输入新鲜冰冻血浆、常规止血药及手术治疗。近年来,有报道采用人重组凝血因子Ⅶa治疗产后出血,取得了令人满意的效果[2,3]。本研究对13例产后出血常规治疗难以控制的患者,采用rF Ⅶ a治疗,取得了较好的疗效,现报道如下。
1 资料与方法
1.1一般资料收集2014年9月至2015年9月,南华大学附属第二医院ICU产后出血患者13例,患者年龄20~37岁,其中初产妇3例,经产妇10例,早产1例,足月妊娠12例,阴道分娩6例,剖宫产7例。所有患者均为反复或持续出血量>1 000 mL。
1.2方法13例患者经传统止血治疗,如输入新鲜冰冻血浆、冷沉淀及常规止血药(血凝酶、止血敏、氨甲环酸等)无效,给予rFⅦa 90μg/kg治疗,若止血效果欠佳,加用1次rFⅦa 45μg/kg;如若出血仍然不能有效控制,再加用1次rFⅦa 45μg/kg;在上述治疗出血再得不到有效控制,行外科手术止血(动脉结扎、子宫切除等)治疗。
2 结 果
2.1治疗效果8例患者应用rFⅦa后有效控制了产后出血,其中5例患者应用rFⅦa首剂后产后出血即得到有效控制,2例应用rFⅦa第2次后控制了出血,1例应用rFⅦa第3次后出血停止;另外5例行子宫切除手术,其中2例在子宫切除手术前应用rFⅦa,3例在手术后应用rFⅦa。13例患者均康复出院,治疗后没有栓塞等副作用的出现。
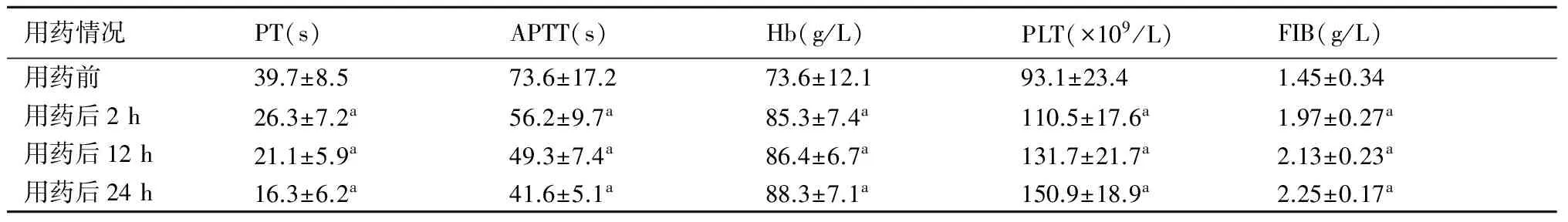
2.2血常规、凝血功能指标所有患者治疗后2小时凝血时间(PT)、部分凝血活酶时间(APTT)均明显降低,而血红蛋白(Hb)、血小板数量(PLT)、纤维蛋白原(FIB)则明显升高(P<0.05),且12小时、24小时无明显差别(表1)。
3 讨 论
rFⅦa含有激活的重组凝血因子VIIa,凝血因子VIIa能与组织因子结合,直接激活凝血因子X成为凝血因子Xa,激发凝血酶原向凝血酶的转换,进而使纤维蛋白原向纤维蛋白转换形成止血栓。凝血因子VIIa激活凝血因子IX,成为凝血因子IXa,凝血因子IXa和Xa使血栓的形成进一步增加。在血管壁损伤的局部,凝血因子VIIa与组织因子/磷脂形成复合物,处于激活状态,从而起到止血的作用,同时还可以促进血小板的黏附、聚集和血小板因子的释放,有利于凝血酶的形成[4]。
表1rFⅦa治疗前、后血常规、凝血功能指标比较(n=13)
用药情况PT(s)APTT(s)Hb(g/L)PLT(×109/L)FIB(g/L)用药前39.7±8.573.6±17.273.6±12.193.1±23.41.45±0.34用药后2h26.3±7.2a56.2±9.7a85.3±7.4a110.5±17.6a1.97±0.27a用药后12h21.1±5.9a49.3±7.4a86.4±6.7a131.7±21.7a2.13±0.23a用药后24h16.3±6.2a41.6±5.1a88.3±7.1a150.9±18.9a2.25±0.17a
9:40 2017-12-25与用药前比较,a:P<0.05
2001年Moscardo,等[5]首次报道了1例产后大出血的妇女,使用了 rFⅦa后成功地控制了产后出血。随后对于rFⅦa 用于治疗常规处理无效的难治性产科出血性疾病的报道逐渐增多,且大多都取得满意疗效。目前,陆续有不同国家或地区将rFⅦa 用于治疗难治性妇产科出血性疾病的数据发布,同时还发布了相关的初级应用指南[6]。北欧地区2000年~2004年的数据[7]显示,在531家医院中有65家使用rFⅦa,报道128例产后出血应用rFⅦa的患者,大部分(81%)只接受了90μg/kg甚至更少剂量的rFⅦa治疗,效果明显。另外,有研究报道[8]27例产后出血的患者接受了rFⅦa治疗,其中位剂量是91 μg/kg (75~103 μg/kg),大部分的患者出血减少或停止。日本在2005~2010年[9],有25例患者使用rFⅦa治疗产后出血,其中位治疗剂量为97.9 μg/kg (55.0~358.9 μg/kg),大部分(96%)患者出血减少或停止。Massimo等[4]统计了272例患者,发现rFⅦa 的平均用量为81.5 μg/kg可实现85%以上的患者出血减少或停止,推荐rFⅦa治疗流程:在常规治疗无效的情况下,给予首次90 μg/kg的rFⅦa,20分钟后如仍有出血,再次给予90 μg/kg的rFⅦa,如治疗无效,需行外科手术治疗。最近法国完成的一项多中心、随机、开放对照研究,84例对子宫收缩药物治疗无效的产后出血患者,其中42例患者早期给予1次rFⅦa治疗,另外42例患者给予常规治疗,发现常规治疗的患者93%需手术治疗,而rFⅦa治疗后仅有52%患者需手术治疗[10]。
但也有报道指出[11],当患者本身的纤维蛋白原浓度过低时,rFⅦa可能并不能发挥其止血的作用,主要是因为rFⅦa启动凝血过程,促进凝血酶的形成,需通过纤维蛋白原转化为纤维蛋白来完成。因此,使用rFⅦa前必须输注足够的其他血液制品,补充患者的其他凝血因子及纤维蛋白原。同时不同国家的报道,使用rFⅦa后可出现血栓形成、肺栓塞、心肌梗死等并发症[12]。由于产后出血使患者体内凝血系统激活,导致凝血过度引起的并发症,但是部分产后出血并非凝血功能障碍,而是有动静脉血管损伤等导致。对rFⅦa的安全性研究中也发现,使用高剂量治疗时可能导致血栓风险明显增加,且老年人更为明显[13]。因此,使用rF Ⅶ a治疗产后出血时,应严格控制使用剂量,预防血栓形成等并发症。
本研究参考国内外同行使用rFⅦa治疗产后出血的经验,在13例产后出血患者常规治疗的基础上,采用rFⅦa治疗后,均康复出院。rFⅦa治疗后外科手术干预明显减少,仅2例应用rFⅦa后采取了外科干预。另外,3例已行外科干预后出血的患者,应用rFⅦa后取得了满意的效果,且首次给药后实现了止血。所有患者治疗后2小时PT、APTT均明显降低,而血红蛋白、血小板数量、纤维蛋白原则明显回升。但本研究观察的病例数还比较少,出血的原因没充分考虑,只是在常规治疗失败的情况下,采用rFⅦa辅助治疗后,有61.5%产后出血得到有效控制,还有一些需要手术治疗。因此,对rFⅦa辅助治疗难治性产后出血,在充分了解病因的基础上,还需要做到个体化治疗。
[1] Carroli G,Cuesta C,Abalos E,et al.Epidemiology of postpartum haemorrhage:a systematic review[J].Best Pract Res Clin Obstet Gynaecol,2008,22(6):999-1012.
[2] 范建辉,陈新娟,滕奔琦,等.重组活化凝血因子VIIa在产科出血中的应用[J].中国新药杂志,2011,(6):523-525.
[3] 蒋芳莲,罗俊标.人重组活化因子Ⅶa在难治性产后出血患者中的应用价值[J].医学临床研究,2014,(7):1416-1417.
[4] Franchini M,Franchi M,Bergamini V,et al.The use of recombinant activated FVII in postpartum hemorrhage[J].Clin Obstet Gynecol,2010,53(1):219-227.
[5] Moscardo F,Perez F,de la Rubia J,et al.Successful treatment of severe intra-abdominal bleeding associated with disseminated intravascular coagulation using recombinant activated factor VII[J].Br J Haematol,2001,114(1):174-176.
[6] Welsh A,McLintock C,Gatt S,et al,Guidelines for the use of recombinant activated factor VII in massive obstetric haemorrhage[J].Aust N Z J Obstet Gynaecol,2008,48(1):12-16.
[7] Lau P,Ong V,Tan WT,et al.Use of activated recombinant factor VII in severe bleeding - evidence for efficacy and safety in trauma,postpartum hemorrhage,cardiac surgery,and gastrointestinal bleeding.Transfus Med Hemother,2012,39(2):139-150.
[8] Isbister J,Phillips L,Dunkley S,et al.Recombinant activated factor VII in critical bleeding:experience from the Australian and New Zealand Haemostasis Register[J].Intern Med J,2008,38(3):156-165.
[9] Kobayashi T,Nakabayashi M,Yoshioka A,et al.Recombinant activated factor VII (rFVIIa/NovoSeven(R)) in the management of severe postpartum haemorrhage:initial report of a multicentre case series in Japan[J].Int J Hematol,2012,95(1):57-63.
[10] Lavigne-Lissalde G,Aya AG,Mercier FJ,et al.Recombinant human FVIIa for reducing the need for invasive second-line therapies in severe refractory postpartum hemorrhage:a multicenter,randomized,open controlled trial[J].J Thromb Haemost,2015,13(4):520-529.
[11] Lewis NR,Brunker P,Lemire SJ,et al.Failure of recombinant factor VIIa to correct the coagulopathy in a case of severe postpartum hemorrhage[J].Transfusion,2009.49(4):689-695.
[12] Rosenfeld SB,Watkinson KK,Thompson BH,et al.Pulmonary embolism after sequential use of recombinant factor VIIa and activated prothrombin complex concentrate in a factor VIII inhibitor patient[J].Thromb Haemost,2002.87(5):925-926.
[13] Patel A,Cooper N,Laffan MA.Safety of recombinant activated factor VII in randomized clinical trials[J].N Engl J Med,2011.364(6):574 -576.
10.15972/j.cnki.43-1509/r.2016.02.024
2015-12-29;
2016-02-25
R714.461
A
秦旭平)
