浓缩液中环状二聚体的含量及晶形分析
2016-12-23彭舒敏颜登峰叶军芳易春旺
彭舒敏,冯 炀,颜登峰,叶军芳,易春旺,3*
(1.湖南师范大学化学化工学院,长沙 410081;2.中石化巴陵分公司己内酰胺事业部聚合车间,岳阳 414014;3.石化新材料与资源精细利用国家地方联合工程实验室,长沙 410081)
浓缩液中环状二聚体的含量及晶形分析
彭舒敏1,冯 炀1,颜登峰2,叶军芳2,易春旺1,3*
(1.湖南师范大学化学化工学院,长沙 410081;2.中石化巴陵分公司己内酰胺事业部聚合车间,岳阳 414014;3.石化新材料与资源精细利用国家地方联合工程实验室,长沙 410081)
以己内酰胺聚合装置中不同浓度的萃取水和浓缩液为研究对象,通过高效液相色谱对其中的环状二聚体进行了定性定量分析,研究了不同浓度浓缩液中环状二聚体的结晶形态,并对环状二聚体的吸附团聚行为进行了静态模拟。结果表明: 环状二聚体在浓缩液中以β晶型存在;浓缩液浓度越高,环状二聚体的聚集密度越高,团聚现象越严重;即使在低浓度的萃取水中,环状二聚体也会吸附己内酰胺发生团聚;红外光谱和X衍射分析表明随着浓缩液浓度的增加,环状二聚体的特征峰强度逐渐减弱直至消失,而己内酰胺的特征峰强度则越来越强。
己内酰胺 浓缩液 环状二聚体 高效液相色谱 定性定量分析 晶形
己内酰胺聚合达到平衡时,聚合物体系中含有质量分数约10%的低分子可萃取物[1-2],其中己内酰胺单体质量分数约8%,环状二聚体质量分数约0.6%。低分子可萃取物在蒸发浓缩过程中,随着浓缩液的浓度增高,低分子可萃取物的含量也越来越高,容易在设备和管道死角产生团聚堵塞。长期以来,科研人员致力于研究有关低分子可萃取物的组成并形成共识:环状二聚体的存在是引发低聚物团聚堵塞的最重要原因[3-6]。
20世纪50年代,荷曼斯[7]首次观察到环状二聚体的存在并发现其有2种晶型,这2种晶型可以在一定条件下相互转变。荷曼斯认为针状α晶型环状二聚体更加稳定,但在水和极性溶剂中会转变成为不稳定的片状β晶型。作者前期研究[1]发现,浓缩液中的环状二聚体易吸附己内酰胺和其他低分子可萃取物并发生团聚。邢玉林等[8-9]利用高效液相色谱对浓缩液和切片中的低聚物进行了定性定量分析,但没有人定性定量研究过环状二聚体在不同浓度萃取水和浓缩液中的含量,也没有对蒸发浓缩过程中的环状二聚体晶形变化、团聚机理和破坏机理进行深入研究。
近年来,随着己内酰胺聚合装置单线生产能力增加,用于储存和输送蒸发浓缩液的设备和管道越来越大,一旦发生堵塞,将会严重影响装置的安全运行。基于上述原因,作者对己内酰胺聚合装置浓缩液中的低分子可萃取物进行了系列研究:(1)对不同浓度浓缩液中己内酰胺和环状二聚体的含量进行了定性定量分析;(2)对环状二聚体对己内酰胺和其他低分子可萃取物的吸附作用进行了初步探讨;(3)分析了团聚发生后升高温度对低聚物的影响,以期对工业装置正确处理浓缩液堵塞提出具有价值的指导性建议;重点研究了不同浓度浓缩液中己内酰胺和环状二聚体含量的变化并进行了定性定量分析,模拟研究了静态条件下浓缩液中环状二聚体的晶形变化及其吸附团聚行为。
1 实验
1.1 试样
萃取水(可萃取物质量分数10%)、一效浓缩液、二效浓缩液、二效浓缩液/己内酰胺混合物:均由巴陵石化公司己内酰胺事业部聚合装置提供。
1.2 实验方法
将可萃取物质量分数10%的萃取水、一效浓缩液、二效浓缩液、二效浓缩液/己内酰胺混合物分别编为1#,2#,3#,4#试样。待各试样静置后用移液管移取1#~4#试样的上清液各1 mL,分别用去离子水稀释2 000,2 000,6 000,6 000倍,稀释后的试样经0.45 μm 微孔滤膜过滤后待用。
1.3 分析测试
高效液相色谱(HPLC)分析:采用美国Alltech公司的液相色谱仪进行测试,检测器UVIS-201,色谱柱为 Alltima C18,250 mm×4.6 mm,流动相采用甲醇:纯水体积比为70:30的混合溶剂,流速为0.6 mL/ min,检测波长209 nm。以保留时间定性,以外标法定量,计算己内酰胺的含量。
X射线衍线光谱(XRD)分析:采用帕纳科公司制造的X′ Pert Pro M PD X射线仪进行测试,扫描2θ为5°~ 50°,扫描速率为2(°)/min。
傅里叶变换红外光谱(FTIR)分析:使用美国Nicolet Magna IS10傅里叶变换红外光谱仪进行分析,精度为4 cm-1,扫描波数500~4 000 cm-1。
结晶形态:采用上海长方光学仪器有限公司XPV-880E透反偏光显微镜进行观察并拍照。
2 结果和讨论
2.1 环状二聚体的定性定量分析
从表1可看出,1#,2#,3#,4#试样中的低分子可萃取物质量分数分别为8.58%,24.83%,71.28%,87.24%,其中1#,2#,3#试样的己内酰胺和环状二聚体比例基本固定,说明随着浓缩液中水不断蒸发,低分子可萃取物的浓度虽然会相应增高,但己内酰胺和环状二聚体的比例基本不会发生变化,同时这个比例比文献值偏大[4]。这是因为浓缩液直接聚合时,环状二聚体没有完全参与反应,从而导致聚合物中环状二聚体的含量偏高。4#试样中由于是二效浓缩液额外添加了适量的新鲜己内酰胺,因此己内酰胺的含量明显高于环状二聚体和其他低分子可萃取物的含量,比较4#试样和3#试样的环状二聚体和其他低分子可萃取物的含量可以得知,二者的含量基本没有发生变化,增加的只是新鲜己内酰胺的质量。
表1 浓缩液中己内酰胺与环状二聚体含量分析结果
Tab.1 Analysis result of content of caprolactam and cyclic dimmer in concentrated solution
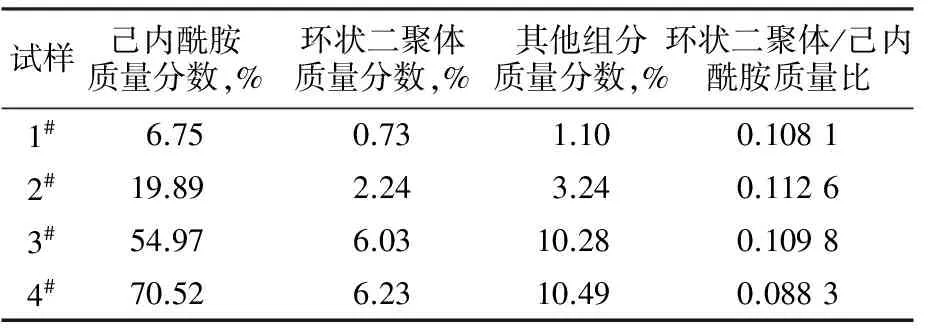
试样己内酰胺质量分数,%环状二聚体质量分数,%其他组分质量分数,%环状二聚体/己内酰胺质量比1#6.750.731.100.10812#19.892.243.240.11263#54.976.0310.280.10984#70.526.2310.490.0883
2.2 环状二聚体吸附沉降模拟
高浓度浓缩液在设备管道死角处容易发生团聚沉降,其原因是温度过低及流速减缓,导致低分子可萃取物特别是不溶于水的环状二聚体沉降。为了模拟这种团聚沉降行为,将不同浓度的浓缩液在氮气保护下80 ℃静置处理,一段时间后低浓度萃取水和高浓度浓缩液中都出现白色沉淀。浓缩液浓度越高,沉淀量越大,同时上清液中可以观察到大量悬浮颗粒。静置一周以后,所有试样的沉淀量不再增加,上清液中悬浮颗粒也完全消失。
从图1可看出,所有浓缩液的上清液HPLC谱图中均只出现了一个己内酰胺的吸收峰,这表明在80 ℃静态保温条件下,己内酰胺水溶液基本不会溶解环状二聚体和其他低分子可萃取物,表明静态下低分子可萃取物团聚是不可避免的现象。
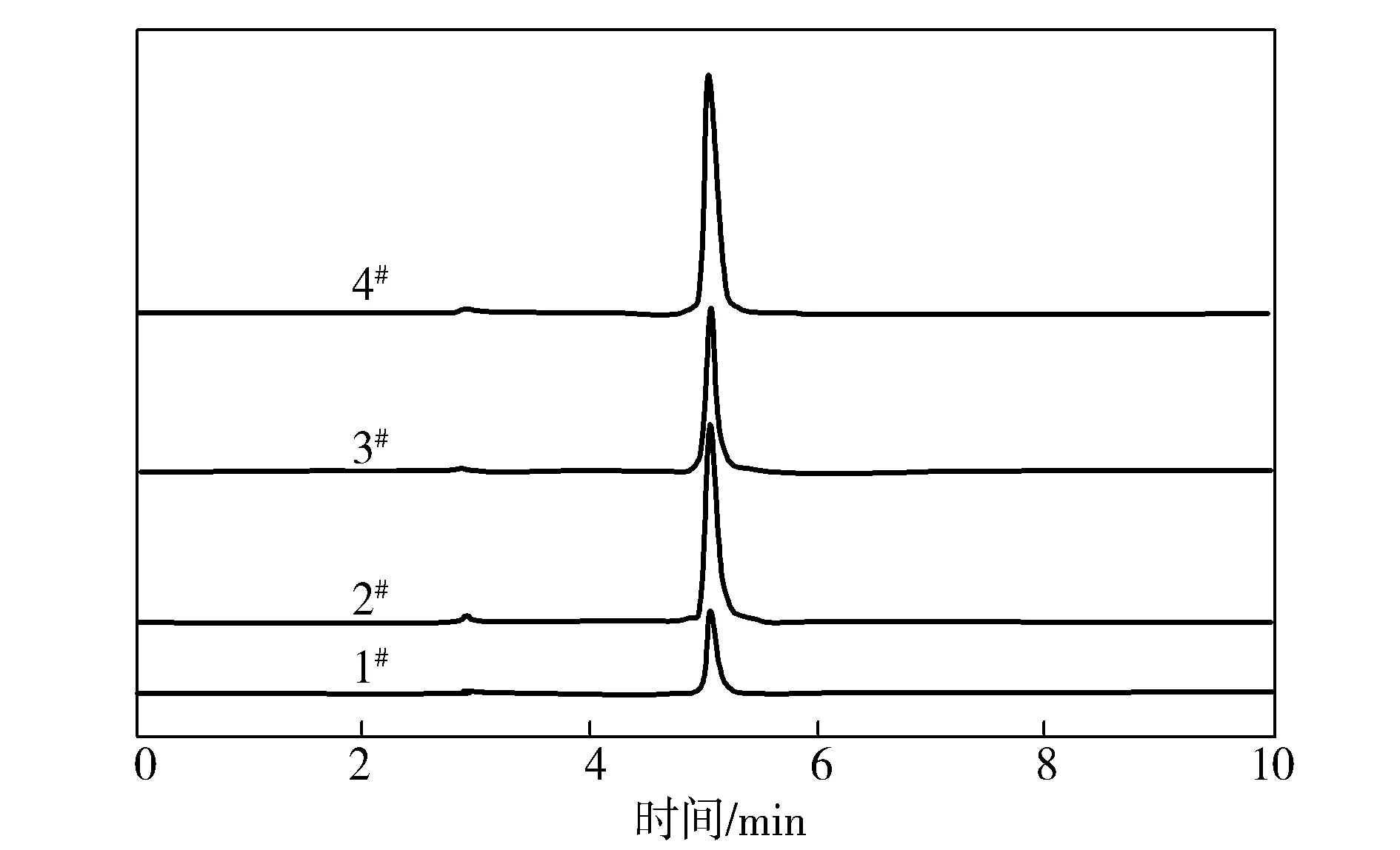
图1 试样上清液的HPLCFig.1 HPLC curves of supernatant
从表2可看出,所有试样上清液中的己内酰胺含量都小于原样中的实测值,随着试样浓度的增加,上清液中己内酰胺的含量和原样实测值的差值越大,这表明在所有的萃取水浓缩液中,只要环状二聚体发生沉降,都会吸附部分己内酰胺共同沉降,而且浓缩液的浓度越高,环状二聚体吸附的己内酰胺量越多,因此越容易发生团聚堵塞。
表2 上清液和原样浓缩液中的己内酰胺含量
Tab.2 Caprolactam content of supernatant and concentrated solution
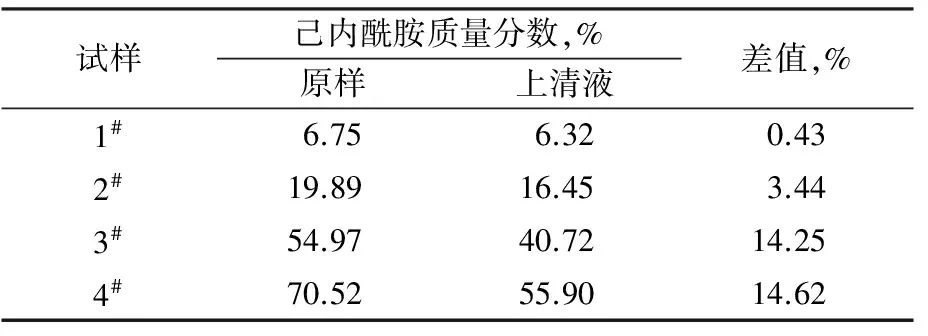
试样己内酰胺质量分数,%原样上清液差值,%1#6.756.320.432#19.8916.453.443#54.9740.7214.254#70.5255.9014.62
由于静置处理溶液80 ℃非常接近甚至高于萃取水储罐、三效蒸发的一效和二效蒸发器的工作温度,以上分析结果证明在可萃取物浓度较低的情况下,如果浓缩液长期处于静止状态下,环状二聚体也会发生沉降。
2.3 浓缩液中环状二聚体的结晶形态
萃取水在蒸发浓缩时,低分子可萃取物的含量因为水不断蒸发损失而升高,溶液中环状二聚体的含量也相应增加,由于环状二聚体在己内酰胺/水溶液中的溶解度非常低,即使在高温下环状二聚体也易于形成片状β结晶,而且只能形成β晶型。由图2可见,1#试样的环状二聚体的β片晶较少团聚,晶片之间保持着一定的空间,2#试样的环状二聚体密度明显增加,且趋于堆积团聚,3#,4#试样可以观察到己内酰胺和少量环状二聚体片状晶体的存在。
1#~4#试样都观察到片状环状二聚体的存在,而且浓度越高,溶液中环状二聚体片状晶体越多。与1#试样比较,2#试样环状二聚体的含量和密度都显著增加,因而环状二聚体晶片更易于堆积团聚,但相对于3#试样,4#试样中由于环状二聚体的浓度被稀释(即与己内酰胺的比值较小),片晶数量有所下降,团聚现象有所好转。但并不能据此认为添加新鲜己内酰胺可以有效防止环状二聚体团聚,因为这与添加比例、温度和运动状态都有关系。
2.4 XRD分析
由图3可看出,1#,2#,3#试样的X衍射谱带上可以清晰地观察到9.9°和11.53°两处衍射特征峰,其中9.9°为己内酰胺的特征衍射峰,11.53°是环状二聚体的特征衍射峰。从图中还可以清楚看出,随着浓缩液浓度的增加,己内酰胺的衍射峰强度越来越强,环状二聚体的衍射峰强度则越来越弱,4#试样谱带上环状二聚体的特征峰基本消失,而己内酰胺的特征峰变得特别强。这是因为在蒸发过程中,随着水的蒸发,环状二聚体会吸附包裹大量的己内酰胺团聚,形成糊状的厚片层团聚物。吸附包裹在环状二聚体表面的己内酰胺会削弱环状二聚体的衍射作用,水蒸发越彻底,己内酰胺的含量越高,环状二聚体吸附包裹的己内酰胺越多,因此其特征衍射峰强度显著减弱直至完全消失。

图3 试样的XRD图谱Fig.3 XRD curves of samples
2.5 FTIR分析
从图4可以看出,1#,2#,3#,4#试样的FTIR谱带图形基本重合,说明试样中组份和含量基本一致。其中3 271 cm-1为环状二聚体的N—H伸缩振动吸收峰,3 225 cm-1附近出现己内酰胺特征吸收峰。随着浓缩液浓度的增加,环状二聚体的特征峰吸收强度逐渐减弱直至消失,而己内酰胺的特征吸收峰强度则越来越强。

图4 试样的FTIRFig.4 FTIR spectra of samples
3 结论
a. 环状二聚体在浓缩液中以片状β晶型存在,浓缩液浓度越高,片晶的密度越大,团聚现象越严重。
b. 高效液相色谱定性定量分析结果表明:在蒸发过程中,随着水的蒸发,环状二聚体和己内酰胺的浓度会相应增高,但二者的相对质量比基本保持不变。
c. 静止状态下,低浓度的萃取水中环状二聚体也会吸附己内酰胺发生团聚,上清液中只有己内酰胺存在,环状二聚体和其他低分子可萃取物全部沉降。
d. 环状二聚体和己内酰胺共存时,己内酰胺对环状二聚体的特征吸收峰和衍射峰会造成干扰。随着浓缩液浓度的增加,环状二聚体的特征峰强度逐渐减弱直至消失,而己内酰胺的特征峰强度则越来越强。
[1] 易春旺, 王华平, 王朝生. 聚酰胺6聚合中低分子可萃取物的特性研究[J]. 合成纤维,2008,37(6):24-27.
Yi Chunwang, Wang Huaping, Wang Chaosheng. The characteristic analysis of oligomer in caprolactam polymer[J]. Syn Fiber Chin, 2008, 37(6):24-27.
[2] 易春旺. 锦纶6切片萃取后产生白点的原因及预防[J]. 合成纤维, 2005, 34( 7):41-43.
Yi Chunwang. Origination and prevention of the white point in
nylon 6 chips after extracting[J]. Syn Fiber Chin, 2005, 34(7):41-43.
[3] 陈毅荷. 己内酰胺浓缩液直接回用的工艺技术[J]. 合成纤维工业, 2001, 24( 6):41-44.
Chen Yihe. Direct reclamation process of caprolactam concentrate liquid[J]. Chin Syn Fiber Ind, 2001, 24( 6):41-44.
[4] Roberto Filippini Fantoni. Basic chemistry of caprolactam polymerization[M]. Italy: NOY Engineering,1990:3-63.
[5] 颜焕敏, 刘国强, 欧金华. 尼龙6聚合中几种浓缩液直接回用工艺的对比[J].合成纤维工业,2003,26(3):31-34.
Yan Huanmin, Liu Guoqiang, Ou Jinhua. Comparison of direct recovery process for concentrated liquid in nylon 6 polymerization[J]. Chin Syn Fiber Ind ,2003,26(3):31-34.
[6] 陈庆, 肖朝晖,颜登峰,等. 降低PA 6切片中可萃取物含量的工艺研究[J].化工进展,2003,22(8):889-891.
Chen Qing, Xiao Zhaohui, Yan Dengfeng, et al. Study on reduction of the extractant content in the polyamide 6 chip[J].Chem Ind Eng Pro, 2003,22(8):889-891.
[7] Hermans P H. Cyclic oligomers of caprolactam:(An unusual case of stereo isomerism in higher-membered rings)[J]. Recueil Trav Chim,1953,72(9):798-805.
[8] 邢玉林.尼龙6生产过程中的环状二聚体控制策略[D]. 上海:华东理工大学, 2014.
Xing Yulin. Control stratege of cyclic dimmer in nylon manufacture process[D]. Shanghai : East China University of Science and Technology, 2014.
[9] 王建华, 李铭瑜, 贺谷辉.高效液相色谱法测定尼龙6试样中的环状齐聚物[J]. 合成纤维工业,2000,23(2):50-53.
Wang Jianhua, Li Mingyu, He Guhui. The determination of cyclic oligomers in nylon 6 samples by HPLC[J]. Chin Syn Fiber Ind , 2000,23(2):50-53.
Analysis of cyclic dimmer content and crystalline morphology in concentrated solution
Peng Shumin1, Feng Yang1, Yan Dengfeng2, Ye Junfang2, Yi Chunwang1,3
(1.CollegeofChemistryandChemicalEngineering,HunanNormalUniversity,Changsha410081; 2.PolymerizationWorkshopofCaprolactamDivision,SINOPECBalingPetrochemicalCompany,Yueyang414014; 3.NatioanlandLocalJointEngineeringLaboratoryforNewPetrochemicalMaterialsandFineUtilizationofResources,Changsha410081)
The qualitative and quantitative analysis of cyclic dimmer was performed for extraction water and concentrated solution with different concentration from a caprolactam polymerization plant by high-performance liquid charomatography. The crystalline morphology of cyclic dimmer was studied in the concentrated solution with different concentration. The static simulation of the adsorption aggregation behavior of cyclic dimmer was conducted. The results showed that the cyclic dimmer existed in the concentrated solution in the form of β crystal; the higher the concentration of concentrated solution, the higher the aggregation density and the severer the agglomeration of cyclic dimmer; cyclic dimmer could agglomerate with caprolactam even in the low-concentration concentrated solution; the characteristic peak intensity of cyclic dimmer was weakened until disappeared and the characteristic peak of caprolactam became more and more intensive as the concentration of the concentrated solution was increased.
caprolactam; concentrated solution; cyclic dimmer; high-performance liquid charomatography; qualitative and quantitative analysis; crystalline morphology
2016- 09-13; 修改稿收到日期:2016-10-18。
彭舒敏(1991—),女,硕士研究生,主要从事己内酰胺聚合工程、 功能性聚酰胺的研究。E-mail:1326931485@qq.com。
十三五国家重点研发计划项目(2016YFB0302700)。
TQ225.26+1
A
1001- 0041(2016)06- 0074- 04
* 通讯联系人。E-mail:cwyi@hunnu.edu.cn。
