LC-MS/MS测定血液中利眠宁成分
2016-12-22孙会会仲建军翟晚枫
孙会会,仲建军,*,翟晚枫
(1.德州市公安局物证鉴定研究中心, 山东 德州 253000; 2.公安部物证鉴定中心,北京 100038)
LC-MS/MS测定血液中利眠宁成分
孙会会1,仲建军1,*,翟晚枫2
(1.德州市公安局物证鉴定研究中心, 山东 德州 253000; 2.公安部物证鉴定中心,北京 100038)
目的 建立一种液相色谱-串联质谱(LC-MS/MS)方法对血液中利眠宁成分进行定性定量分析。方法采用LC-MS/MS的多反应监测模式,通过利眠宁的保留时间和两对母离子/子离子对进行分析。前处理利用乙腈作为沉淀剂,沉淀血液中的蛋白,振荡离心后,过有机微孔滤膜,上清液通过LC-MS/MS进行检测。结果 通过该方法测定,血液中利眠宁成分在0.5~200 ng/mL浓度范围内具有良好线性,相关系数达0.9987。该方法最低检出限0.1 ng/mL,日内精密度在3 %以下,日间精密度在4 %以下,重现性好,回收率高。结论 采用该方法检测血液中的利眠宁成分,快速、简便、准确、可靠,能够满足公安机关侦破利用利眠宁杀人、抢劫、强奸等案件的检验要求。
液相色谱-串联质谱;血液;利眠宁
利眠宁(Chlordiazepoxide),又称为氯氮卓、甲氨二氮卓、7-氯-2-甲氨基-5-苯基-3H-1、4-苯并二氮杂卓-4-氧化物,属于苯二氮卓类药物(Benzodiazepines, BZD)。利眠宁在临床医学中常用于治疗失眠、焦虑等,主要作用于中枢神经系统。
近几年,利用安眠镇静类药物实施的案件数量不断上升,比如利用该类药物进行抢劫、杀人、强奸等,引起了公安部门的高度重视。国内目前报道的利眠宁检测方法中,有的利用利眠宁中含有甲氨基,作为电子给予体与电子接受体在一定pH的缓冲盐条件下反应,生成一种稳定的配合物,利用这种配合物在紫外-可见光范围内的吸收测定利眠宁的含量[1-2];有的利用红外光谱分析利眠宁的结构,通过分析利眠宁在红外光谱上的吸收,对其进行定性[3];有的利用利眠宁的化学修饰电极、极谱法来对利眠宁含量进行分析[4-5]。在色谱质谱方法方面,近年有研究利用快速溶剂萃取[6]、表面经过修饰的磁性纳米材料作为吸附剂[7]对生物检材中的安眠镇静类药物进行萃取浓缩后,通过气相色谱-质谱联用仪进行分析,但目前尚无采用液相色谱-质谱法检测的文献报道。相关文献中仅有利用液质联用技术筛选分析血液中苯二氮卓类、吩噻嗪类安眠镇静药物[8],以及同时分析血液中5种巴比妥类药物[9]等研究。液相色谱质谱联用法具有灵敏度高、分离效率高、前处理简便、适用范围广等优点,适合用于进行利眠宁的分析检测。本研究采用岛津LC-20AD高效液相色谱仪与AB Sciex QTrap 3200四级杆-离子阱串联质谱仪联用,采取多反应监测模式建立了对血液中利眠宁成分进行定性、定量分析的方法。该方法分析时间短,重现性好,灵敏度和回收率高,适于血液中利眠宁的检测,能够满足实际办案需要。
1 材料与方法
1.1 仪器与试剂
岛津LC-20AD高效液相色谱仪(日本岛津公司);AB Sciex QTrap 3200串联质谱仪(美国AB公司);BSA-323S型电子天平(德国赛多利斯);移液枪(上海华运分析仪器有限公司);TGL-16C离心机(上海安亭科学仪器厂);VORTEX-GENIE2涡轮振荡器(美国Scientifi c Industries);0.22μm有机微孔滤膜(上海富达医用塑料有限公司);容量瓶(北京博美玻璃有限公司)。高纯水;乙腈、甲醇(色谱纯,美国 Fisher公司);利眠宁标准品购自公安部物证鉴定中心,纯度大于99.1 %。将利眠宁标准物质配制成1.0 μ g/mL的标准工作液,备用。
1.2 色谱条件
Phenomenex C18(50 mm×2 mm, 2.5 μm)液相色谱柱,柱温40 ℃,进样量1 μL,流速0.5 mL/min,流动相采用梯度洗脱,所用溶液为高纯水(A相)-乙腈(B相),见表1。
1.3 质谱条件
AB Sciex QTrap 3200三重四级杆离子阱串联质谱仪,采用电喷雾离子化模式(electrospray ionization, ESI),选择正离子扫描,采用MRM作为检测方法,离子喷射电压IS为+5500 V,碰撞气氮气碰撞活化解离模式设定为Medium;气帘气为20 psi,离子源气Gas1为15 psi,离子源气Gas2为15 psi,离子源温度为500 ℃。
对利眠宁通过Q1 MS得到一级质谱,该物质的母离子300.1;Production(MS2)得到二级质谱,子离子227.2和282.1;在MRM模式下,两对离子对的去簇电压(declustering potential, DP)为36 V,300.1/227.2离子对的碰撞能量(collision energy, CE)为29 V,300.1/282.1离子对CE为27 V。
1.4 样品前处理
取1mL待测血液于试管中,加入3 mL乙腈作为沉淀剂,振荡离心20 min,取出上清液,过0.22 μm有机微孔滤膜,备检。
2 结果与讨论
2.1 色谱柱的选择
选择型号为Synergi 2.5u Fusion-RP 100A的色谱柱A和型号为Synergi 4u Fusion-RP 80A的色谱柱B进行比较研究,其中色谱柱A和B的粒径分别为2.5 μ m和4.0 μ m。实验结果如图1和表2所示,采用相同流动相和梯度程序、相同质谱条件分析同一样品,色谱柱A出峰快、响应强,与色谱柱B的峰展宽无明显差异,更适合于利眠宁的分析检验。
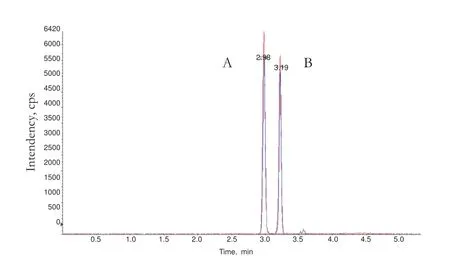
图1 相同条件下色谱柱A和色谱柱B分别分析利眠宁的MRM色谱叠加图Fig.1 The overlaid MRM chromatogram of chlordiazepoxide by columns of A and B under the same experimental conditions
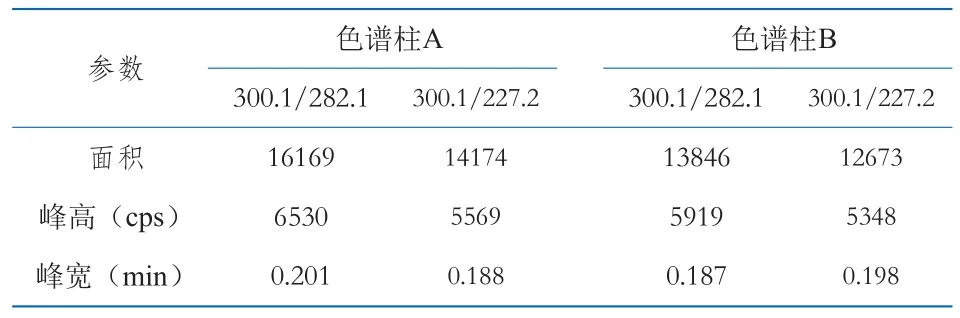
表2 相同条件下色谱柱A和色谱柱B分别分析利眠宁的峰参数Table 2 Peak parameters of chlordiazepoxide by columns of A and B under the same experimental conditions
2.2 定性与定量离子对的选择
选取准分子离子峰m/z 300.1作为母离子,选择质荷比较大、强度较稳定的m/z 282.1、m/z 227.2两个碎片作为子离子组成定性离子对300.1/227.2和300.1/282.1,将两对离子对的去簇电压DP和碰撞能量CE进行优化以得到最佳的相应强度,参数优化后的子离子扫描图见图2。由于300.1/282.1的响应强度更高,选择该对离子对作为利眠宁的定量离子对。
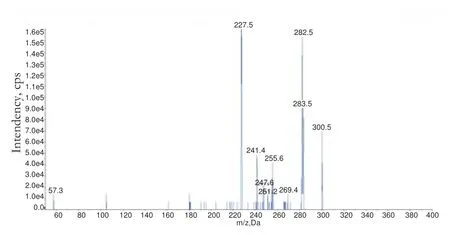
图2 利眠宁的子离子扫描图Fig.2 The image of scanning the product ion of chlordiazepoxide
2.3 流动相及其流速的选择
相比较甲醇-高纯水而言,选择乙腈-高纯水作为流动相进行梯度洗脱,在较短的分析时间内能达到较好的分离效果,而且实验中选择了乙腈作为沉淀剂,所以综合以上,实验选择乙腈-高纯水作为流动相。
实验中采用单因素实验的方式对有机相初始浓度和梯度陡度即梯度洗脱斜率进行考察,比较了有机相浓度分别为20 %、30 %、40 %、50 %、60 %、70 %、80 %的等度洗脱程序和以20 %为有机相初始浓度并保持1 min后,分别以10 %、20 %、30 %的梯度陡度进行洗脱的梯度洗脱程序,实验结果如表3所示。可以看出,有机相浓度升高或梯度陡度增加时,保留时间缩短,质谱响应增加,峰宽减少;采用梯度洗脱时目标物的质谱响应明显高于采用相同初始浓度的等度洗脱。考虑到保留时间过短不利于目标物与体内检材中复杂组分的分离,选择以20 %为初始浓度、20 %/min为梯度陡度的洗脱程序。另外综合考虑高效液相色谱柱所能承受的最大压力以及分析时间,将流动相的流速设置为0.5 mL/min。
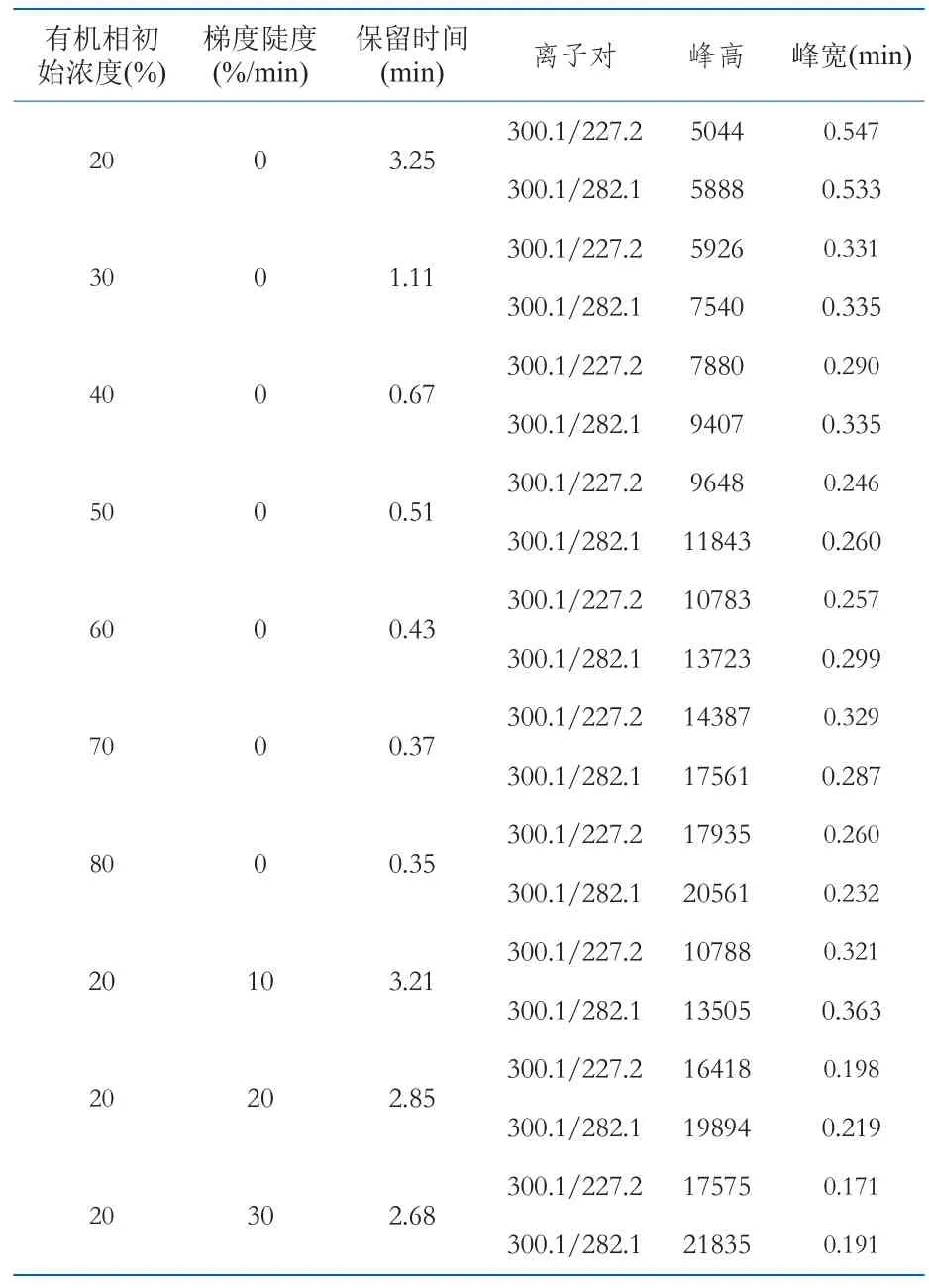
表3 不同的洗脱程序及与之对应的峰参数Table 3 Results of different gradient procedures and corresponding peak parameters
2.4 标准曲线、线性范围和方法检出限
以300.1/282.1作为利眠宁定量分析的离子对。在空白血中依次添加不同浓度的利眠宁标准溶液,进行定量分析,作利眠宁在一定浓度范围内的标准曲线。在实验条件下利眠宁在0.5~200 ng/mL浓度范围内呈良好的线性,线性方程:y=1873.5x+213.1(其中x表示利眠宁的进样浓度,y表示峰面积),相关系数r=0.9987(见图3)。根据S/N≥3测定这种方法的最低检出限(limit of detection, LOD),测得利眠宁的LOD是0.1 ng/mL。
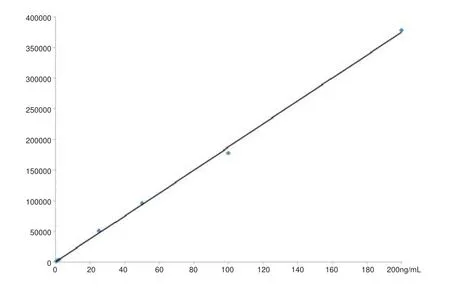
图3 利眠宁的标准工作曲线Fig.3 The standard working curve of chlordiazepoxide
2.5 精密度与回收率
在空白血液中分别加入利眠宁的标准溶液,配制成浓度分别为0.5、10.0、50.0 ng/mL的样品溶液,对每种浓度的样品平行进样6次,连续分析6日,计算利眠宁的日内精密度和日间精密度。
在空白血液中分别加入利眠宁标准溶液,配制成浓度分别为0.5、10.0、50.0 ng/mL的样品溶液,对每种浓度平行分析3次,测定回收率。结果表明该实验方法具有良好的重现性和较高的回收率(表4)。
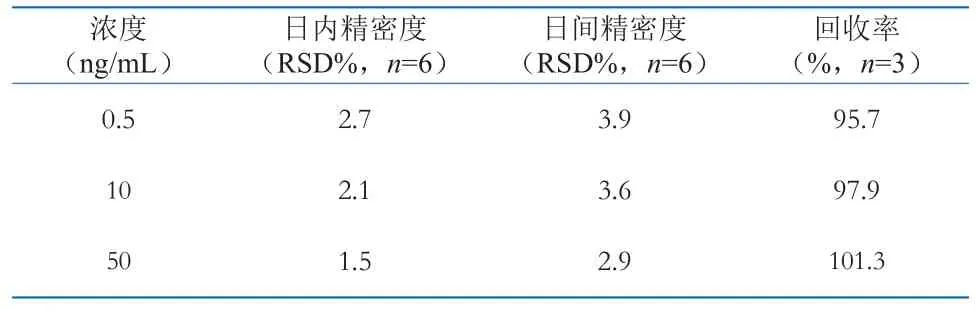
表4 血液中利眠宁精密度和回收率测定Table 4 RSDs and average recoveries of chlordiazepoxide in blood sample
2.6 案例应用
2015年1月,本市某县公安局送检一起抢劫强奸案件中被害人的血液,要求进行毒物成分定性定量分析,利用本实验建立的测定血液中利眠宁的方法对检材血进行分析,检验结果显示,检材血中检出利眠宁成分,含量为37 ng/mL,谱图见图4。
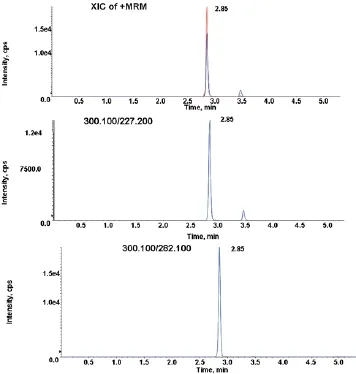
图4 利眠宁的MRM色谱图Fig.4 The MRM chromatogram of chlordiazepoxide
3 结语
紫外-分光光度法测定利眠宁成分,检材多是制剂,该方法前处理对于络合剂、缓冲液的浓度、反应时间和温度都有要求,检测的线性范围窄,检材中的某些杂质在紫外-可见中会有吸收,干扰检测;红外光谱属于振动光谱,通过谱图的解析可以获得分子的化学结构,但是红外光谱灵敏度低,对样品的纯度要求高,杂质会使红外光谱图复杂化而干扰鉴定;气相色谱-质谱联用技术检测生物检材中的镇静安眠类药物,前处理繁琐,对于某些难以气化的目标物需要衍生化。
液相色谱-质谱联用技术结合了液相色谱仪有效分离高沸点化合物、热不稳定性化合物能力与质谱仪高鉴别能力,是分析复杂有机混合物的有效手段。本文采用液相色谱-质谱联用法对血液中利眠宁成分进行分析,提高了检测的专一性和灵敏度,降低了杂质干扰,定性、定量准确,方法前处理简单,使用有机溶剂少,无需进行衍生化处理,方法检出限低,重现性好,回收率高,为公安部门侦破利用利眠宁作案的案件提供了重要的技术支持。
[1]宣春生,宋健玲. 2,4-二硝基酚分光光度法测定氯氮卓[J].分析测试技术与仪器,2001, 7(4):226-229.
[2]宣春生. 对硝基酚分光光度法测定氯氮卓的含量[J]. 光谱实验室,2002, 19(1):108-110.
[3]蔡锡兰. 红外差谱技术用于混合安眠药的鉴定[J]. 光谱学与光谱分析,2000, 20(3):329-332.
[4]钟爱国. 利眠宁-碘铋酸盐修饰碳糊电极的制作及应用[J].化学分析计量,2002, 11(4):36-37.
[5]林洪,李明,李德良,等. 利眠宁的二阶导数单扫描示波极谱测定及其电化学行为[J]. 理化检验(化学分册),2007, 43(7):585-587.
[6]李文海,蔺大伟,孙红雷,等. ASE-GC/MS法检测血液中常见镇静安眠类药物[J]. 中国法医学杂志,2014, 29(5):451-454.
[7]陈建虎,徐文涛,高元,等. 磁性纳米材料固相萃取与GC/ MS联用检测尿中安眠药残留[J]. 刑事技术,2014(4):3-6.
[8]沈敏,向平,沈保华,等. LC-MS/MS多反应监测筛选分析血液中132种毒药物[J]. 中国司法鉴定,2006(1):14-20.
[9]卓先义,向平. LC-MS/MS同时分析血液中五种巴比妥类药物[J]. 中国司法鉴定,2007(2):17-19.
Determination of Chlordiazepoxide in Blood Sample by LC-MS/MS
SUN Huihui1, ZHONG Jianjun1,*, ZHAI Wanfeng2
(1. Center of Material Evidence Authentication and Research, Dezhou Public Security Bureau, Shandong, Dezhou 253000, China;
2. Institute of Forensic Science, Ministry of Public Security, Beijing 100038, China)
Objective To develop and validate a sensitive, specifi c and rapid method for determining the chlordiazepoxide in blood sample by liquid chromatography-quadrupole ion trap mass spectrometry (LC-MS/MS). Methods Chlordiazepoxide was qualitatively analyzed by its retention time and two ion pairs of precursor/product in multiple reaction monitoring (MRM) mode. The blood sample was precipitated with acetonitrile, and then oscillated and centrifugalized. After fi ltration with organic membrane, the supernatant was analyzed by LC-MS/MS. Results With the optimized method, the correlation coeffi cient of chlordiazepoxide was 0.9987 within the linear range of 0.5~200ng/mL. The limit of detection (LOD) for chlordiazepoxide in blood was 0.1ng/mL. The intra- and inter-day relative standard deviations (RSDs) were below 3% and 4%, respectively. The results of recovery met the acceptance criteria. Conclusion This method was simple, rapid, reliable and highly accurate for analysis of chlordiazepoxide in blood, suitable for chlordiazepoxide-invloved cases of murder, robbery and rape.
LC-MS/MS; blood; chlordiazepoxide
DF795.1
A
1008-3650(2016)05-0376-04
2015-12-30
格式:孙会会,仲建军,翟晚枫. LC-MS/MS测定血液中利眠宁成分[J]. 刑事技术,2016,41(5):376-379.
10.16467/j.1008-3650.2016.05.0 07
孙会会(1987—),女,山东临沂人,硕士,助理工程师,研究方向为毒物、毒品检验。E-mail: shqcome@163.com
* 通讯作者:仲建军(1975—),男,山东德州人,学士,主检法医师,研究方向为法医毒理学。E-mail: dezhoudna@126.com
