水飞蓟素肠溶聚乳酸-羟基乙酸共聚物纳米粒的制备及体外释药研究Δ
2016-12-22邱妍川杨延音刘松青林凤云江尚飞朱照静重庆医药高等专科学校继续教育学院重庆4011重庆医药高等专科学校药学院重庆4011第三军医大学第一附属医院药剂科重庆40008
何 静,邱妍川,杨延音,刘松青,林凤云,江尚飞,朱照静(1.重庆医药高等专科学校继续教育学院,重庆 4011;.重庆医药高等专科学校药学院,重庆 4011;.第三军医大学第一附属医院药剂科,重庆 40008)
水飞蓟素肠溶聚乳酸-羟基乙酸共聚物纳米粒的制备及体外释药研究Δ
何 静1*,邱妍川2,杨延音2,刘松青3,林凤云2,江尚飞2,朱照静2(#1.重庆医药高等专科学校继续教育学院,重庆 401331;2.重庆医药高等专科学校药学院,重庆 401331;3.第三军医大学第一附属医院药剂科,重庆 400038)
目的:制备水飞蓟素肠溶聚乳酸-羟基乙酸共聚物(PLGA)纳米粒,并研究其体外释药行为。方法:以羟丙基甲基纤维素邻苯二甲酸酯(HPMCP)为肠溶材料,采用纳米沉淀法制备水飞蓟素肠溶PLGA纳米粒和水飞蓟素PLGA纳米粒,观察其形态,检测其粒径、Zeta电位、包封率、载药量、稳定性、体外释放度(Q)。以粒径、包封率、载药量为指标筛选水飞蓟素肠溶PLGA纳米粒中PLGA-HPMCP质量比。结果:PLGA-HPMCP的最佳质量比为1∶0.25。所制水飞蓟素肠溶PLGA纳米粒和水飞蓟素PLGA纳米粒的粒径分别为224、193 nm,Zeta电位分别为-37.8、-40.7 mV;包封率分别为(74.7±2.2)%、(71.7±2.5)%,载药量分别为(5.39± 0.24)%、(5.21±0.22)%;4℃下储存3个月后的渗漏率分别为0.2%、0.5%;人工胃液中Q48h分别为38.6%、70.5%,人工肠液中Q48h分别为80.2%、73.5%。结论:成功制得水飞蓟素肠溶PLGA纳米粒,其稳定性较好,能有效抑制水飞蓟素在人工胃液中的释放。
水飞蓟素;聚乳酸-羟基乙酸共聚物;羟丙基甲基纤维素邻苯二甲酸酯;纳米粒;体外释放度
水飞蓟素(Silymarin)是从菊科植物水飞蓟中提取精制而成的一类黄酮类化合物的总称,主要包含水飞蓟宾、水飞蓟宁和水飞蓟亭等,其中水飞蓟宾及其异构体异水飞蓟宾含量最高,约占该化合物的60%~70%,且具有最强的药理活性[1]。水飞蓟素在临床上是治疗肝脏疾病最为常用的一种植物药,体外研究证明其可通过抑制核因子κB(NF-κB)细胞发挥抗炎和免疫调节作用[2];还可以通过影响丙型肝炎核心蛋白和NS5A病毒的表达,发挥治疗慢性丙型肝炎病毒感染的作用[3]。此外,临床研究显示,水飞蓟素可有效用于非酒精性脂肪性肝病的治疗[4],并可减轻抗肺结核药物引起的肝损伤[5],减少化疗过程中顺铂造成的肾毒性等[6]。
尽管水飞蓟素在体外表现出了较好的药理活性,但由于其溶解度很低、体内吸收较差、生物利用度低,严重影响了其在临床的使用。目前临床上使用的水飞蓟素片剂或胶囊剂,患者需要每日给药3次,即每天需使用1.2~1.5 g才能维持有效的血药浓度。尽管水飞蓟素临床应用安全性较好,但高剂量长期使用仍会造成恶心、呕吐、腹泻等消化道不良反应。为提高水飞蓟素的生物利用度,国内外研究主要集中于制备其固体分散体、纳米脂质体、纳米混悬剂等[7-8],能一定程度上改善其体内吸收和靶向特征,但目前均未应用于临床。近年来,肠溶纳米粒的研究逐渐成为热点,已有研究显示其与普通纳米粒相比,可使药物以分子形态分布于肠溶载体,进一步提高药物的物理化学稳定性,减少对胃肠道的刺激;此外,以小肠定位给药可有效减少或避免用药的个体差异[9-10]。因此,本试验通过制备水飞蓟素肠溶聚乳酸-羟基乙酸共聚物(PLGA)纳米粒,以改善其溶解状况,降低其在人工胃液中的突释现象,进一步提高其口服给药的生物利用度和疗效,减少临床使用的不良反应。
1 材料
1.1 仪器
LC-2010C HT高效液相色谱仪(日本岛津公司);Tecnai G2 20200kV透射电子显微镜(厦门亿辰科技有限公司);纳米激光粒度仪(德国新柏泰克公司);超速离心机(美国贝克曼库尔特有限公司)。
1.2 药品与试剂
水飞蓟素对照品(西安瑞林生物科技有限公司,批号:130802,纯度:>98%);PLGA[中国科学院成都有机化学研究所,批号:141245-359,乙交酯(GA)-丙交酯(LA)(75∶25)];羟丙基甲基纤维素邻苯二甲酸酯(HPMCP,HP55,日本信越化学工业株式会社,批号:130906);聚乙烯醇(PVA,美国Sigma-Aldrich公司);甘露醇(重庆博方医药有限责任公司);丙酮(重庆川江化学试剂厂,化学纯);甲醇为色谱纯,水为去离子水。
2 方法与结果
2.1 水飞蓟素的含量测定
2.1.1 色谱条件 色谱柱为Dikma-C18(150 mm×4.6 mm,5 μm);流动相为甲醇-0.05 mol/L磷酸盐缓冲液(pH 2.77)(48∶52,V/V,经0.2 μm微孔滤膜滤过后使用),流速为1 ml/min;检测波长为288 nm;柱温为30℃;进样量为10 μl。该色谱条件下,水飞蓟宾和异水飞蓟宾的出峰时间分别为16.7、18.9 min,以两者峰面积之和计算水飞蓟素含量;其他辅料不影响水飞蓟素的含量测定。
2.1.2 方法学考察 按方法学考察相关方法进行试验。水飞蓟素峰面积(y)与质量浓度(x)的回归方程为y=16 548.6x+ 344.1(r=0.999 8,n=6),线性范围为5.03~150.9 μg/ml;日内(n=5)、日间(n=3)精密度试验的RSD均小于4.29%;10.06、50.30、100.60 μg/ml水飞蓟素溶液的方法回收率分别为(97.68±3.22)%、(98.32±3.51)%、(99.65±1.24)%(n=5)。
2.2 PLGA纳米粒的制备
采用纳米沉淀法制备PLGA纳米粒。称取水飞蓟素、PLGA各约0.7 g与一定量的HPMCP溶于10 ml丙酮,在磁力搅拌条件下,缓慢滴加到5%PVA水溶液中,调节pH至4~8,继续搅拌2 h。12 000 r/min(离心半径15 cm)离心10 min去除非目标粒径颗粒,加入甘露醇6 g,冷冻干燥,得水飞蓟素肠溶PLGA纳米粒。另精密称取水飞蓟素和PLGA各约0.7 g溶于丙酮中,之后照上述方法制备得到水飞蓟素PLGA纳米粒。
2.3 包封率和载药量测定
称取葡聚糖凝胶,加纯化水溶胀、煮沸、放冷、装柱。取制备好的水飞蓟素肠溶PLGA纳米粒或水飞蓟素PLGA纳米粒,采用蒸馏水重新分散为纳米粒混悬液后,精密吸取5.0 ml上样。脱气后超纯水洗脱,流速1.0 ml/min,收集洗脱液,弃去前20 ml洗脱液,取后55 ml,旋转蒸发浓缩至干,甲醇清洗旋蒸瓶并定容。用高效液相色谱法测定水飞蓟素含量,计算包封率和载药量。包封率(%)=Ws/Wa×100%,载药量=Ws/Wnp×100%,式中Wa为水飞蓟素投药量,Ws为包裹在纳米粒中的药物量,Wnp为载药纳米粒的量。
2.4 肠溶材料对水飞蓟素肠溶PLGA纳米粒的影响
固定水飞蓟素和PLGA处方量,以粒径、包封率和载药量为指标,考察不同比例PLGA-HPMCP(1∶0、1∶0.1、1∶0.25、1∶0.5、1∶0.75、1∶1)对水飞蓟素肠溶PLGA纳米粒的影响。结果显示,PLGA-HPMCP比例在1∶0.25之后,随HPMCP比例增大,纳米粒粒径增大,但包封率和载药量趋于稳定。因此,本试验选择PLGA-HPMCP比例为1∶0.25。不同比例PLGAHPMCP对水飞蓟素肠溶PLGA纳米粒的影响见表1。

表1 不同比例PLGA-HPMCP对水飞蓟素肠溶PLGA纳米粒的影响Tab 1 Effects of different ratios of PLGA-HPMCP on enteric-coated silymarin-PLGAnanoparticles
2.5 PLGA纳米粒质量评价
2.5.1 形态观察 按“2.3”项下方法制备水飞蓟素肠溶PLGA纳米粒和水飞蓟素PLGA纳米粒的混悬液,采用透射电子显微镜观察纳米粒的形态。结果显示,二者均呈圆形。透射电子显微镜图见图1。
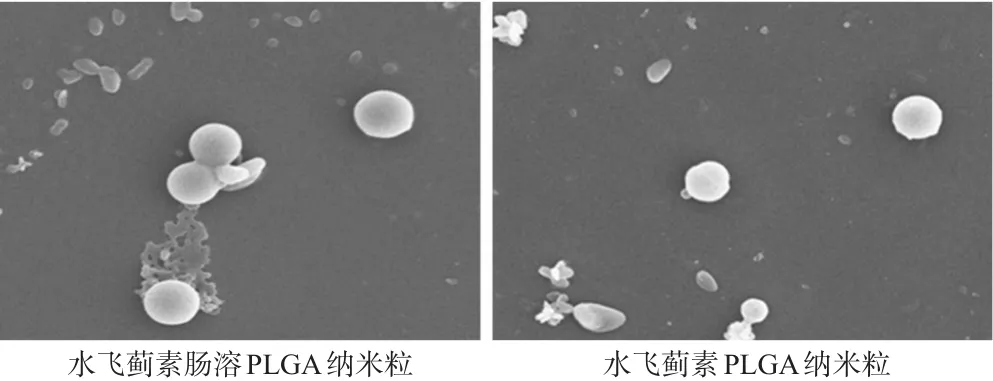
图1 两种纳米粒的透射电子显微镜图(×2 300)Fig 1 TEM of 2 kinds of nanoparticles(×2 300)
2.5.2 粒径和Zeta电位 按“2.3”项下方法制备水飞蓟素肠溶PLGA纳米粒和水飞蓟素PLGA纳米粒混悬液,加水稀释10倍,用纳米激光粒度仪测定其粒径和Zeta电位。结果显示,二者的平均粒径分别为224、193 nm,粒径分布为正态分布;Zeta电位分别为-37.8、-40.7 mV,表明两种纳米粒均较为稳定。两种纳米粒的粒径分布见图2。
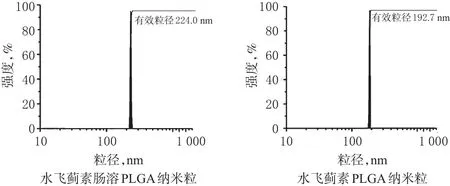
图2 两种纳米粒的粒径分布Fig 2 Particle size distribution of 2 kinds of nanoparticles
2.5.3 含量测定 取水飞蓟素肠溶PLGA纳米粒和水飞蓟素PLGA纳米粒,加入甲醇溶解并稀释混匀,进样测定水飞蓟素含量。结果,二者水飞蓟素的含量分别为(53.96±1.06)、(54.68±1.21)mg/g(n=6)。
2.5.4 稳定性考察 将水飞蓟素肠溶PLGA纳米粒和水飞蓟素PLGA纳米粒分别置于25 ml的敞口试管中,4℃下保存,分别于1、2、3个月时取出样品测定平均粒径与渗漏率(LR),LR(%)=(1-EEt/EE0)×100%,式中,EEt和EE0分别为在t时刻的包封率和初始包封率。结果显示,二者在4℃下储存3个月后粒径基本无变化,LR分别为0.2%、0.5%,具体结果见表2。
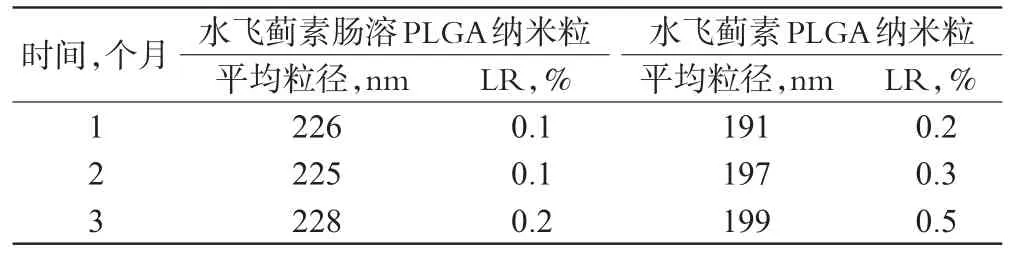
表2 两种纳米粒的稳定性试验结果Tab 2 Results of stability test of 2 kinds of nanoparticles
2.6 体外释放度考察
分别取水飞蓟素肠溶PLGA纳米粒和水飞蓟素PLGA纳米粒45 mg,放入棕色瓶中,分别加入150 ml人工胃液和人工肠液,37℃气浴恒温振荡,转速100 r/min。分别于试验前和开始振荡后0.5、1、2、4、8、12、24、48 h取样4 ml,并补充等体积的释放介质。接收液用0.22µm的微孔滤膜过滤,以甲醇稀释后于288 nm波长处测定吸光度,计算累积释放度,绘制体外释放曲线,结果见图3。
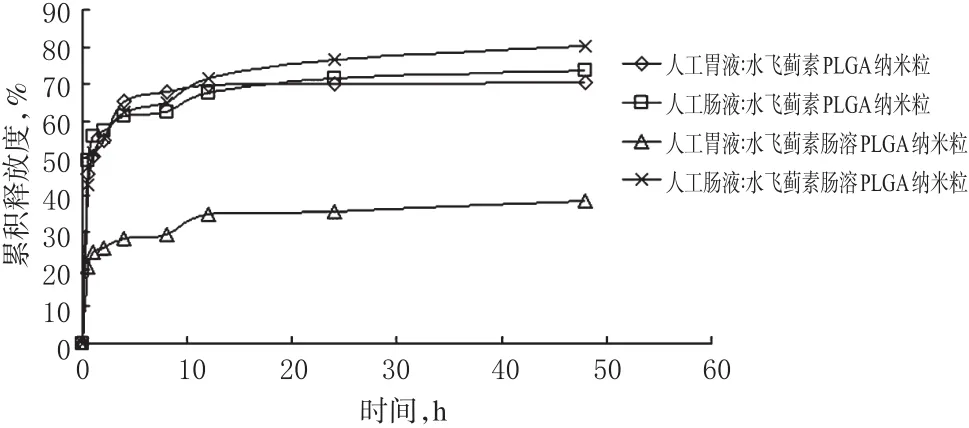
图3 两种纳米粒的体外释放曲线Fig 3 Release curves of 2 kinds of nanoparticles in vitro
由图3可见,水飞蓟素肠溶PLGA纳米粒在人工胃液中的释放速度和累积释放度明显低于水飞蓟素PLGA纳米粒;而在人工肠液中,水飞蓟素肠溶PLGA纳米粒的释放速度和累积释放度略高于水飞蓟素PLGA纳米粒。这是因为水飞蓟素溶解度较差,当人工肠液中肠溶材料溶解后,PLGA骨架对药物的阻滞作用占优势;而水飞蓟素肠溶PLGA纳米粒粒径较大,PLGA骨架对药物溶出的阻滞作用也相对较差,所以水飞蓟素溶出更快、溶出量更大。
3 讨论
PLGA是目前开发最为成功的一种生物可降解聚合物,可在机体内降解为乳酸和乙醇酸,进一步分解为二氧化碳和水排出体外,具有较好的生物相容性。其也是目前美国FDA和欧盟药品监管局(EMA)均批准的一种血管外给药的药物传递系统,可用于多种药物制剂的处方,包括亲水性、疏水性药物,也包括各种大分子或小分子药物,可有效用于延缓药物在体内的释放,降低药物在体内的代谢速度以及实现药物的靶向给药[11]。
由于PLGA纳米粒在胃液中有较强的突释现象,因此,本试验在制备水飞蓟素PLGA纳米粒的基础上,开发其肠溶剂型,以降低其在胃液中的突释,提高其在肠道的吸收,从而提高其口服给药的生物利用度;同时,还能有效避免其对胃肠道的刺激,减少不良反应的发生。从研究结果看,水飞蓟素肠溶PLGA纳米粒能有效抑制水飞蓟素在人工胃液中的释放。此外,笔者还需进一步试验评价其口服给药后体内的靶向作用,为其制剂的开发和临床应用提供依据。
[1] Cacciapuoti F,Scognamiglio A,Palumbo R,et al.Silymarin in non alcoholic fatty liver disease[J].World J Hepatol,2013,5(3):109.
[2]Morishima C,Shuhart MC,Wang CC,et al.Silymarin inhibits in vitro T-cell proliferation and cytokine production in hepatitis C virus infection[J].Gastroenterology,2010,138(2):671.
[3] Bonifaz V,Shan Y,Lambrecht RW,et al.Effects of silymarin on hepatitis C virus and haem oxygenase-1 gene expression in human hepatoma cells[J].Liver Int,2009,29(3):366.
[4] Aller R,Izaola O,Gómez S,et al.Effect of silymarin plus vitamin E in patients with non-alcoholic fatty liver disease.A randomized clinical pilot study[J].Eur Rev Med Pharmacol Sci,2015,19(16):3 118.
[5] Luangchosiri C,Thakkinstian A,Chitphuk S,et al.A double-blinded randomized controlled trial of silymarin for the prevention of antituberculosis drug-induced liver injury[J].BMC Complement Altern Med,2015,15(1):334.
[6] Momeni A,Hajigholami A,Geshnizjani S,et al.Effect of silymarin in the prevention of cisplatin nephrotoxicity,a clinical trial study[J].JCDR,2015,29(7):1 046.
[7] 陈晴宇,周建平,霍美蓉.水飞蓟素新型纳米制剂的研究进展[J].中国药科大学学报,2015,46(3):376.
[8] 李庆国,关世侠,郭慧珍.水飞蓟素缓释片的制备及体外释药机制研究[J].中国药房,2013,24(19):1 770.
[9] 王陆军,邱瑞桂,李建宇,等.葛根素肠溶纳米粒的制备及体外释放度研究[J].解放军药学学报,2009,25(6):514.
[10] 黄雅洁,李雅彬,袁海龙,等.南五味子总木脂素肠溶纳米粒的制备和药代动力学初步研究[J].药学学报,2009,44(9):1 046.
[11] Danhier F,Ansorena E,Silva JM,et al.PLGA-based nanoparticles:an overview of biomedical applications[J]. J Control Release,2012,161(2):505.
Preparation and in vitro Drug Release of Enteric-coated Silymarin-PLGA Nanoparticles
HE Jing1,QIU Yanchuan2,YANG Yanyin2,LIU Songqing3,LIN Fengyun2,JIANG Shangfei2,ZHU Zhaojing2(1.College of Extended Education,Chongqing Medical and Pharmaceutical College,Chongqing 401331,China;2.College of Pharmacy,Chongqing Medical and Pharmaceutical College,Chongqing 401331,China;3.Dept.of Pharmacy,the First Affiliated Hospital to Third Military Medical University,Chongqing 400038,China)
OBJECTIVE:To prepare enteric-coated silymarin-PLGA nanoparticles,and to study its in vitro release behavior. METHODS:Using HPMCP as enteric-coated material,nanoprecipitation method was used to prepare enteric-coated silymarin-PLGA nanoparticles and silymarin-PLGA nanoparticles.The morphology of nanoparticles were observed,and the particle size,Zeta-potential,encapsulation efficiency,drug-loading amount,stability and in vitro release rate(Q)were detected.The ratio of PLGA-HPMCP in enteric-coated silymarin-PLGA nanoparticles was screened by using particle size,encapsulation ratio and drug-loading capacity as indexes.RESULTS:The best PLGA-HPMCP ratio was 1∶0.25.The particle size of enteric-coated silymarin-PLGA nanoparticles and silymarin-PLGA nanoparticles were 224 nm and 193 nm,Zeta potential were-37.8 mV and-40.7 mV;encapsulation ratio were(74.7±2.2)%and(71.7±2.5)%,and drug-loading amount were(5.39±0.24)%and(5.21± 0.22)%;the percolation rates of them were 0.2%and 0.5%at 4℃ 3 months later;Q48hof them in simulated gastric fluid were 38.6%and 70.5%,and Q48hof them in simulated intestinal fluid were 80.2%and 73.5%,respectively.CONCLUSIONS:The enteric-coated silymarin-PLGA nanoparticles are prepared successfully with good stability,and can effectively inhibit the release of silymarin in simulated gastric fluid.
Silymarin;PLGA;HPMCP;Nanoparticle;Release rate in vitro
R943;R927
A
1001-0408(2016)34-4842-03
2016-02-05
2016-04-22)
(编辑:邹丽娟)
重庆市科技攻关计划项目(No.cstc2012gg-yyjs 10008);重庆市卫生局医学科研计划项目(No.2012-2-256)
*副教授,硕士。研究方向:缓控释制剂。E-mail:hejingt@126. com
#通信作者:教授,博士。研究方向:药剂学。E-mail:zhaojing6271@126.com
DOI 10.6039/j.issn.1001-0408.2016.34.28
