谷胱甘肽修饰金纳米棒的制备及与Cu2+的作用
2016-12-21张龄月迟娅楠单桂晔陈艳伟
张龄月, 迟娅楠, 单桂晔, 陈艳伟, 刘 娜
(1. 东北师范大学物理学院, 长春 130024;2. 吉林大学环境与资源学院, 长春 130012)
谷胱甘肽修饰金纳米棒的制备及与Cu2+的作用
张龄月2, 迟娅楠1, 单桂晔1, 陈艳伟1, 刘 娜2
(1. 东北师范大学物理学院, 长春 130024;2. 吉林大学环境与资源学院, 长春 130012)
制备了谷胱甘肽(GSH)功能化的金纳米棒复合材料, 根据金纳米棒的等离子体吸收峰对其组装排列敏感的特性, 研究了功能化的金纳米棒在不同pH值下的组装行为及与Cu2+离子作用后引起的聚集程度、 排列方式和光学吸收等变化. 同时, 测试了纯金纳米棒和谷胱甘肽修饰的金纳米棒分别与铜离子作用后所得复合材料的光热转换性能. 结果表明, 相对于纯金纳米棒材料强的光热转换效应, 铜离子能明显降低复合材料的光热转换效应, 与其它金属离子比较, GSH修饰的金纳米棒的等离子光学特性对铜离子具有选择性的变化.
金纳米棒; 谷胱甘肽; 铜离子; 等离子体共振吸收; 无机纳米复合材料
近年来, 金纳米棒因具有独特的物理化学特性而被广泛应用于生物识别标记、 化学检测、 光热治疗及催化等领域[1~6]. 金纳米棒的消光特性包括吸收消光和散射消光, 它一方面受入射光的波长影响, 另一方面还依赖于颗粒的长径比. 金纳米棒具有纵向表面等离子体共振(LSPR)吸收带和横向表面等离子体共振(TSPR)吸收带[7~10], 通过改变金纳米棒的横纵尺寸比例, 金纳米棒的LSPR吸收峰位可以从可见光区调节到近红外区域. 金纳米棒的聚集程度也和LSPR峰位有关, 当金纳米棒的聚集程度增大时, LSPR的峰位会发生红移, LSPR吸收峰的半峰宽也会展宽. 利用金纳米棒等离子体吸收吸收光谱的这些变化, 可以了解其组装过程. 谷胱甘肽(GSH)是一种含γ-酰胺键和巯基的三肽, 由谷氨酸、 半胱氨酸及甘氨酸组成. 半胱氨酸上的巯基为谷胱甘肽的活性基团, 可与金属作用, 这也是GSH诱导金纳米棒材料形成不同聚集状态的主要原因[11~13].
在金纳米棒表面吸附GSH可以改变金纳米棒的介电常数, 进而改变其折射率, 而折射率的改变会诱导等离子体移动, 所以金纳米棒可被用于超灵敏、 轻型以及远程的化学和生物医药传感器[14~18]. 重金属离子可以使金纳米棒进行组装, 组装后, 金纳米棒在相互接近过程中等离子体耦合会引起光谱的移动[19,20], 由于金纳米棒的LSPR峰对长径比的变化敏感[21~25], 在不同的pH环境下, GSH修饰金纳米棒的排列方式不同会影响纵向LSPR峰峰位的变化. 本文利用金纳米棒材料的尺寸依赖及各向异性等性质, 研究了Cu2+离子引起的金纳米棒的聚集程度、 排列方式和光学吸收等的变化(在吸收光谱上体现出明显的纵向吸收峰的移动). 通过研究金属离子诱导GSH修饰金纳米棒的选择性排布聚集, 建立了一种能够用于检测有害物质的有效方法.
1 实验部分
1.1 试剂与仪器
十六烷基三甲基溴化铵(CTAB, 中国惠世生化试剂有限公司); 无水乙醇(C2H5OH, 北京化工厂); 硼氢化钠(NaBH4, 国药集团化学试剂有限公司); 硝酸银(AgNO3)、 氯金酸(HAuCl4·3H2O)和抗坏血酸(C6H8O6)购于Sigma公司. 所用试剂均为分析纯.
JEM-2100F 型透射电子显微镜(TEM, 日本电子公司); Nano Zetasizer 2000 型动态光散射仪(英国Malvern 公司); F-4500 型荧光光谱仪(日本Hitachi 公司); HarshawTLD 3500 型手动热释光测量仪(美国Thermo Fisher 公司) .
1.2 实验过程
1.2.1 金纳米棒的制备 采用种子生长法[5]制备金纳米棒. 首先制备种子溶液: 配制0.25 mL 0.01 mol/L的氯金酸溶液和9.75 mL 0.1 mol/L的CTAB溶液, 并将两溶液混合, 再加入0.6 mL 0.01 mol/L的硼氢化钠溶液, 快速晃动2 min左右, 于室温下放置2 h后使用; 然后将2 mL 0.01 mol/L的氯金酸溶液、 0.4 mL 0.01 mol/L的AgNO3溶液和40 mL 0.1 mol/L的CTAB溶液混合, 再依次加入新鲜配制的0.32 mL 0.01 mol/L抗坏血酸和0.8 mL 1.0 mol/L的盐酸, 将溶液混合摇匀后, 向其中加入96 μL种子溶液, 将混合溶液均匀晃动10 s后, 再静置6 h, 即获得金纳米棒溶液.
1.2.2 谷胱甘肽修饰金纳米棒的制备 取10 mL上述金纳米棒溶液, 加入10 mL 0.2 mmol/L的GSH, 放置10 min后将反应后的混合物平均分成10份, 取其中的7份, 用盐酸和氢氧化钠调节溶液pH值分别为2, 3, 4, 5, 6, 11, 12, 再搅拌50 min, 然后将混合物在室温下放置12 h. 反应后的复合物溶液经超声离心(4000 r/min)后用水洗涤, 去除游离的GSH, 即得到GSH修饰的金纳米棒复合材料, 记为GSH-Au NRs.
1.2.3 Cu2+离子对金纳米棒组装的影响 用CuSO4·5H2O配制Cu2+浓度分别为0.08, 0.205和0.425 mol/L的溶液. 另取3份各1 mL上述GSH修饰的金纳米棒溶液, 调节pH值均为5, 然后分别加入100 μL Cu2+浓度为0.08, 0.205和0.425 mol/L的溶液, 在室温、 避光条件下放置2 h, 利用紫外-可见吸收光谱仪和透射电子显微镜研究铜离子对金纳米棒组装的影响.
2 结果与讨论
2.1 pH值变化对GSH修饰金纳米棒的影响

Fig.1 LSPR spectra of pure Au nanorods(a) and Au nanorods modified with GSH molecular at different pH values
图1示出了GSH修饰的金纳米棒(GSH-Au NRs)在pH改变后LSPR吸收峰的变化. 图1谱线a为未修饰GSH的金纳米棒, 其LSPR吸收峰位于780 nm, 显示出了半峰宽窄、 对称性好的特性, 说明获得的材料尺寸具有均一性. 图1谱线b~h示出了GSH修饰的金纳米棒溶液在不同pH值下的等离子共振吸收曲线, 可以看到, pH从2.0至13.0的改变会明显影响金纳米棒的等离子共振吸收: 在酸性条件下(谱线b~e), 金纳米棒的LSPR吸收峰红移明显; 在碱性条件下(谱线g~h), LSPR吸收峰红移较小, 并且对称性降低, LSPR吸收峰的变化表明pH值会影响GSH修饰金纳米棒的聚集行为.
2.2 GSH修饰金纳米棒的形貌及电位分析
为了进一步证明GSH修饰的金纳米棒在不同pH下的聚集行为, 分别选择未修饰的金纳米棒及在pH值为2和12条件下GSH修饰的金纳米棒进行TEM表征(图2). 图2(A)为未修饰GSH的金纳米棒的TEM照片, 可见金纳米棒是随机分布的, 没有特殊的排列. 图2(B)是pH=2.0下GSH修饰的金纳米棒的组装排列照片, 可见金纳米棒以头对头方式分布, 与图1中在低pH下LSPR光谱红移明显相对应, 头对头的排列聚集实质增加了金纳米棒的长径比, 这会使金纳米棒的LSPR峰移动明显. 由图2(C)可见, 在pH=12.0条件下GSH-Au NRs是以侧面与侧面并排方式存在, 与图1的碱性条件下GSH修饰的金纳米棒吸收峰位移动红移不明显并且半峰宽展宽相对应. 在碱性条件下, 以肩并肩方式组装的金纳米棒使长径比范围宽化, 但长径比变化范围很小, 因此导致吸收峰位红移小, 但半峰宽宽化.
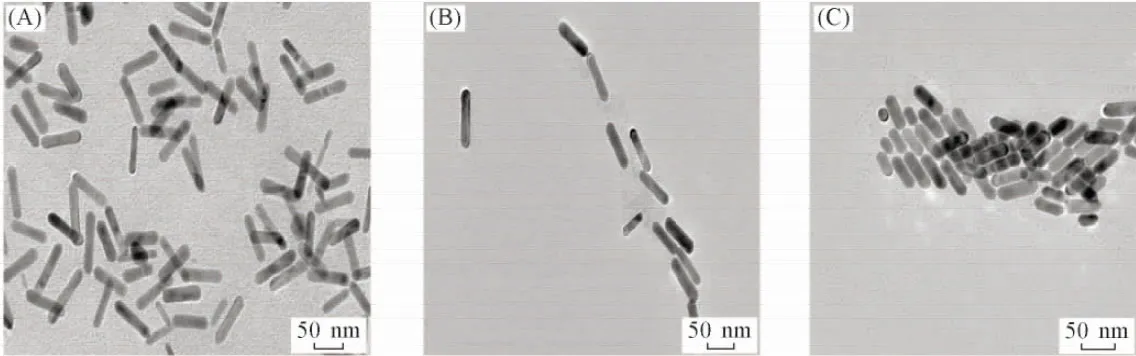
Fig.2 TEM images of pure Au nanorods(A), GSH-Au NRs at pH=2(B) and pH=12(C)

Fig.3 Surface zeta potential of GSH-Au NRs at different pH values
为进一步研究金纳米棒被GSH修饰后pH的改变对其表面电位的影响, 表征了不同pH值下样品的Zeta表面电位.Zeta电位的变化反映了GSH修饰金纳米棒表面电荷在不同pH下的变化(图3). 结果表明, 在不同pH值的溶液中, GSH修饰的金纳米棒的表面电位值发生了明显变化, 纯金纳米棒为酸性(pH=2), 此时带正电荷的CTAB分子的双层覆盖金纳米棒, 表面电位为+35 mV. 当金纳米棒与GSH结合后, GSH的氨基(—NH2)、 羧基(—COOH)官能团的电离常数在不同的pH值下会发生改变, GSH分子的结构也会改变, 所以表现出不同的表面电位. 在酸性条件下, 正电荷的CTAB分子的双层覆盖金纳米棒, GSH在酸性条件下也显示正电性, 此时CTAB与GSH形成排斥作用, 因此GSH会利用巯基官能团在CTAB少的头部位置组装, 形成了如图2(B)的头对头的组装方式; 随着pH值的增大, GSH逐渐转变为负电性, 此时溶液中GSH会首先与CTAB发生静电吸引, 从而使得金纳米棒的表面电位降为负值, 并形成图2(C)中肩并肩的组装方式.
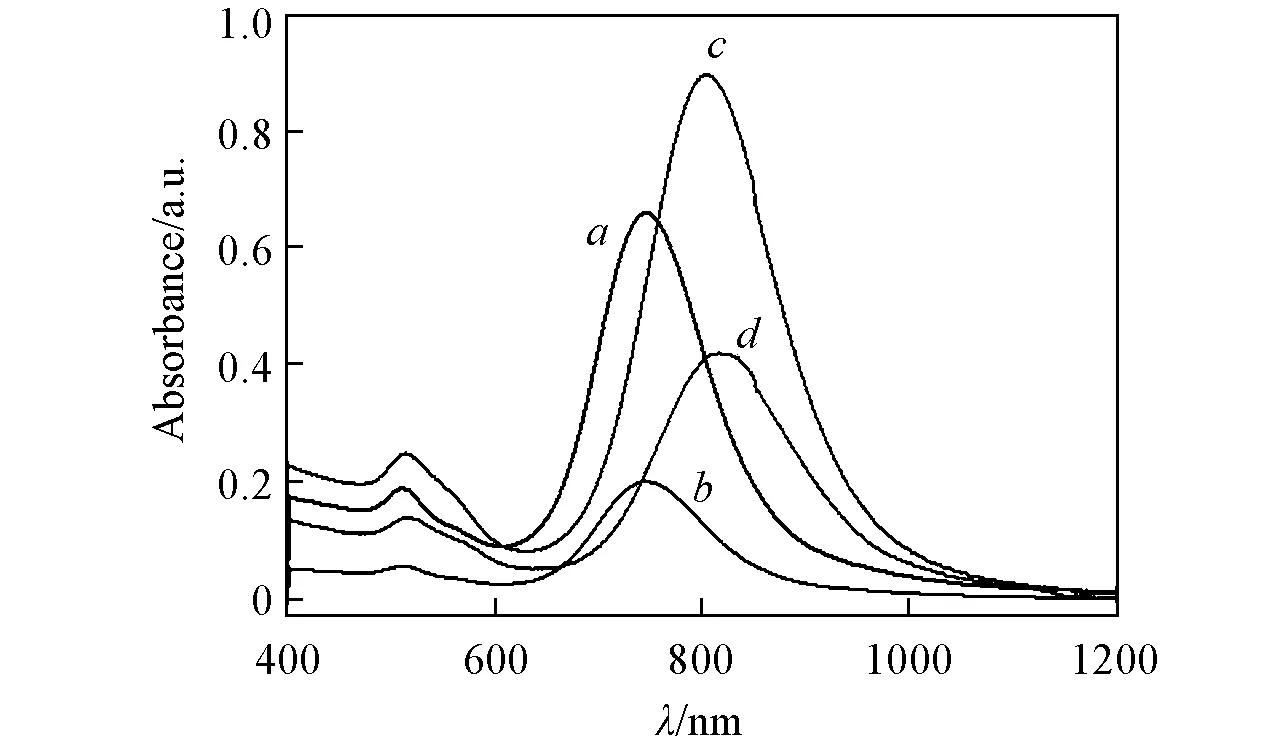
Fig.4 Absorption spectra of GSH-Au NRs with Cu2+ of different concentrations
2.3 Cu2+对GSH-Au NRs的聚集及光学特性的影响
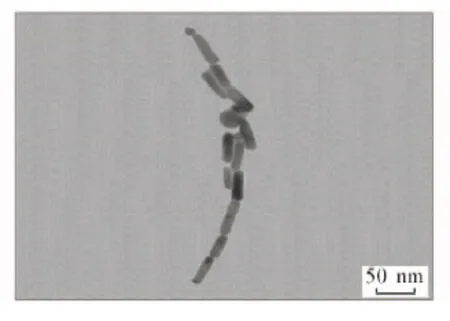
Fig.5 TEM image of GSH-Au NRs with 0.205 mmol/L Cu2+ at pH=5

Fig.6 Effects of different metal ions on LSPR absorption of GSH-Au NRs
谷胱甘肽的氨基与羧基能够分别与具有d轨道的过渡金属离子发生配位螯合作用, 因此选用不同的金属离子, 研究其与GSH-Au NRs的作用及对金纳米棒光学特性的影响. 首先选用对环境和健康具有重要影响的Cu2+作为研究对象, 研究了pH=5时不同浓度Cu2+对金纳米棒LSPR峰的影响. 将100 μL浓度为0.080, 0.205和0.425 mmol/L的Cu2+离子分别加入到3份1 mL相同浓度GSH修饰的金纳米棒溶液中, 结果发现, 加入Cu2+离子后, 金纳米棒的等离子体吸收峰发生了明显变化(图4). 图4谱线a是GSH修饰的金纳米棒在pH=5时的等离子共振吸收光谱, 其LSPR峰位在760 nm处; 加入少量Cu2+后(谱线b), 金纳米棒的LSPR吸收峰的峰位未发生明显红移; 当向溶液中加入0.205 mol/L Cu2+后(谱线c), LSPR峰位发生了明显红移(红移至850 nm); 继续加入铜离子(谱线d), LSPR吸收峰则不再继续移动, 这可能是在低浓度范围内, Cu2+可能引起少量的GSH修饰的金纳米棒聚集; 当Cu2+浓度继续增加, 使金纳米棒完全组装之后, 再加入铜离子则不能使LSPR吸收峰继续移动. 为了验证Cu2+的加入对金纳米棒组装的影响, 对加入0.205 mol/L Cu2+的金纳米棒进行形貌分析, 图5为加入Cu2+后金纳米棒的TEM照片. 在酸性条件下, 与GSH依靠静电相互作用引起金纳米棒松散的组装相比, 加入Cu2+后金纳米棒能够更加紧密地排布到一起, 这也证明了GSH的氨基中的N与羧基中的O的孤对电子能够与Cu2+的空d轨道形成强配位作用, 进而引起纳米棒的紧密排布.

Fig.7 Photothermal curves before and after irradiation(A) and the infrared images of Au NRs(B), GSH-Au NRs+0.01 mmol/L Cu2+(C) and GSH-Au NRs+1 mmol/L Cu2+(D) under laser irradiation
为了进一步验证金纳米棒复合材料对金属离子的选择性, 在pH=5时选取Ca2+, Zn2+, Mg2+, Mn2+, Na+, Fe3+, Al3+做比较(浓度均为0.205 mol/L), 结果如图6所示. 其它离子的加入使金纳米棒的等离子吸收峰红移较小, Cu2+引起吸收峰的移动明显强于其它离子. 其它离子峰位的移动可能是来源于溶液中介电常数的改变, 按照Mie理论[26], 溶液介电常数的变化会改变纳米材料的消光截面, 导致其吸收峰位红移, 通过比较也发现不同离子引起的吸收峰位变化基本一致, 证明了其红移是介电常数的改变引起的; 但Cu2+的加入除了会影响溶液介电常数外, 还会使GSH修饰的金纳米棒进一步聚集, 即GSH与Cu2+的螯合作用加强了金纳米棒的聚集排列, 导致了其吸收光谱的峰位明显移动.
通过上述表面等离子体共振吸收实验, 发现Cu2+对修饰谷胱甘肽的金纳米棒有明显影响, 这可能是由于Cu2+和GSH之间的配位作用引起金纳米棒的取向聚集. 为了进一步验证铜离子对金纳米棒光学性质的影响, 比较了未修饰GSH的金纳米棒与修饰GSH的金纳米棒与Cu2+作用后的光热转换效应. 图7示出了激光照射不同时间后溶液温度的变化.实验采用808 nm激光器对样品进行激发. 选用这一激发波长是考虑金纳米棒的表面等离子体共振吸收与光学激发之间存在共振效应, 能够产生强烈的光响应. 图7(B)~(D)分别对应纯金纳米棒、 GSH-Au NRs+0.01 mmol/L Cu2+和GSH-Au NRs+1 mmol/L Cu2+溶液在激光照射不同时间时的红外成像照片. 由图7(A)可见, 随着铜离子浓度的升高, 金纳米棒的温度升高幅度减小, 光热转换效应下降. 这可能是由于在金纳米棒与铜之间发生了电荷转移效应, 导致金纳米棒等离子体共振激发的电荷发生从金向铜的转移. 由图7(B)—(D)可以看出, 随着激光照射时间延长, 系统整体温度逐渐升高. 而且金纳米棒材料在复合Cu2+后, 体系光热转换效应明显下降, 更能说明Cu2+的加入对金棒纳米材料光热性质的影响.
3 结 论
制备了GSH修饰的金纳米棒, 根据金纳米棒材料的尺寸依赖及各向异性性质, 研究了Cu2+离子引起的金纳米棒的聚集程度、 排列方式和光学吸收等的变化. 结果显示, 在酸性条件下, GSH修饰的金纳米棒加入Cu2+离子后, 其表面等离子体共振吸收光谱发生明显红移, 而加入其它离子未导致金纳米棒的等离子体吸收峰明显红移. 分别利用纯金纳米棒和与铜离子作用的GSH修饰的金纳米棒进行了光热转换测试, 结果表明, 纯金纳米棒材料具有明显的光热转换效应, 但当铜离子与其作用后光热转换效应发生明显下降, 表明铜离子诱导金纳米棒的排布进而影响其光学特性具有选择性, 这为实现对未知金属的检测提供了一种新方法.
[1] Zhang W., Zhang H., Williams S. E., Zhou A.,Talanta, 2015, 132, 321—326
[2] Tsekenisa G., Filippidoub M. K., Chatzipetrouc M., Tsoutib V., Zergiotic I., Chatzandroulis S.,SensorsandActuatorsB, 2015, 208, 628—635
[3] Schneider E., Clark D. S.,Biosens.Bioelectron., 2013, 39, 1—13
[4] Turnlund J. R.,Am.J.Clin.Nutr., 1998, 67, 960—964
[5] Yuan C., Zhang K., Zhang Z., Wang S.,Anal.Chem., 2012, 84, 9792—9801
[6] Fu X., Lou T., Chen Z., Lin M., Feng W., Chen L.,ACSAppl.Mater.Interfaces, 2012, 4, 1080—1086
[7] Wang Y., DePrince A. E., Gray S. K., Lin X. M., Pelton M.,J.Phys.Chem.Lett., 2012, 1, 2692—2698
[8] Nie Z., Fava D., Kumacheva E., Zou S., Walker G. C., Rubinstein M.,Nat.Mater., 2007, 6, 609—614
[9] Thomas K. G., Barazzouk S., Ipe B. I., Joseph S. T. S., Kamat P. V.,J.Phys.Chem.B, 2004, 108, 13066—13068
[10] Varghese N., Vivekchand S. R. C., Govindaraj A., Rao C. N. R.,Chem.Phys.Lett., 2008, 450, 340—344
[11] Moussawi R. N., Patra D.,J.Phys.Chem.C, 2015, 119, 19458—19468
[12] Lu L.L., Xia Y. S.,Anal.Chem., 2015, 87, 8584—8591
[13] Wang J., Dong B., Chen B., Xu S., Zhang S., Yu W., Xu C.X., Song H.W.,DaltonTrans., 2013, 42, 11548—11558
[14] Thomas K. G., Barazzouk S., Ipe B. I., Joseph S. T. S., Kamat P. V.,J.Phys.Chem.B, 2004, 108, 13066—13068
[15] Varghese N., Vivekchand S. R. C., Govindaraj A., Rao C. N. R.,J.Chem.Phys.Lett., 2008, 450, 340—344
[16] Joseph S. S. T., Ipe B. I., Pramod P., Thomas K. G.,J.Phys.Chem.B, 2005, 110, 150—157
[17] Nakashima H., Furukawa K., Kashimura Y., Torimitsu K.,Chem.Commun., 2007, 1080—1082
[18] Deng J. J., Yu P., Wang Y. X., Yang L. F., Mao L. Q.,Adv.Mater., 2014, 26, 6933—6943
[19] Sudeep P. K., Joseph S. T. S., Thomas K. G. S.,J.Am.Chem.Soc., 2005, 127, 6516—6517
[20] Zhang Z.Y., Chen Z. P., Qu C. L., Chen L. X.,Langmuir, 2014, 30, 3625—3630
[21] Chai F., Wang C. G., Wang T. T., Li L., Su Z. M.,ACSNano, 2010, 2, 1466—1470
[22] Niidome T., Akiyama Y., Shimoda K., Kawano T., Mori T., Katayama Y., Niidome Y.,Small, 2008, 4, 1001—1007
[23] Kou X. S., Zhang S. Z., Yang Z., T sung C. K., Stucky G. D., Sun L. D., Wang J. F., Yan C. H.,J.Am.Chem.Soc., 2007, 129, 6402—6404
[24] Xiao M. D., Chen H. J., Ming T., Shao L., Wang J. F.,J.Am.Chem.Soc., 2010, 11, 6565—6572
[25] Muhammed M. A. H., Döblinger M., Rodríguez-Fernndez J.,J.Am.Chem.Soc., 2015, 137, 11666—11677
[26] Staveren H. J. V., Moes C. J. M., Marie J. V., Prahl S. A., Gemert M. J. C., Appl. Opt., 1991, 30, 4507—4514
(Ed.: F, K, M)
Preparation of GSH-Modified Au Nanorods and Their Interaction with Copper Ions†
† Supported by the National Natural Science Foundation of China(Nos.11174047, 11374046).
ZHANG Lingyue2, CHI Yanan1, SHAN Guiye1*, CHEN Yanwei1, LIU Na2
(1.SchoolofPhysics,NortheastNormalUniversity,Changchun130024,China;2.CollegeofEnvironmentandResources,JilinUniversity,Changchun130012,China)
Au nanorods(Au NRs) modified by glutathione(GSH) were prepared. Based on the dependence of localized surface plasmon resonance(LSPR) peak shift on their arrangement, the structure and optical properties of GSH-modified Au NRs was studied at different pH conditions. At pH=5, some metal ions were chosen to detect the effect of their interaction with GSH-Au NRs on the LSPR peak of Au NRs. The results demonstrate that Cu2+can obviously induce red shift of LSPR peak comparing with other metal ions. The reason is the rearrangement of Au NRs induced by Cu2+. Meanwhile, the photothermal experiment for pure Au NRs and GSH-Au NRs with copper ions were carried out to detect the effect of copper ions on optical properties of Au NRs. Comparing with pure Au NRs, GSH-Au NRs with copper ions decreased the efficiency of phothothermal conversion. During photothermalcoversion process, copper maybe capture the electron of Au NRs and decrease the efficiency of nonirradiation. So, Au NRs modified by GSH show the selective detection for Cu2+. The results here maybe provide a new method for detection of heavy metal ions.
Au Nanorods; Glutathione(GSH); Cu2+ion; Localized surface plasmon resonance(LSPR) absorption; Inorganic nanocomposite
2016-06-06.
日期: 2016-06-30.
国家自然科学基金(批准号: 11174047, 11374046)资助.
10.7503/cjcu20160406
O614
A
联系人简介: 单桂晔, 女, 博士, 副教授, 主要从事功能纳米材料的应用研究. E-mail: shangy229@nenu.edu.cn
