XE L OX方案治疗索拉菲尼耐药晚期原发性肝癌的临床疗效及预后生存分析
2016-12-21袁云
袁云
(江西省新余第二医院肿瘤科,江西 新余 338000)
XE L OX方案治疗索拉菲尼耐药晚期原发性肝癌的临床疗效及预后生存分析
袁云
(江西省新余第二医院肿瘤科,江西 新余 338000)
目的 探讨XELOX方案治疗索拉菲尼耐药晚期原发性肝癌的临床疗效及对预后生存的影响。方法 选取2012年1月至2013年1月收治的经单纯索拉菲尼治疗耐药的原发性肝癌患者64例,均采用XELOX方案治疗,其中肝细胞癌50例为A组,胆管细胞癌10例为B组,肝细胞癌/胆管细胞癌混合型4例为C组。采用系统性回顾法分析患者的临床和随访资料,统计所有患者在予以XELOX方案治疗过程中血清甲胎蛋白(AFP)水平及合并慢性乙肝患者其HBV DNA水平的变化,并评价XELOX方案治疗后患者的临床疗效、不良反应及预后生存情况。结果 64例患者中,疾病总控制率为84.38%(54/64),且在乙型肝炎患者中4例患者HBV DNA被再次激活,予相关抗病毒治疗后恢复正常,甲胎蛋白下降28例(43.75%)。不良反应最严重的为Ⅰ~Ⅱ级手足皮肤反应,共12例(18.75%),除肝功能损害给予相关药物治疗好转外,其他不良反应在停药数天后均自行消失,且均可耐受不良反应。所有患者的生活质量均良好,其中肝细胞癌患者预后最好,其他2种类型尚可,差异无统计学意义(P>0.05);中位无进展生存期为5.84个月,中位总生存期为11.94个月。结论 XELOX方案治疗对索拉菲尼耐药的晚期原发性肝癌临床疗效良好,预后生存率及生活质量均较好,可作为临床治疗原发性肝癌的一线治疗方案。
XELOX方案;索拉菲尼;晚期原发性肝癌;耐药
原发性肝癌是指肝脏上皮组织或间叶组织发生恶性病变,相关数据表明,其中90%为肝细胞癌,少部分为胆管细胞癌或混合性肝癌[1]。随着肝癌患病率不断上升,其已成为世界范围内的常见恶性肿瘤之一[2]。由于原发性肝癌起病隐匿,大部分患者在明确诊断时已错失最佳手术时机。索拉菲尼是唯一被多国批准用于不可手术切除的晚期肝癌的多靶点治疗药物,但长期应用会产生耐药性,导致临床有效率降低,疾病进展加快,预后生存期缩短,因此寻找更有效、安全的新药物治疗原发性肝癌已成为临床一个值得重视的问题[3-5]。本研究中通过观察采用奥沙利铂为主的XELOX方案治疗原发性肝癌患者的临床效果,探讨了XELOX方案对索拉菲尼耐药的晚期原发性肝癌的临床疗效及其预后生存的影响。现报道如下。
1 资料与方法
1.1 一般资料
纳入标准:符合2005年世界卫生组织(WHO)制订的原发性肝癌诊断标准[6];给予索拉菲尼治疗后病情未见好转,甚至进展;行影像学检查示有肿瘤且病灶直径不小于1 cm;患者及其家属签署知情同意书。
排除标准:接受除索拉菲尼以外的化学治疗(简称化疗);自愿退出本研究。
病例选择与分组:选择我院2012年1月至2013年1月收治的原发性肝癌患者64例,其中男38例,女26例;年龄34~75岁,平均(52.02±9.72)岁;合并乙型肝炎22例。将64例患者分为3组,肝细胞癌50例为A组,胆管细胞癌10例为B组,肝细胞癌/胆管细胞癌混合型4例为C组。
1.2 方法
所有患者既往均接受索拉菲尼治疗,确诊使用该药物患者出现病情进展后使用XELOX方案,包括注射用奥沙利铂(江苏恒瑞医药股份有限公司,国药准字H20093811,规格为每瓶50 mg)130 mg/m2,静脉滴注,第1天;卡培他滨(Hoffmann-La Roche Inc,国药准字J20080101)850~1 250 mg/m2,2次/日,静脉滴注,第1~14天;每3周重复1次,3周为1个疗程,共治疗8个疗程。观察并记录在治疗过程中出现的不良反应,化疗前后患者均行血常规、肝肾功能等检查情况。出院后,进行门诊复查或电话随访,随访截至2016年5月31日。
1.3 观察指标及疗效判定标准
治疗结束后评价患者的临床疗效,记录治疗过程中发生的不良反应及评价随访患者的预后生存质量及生存率。
临床疗效判定标准:采用实体瘤客观评价疗效标准(RECIST1.1)[7],分为完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)和疾病进展(PD),疾病控制(DCR)=CR+PR+SD。
不良反应:参照NCI CTC3.0标准[8]评价,分为Ⅰ~Ⅳ级,级别越高,程度越高。
生活质量评分(KPS)标准[9]:采用WHO的KPS评分表进行评价,量体包括躯体功能、健康感觉、认知水平、角色功能、情感功能、社会功能。其中每项总分为100分,得分越高,生活质量越好。
生存情况:可分为总生存期(OS),从化疗开始至死亡当天或随访截止;无进展生存期(PFS),从化疗开始至首次发现肿瘤进展或死亡时间。
1.4 统计学处理
采用 SPSS 18.0统计软件包处理。计量资料以均数±标准差(s)表示,采用 t检验;计数资料以百分比描述,采用 χ2检验;不同化疗方案晚期非小细胞肺癌的生存率采用Kaplan-Meier法估计,并采用Log-rank检验进行比较。P<0.05为差异有统计学意义。
2 结果
2.1 临床疗效
64例患者中,疾病总控制率为84.38%(54/64),明显良好,且在4例乙型肝炎患者中HBV DNA被再次激活,给予相关抗病毒治疗后恢复正常,甲胎蛋白(AFP)下降者28例(43.75%)。详见表1。
2.2 不良反应
64例患者中,不良反应最严重的为Ⅰ~Ⅱ级手足皮肤反应,共12例(18.75%),其次为Ⅰ~Ⅱ级周围神经毒性反应,共9例(14.06%),除肝功能损害给予相关药物治疗好转外,其他不良反应在停药数天后均自行消失,所有患者均可耐受不良反应。详见表2。
2.3 生活质量情况
所有患者生活质量均良好,其中肝细胞癌患者预后最好,其他2种类型尚可,差异无统计学意义(P>0.05)。详见表3。
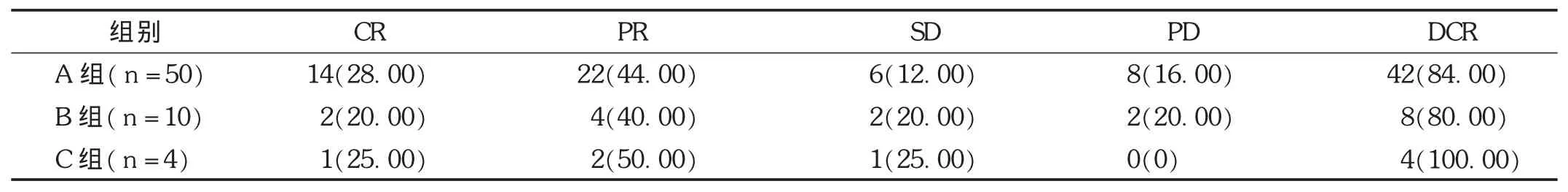
表1 3组患者临床疗效比较[例(%)]

表2 3组患者不良反应发生情况比较[例(%)]
表3 3组患者KPS评分比较(s,分)
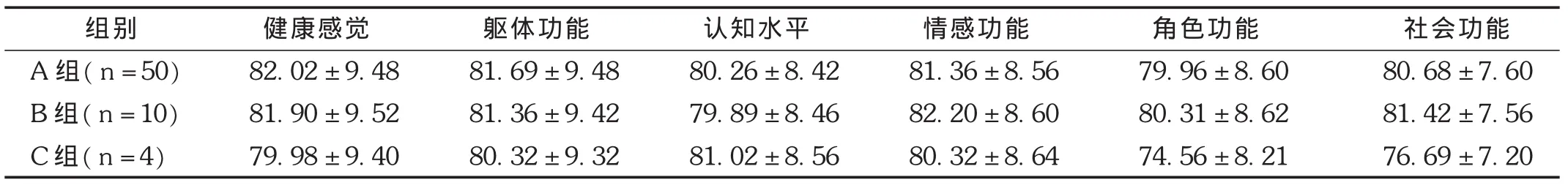
表3 3组患者KPS评分比较(s,分)
组别A组(n=50)B组(n=10)C组(n=4)健康感觉82.02±9.48 81.90±9.52 79.98±9.40躯体功能81.69±9.48 81.36±9.42 80.32±9.32认知水平80.26±8.42 79.89±8.46 81.02±8.56情感功能81.36±8.56 82.20±8.60 80.32±8.64角色功能79.96±8.60 80.31±8.62 74.56±8.21社会功能80.68±7.60 81.42±7.56 76.69±7.20
2.4 预后分析
随访截至2016年5月31日,未出现失访,随访率为100.00%;中位随访时间10.12个月(2.12~22.26个月)。共死亡54例(84.38%),存活10例(15.62%)。中位PFS为5.84个月(95%CI:5.52~7.84),5个月占50.82%,12个月占 19.26%;中位 OS为 11.94个月(95%CI:9.46~12.66),12个月占46.82%,24个月占20.64%。
3 讨论
研究表明,原发性肝癌是临床常见高发的消化系统肿瘤,在全世界的发病率呈逐年上升趋势,我国尤为常见,在我国肿瘤致死病因中,仅次于肺癌,位居第2位,且该疾病预后较差,自然病程较短,已成为严重影响居民健康生活的公共卫生问题[10]。早中期患者的最佳治疗手段为手术切除、肝移植及射频消融术,晚期患者更合适保守治疗。随着药物治疗时间的延长,患者对所用药物逐渐产生耐药性,大大降低其临床疗效,影响预后生存,因此探索新型的有效、安全的药物治疗对于具有耐药性的原发性肝癌患者尤为重要。
国内外研究表明,XELOX方案在治疗原发性肝癌临床疗效良好[11]。索拉菲尼目前在临床为治疗晚期原发性肝癌的一线治疗药物,是一种多靶点、多激酶抑制剂,具有抑制肿瘤新生血管形成和抑制肿瘤细胞增殖的双重作用,但随着使用时间的延长及机体内机制的改变,索拉菲尼治疗原发性肝癌的临床疗效逐渐减弱,预后不良较多。XELOX方案由奥沙利铂联合卡培他滨使用特定用量用法治疗原发性肝癌患者的一种化疗方案[12]。奥沙利铂属第3代铂类化合物,化学名为左旋反式二氨环己烷草酸铂,国际通用名为草酸铂,具有细胞毒作用,对多种肿瘤细胞均有抗肿瘤活性[13]。卡培他滨是抗代谢氟嘧啶脱氧核苷氨基甲酸酯类药物,可在体内转变成5-氟尿嘧啶,通过抑制细胞分裂和干扰RNA和蛋白质的合成对治疗肿瘤有一定疗效[14]。
本研究结果表明,使用XELOX方案治疗对索拉菲尼治疗后耐药的原发性肝癌患者临床疗效良好,可有效降低患者AFP水平,但在治疗过程中对合并乙型肝炎患者有激活其HBV DNA可能,提示在治疗过程中应密切监测HBV DNA和肝功能的变化情况。手足皮肤不良反应较多见,除肝功能损害给予相关药物治疗好转外,其他不良反应均在停药数天后自行消失,且患者均可耐受。另一方面,此方案治疗的原发性肝癌患者也有较好的预后效果,近期生存率较高,生活质量较好,符合既往研究报道结果[15]。
综上所述,XELOX方案对索拉菲尼治疗耐药的原发性肝癌患者临床疗效良好,不良反应均可耐受,预后生存率及生活质量均较良好,可考虑为临床治疗原发性肝癌的一线治疗方案。
[1]Kim AY,Jeong WK.Intraductal malignant tumors in the liver mimicking cholangiocarcinoma:Imaging features for differential diagnosis[J].Clinical& Molecular Hepatology,2016,22(1): 192-197.
[2]汤桂丽.4种肿瘤标志物联合检测对原发性肝癌的早期诊断价值[J].中国药业,2015,24(7):127-128.
[3]吕 毅,郭 卉.索拉非尼在中晚期肝细胞癌中的应用价值[J].中华肝脏外科手术学电子杂志,2014,2(4):1-3.
[4]王 程,王宁菊.索拉菲尼治疗晚期原发性肝癌患者的临床疗效及毒副反应观察[J].宁夏医学杂志,2015,37(12):1 139-1 140.
[5]于志海,成 科,王海涛.奥沙利铂联合表柔比星介入治疗原发性肝癌的临床研究[J].中华全科医学,2016,14(2): 326-327.
[6]冉广汉.康莱特联合化学治疗药物腹腔循环热灌注治疗原发性肝癌伴恶性腹腔积液60例[J].中国药业,2015,24(10): 125-127.
[7]石力夫,雷 振.不同疗效评价标准对结肠癌肝转移瘤疗效评价的一致性研究[J].解放军医学院学报,2014,35(1): 25-27.
[8]彭 媛,王程程,唐 利,等.应用Bradford Hill标准评价西格列汀与消化系统不良反应的因果关系[J].中国医院药学杂志,2014,34(16):1 414-1 417.
[9]武敬参,鄢秀英,王 羽,等.健康调查简表与世界卫生组织生存质量测定量表简表在评价肺结核患者生存质量中的应用比较[J].华西医学,2016,30(3):463-466.
[10]张 ,曲春枫,任建松,等.中国肝癌发病与死亡数据集[J].中华肿瘤杂志,2015,36(9):258-259.
[11]王 锋,秦叔逵,华海清,等.含奥沙利铂化疗方案治疗对索拉非尼耐药的晚期原发性肝癌的临床观察[J].临床肿瘤学杂志,2014,19(3):226-230.
[12]杨 兰,邓 颖,胡洪林,等.XELOX方案与FOLFOX4方案治疗晚期结直肠癌疗效比较[J].武警医学,2014,25(3): 221-223.
[13]Hu F,Fei W,Wang Y,et al.EGCG synergizes the therapeutic effect of cisplatin and oxaliplatin through autophagic pathway in human colorectal cancer cells[J].Journal of Pharmacological Sciences,2015,128(1):27-34.
[14]杨德君,朱振新,杨光达,等.RNA干扰沉默细胞分裂周期蛋白42对耐药胰腺癌侵袭转移的影响[J].中华普通外科杂志,2014,29(5):364-365.
[15]钟 锋,程新生,王金重,等.原发性肝癌自发破裂出血患者近期及远期预后因素分析[J].中华肝脏外科手术学电子杂志,2016,5(2):95-100.
Clinic Efficacy and Prognosis Analysis of Xelox on Sorafenib Drug Treating Fast Advanced Primary Hepatic Cancer
Yuan Yun
(Department of Oncology,Xinyu Second Hospital,Xinyu,Jiangxi,China 338000)
Objective To investigate the clinic efficacy and prognosis analysis of Xelox on sorafenib drug treating fast advanced primary hepatic cancer.Methods 64 cases failed by simple sorafenib in the hospital from January 2012 to January 2013 were selected.All patients were treated with Xelox regimen.Among them,50 cases of hepatocellular carcinoma were group A,10 cases of cholangiocarcinoma were group B,and 4 cases of hepatocellular carcinoma/cholangiocarcinoma were group C.Retrospective analysis was conducted on the clinical and follow-up patient data.The AFP level and HBV DNA changes of patients after treatment of Xelox were recorded,the clinic efficacy,adverse reactions and prognosis of the patients were evaluated.Results After treatment,the total control rate of all patients was 84.38% (54/64);4 cases with hepatitis B,the HBV DNA of were reactivate and returned to normal after antivirus treatment;28 cases(43.75%)had AFP declination.During treatment,the most severe adverse reaction wasⅠ-Ⅱlevel hand-foot skin reaction(12 cases,18.75%);besides the liver function lesion improvement after relevant medication,other adverse reactions disappeared a few days after the stop of medication,and were all tolerable adverse reactions.The prognosis of the patients with hepatocellular carcinoma improved best,other 2 types were fair,and the difference was not statistic significant(P>0.05).The total meso-position PFS was 5.84 months,OS meso-position was 11.94 months.Conclusion Xelox achieves better clinic effect on sorafenib drug treating fast advanced primary hepatic cancer,and the survival rate,life quality are better,which can be seen as a first therapeutic schedule for primary liver cancer.
Xelox scheme;sorafenib;advanced primary hepatic cancer;drug resistance
R969.4;R979.1
A
1006-4931(2016)21-0052-03
袁云(1980-),男,大学本科,主治医师,主要从事肿瘤内科诊断与治疗,(电子信箱)lwbjb5000@163.com。
2016-07-13)
