基准草酸钠标定高锰酸钾标准溶液方法的讨论
2016-12-20佟桂梅冯小红王雪梅
佟桂梅,冯小红,王雪梅,韩 灵,刘 瑾
(唐山三友化工股份有限公司 质量监督部,河北唐山 063305)
科 学 试 验
基准草酸钠标定高锰酸钾标准溶液方法的讨论
佟桂梅,冯小红,王雪梅,韩 灵,刘 瑾
(唐山三友化工股份有限公司 质量监督部,河北唐山 063305)
对基准草酸钠标定高锰酸钾标准溶液的原方法和实验方法进行对比讨论,目的仅在于配出精准溶液,确保优质分析。
草酸钠基准溶液;配制;高锰酸钾标准溶液;标定;对比
基准草酸钠,用于高锰酸钾标准溶液的标定,此两种标准溶液应用于水质分析中化学耗氧量(COD)的测定,在日常工作中,用原用方法基准草酸钠标定高锰酸钾标准溶液时常出现数据不平行的现象,致使滴定次数增加,不能及时标定出高锰酸钾标准溶液;称取草酸钠基准试剂的次数增加,浪费了草酸钠基准试剂,增加了成本。为此,我们进行了配制草酸钠基准溶液的方法实验,并且为验证准确度增加了基准溶液对比标定,下面把原用方法和实验方法加以对比介绍。
1 原用方法
1.1 仪器及试剂
电烘箱(105~110 ℃),分析天平(万分之一),50 mL棕色酸式滴定管,250 mL三角瓶,100 mL量筒,温度计,电炉,8+92硫酸。
1.2 标定方法
称取0.2 g(精确至0.0001 g)于105~110 ℃电烘箱中干燥至恒重的草酸钠基准试剂,溶于100 mL硫酸溶液(8+92)中,用配制好的高锰酸钾标准滴定溶液[C(1/5KMnO4)=0.1 mol/L]滴定,近终点时,加热至约65 ℃,继续滴定至溶液呈粉红色,保持30 s不褪色为终点。同时做空白试验。
计算公式:
(1)
式中:V滴—— 50 mL滴定管校正值,+0.01 mL;V空——空白试验消耗高锰酸钾体积数, 0.00 mL;
VKMnO4——滴定消耗高锰酸钾体积数,mL;
m——称取草酸钠基准试剂质量,g;
0.06700——草酸钠摩尔质量, kg/mol。
结果如表1。
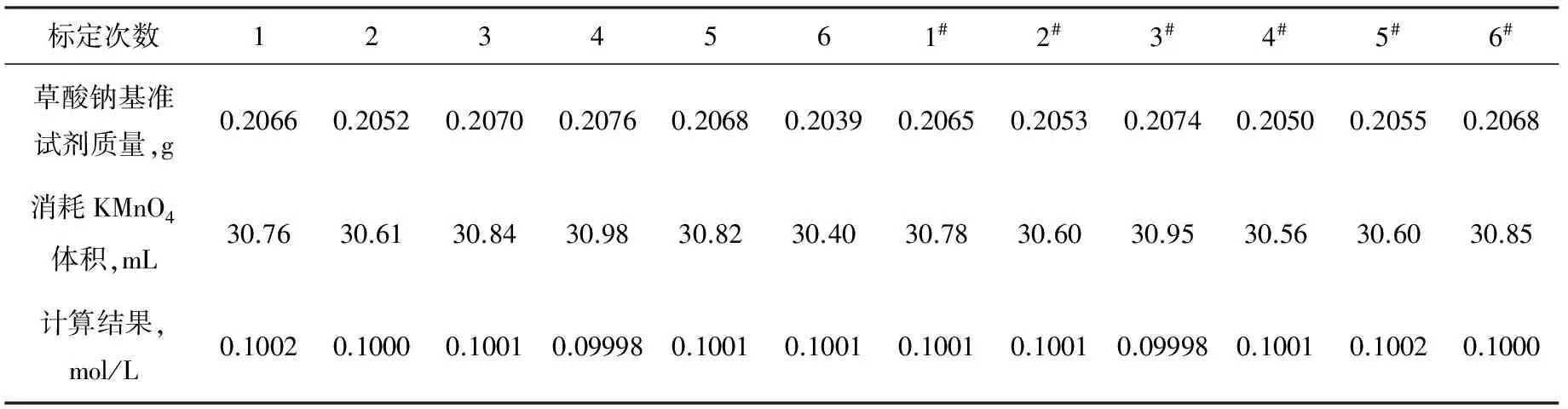
表1 原用方法草酸钠基准试剂标定高锰酸钾标准溶液结果
由表1可得:分析数据不易平行(工作要求严格:两次平行测定结果之差不大于0.0002 mol/L),平行测定次数增加,除去不平行数据,高锰酸钾标准溶液的浓度为0.1001 mol/L,即C(1/5KMnO4)=0.1001 mol/L。
2 实验方法
此方法分两部分,一是C(1/2Na2C2O4)草酸钠基准溶液的配制:包括烘干、恒重、称量、溶解样品,二是草酸钠基准溶液对比标定,共需要一周时间。
2.1 C(1/2Na2C2O4)草酸钠基准溶液的配制
2.1.1 使用仪器
电烘箱(105~110 ℃),分析天平(万分之一),大瓷坩埚1个,小瓷坩埚4个,1 000 mL容量瓶4个,漏斗4个, 玻璃棒4个,洗瓶4个。
2.1.2 操作步骤
称取Na2C2O4基准试剂约30 g于大瓷坩埚中,放在105~110 ℃电烘箱中烘至恒重,准确称取4份Na2C2O4基准试剂各6.7 g(精确至0.0001 g),用水溶解,移入1000 mL容量瓶中,稀释至刻度,摇匀,备用。
2.1.3 烘干、恒重、称量
称量记录如表2。
注意事项:
①每天操作时间点要保持一致,包括开、关烘箱,在烘箱中取放瓷坩埚和样品,在天平室的称量时间等。
②烘箱温度升到110 ℃后再放坩埚和样品,并且烘箱在烘基准试剂时,不能同时烘其它物品。
③控制好天平室温度18~26 ℃,湿度65%~75%,每次称量时温度、湿度必须保持一致。
④称量前后调节天平,看指针是否在“0”点,并且在称量时读数时间差要保持一致。
⑤烘干、恒重、称量4个小瓷坩埚时,记住顺序,每天依次完成。

表2 称量记录
由表2可得:
①小瓷坩埚恒重后才能加样品,样品恒重后才能溶解样品,两次称重之差不大于0.0002 g。
②向4个小瓷坩埚加样品时,尽量做到一次加成,以后称量时最好不要再加、减样品,避免称量质量波动大。并且向4个小瓷坩埚加样品的克数,应保证最后恒重结果在恒重误差范围以内。
2.1.4 溶解样品
先用洗瓶沿玻璃棒缓缓加少量蒸馏水于小瓷坩埚中,不断搅拌,若一次加水不能溶解,先将上部溶液通过漏斗转入1 000 mL容量瓶中,再加少量水溶解,直至草酸钠全部溶解,洗涤小瓷坩埚3~4次,洗涤液转入容量瓶中,加蒸馏水至容量瓶的刻度线以下,第二天基准溶液对比标定时再定容、摇匀、备用。
2.2 C(1/2Na2C2O4)草酸钠基准溶液对比标定
为了验证新配的草酸钠基准溶液准确度,用一支草酸钠粉剂摩尔标准,溶于500 mL容量瓶中,制成C(1/2Na2C2O4)(标)=0.1000 mol/L草酸钠标准溶液,以此为标准,标定KMnO4标准溶液。再用新配的C(Na2C2O4)(新)=0.1000 mol/L草酸钠基准溶液标定此KMnO4标准溶液,二者结果对比。
2.2.1 仪器及试剂
25 mL棕色酸式滴定管,20 mL移液管,250 mL三角瓶,100 mL量筒,温度计,电炉,8+92 硫酸。
2.2.2 标定原理
草酸钠和高锰酸钾在酸性(硫酸)条件下发生氧化还原反应
2.2.3 标定方法
用移液管准确移取20.00 mL草酸钠基准溶液于250 mL三角瓶中,加8+92 H2SO4100 mL,在电炉上低温预热(三角瓶内壁微见有水珠,不太烫手为止),用高锰酸钾标准滴定溶液[C(1/5KMnO4)=0.1 mol/L]滴定近终点时,加热至约70 ℃,继续滴定至溶液呈粉红色,保持30 s不褪色为终点。同时做空白试验。
注意:溶液温度低于60 ℃时,草酸钠与高锰酸钾反应速度慢,为了加速反应,须将溶液温度加热至70 ℃左右,不可太高,大于90 ℃时将引起H2C2O4的分解:
H2C2O4=CO2↑+CO↑+H2O
2.2.4 用C(1/2Na2C2O4)(标)=0.1000 mol/L草酸钠标准溶液标定KMnO4标准溶液
计算公式:
(2)
式中:V移——20 mL移液管校正值,-0.010 mL;V滴——25 mL滴定管校正值,+0.01 mL;V空——空白试验消耗高锰酸钾体积数,0.00 mL;
VKMnO4——滴定消耗高锰酸钾体积数,mL;
C(1/2Na2C2O4)——草酸钠标准溶液摩尔浓度,C(1/2Na2C2O4)(标)=0.1000 mol/L。
结果如表3。
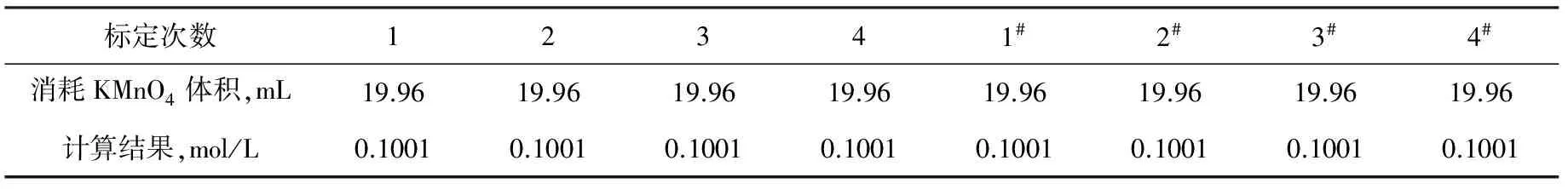
表3 草酸钠标准溶液标定KMnO4标准溶液结果
由表3可得:用C(1/2Na2C2O4)(标)=0.1000 mol/L草酸钠标准溶液标定KMnO4标准溶液的浓度为0.1001 mol/L,即C(1/5KMnO4)=0.1001 mol/L。
2.2.5 再用新配的C(1/2Na2C2O4)(新)=0.1000 mol/L草酸钠基准溶液标定此KMnO4标准溶液
按公式(2)计算,结果如表4。
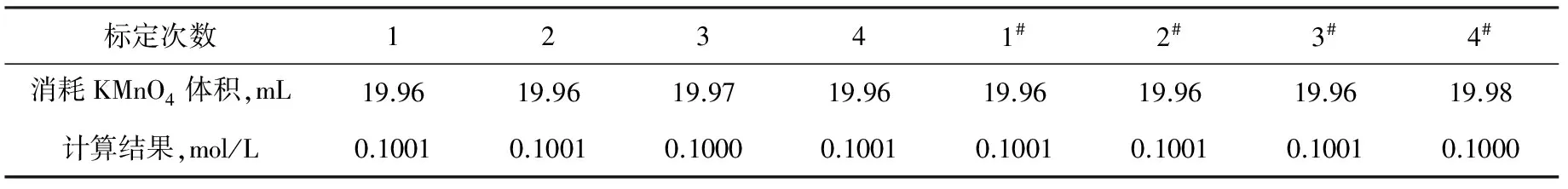
表4 草酸钠基准溶液标定KMnO4标准溶液结果
由表4可得:用新配的C(1/2Na2C2O4)(新)=0.1000 mol/L草酸钠基准溶液标定此KMnO4标准溶液的浓度为0.1001 mol/L,即C(1/5KMnO4)=0.1001 mol/L ,且结果平行。
3 结果分析
①表2中烘干、恒重、称量严格按照规定操作,结果准确可靠。
②表3和表4结果相同,说明新配的草酸钠基准溶液浓度和草酸钠粉剂摩尔标准溶液浓度相同,都是0.1000 mol/L ,即C(1/2Na2C2O4)(新)=0.1000 mol/L,结果准确可靠。
③表1和表4中,虽然标定的高锰酸钾标准溶液浓度都是0.1001mol/L,即C(1/5KMnO4)=0.1001 mol/L,但是表1中分析数据不易平行,平行测定次数增加,表4中数据平行可靠,证明此方法可行。
4 结 语
通过对基准草酸钠标定高锰酸钾标准溶液的原方法和实验方法的对比讨论,实验方法使标准溶液配制更加精准,分析数据准确可靠,能提高效率,降低草酸钠试剂成本,及时有效指导生产。
TQ014;O655.2
A
1005-8370(2016)03-12-04
2016-04-07
佟桂梅(1969—),唐山三友化工股份有限公司质量监督部技术员,化工工程师。
