右美托咪定鞘内注射对老年患者硬膜外麻醉效果及术后认知功能的影响
2016-12-17姜景卫鲁华荣毛桂琴何利方毛晨俊
姜景卫 鲁华荣 毛桂琴 何利方 毛晨俊
(江山市人民医院麻醉科,浙江 江山 324100)
右美托咪定鞘内注射对老年患者硬膜外麻醉效果及术后认知功能的影响
姜景卫 鲁华荣 毛桂琴 何利方 毛晨俊
(江山市人民医院麻醉科,浙江 江山 324100)
目的 探讨右美托咪定鞘内注射对老年患者硬膜外麻醉效果及术后认知功能的影响。方法 将60例择期老年手术患者随机分为右美托咪定组(D组)和对照组(C组),每组30例,采用腰硬联合麻醉包于L3、L4间隙行硬膜外穿刺,针内针法行鞘内注射,D组注射右美托咪定12 μg,C组注射等容量的生理盐水,然后头向硬膜外腔置管3.5 ml,平卧后先注入2%利多卡因3 ml,5 min后无全脊麻症状后再注入0.75%罗哌卡因12 ml,记录麻醉前(T0)、注入罗哌卡因后5 min(T1)、10 min(T2)、20 min(T3)、30 min(T4)、60 min(T5)的平均血压(MBP)、心率(HR)、血氧脉搏饱和度(SpO2)、脑电双频指数(BIS);观察两组感觉和运动阻滞的起效时间及持续时间,最高阻滞平面、达到最高阻滞平面所需时间以及并发症发生情况;分别于术前1 d(D0)、术后1 d(D1)、3 d(D2)、7 d(D3)对患者进行简易精神状态量表(MMSE)评分。结果 与C组相比,D组硬膜外麻醉感觉阻滞起效时间缩短,感觉及运动持续时间延长;D组达到最高阻滞平面高且所需时间短(P<0.05)。与T0及C组相比,D组HR、BIS在T1~T5各时间点均降低(P<0.05)。与D0时及D组比较,C组在D1,D2时MMSE评分降低(P<0.05)。结论 右美托咪定鞘内注射能缩短硬膜外麻醉感觉阻滞起效时间,延长感觉及运动持续时间,并能改善老年患者术后认知功能。
右美托咪定;脊髓注射;硬膜外麻醉;术后并发症;记忆障碍
右美托咪定(Dex)作为一种新型高效的α2肾上腺素受体激动剂,具有镇静、催眠、镇痛作用,还有抑制交感神经活性等效应,并且对呼吸和循环系统的影响很小,已广泛用于临床〔1,2〕。有研究表明,Dex鞘内注射能增强脊麻效果〔3〕;另有研究表明,Dex静脉输注能改善老年全麻患者的术后认知功能〔4〕。本研究通过观察鞘内注射Dex对老年患者硬膜外麻醉效果及术后认知功能的影响。
1 资料与方法
1.1 一般资料 选择江山市人民医院2012年9月至2013年12月择期老年手术患者60例,男26例,女34例,年龄60~75岁,体重41~72 kg,美国麻醉协会(ASA)Ⅰ或Ⅱ级,根据随机数字表法随机分为Dex组(D组)和对照组(C组),每组30例。排除标准:有椎管内麻醉禁忌者,麻醉效果欠佳,酰胺类局麻药过敏,有明显的呼吸系统、循环系统和神经系统等病史者,2年内服用精神类药物者;有明显的视觉及听觉障碍者,简易精神状态量表(MMSE)<17分者,有明显语言及记忆障碍者,不能配合完成认知功能测试者,手术时间>3 h者等。手术种类包括:胫骨手术,股骨手术,斜疝手术,跟骨手术及大隐静脉手术等。本研究通过本院伦理委员会批准,并与患者签署知情同意书。
1.2 方法 两组患者均未用术前药,进入手术室,常规Datex-Ohmeda S/5监护仪监测平均血压(MBP)、心率(HR)、心电图(ECG)及血氧脉搏饱和度(SpO2)等,Model A-2000TM脑电双频指数(BIS)监测仪监测BIS。鼻导管给氧2~4 L/min,开放上肢外周静脉补液,预输乳酸林格液500 ml后,采用侧卧位,选点L3、L4,直入法行硬膜外腔穿刺,成功后采用针内针法行鞘内注射,D组以每5秒0.1 ml的速度注射含右美托咪定(批号:12100734,江苏恒瑞医药股份有限公司)12 μg的生理盐水3ml,C组注射等容量的生理盐水,然后头向行硬膜外腔置管3.5 cm,平卧后先注入2%盐酸利多卡因3 ml,5 min后无全脊麻症状后再注入0.75%盐酸罗哌卡因(批号:LACB,AstraZeneca公司,Sweden)12 ml,麻醉操作由经验丰富的麻醉医师完成。
1.3 观察指标 记录麻醉前(T0)、注罗哌卡因药后5 min(T1)、10 min(T2)、20 min(T3)、30 min(T4)、60 min(T5)的MBP、HR、SpO2、BIS。HR<50次/min,给予阿托品0.25 mg静注,MBP<20%基础血压,给予6~10 mg麻黄碱静注。术中从注入罗哌卡因后每5 min测定感觉及运动阻滞情况,术后每30 min测定感觉及运动阻滞情况,效果测定由另一名不清楚分组情况的麻醉医师完成。(1)感觉阻滞评定:采用针刺法测定感觉阻滞平面,记录起效时间(注药后至感觉平面达T10的时间)、持续时间(感觉平面首次达T10至该平面恢复正常感觉的时间)、最高平面及达最高平面的时间。(2)运动阻滞评定:采用改良Bromage运动评分(0分:髋、膝和髁关节均能运动;1分:髋关节不能运动,膝和髁关节均能运动;2分:髋和膝关节不能运动,髁关节均能运动;3分:髋、膝和髁关节均不能运动)。记录运动阻滞起效时间(注药后至Bromage运动评分为1分的时间)、持续时间(从Bromage运动评分为1分到运动恢复到Bromage运动评分为0分的时间)。(3)认知功能评定:MMSE评分内容包括:①定向力:时间定向力(5分)和地点定向力(5分);②记忆力:即刻记忆力(3分)和延迟记忆力(3分);③语言能力:命名(2分)、复述(1分)和书写(1分);④执行能力(5分);⑤计算力(5分);共30分。由另一名不清楚分组情况的医生分别于术前1 d(D0)、术后1 d(D1)、术后3 d(D2)、术后7 d(D3)对患者进行MMSE评分。术后评分与术前评分比较≥2个标准差时即发生术后认知功能障碍(POCD)。
1.4 统计学方法 采用SPSS16.0统计软件进行χ2及t检验。
2 结 果
2.1 一般临床资料比较 两组年龄、性别、体质量、体重指数(BMI)及手术时间比较无统计学意义(P>0.05),见表1,两组麻醉效果为优,由于手术时间均小于3 h,硬膜外均未追加局麻药,麻醉方法具有可比性。

表1 两组一般情况比较
2.2 血流动力学、BIS及不良反应比较 两组MBP在T1~T5比T0时有所下降,D组下降明显,但组内及组间比较无统计学差异(P>0.05);两组SpO2在T0~T5各时间点变化无统计学意义(P>0.05),D组HR、BIS在T1~T5各时间点比T0时及C组均降低(P<0.05),见表2。两组均未出现恶心、呕吐、呼吸抑制等并发症。
2.3 两组麻醉效果比较 与C组相比,D组硬膜外麻醉感觉阻滞起效时间缩短,感觉及运动持续时间延长,D组更快达到最高平面且达到的平面高(P<0.05),见表3。

表2 两组血流动力学及BIS比较
与同组T0点比较及与C组同时点比较:1)P<0.05

表3 两组麻醉效果比较
2.4 两组MMSE评分比较 与D0时及D组比较,C组D1,D2时MMSE评分明显降低(P<0.05),见表4。与术前相比,C组发生POCD 8例(26.67%),D组发生POCD 1例(3.33%),两组差异显著者(χ2=4.71,P=0.03)。
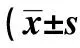
表4 两组MMSE评分比较,分,n=30)
与D0比较:1)P<0.05;与C组比较:2)P<0.05
3 讨 论
Dex用药途径不同对麻醉效果影响也不同,Coskuner等〔5〕报道的静脉输注Dex可延长布比卡因硬膜外阻滞感觉恢复时间,但感觉起效时间没有缩短。Salgado等〔6〕报道罗哌卡因混合Dex硬膜外麻醉具有明显协同作用,Dex不影响罗哌卡因麻醉起效时间,但可延长其感觉和运动阻滞持续时间并推迟硬膜外镇痛给药时间。Kanazi等〔7〕报道布比卡因12 mg混合Dex 3 μg与布比卡因12 mg比较,腰麻中感觉阻滞起效时间缩短,感觉和运动消退时间明显延长。本研究显示鞘内注射Dex使硬膜外麻醉感觉阻滞起效时间缩短,感觉和运动持续时间延长,更快达到最高平面且达到的平面高。可能原因是鞘内注射Dex,直接作用中枢神经系统,提高中枢的α2肾上腺素受体周围的药物浓度,通过与突触前C神经纤维和突触后脊髓背角神经元受体结合,从而抑制突触前神经递质的释放和使背角神经元超极化〔8〕,去甲肾上腺素的释放受到抑制,疼痛信号的传导从而被阻断〔9〕,与局麻药阻断Na+内流引起的阻滞效应发挥协同作用,因而很快增强麻醉效果。而Dex静脉注射要通过血脑屏障进入中枢神经系统需要一定的时间,药物的再分布影响药物的作用,因而对局麻药麻醉的起效时间影响不大。本研究感觉阻滞起效时间C组比郑红等〔10〕报道短〔(9.2±1.7)min和(9.8±1.8)min〕,可能的原因有本研究腰穿针刺破硬脊膜,局麻药可能通过此孔直接进入蛛网膜下腔;另一原因是本研究对象是老年患者,随年龄的增加,中枢和外周神经系统的结构、功能发生改变,神经纤维数量和密度减少,细胞骨架蛋白表达降低及轴突运输能力下降致轴突萎缩和退化,使神经对局麻药的敏感性增加,局麻药对神经阻滞的效应明显增强。
Dex静脉注射起效时间快,分布半衰期约为6 min,消除半衰期约为2 h〔11〕。Coskuner等〔5〕报道静脉输注Dex术中BIS低于对照组,不良反应较少,本研究与之相似,只是用药的途径不同。本研究鞘内注射Dex,可以通过脑脊液循环进入大脑中枢,通过激动中枢神经系统α2受体最为密集的脑干蓝斑区(负责调节睡眠和觉醒),产生并保持自然非动眼睡眠状态〔12〕,达到镇静作用,同时通过激动突触后膜α2受体,使交感神经紧张度降低,产生抗焦虑作用,因而出现用药后心率下降及BIS值的降低。两组均未出现恶心、呕吐、呼吸抑制等并发症。
POCD是指患者在麻醉及术后出现的中枢神经系统异常现象,表现为精神错乱、焦虑和人格改变以及记忆受损,是老年患者术后常见的并发症〔13〕。有研究表明,超过41%以上的老年患者在术后会发生认知功能障碍的情况〔14〕。老年患者POCD发生的原因仍不清楚,但研究显示该病的发生可能与患者的年龄、疾病史、手术、麻醉和镇静等因素有关〔15〕。最近有人提出了炎症反应学说,推测炎症可能是引起POCD的原因之一,他们认为手术、麻醉等因素可引起机体产生大量的炎症因子如肿瘤坏死因子(TNF)、白细胞介素(IL)-1、IL-6等,炎症因子通过血脑屏障,使细胞膜通透性增加,引起细胞水肿,干扰神经系统,影响突触连接的功能,同时这些炎症因子可激活中枢神经系统中的小胶质细胞,分泌炎症细胞因子、活性氧、趋化因子、兴奋性类毒素及神经毒素,加重炎症反应,抑制海马区的神经细胞的功能,产生认知功能障碍。有研究表明静脉注射Dex对患者术后认知功能有保护作用〔16〕。Kawasaki等〔17〕研究证实在人体外培养全血细胞实验中,Dex能抑制脂多糖诱导的促炎因子的产生;Peng等〔18〕研究表明Dex能抑制体外小胶质细胞的激活及炎症因子的释放。有研究表明POCD的发病高峰一般出现在术后1~3 d〔19〕,因此本研究于术后1、3、7d进行认知能的评价。本研究通过鞘内注射Dex直接抑制中枢的小胶质细胞,减少炎症因子的释放,结果显示MMSE评分于术后1、3 d下降不明显,POCD发生率降低。
综上,Dex鞘内注射能缩短硬膜外麻醉感觉阻滞起效时间,延长感觉及运动持续时间,并能改善老年患者术后认知功能。
1 Kukida A,Fujimoto Y,Shimoyama K,etal.Dexmedetomidine is useful for sedation during laryngoplasty with voice monitoring〔J〕.Masui,2014;63(4):431-4.
2 Smiley MK,Prior SR.Dexmedetomidine sedation with and without midazolam for third molar surgery〔J〕.Anesth Prog,2014;61(1):3-10.
3 Mohamed AA,Fares KM,Mohamed SA.Efficacy of intrathecally administered dexmedet-omidine versus dexmedetomidine with fentanyl in patients undergoing major abdominal cancer surgery〔J〕.Pain Phys,2012;15(4):339-48.
4 Chen J,Yan J,Han X.Dexmedetomidine may benefit cognitive function after laparoscopic cholecystectomy in elderly patients〔J〕.Exp Ther Med,2013;5(2):489-94.
5 Coskuner I,Tekin M,Kati I,etal.Effects of dexmedetomidine on the duration of anaesthesia and wakefulness in bupivacaine epidural block〔J〕.Eur J Anaesthesiol,2007;24(6):535-40.
6 Salgado PF,Sabbag AT,Silva PC,etal.Synergistic effect between dexmedetomidine and 0.75% ropivacaine in epidural anesthesia〔J〕.Rev Assoc Med Bras,2008;54(2):110-5.
7 Kanazi GE,Aouad MT,Jabbour-Khoury SI,etal.Effect of low-dose dexmedetomidine orclonidine on the characteristics of bupivacaine spinal block〔J〕.Acta Anaesthesiol Scand,2006;50(2):222-7.
8 Alka Shah,Lla Patel,Rachana Gandhi.Haemodynamic effects of intrathecal dexmedetomidine added to ropivacaine intraoperatively and for postoperative analgesia〔J〕.Int J Basic Clin Pharmacol,2013;2(1):26-9.
9 Nelson LE,Lu J,Guo TZ,etal.The α2-adrenocepter agonist dexmedetomidine converges on an endogenous sleep-promoting pathway to exert its sedative effects〔J〕.Anesthesiology,2003;98(2):428-36.
10 郑 红,张 庆,夏智群,等.舒芬太尼静脉或硬膜外给药对子宫切除术病人罗哌卡因硬膜外麻醉效果的影响〔J〕.中华麻醉学杂志,2006;6(26):804-6.
11 Bajwa S,Kulshrestha A.Dexmedetomidine:an adjuvant making large inroads into clinical practice〔J〕.Ann Med Health,2013;3(4):475-83.
12 Xia ZQ,Chen SQ,Yao X,etal.Clinical benefits of dexmedetomidine versus propofol in adult intensive care unit patients:a meta-analysis of randomized clinical trials〔J〕.J Surg Res,2013;185(2):833-43.
13 Damuleviciene G,Lesauskaite V,Macijauskiene J.Postoperative cognitive dysfunction of older surgical patients〔J〕.Medicina(Kaunas,Lithuania),2010;46(3):169-75.
14 Monk TG,Weldon BC,Garvan CW,etal.Predictors of cognitive dysfunction after major noncardiac surgery〔J〕.Anesthesiology,2008;108(1):18-30.
15 Hanning CD.Postoperative cognitive dysfunction〔J〕.Br J Anaesth,2005;95(1):82-7.
16 张奕文,邢祖民,徐颖华,等.不同剂量右美托咪定对老年患者腹腔镜下结直肠癌手术术后早期认知功能障碍的影响〔J〕.南方医科大学学报,2014;34(5):743-6.
17 Kawasaki T,Kawasaki C,Ueki M,etal.Dexmedetomidine suppresses proinflammatory mediator production in human whole blood in vitro〔J〕.J Trauma Acute Care Surg,2013;74(5):1370-5.
18 Peng M,Wang CY,Wang CY,etal.Dexmedetomidine attenuates lipopolysaccharide-induced proinflammatory response in primary microglia〔J〕.J Surg Res,2013;179(1):e219-25.
19 Bickel H,Gradinger R,Kochs E,etal.Incidence and risk factors of delirium after lip surgery〔J〕.Psychiatr Prax,2004;31(7):360-5.
〔2015-05-04修回〕
(编辑 苑云杰/曹梦园)
浙江省医学会临床科研基金项目(No.2012ZYC-A93)
姜景卫(1974-),男,副主任医师,硕士,主要从事临床麻醉研究。
R614.4
A
1005-9202(2016)22-5661-04;
10.3969/j.issn.1005-9202.2016.22.077
