泽及流浸膏对大鼠长期毒性研究
2016-12-16钮晓红卞勇蒋宝平许立
钮晓红,卞勇,蒋宝平,许立*
(1.南京中医药大学附属南京市中西医结合医院,江苏 南京 210014;2.南京中医药大学,江苏 南京 210023)
泽及流浸膏对大鼠长期毒性研究
钮晓红1,卞勇2,蒋宝平2,许立2*
(1.南京中医药大学附属南京市中西医结合医院,江苏 南京 210014;2.南京中医药大学,江苏 南京 210023)
目的:观察连续外用泽及流浸膏对大鼠的长期毒性。方法:SD大鼠随机分为泽及流浸膏9.50 g/kg、4.75 g/kg、2.38 g/kg三个剂量组和对照组,每组30只。制备破损皮肤后连续给药3个月,停药后恢复1个月。分别于给药及恢复期结束后,进行一般状况、体质量、饲料摄入量、血液学、血液生化学、尸体解剖和脏器病理组织学检查。结果:各组受试动物一般状况良好,外观、行为、排泄物等方面均未见异常变化。体重增长及摄食量与对照组比较无明显差异(P>0.05)。血常规、凝血四项、血液生化各指标未见与药物相关的明显异常。尸检及病理组织学各脏器未见异常。结论:泽及流浸膏破损皮肤外用对大鼠无明显毒性作用。
泽及流浸膏;SD大鼠;长期毒性研究
结核性窦道多为淋巴结核(瘰疬)或骨结核(流痰)特异性感染后,引流不畅或残留坏死组织,潜在死腔、脓水淋漓不尽,经久难愈所致。已破溃者需引流和换药,但所用药物种类颇多,疗效往往不够确切,容易贻误治疗时机,因此需要有科学的证据使治疗进一步规范化[1]。中医学认为结核性窦道形成窦道和缠绵难愈的根本原因是由于“腐”“毒”“瘀”的存在。因此,中医治疗常采用“袪腐化瘀、解毒生新”基本外治法,通过中药窦道灌注,促进创面腐烂坏死组织脱落,或将其清稀脓液转化成浓稠脓液,促进创面愈合。
泽及流浸膏由泽漆、白芨等组成的中药复方外治药,具有提脓祛腐、解毒活血、生肌收敛等功效,为南京市中西医结合医院临床经验方,经多年临床应用观察,该药对溃疡日久,腐肉难脱,新肉不长,久不收口之结核性窦道具有良好疗效[2]。为进一步在临床推广应用该验方,本研究对该膏药进行了皮肤给药的长期毒性观察,现报告如下。
1 材料与方法
1.1 受试药
泽及流浸膏,褐色浸膏,4.37 g/ml。人临床用量:1.9 g/ml,5 ml/60 kg。南京市中西医结合医院提供,批号14121501。
1.2 动物
清洁级SD大鼠,体质量80~100 g,雌雄各半,由浙江省实验动物中心提供。合格证:SCXK(浙)2014-0001。动物检疫后饲养观察1周后开始试验。给药前后,动物自由饮水饮食,室温20~25℃,每天人工光照12 h,室内通风良好,实验室相对湿度:60%~70%。
1.3 仪器
日立7100型全自动生化分析仪;SIEMENS ADVIA 2120i血液分析仪;Stago STA Compact全自动血凝仪。
1.4 动物分组及剂量设计[3-4]
将大鼠随机分为泽及流浸膏高、中、低剂量组和对照组,每组30只。其中三个剂量分别为12.67 g/kg、6.33 g/kg、3.17 g/kg,相当于人临床给药量的80、40、20倍;对照组为生理盐水。
1.5 破损皮肤制备及给药
试验前各组大鼠背部脊柱两侧剃毛,面积约4 cm×4 cm,用针头在剃毛区皮肤划井字,深浅以渗血为度,造成破损皮肤。试验期间动物被毛长出后,重新进行脱毛和破损皮肤处理。各组大鼠按5 ml/kg将相应浸膏均匀涂抹于脱毛区,涂药后用无菌纱布加以固定,第2天用生理盐水洗去后重新涂药、固定;对照组涂以生理盐水。每天1次,连续3个月。
1.6 观察方法
大鼠分笼饲养,每笼5只。试验期间每天观察各组大鼠外观、行为体征、活动、精神状态、进食、粪便及尿液等情况。每周称体质量1次,称量每笼摄取饲料量。如发现死亡或濒死者及时尸检。给药结束后每组剖杀20只动物(雌雄各半),进行指标观察,其余继续进行1个月的恢复期观察。
1.7 检测指标
给药3个月及恢复1个月后,将大鼠10%水合氯醛麻醉,颈总动脉取血作血液学检查、凝血四项及血液生化指标测定。颈椎脱臼处死并解剖大鼠,作主要脏器的肉眼观察,取心、肝、脾、肺、肾脏等主要脏器重量,计算脏器系数,并对给药部位皮肤和所有脏器进行组织学检查。
1.8 统计学处理

2 结果
2.1 一般状况
整个给药期间,泽及流浸膏三个剂量组及对照组大鼠健康状况良好,行为、排泄物等方面均未见异常变化。泽及流浸膏三个剂量组给药后大鼠体重增长、摄食量正常,与对照组比较无明显异常。
2.2 对大鼠血液学指标的影响
血常规实验检查结果表明,给药3个月后,高、中、低剂量组MPV均升高,与对照组相比P<0.01;恢复期高、中、低剂量组MPV均升高,与对照组相比具有统计学差异(P<0.05,P<0.01)。但这些指标的变化在本实验室正常生理值范围内,并无生理学意义。其余指标与对照组比较均未见有显著性差异(P>0.05)。结果见表1~2。

表1 泽及流浸膏对给药3个月大鼠血常规的影响
注:与对照组比较,*P<0.05,**P<0.01。

表2 泽及流浸膏对恢复期大鼠血常规的影响
注:与对照组比较,*P<0.05,**P<0.01。
2.3 凝血指标比较
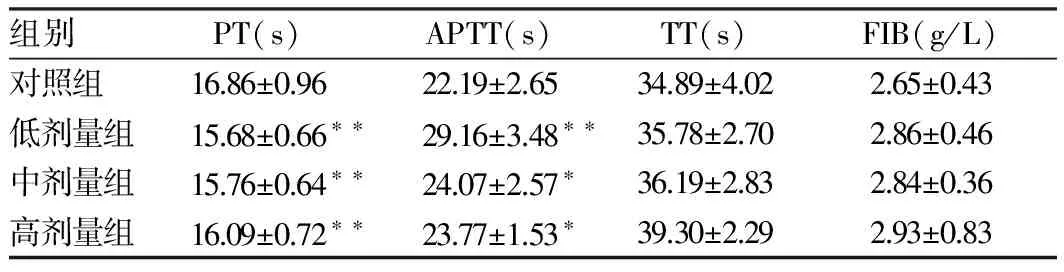
凝血四项实验检查结果表明:泽及流浸膏给药3个月,高、中、低剂量组PT降低,低剂量组APTT升高;恢复期中、低剂量组PT降低,与对照组相比有显著性统计学差异(P<0.01)。但这些指标的变化在本实验室正常生理值范围内,并无生理学意义。其余指标与对照组比较均未见有显著性差异(P>0.05)。结果见表3~4。
表3 泽芨流浸膏对给药3个月大鼠凝血四项的影响

组别PT(s)APTT(s)TT(s)FIB(g/L)对照组16.86±0.9622.19±2.6534.89±4.022.65±0.43低剂量组15.68±0.66∗∗29.16±3.48∗∗35.78±2.702.86±0.46中剂量组15.76±0.64∗∗24.07±2.57∗36.19±2.832.84±0.36高剂量组16.09±0.72∗∗23.77±1.53∗39.30±2.292.93±0.83
注:与对照组比较,*P<0.05,**P<0.01。

表4 泽芨流浸膏对恢复期大鼠凝血四项的影响
注:与对照组比较,*P<0.05,**P<0.01。
2.4 血液生化指标比较
血液生化指标检查结果表明,恢复期中、低剂量组GLU升高,与正常组大鼠比较有明显差异(P<0.05,P<0.01);但这些指标的变化在本实验室正常生理值范围内,并无生理学意义。其余指标与对照组比较均未见有显著性差异(P>0.05)。结果见表5~6。

表5 泽及流浸膏对给药3个月大鼠血液生化的影响
注:与对照组比较,*P<0.05,**P<0.01。

表6 泽及流浸膏对恢复期大鼠血液生化的影响
注:与对照组比较,*P<0.05,**P<0.01。
2.5 病理组织学检查
给药3个月后,对照组9例肝脏可见肝细胞轻度脂肪变性,4例肺及气管黏膜下层可见灶性炎细胞浸润,高剂量组7例肝脏可见肝细胞轻度脂肪变性,5例肺部和4例气管黏膜下层可见轻度炎细胞浸润。高剂量组及对照组均出现肝脏肝细胞轻度脂肪变性、肺脏灶性炎细胞浸润、气管黏膜下层炎细胞浸润为动物的自发性病变,并非药物引起的不良反应。其余脏器组织学结构正常,未见明显的病理学改变。停药1个月后各组动物未查见新出现的迟发性病变。高剂量组及对照组均出现肝脏肝细胞轻度脂肪变性、肺脏灶性炎细胞浸润、气管黏膜下层炎细胞浸润为动物的自发性病变,并非药物引起的不良反应。表明受试药物在所设剂量下对大鼠所检脏器无毒性作用,也未引起延迟性毒性反应。
3 讨论
泽漆,俗称猫儿眼睛草,性味辛苦,凉,有毒。有行水消痰,杀虫解毒功能,治瘰疬,结核性窦道。《便民图篡》记载“可治瘰疬”;江西《草药手册》记载“治淋巴结结核。”临床上常配合白芨以加强杀菌消炎生肌的作用。现代药理研究表明,对人型结核杆菌有显著抑制作用。现代研究显示,泽漆主要含二萜酯类、黄酮类化合物,是其主要的生物活性物质,此外,还含有三萜、甾醇、多酚类、氨基酸、天然油脂类化合物等多种成分,具有抗肿瘤、平喘止咳、抑菌等药理活性[5]。但传统记载有毒,有临床报道显示,泽漆鲜草乳状汁液对皮肤、黏膜有很强的刺激性。接触皮肤可致发红,甚至发炎、溃烂。如误服泽漆鲜草或乳白汁液后,口腔、食管、胃黏膜均可发炎、糜烂,有灼痛、恶心、呕吐、腹痛、腹泻水样便,严重者可致脱水,甚至出现酸中毒[5-6]。实验研究显示,泽漆乙酸乙酯萃取物对小鼠有明显毒性,可造成心、肝、脾、肺、肾等多个脏器的损伤[7]。但是,另一方面,泽漆水煎液则安全性良好,小鼠灌胃泽漆125 g/kg亦未致死。临床用其煎液内服,即使剂量大至150 g/d,也末见明显毒性反应[6]。甚至有报道显示,泽漆水煎液对复发性口疮有良好疗效[8]。
在本研究中,所观察泽及流浸膏为以泽漆为主要药物的中药复方,考虑到临床用于结核性窦道,因此设计观察其长期对破损皮肤外用可能的毒性作用及其靶器官。结果显示,该复方应用三个月对大鼠无明显毒性作用,动物外观行为、活动、体重增长、血常规、血液生化等指标与对照组比较无明显改变,脏器器官也未见的明显的组织学改变。此外,相关的安全性研究显示该浸膏外用无明显皮肤刺激性、皮肤致敏性,表明泽及流浸膏外用比较安全。
曾有学者推测,泽漆毒性成分可能不溶于水[6],本研究中所药浸膏为水煎剂,长期外用未见的明显毒性,是因为水煎毒性成分未溶出,还是因为中药复方配伍减毒,尚不得面知,值得今后进一步研究。
[1] 朱莉贞.加强对肺外结核病的协作研究[J].中华结核和呼吸杂志,2008,31(2):81-82.
[2] 黄子慧.提脓祛腐液外用治疗结核性窦32例临床观察[J].天津中医药大学学报,2009,28(1):14-15.
[3] 袁伯俊,廖明阳,李波.药物毒理学实验方法与技术[M].北京:化学工业出版社,2007:190-205.
[4] 林小凤,陈开杰,石鹤坤,等.复方镰形棘豆凝胶剂的皮肤安全性评价[J].中国医院药学杂志,2015,35(5):449-453.
[5] 杨莉,陈海霞,高文远.泽漆化学成分及药理作用研究进展[J].中草药,2007,38(10):1585-1589.
[6] 段强,周永安,景文文.猫眼草致刺激性接触性皮炎4例[J].临床皮肤科杂志,2014,43(10):622-623.
[7] 孙雪,李明会,张庆,等.泽漆乙酸乙酯萃取物对小鼠经口急性毒性[J].东北林业大学学报,2015,43(3):109-111.
[8] 赵忆文,唐苾芯,吴昆仑.泽漆含漱液治疗复发性口疮的临床观察与护理[J].上海护理,2010,10(6):62-64.
Experimental Study on Long-term Toxicity of Zeji Liquid Extract on Rats
NIU Xiao-hong1,BIAN Yong2, JIANG Bao-ping2,XU Li2*
(1.NanjingIntegratedTraditionalChineseandWesternMedicineHospitalAffiliatedtoNanjingUniversityofChineseMedicine,Nanjing210014,China;2.NanjingUniversityofChineseMedicine,Nanjing210023,China)
Objective: To observe the chronic toxicity of Zeji liquid extract(ZJLE) of external application in rats. Methods: SD rats were randomly divided into a control group and ZJLE 9.50,4.75 and 2.38 g/kg groups with 30 rats in each group. The damaged skins were pasted with ZJLE for 3 months. Then the therapy was stopped for a month for recovery. The general condition, body weight, feed intake, hematology, blood chemistry, autopsy, organ coefficiency and histopathology were examined after treatment and recovery period. Results: All the rats were normal in good condition, appearance, behavior, excreta and so on. Compared with the control group, there was no significant difference in the body weight and feed intake in ZJFE groups. Moreover, the hematology, blood chemistry, autopsy, organ coefficiency and histopathology were normal. Conclusion:ZJLE of external application has no significant toxicity on rats with damaged skin.
Zeji liquid extract;SD rats;Research of long-term toxicity
2009-2014年度江苏省中医药领军人才培养项目(No.LJ200921)
钮晓红(1959-),女,主任中医师,教授,硕士研究生导师,主要研究方向:中医外科疾病、淋巴结核等肺外结核。
许立*(1964-),男,博士,教授,硕士研究生导师,主要研究方向:中药药理学与毒理学。
2016-04-12
R285
A
1002-2406(2016)06-0028-03
修回日期:2016-05-10
