酰腙类Schiff碱汞(Ⅱ)配合物的合成及晶体结构
2016-12-15黄超张文龙陈冬梅张奇龙朱必学
黄超 张文龙 陈冬梅 张奇龙 朱必学*,
(1贵州大学大环及超分子化学重点实验室,贵阳550025)
(2贵州医科大学化学教研室,贵阳550004)
酰腙类Schiff碱汞(Ⅱ)配合物的合成及晶体结构
黄超1张文龙1陈冬梅1张奇龙2朱必学*,1
(1贵州大学大环及超分子化学重点实验室,贵阳550025)
(2贵州医科大学化学教研室,贵阳550004)
合成了Schiff碱配体3-乙酰吡啶缩邻氨基苯甲酰腙(L1)及4-乙酰吡啶缩邻氨基苯甲酰腙(L2),并分别与HgCl2进行了配位反应,得到2个配位聚合物{[Hg(L1)Cl2]·CH3OH}n(1)和[Hg(L2)Cl2]n(2),采用1H NMR、FTIR和元素分析等手段对化合物进行了表征,并对配合物的热稳定性进行了考察。通过X射线单晶体衍射技术测定了2个配合物的单晶结构,结构解析表明,配合物1属于三斜晶系,P1空间群,配合物2属于单斜晶系,P21/n空间群。
Schiff碱;汞(Ⅱ)配合物;晶体结构
Schiff碱化合物是一类重要的有机配体,易与过渡金属进行有效的配位作用,Schiff碱配合物在催化、生物模拟及医药等领域中具有重要应用价值[1-3]。在与Schiff碱进行配位作用的过渡金属离子中,汞(Ⅱ)离子具有d10电子组态,具有不同的配位数,其与有机配体作用过程中能采用不同的配位模式,便于实现结构新颖的超分子组装体构筑,使得汞(Ⅱ)的超分子化学一直是有趣的研究领域[4-8]。同时,汞是一种剧毒并对环境有害的元素,合理设计有机配体分子与汞进行有效的选择性键合作用,达到混合体系中汞的有效提取与分离一直是富有挑战性的研究课题[9-10]。据此,本文设计合成了2个含有N、O配位原子的酰腙类Schiff碱有机配体[11-15],并分别与氯化汞(HgCl2)进行配位作用,得到2个汞(Ⅱ)的配位聚合物,在对配合物的晶体结构解析的基础上,进一步考察了它们的热稳定性。
1 实验部分
1.1 试剂
邻氨基苯甲酸甲酯,水合肼(80%,w/w),3-乙酰吡啶,4-乙酰吡啶,HgCl2,以及其它所用试剂均为分析纯。
1.2 测试仪器
JEOL ECX 400 MHz核磁共振仪(TMS,DMSO-d6);Ry-2型熔点仪(温度计未校正);Bio-Rad型傅立叶红外光谱仪(4 000~400 cm-1);Vario ELⅡ型元素分析仪(德国);晶体结构测定采用Bruker Smart Apex CCD单晶衍射仪。
1.3 配体与配合物合成
配体及配合物的合成路线:

Scheme 1
1.3.1 配体3-乙酰吡啶缩邻氨基苯甲酰腙(L1)的合成
邻氨基苯甲酰肼按文献[16]的方法合成。称取0.453 g(3 mmol)邻氨基苯甲酰肼溶解在80 mL无水乙醇中,在搅拌条件下,滴加0.363 g(3 mmol)3-乙酰吡啶的乙醇溶液(20 mL),滴加完毕后,继续加热回流8 h。减压旋蒸除去溶剂,得白色固体。用乙醇重结晶,抽滤,真空干燥得到白色块状固体,产率62%。m.p.146~147℃。1H NMR(DMSO-d6,400 MHz):δ2.38(s,3H,CH3),6.21(s,2H,NH2),6.59(t,J=7.2 Hz,H,Ar-H),6.76,6.78(d,J=8.0 Hz,H,Ar-H),7.21(t,J= 7.2 Hz,H,Ar-H),7.45(t,J=6.4Hz,H,Py-H),7.55,7.57 (d,J=7.6 Hz,H,Ar-H),8.17,8.18(d,J=7.6 Hz,H,Py-H),8.59,8.60(d,J=3.6 Hz,H,Py-H),8.99(s,H,Py-H),10.65(s,H,CONH)。元素分析(%,按C14H14N4O计算,括号内为计算值):C 66.16(66.13),H 5.57(5.55),N 22.00(22.03)。FTIR(KBr,cm-1):1 622(C=O),1 578 (C=N)。
1.3.2 配体4-乙酰吡啶缩邻氨基苯甲酰腙(L2)的合成
将3-乙酰吡啶换成4-乙酰吡啶,按照L1的合成方法合成L2,得白色絮状固体,产率59%。m.p. 215~216℃。1H NMR(DMSO-d6,400 MHz):δ2.36(s,3H,CH3),6.23(s,2H,NH2),6.59(t,J=7.2 Hz,H,Ar-H),6.76,6.78(d,J=8.0 Hz,H,Ar-H),7.22(t,J=8.4 Hz, H,Ar-H),7.56,7.57(d,J=7.6 Hz,H,Ar-H),7.74,7.76 (d,J=5.6 Hz,2H,Py-H),8.62,8.64(d,J=4.8 Hz,2H,Py-H),10.70(s,H,CONH)。元素分析(%,按C14H14N4O计算,括号内为计算值):C 66.15(66.13),H 5.54 (5.55),N 22.06(22.03)。FTIR(KBr,cm-1):1 621(C=O),1 575(C=N)。
1.3.3 配合物1和2的合成
配合物1的合成:将25.4 mg(0.1 mmol)的配体L1溶解在25 mL甲醇溶液中,逐滴加入HgCl2(27.2 mg,0.1 mmol)的甲醇溶液(25 mL),室温搅拌1 h,旋蒸除去溶剂,粗产品用甲醇重结晶,抽滤,真空干燥得1的淡黄色固体21.2 mg,产率38%。元素分析(%,按C30H36Cl4Hg2N8O4计算,括号内为计算值):C 32.33(32.30),H 3.27(3.25),N 10.01(10.04)。FTIR (KBr,cm-1):1 612(C=O),1 547(C=N)。
配合物2的合成:将25.4 mg(0.1 mmol)的配体L2溶解在20 mL乙腈溶液中,逐滴加入HgCl2(27.2 mg,0.1 mmol)的乙腈溶液(20 mL),室温搅拌1 h,旋蒸除去溶剂,粗产品用乙腈重结晶,抽滤,真空干燥得2的黄色固体22.6 mg,产率43%。元素分析(%,按C14H14Cl2HgN4O计算,括号内为计算值):C 32.01 (31.98),H 2.69(2.68),N 10.63(10.66)。FTIR(KBr,cm-1):1 586(C=O),1 546(C=N)。
单晶培养:取少量1的固体产品溶解在甲醇溶液中,取少量2的固体产品溶解在乙腈溶液中,分别室温静置3~4 d后,得到适合于X射线衍射测定的块状晶体。
1.4 晶体结构的测定与解析
选择大小为0.22 mm×0.18 mm×0.17 mm的配合物1和0.24 mm×0.23 mm×0.21 mm的配合物2的单晶,用Bruker Smart Apex单晶衍射仪,采用经石墨单色器单色化的Mo Kα射线(λ=0.071 073 nm),以φ-ω扫描方式收集单晶衍射数据,强度数据进行了经验吸收校正、LP校正。晶体结构由直接法解得,对全部非氢原子坐标及其各向异性热参数进行了全矩阵最小二乘法修正,氢原子由理论加氢法得到。所有计算使用SHELX-97程序完成[17]。
CCDC:1496029,1;1496028,2。

表1 配合物1和2的晶体学及结构修正数据Table 1 Crystal data and structure refinement for complexes 1 and 2
2 结果与讨论
2.1 配合物的晶体结构与组装
2.1.1 配合物1的结构与组装
配合物1的不对称单元结构如图1a,主要键长和键角列在表2中。配合物1的中心Hg(Ⅱ)离子为五配位构型,配位原子中包括3个氯,而1个配位氮原子来自于配体L1上的氨基氮,另一个配位氮原子来自于另一配体L1上的吡啶氮。围绕Hg(Ⅱ)中心的3个Hg-Cl键长在0.233 27(18)和0.285 74(17) nm之间,围绕中心Hg(Ⅱ)离子的键角Cl-Hg-Cl在86.23(5)°和118.74(7)°之间,N-Hg-Cl在87.32(14)°和139.87(15)°之间。2个Hg(Ⅱ)离子通过2个氯配位桥连形成HgCl2Hg矩形环(Hg-Cl-Hg 93.77(5)°;Cl-Hg-Cl 101.53(7)°),相邻近的2个矩形环状单元经由2个相互平行排列的配体L1跨连形成长方形的22元金属-有机环状单元(Hg2L12),配体分子所在平面与矩形环(HgCl2Hg)平面之间的二面角接近90°,位于桥连配体分子两端的Hg…Hg距离为1.261 5 nm。以矩形环状亚单元(HgCl2Hg)节点,通过4个配体分子采用2,2-连接方式将其彼此连接形成准1D伸展的链式阶梯状结构。相邻1D梯状链之间通过配体L1中苯环Cg(1)和吡啶环Cg(2)之间的π…π堆积作用沿晶体ac平面平行扩展为2D层结构(图1b),苯环Cg(1)和吡啶环Cg(2)之间的中心间距为0.371 9(4)nm,2个π平面的二面角为9°;2D层结构沿晶体b轴方向平行拓展为3D结构,甲醇分子通过与跨连配体L1分子之间形成N2-H2…O2和O2-H16…O1氢键作用分布在层间孔穴中(图1c,氢键参数见表3),并对3D结构起到进一步稳定作用。
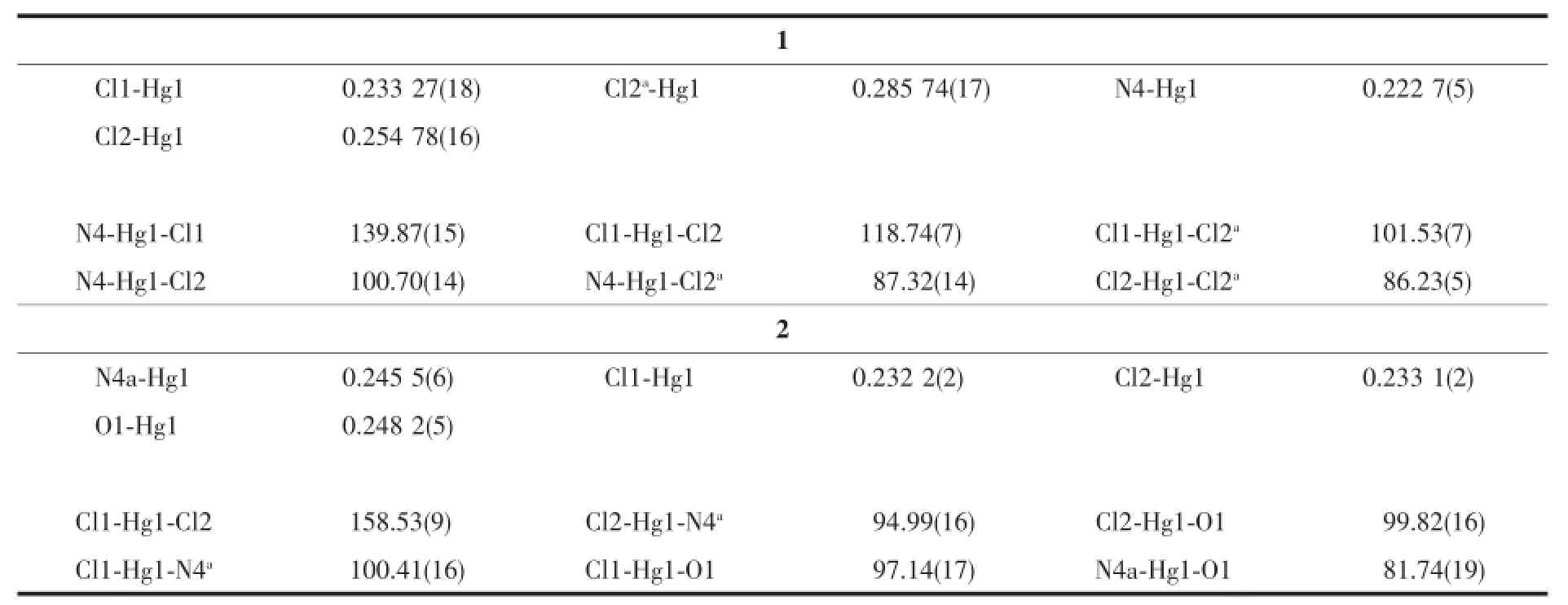
表2 配合物1和2的部分键长和键角Table 2 Selected bond lengths(nm)and bond angles(°)for 1 and 2
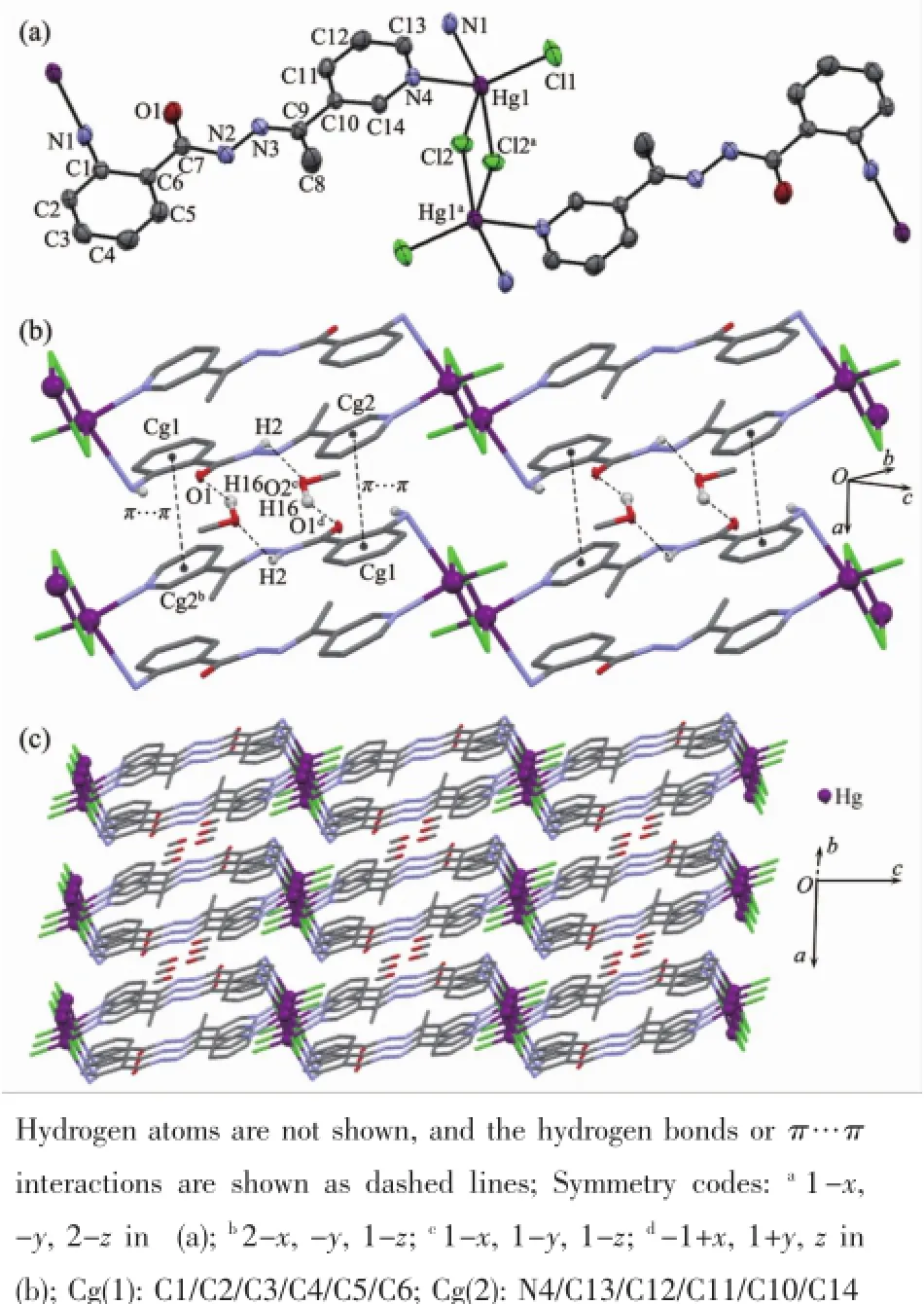
图1 (a)配合物1的不对称单元结构;(b)梯状链之间通过π…π堆积作用形成准2D层结构;(c)沿晶体b轴方向观察的准3D结构Fig.1(a)ORTEP view of the asymmetric unit of the complex 1(probability of ellipsoid is 30%); (b)Layered structure of 1;(c)Part of the quasi 3D structure viewed down the crystallographic b axis
2.1.2 配合物2的结构与组装
配合物2的不对称单元结构如图2a,主要键长和键角列在表2中。与配合物1的配位情形不同,在配合物2中,中心Hg(Ⅱ)离子表现为稍扭曲四面体配位构型,配位原子分别为2个氯,1个氧原子来自于L2中的羰基氧,1个氮原子来自于另一个L2中的吡啶氮,Hg1-Cl1和Hg1-Cl2键长分别为0.232 2(2)和0.233 1(2)nm,Hg1-O1和Hg1-N4的键长分别为0.248 2(5)和0.245 5(6)nm,围绕Hg(Ⅱ)中心的键角N4-Hg1-O1和Cl1-Hg1-Cl2分别为81.74(19)°和158.53(9)°。相邻2个Hg(Ⅱ)离子经由L2配位连接形成具有“S”形结构的1D链,扭曲角N4-Hg1-O2-C7为143°,相邻1D链通过配体分子L2中苯环Cg(3)和吡啶Cg(4)之间的弱π…π堆积作用,沿晶体ac平面平行扩展为2D层结构(图2b),吡啶环Cg(3)和苯环Cg(4)之间的中心间距为0.392 4 (5)nm,2个π平面的二面角为8°;当沿晶体b轴方向看,通过π…π堆积作用的单股1D链组装为平行排列结构,该结构进一步通过分子间C5-H5…Cl2氢键作用在晶体ac平面平行扩展形成准3D结构(图2c,氢键参数见表3)。

表3 配合物的氢键参数Table 3 Structural parameters of hydrogen bonds for the complexes

图2 (a)配合物2的不对称单元结构;(b)单股链之间的π…π堆积作用;(c)沿b轴方向观察的准3D结构Fig.2(a)View of the asymmetric unit of the complex 2 (probability of ellipsoid is 30%);(b)π…π interactions between the double-stranded chains; (c)Part of the quasi 3D structure viewed down the crystallographic b axis
2.21H NMR和红外光谱
配体L1的1H NMR中,酰胺氮上的质子峰出现在10.65处,苯环的质子峰出现在6.59~7.57范围,吡啶环的质子峰7.45~8.99区域。氨基质子和甲基质子分别出现在6.21和2.38处,均表现为单峰。配体L2的1H NMR中,酰胺氮上的质子峰出现在10.70处,苯环的质子峰出现在6.59~7.57范围,吡啶环的质子峰7.74~8.64区域。氨基质子和甲基质子分别出现在6.23和2.36处,均表现为单峰。
配体及配合物的红外光谱测定结果表明,配体L1中,ν(C=O),ν(C=N)的特征吸收振动峰依次出现在1 622和1 578 cm-1处,形成配合物后,配合物1中ν(C=N)频移至1 547 cm-1处;配体L2中,ν(C=O),ν(C=N)的特征吸收振动峰依次出现在1 621和1 575 cm-1处,形成配合物后,配合物2中ν(C=O)和ν(C=N)分别频移至1 586和1 546 cm-1处,与自由配体相比,均向低波数方向位移,证明配体L2中羰基及吡啶氮原子参与了配位,与晶体结构测定的结果一致。
2.3 配合物的热稳定性
以10℃·min-1的升温速率,在N2气氛下于室温~800℃范围分别考察了2个配合物的热稳定性(图3)。配合物1从200℃开始分解,200~450℃快速失重73.6%,可能与失去酰腙配体的吡啶基片段以及氯化汞的气化有关,之后炭化持续缓慢失重12.8%,至800℃残重13.6%。配合物2的失重情况与配合物1类似,从200℃开始分解,200~460℃快速失重82.7%,之后持续缓慢失重7.7%,至800℃残重9.6%,结果表明配合物具有较好的热稳定性。

图3 配合物1和2的TG曲线Fig.3 TG curves of the complexes 1 and 2
[1]Seth P,Ghosh S,Figuerola A,et al.Dalton Trans.,2014,43: 990-998
[2]Tayyebi Sabet Khomami N,Heshmatpour F,Neumüller B. Inorg.Chem.Commun.,2014,41:14-18
[3]Kalita M,Gogoi P,Barman P.Polyhedron,2014,74:93-98
[4]Pitt M A,Johnson D W.Chem.Soc.Rev.,2007,36:1441-1453
[5]Guzmán-Percástegui E,Zakharov L N,Alvarado-Rodríguez J G,et al.Cryst.Growth Des.,2014,14:2087-2091
[6]Beheshti A,Lalegani A,Behvandi F,et al.J.Mol.Struct., 2015,1082:143-150
[7]Jones C D,Tan J C,Lloyd G O.Chem.Commun.,2012,48: 2110-2112
[8]Baul T S B,Kundu S,Mitra S,et al.Dalton Trans.,2013,42: 1905-1920
[9]Khavasi H R,Tahrani A A.CrystEngComm,2013,15:5799-5812
[10]Khavasi H R,Sadegh B M M.Dalton Trans.,2015,44:5488-5502
[11]Chang H Q,Jia L,Xu J,et al.Inorg.Chem.Commun.,2015, 57:8-10
[12]Wang J L,Zhao Y Q,Yang B S.Inorg.Chim.Acta,2014, 409:484-496
[13]LI Xiao-Jing(李晓静),WU Wei-Na(吴伟娜),XU Zhou-Qing (徐周庆),et al.Chinese J.Inorg.Chem.(无机化学学报), 2015,31(11):2265-2271
[14]Radunsky C,Kösters J,Müller J.Inorg.Chim.Acta,2015, 428:14-20
[15]HAN Xue-Feng(韩学锋),CAI Hong Xin(蔡红新),JIA Lei (贾磊),etal.Chinese J.Inorg.Chem.(无机化学学报),2015, 31(7):1453-1459
[16]HUANG Chao(黄超),WU Juan(吴娟),CHEN Dong-Mei(陈冬梅),et al.Chinese J.Inorg.Chem.(无机化学学报),2015, 31(1):109-113
[17]Sheldrick G M.SHELXL-97,Program for X-ray Crystal Structure Solution and Refinement,University of Göttingen, Germany,1997.
Syntheses and Crystal Structures of Hg(Ⅱ)Complexes with Hydrazone Schiff Base
HUANG Chao1ZHANG Wen-Long1CHEN Dong-Mei1ZHANG Qi-Long2ZHU Bi-Xue*,1
(1Key laboratory of Macrocycle and Supramolecular Chemistry,Guizhou University,Guiyang 550025,China)
(2Department of Chemistry,Guizhou Medical College,Guiyang 550004,China)
Two complexes{[Hg(L1)Cl2]·CH3OH}n(1)and[Hg(L2)Cl2]n(2)were synthesized from the reaction of Schiff base ligand 3-acetylpyridine-o-aminobenzoylhydrazone(L1)and ligand 4-acetylpyridine-o-aminobenzoylhydrazone(L2)with HgCl2,respectively.The compounds are characterized by1H NMR,FTIR,and elementalanalysis, and their structures are measured via single crystal X-ray diffraction.The results show that the complex 1 crystallize in triclinic system,space group P1;the complex 2 crystallize in monoclinic system,space group P21/n. Further the thermalstabilities ofthe two complexes were investigated.CCDC:1496029,1;1496028,2.
Schiff base;Hg(Ⅱ)complex;crystal structure
O614.24+3
A
1001-4861(2016)09-1579-06
10.11862/CJIC.2016.202
2016-05-17。收修改稿日期:2016-07-26。
国家自然科学基金(No.21061003)和教育部“春晖计划”项目(No.Z2012054)资助。
*通信联系人。E-mail:bxzhu@gzu.edu.cn
