石灰石湿法脱硫系统中汞的二次释放特性
2016-12-15孟东栋王炫杨涛张成
孟东栋,王炫,杨涛,张成
(1.广州中电荔新电力实业有限公司,广东 广州511340; 2.华中科技大学 能源与动力工程学院,湖北 武汉 430074)
石灰石湿法脱硫系统中汞的二次释放特性
孟东栋1,王炫2,杨涛2,张成2
(1.广州中电荔新电力实业有限公司,广东 广州511340; 2.华中科技大学 能源与动力工程学院,湖北 武汉 430074)

燃煤锅炉;烟气脱硫;汞;二次释放
煤在炉内高温燃烧时,煤中各形态汞转化为气态单质汞释放到炉内烟气中[1]。烟气由炉膛出口到尾部烟道,流经各级受热面,温度逐步降低,汞的形态也随之发生转变。尾部烟气中汞的形态主要分为气相元素汞Hg0、气相二价汞Hg2+和固相颗粒态汞HgP[2]。颗粒态汞易被除尘装置或者湿法烟气脱硫(wet flue gas desulfurization,WFGD)等装置捕集脱除;二价汞易溶于水,也可吸附于颗粒物上,便于被除尘装置和WFGD系统脱除[3]。在WFGD系统内,有部分被吸收的二价汞容易被还原成单质汞而释放出来,这被称为汞的二次释放,使得WFGD对Hg2+的脱除率降低。在美国曼斯菲尔德电厂的试验中,检测到WFGD系统出口处Hg0的质量浓度比进口处增加15%[4]。因此研究汞的二次释放特性对提高WFGD装置的汞的脱除效率具有重要意义。DAZ-SOMOANO等指出脱硫浆液pH值和SO2的质量浓度与汞的脱除有密切联系,脱硫浆液质量浓度对汞脱除的影响较小[5]。鲍静静等发现加大液气比有助于提高汞脱除率[6]。J.Currie 验证了Cl-、S(IV)和pH值是影响汞还原速率的主要因素[7]。王运军等发现SO2和O2的体积分数对汞的吸收影响不大,浆液中CaSO3含量、Cl-的体积分数的物质的量和pH值显著影响Hg2+的吸收[8]。
本文重点研究脱硫浆液中汞的还原释放机理,浆液各参数对Hg2+还原作用的影响,同时考察两种添加剂对汞还原的抑制效果。
1 实验部分
为研究浆液各参数对汞二次释放的影响,设计了图1所示的实验装置。模拟烟气部分由N2、O2、CO2按照80%、5%、15%(体积分数)的比例组成,总流量为2 L/min。气体在混气罐中混合后,通入反应器中,反应器在恒温加热磁力搅拌器中水浴加热。反应浆液采用磷酸氢二钠-磷酸二氢钾pH值缓冲液作为母液,加入质量分数为0.5%的CaSO4·2H2O,反应过程中加入10 mg/L汞标准使用液和其他添加剂,最后用缓冲溶液定容至250 mL。浆液中还原出来的单质汞经过变色硅胶干燥后进入在线测汞仪,VM3000在线测汞仪可通过计算机实时显示进气中Hg0的质量浓度数据,将数据处理后可以计算出一定时间内的Hg0释放量,得到汞在这段时间内的二次释放率。
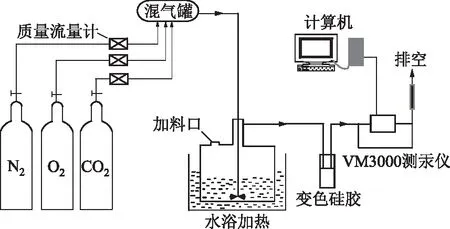
图1 汞二次释放实验台架
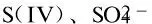
2 实验结果分析
2.1 浆液Hg2+的质量浓度对汞二次释放的影响
在浆液温度为50 ℃,pH值为5.0,未添加S(IV)和其他添加剂,不同初始Hg2+的质量浓度下,Hg0的释放质量浓度随时间变化曲线如图2所示。

图2 初始Hg2+的质量浓度与Hg0释放质量浓度曲线
在10 min时向浆液中添加Hg2+,尾气中的Hg0的质量浓度迅速上升,在达到峰值后,逐渐降低。从图2曲线可以看到,初始Hg2+的质量浓度越高,Hg0的释放质量浓度越大,其释放量也越大。在初始汞的质量浓度为8 μg/L、80 μg/L、200 μg/L、400 μg/L条件下,90 min汞的释放率分别为35.7%、36.3%、32.7%和31.7%,可以认为初始Hg2+的质量浓度对汞的二次释放率影响不显著。由于浆液中CaSO4·2H2O含有Fe2+等还原性金属阳离子(用M2+表示),汞被还原是由于式(1)的存在。
(1)
2.2 浆液温度对汞二次释放的影响
图3表示浆液pH值为5.0,初始Hg2+质量浓度为80 μg/L,未加入S(IV) 和其他添加剂,在40 ℃、50 ℃、60 ℃、70 ℃四种温度下,Hg0的释放质量浓度随时间变化的曲线。从图3可见,随着温度的升高,Hg2+还原过程加剧,汞排放质量浓度升高,二次释放率增大(四种温度下,90 min汞的释放率分别为22.3%、36.3%、48.5% 和54.9%)。反应温度升高有助于增加化学反应的活化分子数量,促进Hg2+向Hg0的转变。汞被还原主要还是式(1)的原因。

图3 四种温度下Hg0的释放质量浓度曲线
2.3 浆液pH值对汞二次释放的影响
浆液pH值与Hg0的释放质量浓度关系如图4所示。

图4 pH值与Hg0的释放质量浓度曲线
从图4可见,pH值增大时,汞的二次释放率呈先增大后降低的趋势(90 min汞的释放率分别为11.7%、17.8%、36.3%、37.69%、8.2%和3.0%),从释放率可以看出pH值对汞还原的影响很大。低pH值(小于4.5)与较高pH值(大于6.0)的条件下,汞的释放质量浓度与二次释放率均较小。pH值在5.0和5.5时的还原率非常高。
在脱硫浆液中存在平衡反应,见表1的式(2)和式(3),从平衡常数值来看,Hg2+与OH-的反应趋向于完全反应。在高pH值时,较多的OH-与Hg2+形成相对比较稳定的Hg(OH)+和Hg(OH)2,同时OH-与Fe2+等还原性的金属离子也会形成难离解的絮状物,阻碍了反应式(1)的进行,这些都抑制了Hg2+的还原。
表1 反应式及其平衡常数

反应式平衡常数编号Hg2++OH- Hg(OH)+2.39×1010(2)Hg2++2OH- Hg(OH)23.42×1020(3)Hg2++SO2-3+H2O Hg0+SO2-4+2H+1.19×1026(4)Hg2++HSO-3+H2O Hg0+SO2-4+3H+6.12×1018(5)
2.4 浆液S(IV)的物质的量对汞二次释放的影响
图5为通入模拟烟气(O2的体积分数为5%)情况下,当加入的S(IV) 的物质的量为0.05 mmol时,90 min内的汞还原率达89.3%,之后还原率随着S(IV)的物质的量增高反而持续降低的曲线。当S(IV)的物质的量增加至0.5 mmol时,汞的二次释放率才降到未加入S(IV)时的水平;S(IV)的物质的量大于0.5 mmol后,汞的还原被抑制。

注:与初始S(IV)的物质的量对应的90 min汞的释放率分别为36.3%、89.3%、67.1%、51.9%、36.7%、13.5%和4.4%。图5 S(IV)的物质的量与Hg0的释放质量浓度曲线(烟气气氛)

(6)
(7)
实际运行时,烟气中的含氧量不能满足氧化浆液中的亚硫酸盐,为保证副产品石膏的品质,则要使用氧化风机等装置将空气强制鼓入脱硫塔的浆液池内。因此本研究还考察了空气气氛(O2和N2的体积分数分别为21%和79%)下S(IV)的物质的量对汞二次释放的影响,其他反应条件与烟气气氛下的实验条件一致,实验结果如图6所示。虽然空气气氛相比烟气气氛O2的体积分数要高许多,但S(IV)的物质的量相同情况下,反而Hg0的释放量要大,原因可能是更高体积分数的O2使S(IV)氧化速率加快,降低了S(IV)的物质的量,使Hg2+更容易被还原。在S(IV)的物质的量较大时,这种情况更明显,Hg0的释放质量浓度甚至有逐步升高的趋势。
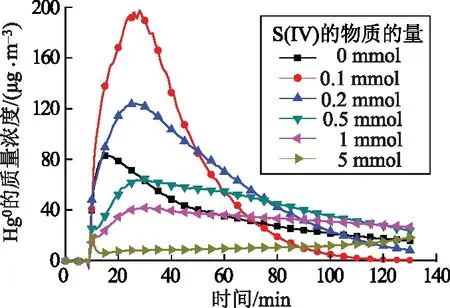
图6 S(IV)的物质的量与Hg0的释放质量浓度曲线(空气气氛)


图的物质的量与Hg0释放质量浓度曲线
(8)
(9)

2.6 浆液Cl-的体积分数对汞二次释放的影响
图8表示温度为50 ℃,pH值为5.0,初始Hg2+的质量浓度为80 μg/L,浆液S(IV)的物质的量为0.05 mmol,实验开始20 min时向浆液中添加NaCl(使浆液中Cl-的体积分数达到5×10-3)后,Hg0的释放质量浓度随时间变化的曲线。
反应前10 min,Hg0大量释放,在加入Cl-后,Hg0的释放质量浓度急剧降低,反应稳定后Hg0几乎不再释放。
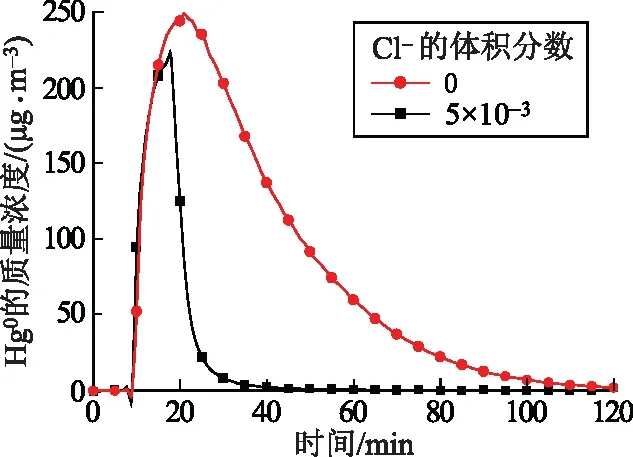
图8 Cl-的体积分数与Hg0的释放质量浓度曲线

(10)
(11)
采用添加沉淀剂或者氧化剂,分别通过固化汞和强制氧化汞的方式来抑制汞的还原也是一种可行方案,本实验研究了Na2S和H2O2溶液对汞再释放的影响。

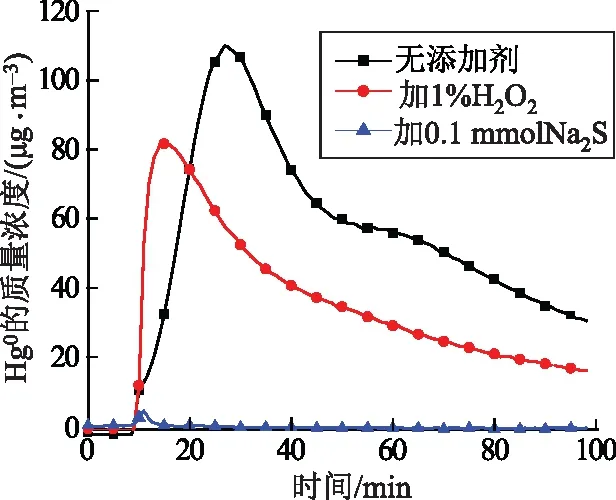
图9 添加剂与Hg0释放质量浓度曲线
(12)
H2O2对汞还原的抑制主要是由于H2O2的强制氧化性,H2O2分解生成强氧化能力的羟基自由基·OH和羧基自由基·OOH。Hg0的氧化机理见反应式(13)和(14)[15-16]。H2O2不仅能氧化Hg0,还能氧化浆液中的S(IV),S(IV)的物质的量降低又促进汞的还原。实验结果表明,加入H2O2溶液后汞的释放率仍然很高,但是可以预计在持续加入H2O2溶液的情况下,能够取得更好的抑制效果。
2Hg0+ 2·OOH++ 2H+→ Hg2++ 2H2O2.
(13)
2Hg2++ 2·OOH + 2H+→Hg2++ 2H2O2.
(14)
3 结论

b) 浆液温度升高导致汞还原反应中的活化分子数增加,使得汞的二次释放加剧;高pH值时溶液中的OH-离子与Hg2+结合,降低了溶液中的离子汞浓度,二次释放率降低。因此,在燃煤电厂WFGD系统实际工作中,在保证有效的脱硫运行工况下,可适当控制脱硫塔内浆液温度及pH值,减少浆液中Hg2+还原。

d) 在浆液中添加Na2S和H2O2两种添加剂,分别生成汞的沉淀与增强溶液氧化性2种方式来抑制汞的还原。Na2S与Hg2+生成HgS沉淀,汞基本不再释放;H2O2溶液本身具有强氧化性,强制氧化单质汞,使汞还原率降低。
[1] 刘迎晖,郑楚光,程俊峰,等.燃煤烟气中汞的形态及其分析方法[J].燃料化学学报,2000,28(5):463-467.
LIU Yinghui,ZHENG Chuguang,CHENG Junfeng,et al.The Form of Mercury and Its Analysis Method in Flue Gas[J].Journal of Fuel Chemistry and Technology,2000,28(5):463-467.
[2] 吴其荣,杜云贵,聂华,等.燃煤电厂汞的控制及脱除[J].热力发电,2012(1):8-11.
WU Qirong,DU Yungui,NIE Hua,et al.Control and Removal of Mercury in Coal-fired Power Plants[J].Thermal Power Gerneration,2012(1):8-11.
[3] SRIVASTAVA R K,HUTSON N,MARTIN B,et al.Control of Mercury Emissions from Coal-fired Electric Utility Boilers[J].Environmental Science & Technology,2006,40(5):1385-1393.
[4] NOLAN P S,REDINGER K E,AMRHEIN G T,et al.Demonstration of Additive Use for Enhanced Mercury Emissions Control in Wet FGD Systems[J].Fuel Processing Technology,2004,85(6):587-600.
[6] 鲍静静,印华斌,杨林军,等.湿法烟气脱硫系统的脱汞性能研究[J].动力工程,2009 (7):664-670.
BAO Jingjing,YIN Huabin,YANG Linjun,et al.Demercuration Performance of Wet Flue Gas Desulfurization Systems[J].Journal of Power Engineering,2009(7):664-670.
[7] CURRIE J,DEBERRY D W,BLYTHE G,et al.Bench-scale Kinetics Study of Mercury Reactions in FGD Liquors[C]//Proceedings of the DOE-NETL Mercury Control Technology Conference.Pittsburgh:[s.n.],2006.
[8] WANG Y,LIU Y,WU Z,et al.Experimental Study on the Absorption Behaviors of Gas Phase Bivalent Mercury in Ca-based Wet Flue Gas Desulfurization Slurry System[J].Journal of Hazardous Materials,2010,183(1):902-907.[9] OMINE N,ROMERO C E,KIKKAWA H,et al.Study of Elemental Mercury Re-emission in a Simulated Wet Scrubber[J].Fuel,2012,91(1):93-101.
[10] LIU Y,WANG Y,WU Z,et al.A Mechanism Study of Chloride and Sulfate Effects on Hg2+Reduction in Sulfite Solution[J].Fuel,2011.90(7):2501-2507.
[11] ABABNEH F A,SCOTT S L,Al-REASI H A,et al.Photochemical Reduction and Reoxidation of Aqueous Mercuric Chloride in the Presence of Ferrioxalate and Air[J].Sci Total Environ,2006,367(2/3):831-939.
[13] WO J,ZHANG M,CHENG X,et al.Hg2+Reduction and Re-emission from Simulated Wet Flue Gas Desulfurization Liquors[J].Hazard Mater,2009.172(2/3):1106-1110.
[14] GHORISHI B,DOWNS B,RENNINGER S.Role of Sulfides in the Sequestration of Mercury by Wet Scrubbers[C]//Combined Power Plant Air Pollutant Control Mega Symposium.Maryland:[s.n.],2006.
[15] LU D,ANTHONY E J,TAN Y,et al.Mercury Removal from Coal Combustion by Fenton Reactions-Part A:Bench-scale Tests[J].Fuel,2007,86(17):2789-2797.
[16] TAN Y,LU D,ANTHONY E J,et al.Mercury Removal from Coal Combustion by Fenton Reactions Paper B:Pilot-scale Tests[J].Fuel,2007,86(17):2798-2805.
(编辑 阚杰)
Secondary Release Characteristic of Mercury in Limestone Wet Flue Gas Desulfurization System
MENG Dongdong1, WANG Xuan2, YANG Tao2, ZHANG Cheng2
(1.Guangzhou China Power Lixin Electricity Industrial Co., Ltd., Guangzhou, Guangdong 511340, China; 2.School of Energy and Power Engineering, Huazhong University of Science and Technology, Wuhan, Hubei 430074, China)

coal-fired boiler; flue gas desulfurization; mercury; secondary release
2016-09-06
广东省省部产学研结合项目(2013B090500008);国家自然科学基金资助项目(51006042)
10.3969/j.issn.1007-290X.2016.11.004
X701
A
1007-290X(2016)11-0018-05
孟东栋(1983),男,河北邢台人。助理工程师,工学学士,主要从事电厂节能技术监督、技术创新方面工作。
王炫(1992),男,湖北洪湖人。在读硕士研究生,主要研究方向为燃煤电厂烟气脱硫脱硝。
杨涛(1978),男,湖北襄阳人。副教授,硕士生导师,工学博士,主要研究方向为热能工程/发电设备自动控制、建模与仿真;旋转机械(风力机)状态监测和故障诊断等。
