HPLC法同时测定风湿关节炎片中4种成分的含量Δ
2016-12-15逯雯洁刘亚蓉韩晓萍刘学良青海省药品检验检测院西宁810016
逯雯洁,刘亚蓉,韩晓萍,刘学良(青海省药品检验检测院,西宁 810016)
HPLC法同时测定风湿关节炎片中4种成分的含量Δ
逯雯洁*,刘亚蓉,韩晓萍,刘学良(青海省药品检验检测院,西宁 810016)
目的:建立同时测定风湿关节炎片中盐酸麻黄碱、盐酸伪麻黄碱、马钱子碱、士的宁含量的方法。方法:采用高效液相色谱法。色谱柱为XTerra-C18,流动相为乙腈-0.01 mol/L庚烷磺酸钠与0.01 mol/L磷酸二氢钾的等量混合溶液(用磷酸调pH至2.8)(梯度洗脱),流速为1.0 ml/min,检测波长为206 nm(盐酸麻黄碱和盐酸伪麻黄碱)、260 nm(马钱子碱和士的宁),柱温为30℃,进样量为10µl。结果:盐酸伪麻黄碱、盐酸麻黄碱、马钱子碱和士的宁检测质量浓度线性范围分别为0.916~18.320 0µg/ml(r=0.999 6)、10.034~200.680 0µg/ml(r=0.999 7)、8.693~121.700 0µg/ml(r=0.999 9)、9.696~193.920 0µg/ml(r=0.999 9);定量限分别为0.03、0.07、0.04、0.03 ng,检测限分别为0.01、0.02、0.01、0.01 ng;精密度、稳定性、重复性试验的RSD<2.0%;加样回收率分别为97.30%~99.79%(RSD=0.96%,n=6)、95.81%~99.36%(RSD=0.38%,n=6)、95.34%~99.93%(RSD=2.00%,n=6)、95.59%~99.80%(RSD=1.76%,n=6)。结论:该方法操作简便、结果准确,可用于同时测定风湿关节炎片中盐酸麻黄碱、盐酸伪麻黄碱、马钱子碱、士的宁的含量。
高效液相色谱法;风湿关节炎片;盐酸麻黄碱、盐酸伪麻黄碱、马钱子碱、士的宁;含量测定
风湿关节炎片由马钱子(调制粉)、麻黄、当归、苍术、续断、桃仁、红花、乳香、没药、千年健、地枫皮、羌活、地龙、桂枝、穿山甲、木瓜、牛膝等17味中药材组成,其中马钱子具有通络止痛、散风消肿的作用,可用于治疗风湿顽癖、麻木瘫痪、关节肿痛;麻黄具有发散风寒、利水消肿的作用,能祛风除湿;苍术、羌活、桂枝、木瓜、地枫皮、桃仁、穿山甲等具有活血通络、消肿止痛的作用;地龙善于走窜,能祛除隐藏在皮肉、筋膜、关节经络等处的风寒湿邪气;牛膝补肝肾、强筋骨、祛风湿、利关节、能引药下行。诸药合用共奏祛风燥湿、活血止痛之功效,可用于风湿痹痛、腰腿疼痛、风湿性关节炎等症的治疗,疗效较好。该制剂收载于卫生部《药品标准中药成方制剂》(第三册)[1],该标准中质量控制项仅有性状鉴别和片剂常规检查,无相应含量测定项[2-8];且现有相关文献[2-3]也仅针对该制剂中的单一成分进行含量测定。因此,笔者采用高效液相色谱法(HPLC)建立了同时测定风湿关节炎片中君药马钱子的主要成分(马钱子碱和士的宁)、麻黄的主要成分(盐酸麻黄碱和盐酸伪麻黄碱)[9]含量的方法,以期为完善该制剂的质量标准提供参考。
1 材料
1.1 仪器
2695型HPLC仪,包括四元泵、2998光电二极管阵列检测器、自动进样器、Empower色谱工作站(美国Waters公司);CPA225D型万分之一电子天平(德国Sartorius公司);XS105DU型十万分之一电子天平(瑞士Mettler-Toledo公司);Milli-QA型超纯水器(美国Millipore公司);KQ5222V型超声波清洗器(昆山市超声仪器有限公司,功率:500 W,频率:40 kHz)。
1.2 药品与试剂
风湿关节炎片(国家评价性市场抽检:厂家A,编号:S1;厂家B,编号:S2;厂家C,编号:S3;厂家D,编号:S4;厂家E,编号:S5;厂家F,编号:S6;厂家G,编号:S7;厂家H,编号:S8;厂家I,编号:S9;厂家J,编号:S10);盐酸伪麻黄碱对照品(批号:171237-200807,纯度:99.9%)、盐酸麻黄碱对照品(批号:171241-201007,纯度:99.7%)、马钱子碱对照品(批号:110706-200505,纯度:95.9%)、士的宁对照品(批号:0705-200005,纯度:96%)均购自中国食品药品检定研究院;乙腈为色谱纯,其余试剂均为分析纯,水为去离子水。
2 方法与结果
2.1 色谱条件
色谱柱:XTerra C18(250 mm×4.6 mm,5µm);流动相:乙腈(A)-0.01 mol/L庚烷磺酸钠与0.01 mo1/L磷酸二氢钾的等量混合溶液(用磷酸调节pH至2.8)(B),梯度洗脱(洗脱程序见表1);流速:1.0 ml/min;检测波长:260 nm(马钱子碱和士的宁)、206 nm(盐酸麻黄碱和盐酸伪麻黄碱);柱温:30℃;进样量:10µl。
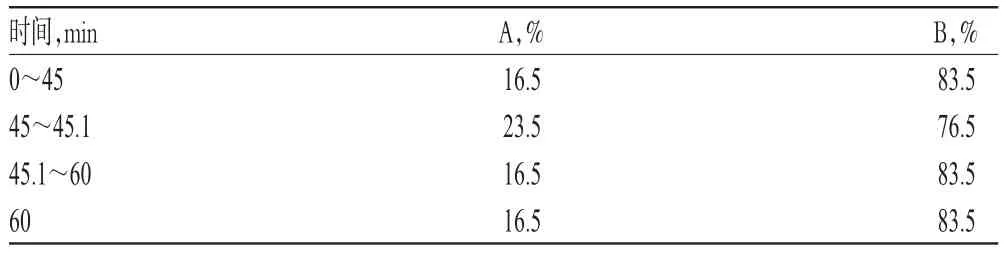
表1 梯度洗脱程序Tab 1 Conditions of gradient elution
2.2 溶液的制备
2.2.1 混合对照品溶液 精密称取盐酸伪麻黄碱对照品9.17 mg、盐酸麻黄碱对照品50.32 mg、马钱子碱对照品63.45 mg、士的宁对照品48.48 mg,分别置于50、25、50、25 ml量瓶中,加甲醇溶解并定容,制成每1 ml含盐酸伪麻黄碱183.2µg、盐酸麻黄碱2 006.8µg、马钱子碱1 217.0µg、士的宁1 939.2µg的单一对照品贮备液。取上述单一对照品贮备液适量,置于50 ml量瓶中,加甲醇制成每1 ml含盐酸伪麻黄碱9.16µg、盐酸麻黄碱100.34µg、马钱子碱86.93µg、士的宁96.96µg的混合对照品溶液。
2.2.2 供试品溶液 取样品适量,研细,取样品粉末约2 g,精密称定,置于20 ml锥形瓶中,加5%氢氧化钠溶液约4 ml,混匀,超声处理2 min;精密加入三氯甲烷25 ml,称定质量,于70℃水浴回流提取120 min,取出,放冷,称定质量,用三氯甲烷补足减失的质量,摇匀,经0.45µm微孔滤膜滤过,取续滤液,即得。
2.2.3 阴性对照溶液 按样品的处方比例和工艺分别制备缺麻黄和马钱子的阴性样品,再按“2.2.2”项下方法制备阴性对照溶液A和B。
2.3 系统适用性试验
精密量取“2.2”项下混合对照品溶液、供试品溶液和阴性对照溶液各适量,按“2.1”项下色谱条件进样测定,记录色谱,详见图1。在该色谱条件下,各成分均能达到基线分离,分离度>1.5;理论板数均>3 000。206 nm波长处阴性对照A未出现与盐酸麻黄碱、盐酸伪麻黄碱对照品保留时间一致的色谱峰,260 nm波长处阴性对照B未出现与马钱子碱、士的宁对照品保留时间一致的色谱峰。结果表明,其他成分对测定无干扰。
2.4 线性关系考察
分别精密量取“2.2.1”项下混合对照品溶液0.1、0.2、0.5、1、2、5 ml,分别置于10 ml量瓶中,加甲醇定容,摇匀,即得系列线性溶液。取上述系列线性溶液适量,按“2.1”项下色谱条件进样测定,记录峰面积。以待测成分质量浓度(x,µg/ml)为横坐标、峰面积(y)为纵坐标进行线性回归,回归方程与线性范围见表2。
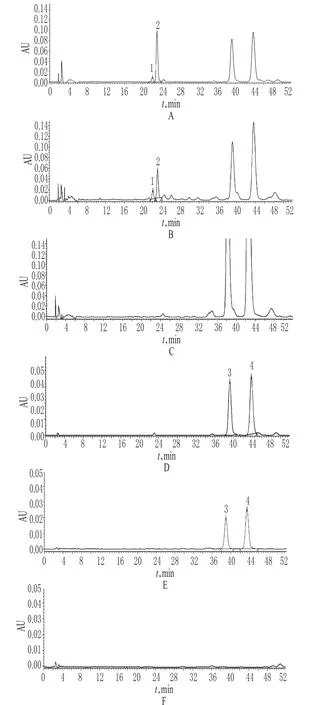
图1 高效液相色谱图A.混合对照品(206 nm);B.供试品(206 nm);C.阴性对照A(206 nm);D.混合对照品(260 nm);E.供试品(260 nm);F.阴性对照B(260 nm);1.盐酸伪麻黄碱;2.盐酸麻黄碱;3.马钱子碱;4.士的宁Fig lHPLC chromatogramsA.mixed reference substance(206 nm);B.test sample(206 nm);C.negative control without A(206 nm);D.mixed reference substance(260 nm);E.test sample(260 nm);F.negative control without B(260 nm);1.pseudoephedrine hydrochloride;2.ephedrine hydrochloride;3.brucine;4.strychnine
2.5 定量限与检测限考察
取“2.2.1”项下混合对照品溶液适量,等倍逐步稀释,按“2.1”项下色谱条件连续进样测定6次,记录峰面积。当信噪比为10:1时,得定量限(LOQ);当信噪比为3∶1时,得检测限(LOD),结果见表3。
2.6 精密度试验

表2 回归方程与线性范围Tab 2 Regression equations and linear ranges

表3 定量限与检测限测定结果Tab 3 Determination results of quantitation limits and detection limits
精密量取“2.2.1”项下混合对照品溶液适量,按“2.1”项下色谱条件连续进样测定6次,记录峰面积。结果,盐酸伪麻黄碱、盐酸麻黄碱、马钱子碱、士的宁峰面积的RSD分别为0.09%、0.09%、0.13%、0.47%(n=6),表明仪器精密度良好。
2.7 稳定性试验
取同一供试品溶液(编号:S1)适量,分别于室温下放置2、4、6、8、10 h时按“2.1”项下色谱条件进样测定,记录峰面积。结果,盐酸伪麻黄碱、盐酸麻黄碱、马钱子碱、士的宁峰面积的RSD分别为0.29%、0.55%、0.14%、0.09%(n=5),表明供试品溶液在室温下10 h内稳定性良好。
2.8 重复性试验
取样品(编号:S1)适量,研细,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并计算样品平均含量。结果,盐酸伪麻黄碱、盐酸麻黄碱、马钱子碱、士的宁平均含量分别为0.07、0.08、0.23、0.33 mg/片,RSD分别为1.7%、1.3%、0.7%、1.0%(n=6),表明本方法重复性良好。
2.9 加样回收率试验
取样品(编号:S1)适量,研细,共6份,分别置于10 ml量瓶中,分别加入一定质量的盐酸伪麻黄碱、盐酸麻黄碱、马钱子碱、士的宁对照品,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并计算加样回收率,结果见表4。
2.10 样品含量测定
取10批样品适量,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并计算样品含量,结果见表5。
3 讨论
3.1 提取方式、提取溶剂和提取时间的选择
本试验比较了超声提取和回流提取两种不同的提取方式对提取效果的影响。结果,回流提取的提取效率更高,故选择回流提取为本试验的提取方式。此外,还考察了甲醇、乙酸乙酯、三氯甲烷3种提取溶剂。结果,三氯甲烷的提取效率最高,故选择三氯甲烷为本试验的提取溶剂。提取时间考察了10、30、60、90、120、140 min。结果,回流提取120 min时盐酸麻黄碱、盐酸伪麻黄碱、马钱子碱、士的宁的提取效果较好,当回流提取超过120 min,各成分提取效率差异不大。因此,确定120 min为本试验的提取时间。
3.2 检测波长的选择

表4 加样回收率试验结果(n=6)Tab 4 Results of recovery tests(n=6)

表5 样品含量测定结果(n=3,mg/片)Tab 5 Determination results of contents in samples(n=3,mg/tablet)
本试验采用光电二极管阵列检测器对盐酸麻黄碱、盐酸伪麻黄碱、马钱子碱、士的宁进行190~400 nm紫外全波长扫描。结果,4种成分均有很强的末端吸收。其中,马钱子碱在264 nm波长处、士的宁在256 nm波长处有次强吸收,盐酸麻黄碱与盐酸伪麻黄碱分别在263、257 nm波长处有极其微弱的吸收。综合考虑4种成分的光谱特点及参考相关文献[10-12],本试验选择206 nm波长检测盐酸伪麻黄碱和盐酸麻黄碱(仅存在末端强吸收)、260 nm波长检测马钱子和士的宁(206 nm波长处吸收值较高,考虑末端吸收存在相应检测弊端,故选择次强吸收260 nm)。
综上所述,本方法操作简便、结果准确,可用于同时测定风湿关节炎片中盐酸麻黄碱、盐酸伪麻黄碱、马钱子碱、士的宁的含量。
[1] 国家药典委员会.中华人民共和国卫生部药品标准中药成方制剂:第三册[S].WS3-B-0560-91:1991.
[2] 胡爽,李晓妮,葛新,等.风湿关节炎片中麻黄碱的HPLC测定[J].中草药,2005,36(1):62.
[3] 蔡州,李海松,张滢.HPLC法测定风湿关节炎片中士的宁的含量[J].中医研究,2006,19(5):24.
[4] 刘会东,李春英,叶敏,等.风湿关节炎片质量标准研究[J].药物分析杂志,2008,28(2):291.
[5] 吴莉莉,杨飞.风湿关节炎片中士的宁含量测定方法的改进[J].风湿病与关节炎,2014,3(11):34.
[6] 王光函,邸子真,赵玥,等.高效液相色谱法测定芩双片中盐酸麻黄碱和盐酸伪麻黄碱含量[J].中国药业,2014,23(2):40.
[7] 周军,张蕾,张茉,等.HPLC法同时测定香连化滞丸中7种成分的含量[J].中国药房,2016,27(6):840.
[8] 周玲,孙汉斌,邓旭坤,等.高效液相色谱法测定3种马钱属药材中士的宁和马钱子碱的含量[J].中国医院药学杂志,2012,32(16):1 301.
[9] 单婷婷,曹红,邢俊波,等.HPLC法测定麝香接骨胶囊中四种生物碱的含量[J].解放军药学学报,2013,29(5):450.
[10] 郭青,孙姗,吕霞,等.反相离子对高效液相色谱法测定疏风活络丸中4种生物碱的含量[J].药物分析杂志,2009,29(1):6.
[11] 刁国兰、张贵华、马云淑,等.HPLC测定马钱子及其提取物中马钱子碱和士的宁含量[J].中国中医药信息杂志,2013,20(12):51.
[12] 陈卫平,王伟影,毛菊华.HPLC法测定追风舒筋活血片中马钱子碱、士的宁的含量[J].中国药师,2016,19(1):191.
Simultaneous Setermination of Four Components of RheumatoidArthritis Tablet by HPLC
LU Wenjie,LIU Yarong,HAN Xiaoping,LIU Xueliang(Qinghai Institute for Drug Control,Xining 810016,China)
OBJECTIVE:To establish a method for simultaneous determination of ephedrine hydrochloride,pseudoephedrine hydrochloride,brucine,strychnine in Rheumatoid arthritis tablet.METHODS:HPLC was performed on column of XTerra-C18with mobile phase of acetonitrile-mixed solution(pH was adjusted to 2.8 with phosphate acid)composing of 0.01 mol/L sodium heptanesulfonate solution and equal quantity of 0.01 mol/L potassium dihydrogen phosphate solution at a flow rate of 1.0 ml/min,detection wavelength was 206 nm for ephedrine hydrochloride and pseudoephedrine hydrochloride,260 nm for brucine and strychnine,column temperature was 30℃,and injection volume was 10µl.RESULTS:The linear range was 0.916-18.320 0µg/ml for pseudoephedrine hydrochloride(r=0.999 6),10.034-200.680 0µg/ml for ephedrine hydrochloride(r=0.999 7),8.693-121.700 0µg/ml for brucine(r=0.999 9)and 9.696-193.920 0µg/ml for strychnine(r=0.999 9);limits of quantification were 0.03,0.07,0.04,0.03 ng,limits of detection were 0.01,0.02,0.01,0.01 ng;RSDs of precision,stability and reproducibility tests were lower than 2.0%;recoveries were 97.30%-99.79%(RSD=0.96%,n=6),95.81%-99.36%(RSD=0.38%,n=6),95.34%-99.93%(RSD=2.00%,n=6)and 95.59%-99.80%(RSD=1.76%,n=6).CONCLUSIONS:The method is simple,accurate,and can be used for the simultaneous determination of ephedrine hydrochloride,pseudoephedrine hydrochloride,brucine,strychnine in Rheumatoid arthritis tablet.
HPLC;Rheumatoid arthritis tablet;Ephedrine hydrochloride;Pseudoephedrine hydrochloride;Brucine;Strychnine;Content determination
R927.2
A
1001-0408(2016)33-4692-04
2015-12-13
2016-09-02)
(编辑:刘 柳)
国家药品计划抽验项目(No.2014)
*主管药师,硕士。研究方向:中藏药检验分析。电话:0971-8232182。E-mail:luwenjie608@hotmail.com
DOI 10.6039/j.issn.1001-0408.2016.33.28
