氟维司群500 mg治疗激素受体阳性复发转移性乳腺癌的疗效观察
2016-12-15宋国红邸立军张如艳宛凤玲李惠平
宋国红,邸立军,邵 彬,张如艳,冉 然,王 环,雷 雯,宛凤玲,李惠平
北京大学肿瘤医院暨北京市肿瘤防治研究所,乳腺肿瘤内科,恶性肿瘤发病机制及转化研究教育部重点实验室,北京 100142
氟维司群500 mg治疗激素受体阳性复发转移性乳腺癌的疗效观察
宋国红,邸立军,邵彬,张如艳,冉然,王环,雷雯,宛凤玲,李惠平
北京大学肿瘤医院暨北京市肿瘤防治研究所,乳腺肿瘤内科,恶性肿瘤发病机制及转化研究教育部重点实验室,北京 100142
复发转移性乳腺癌;氟维司群;激素受体阳性;无进展生存时间
对于激素受体阳性复发转移性乳腺癌,如果疾病进展较缓慢,无内脏转移危象,内分泌治疗是首选的治疗手段[1]。氟维司群是一种新型的选择性雌激素受体(estrogen receptor,ER)下调剂,它能高亲和力地结合、阻断并下调ER,发挥了完全的抗雌激素作用[2]。氟维司群的疗效具有剂量依赖效应[3],CONFIRM研究证实,对既往内分泌治疗后进展的绝经期乳腺癌患者采用氟维司群500 mg与250 mg治疗,二者相比,500 mg在无进展生存期(progression-free survival,PFS)及总生存期(overall survival,OS)方面均都有显著优势[4-5]。本研究回顾性分析了500 mg氟维司群在中国ER阳性复发转移性乳腺癌患者中的疗效和安全性,并对可能的影响因素做相关分析。
1 资料和方法
1.1一般资料
回顾性分析2014年1月—2015年12月在北京大学肿瘤医院乳腺肿瘤内科接受氟维司群500 mg治疗的62例激素受体阳性的复发转移性乳腺癌患者。
1.2治疗方案
氟维司群500 mg于第1、14和28天深部肌肉注射,之后每28 d天重复,28 d为1个周期,治疗至患者出现疾病进展、不良反应不可耐受、患者拒绝用药或失访,每2~3个周期进行疗效评价。6例人表皮生长因子受体2(human epidermal growth factor receptor-2,HER-2)阳性患者,均为既往曲妥珠单抗治疗失败的患者,1例为曲妥珠单抗和拉帕替尼治疗均进展后的患者。2例目前应用拉帕替尼联合氟维司群,4例为单用氟维司群。
1.3观察指标及评价标准
PFS定义为从患者接受氟维司群治疗开始至肿瘤进展或患者死亡的时间。OS定义为从患者接受氟维司群治疗开始至患者死亡或末次随诊的时间。按照实体瘤疗效评价标准(response evaluation criteria in solid tumors,RECIST)1.1对治疗效果进行评价[6]。疗效分为完全缓解(complete response,CR)、部分缓解(partial response,PR)、疾病稳定(stable disease,SD)和疾病进展(progressive disease,PD)。CR为所有病灶消失,无新病灶出现;PR为病灶最大直径之和减少30%;SD为病灶最大直径之和缩小未达到PR,或增大未达到PD;PD为病灶最大直径之和增加大于等于20%,或出现新病灶。客观缓解率(objective response rate,ORR)为发生CR和PR的患者例数与总例数的比值;临床不良反应分级按照美国国立癌症研究院通用毒性标准(National Cancer Institute Common Toxicity Criteria,NCI-CTC) 4.03进行评估[7]。
1.4统计学处理
所有数据均采用SPSS 18.0统计软件进行分析。PFS及OS使用Kaplan-Meier方法进行生存分析。两组间的单变量比较采用Log-rank检验,多因素分析采COX比例风险回归模型。所有P值及置信区间均采用双侧检验,P<0.05为差异有统计学意义。
2 结果
2.1患者临床病理特征
62例接受500 mg氟维司群治疗的患者的中位年龄为59岁(40~92岁),其中44例为绝经后患者,18例为应用卵巢抑制药物患者。所有患者均为受体阳性患者,ER阳性患者59例(95.2%),其他3例为ER阴性,PR阳性。患者临床病理特征见表1。
2.2疗效
62例患者均可以评价近期疗效。其中PR 5例(8.1%),SD 29例(46.8%),PD 28例(45.2%)。中位随访时间为13.3个月(3.6~26.2个月),2例患者失访,50例进展,10例患者尚未进展。患者中位PFS为4.9个月(3.1~6.6个月,图1)。截止到最后随访日期,中位OS尚未达到。死亡14例,46例患者未死亡。患者OS为3~35个月,1年生存率为70.8%,2年生存率为63.6%(图2)。
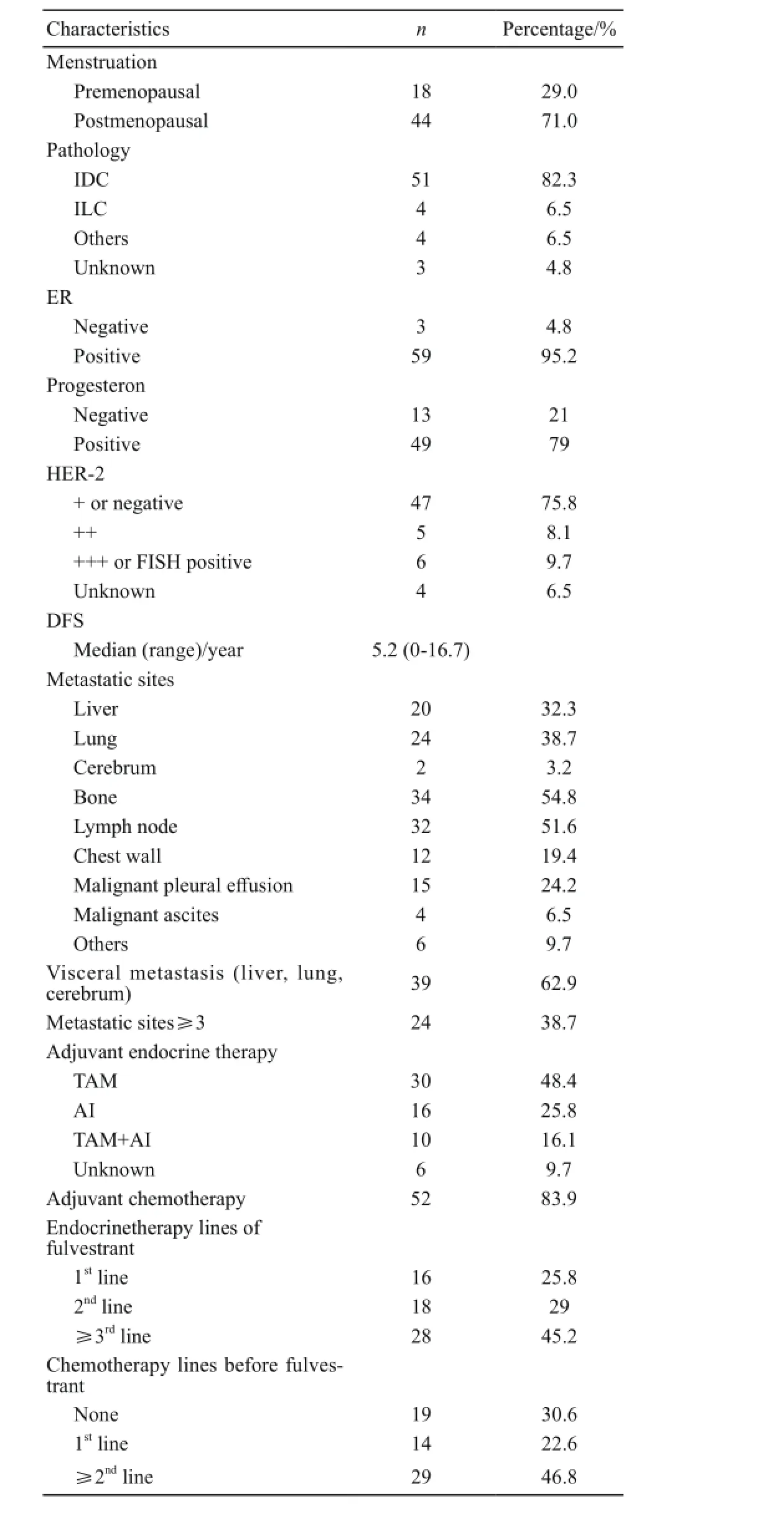
表1 62例氟维司群治疗患者的临床病理特征Tab. 1 The clinicopathological characteristics of the 62 patients received fulvestrant
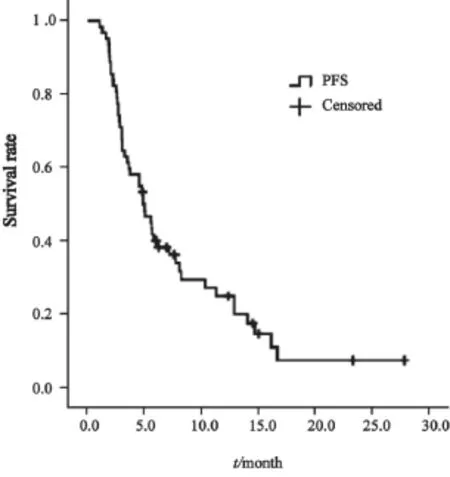
图1 62例氟维司群治疗患者中位PFS为4.9个月(3.1~6.6个月)Fig. 1 The median PFS of 62 patients received fulvestrant was 4.9 months (3.1-6.6 months)
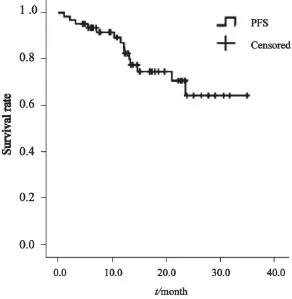
图2 62例氟维司群治疗患者OS分析Fig. 2 The overall survival of the 62 patients received fulvestrant
2.3临床病理特征对PFS的影响
单因素分析:对月经状态、ER、孕激素受体、HER-2、是否内脏转移、大于等于3个转移部位、辅助内分泌治疗分类、是否辅助化疗、氟维司群治疗时内分泌线数、氟维司群治疗前化疗线数、氟维司群治疗时化疗+内分泌线数、无病生存时间(disease free survival,DFS)进行Log-rank单因素分析,差异均无统计学意义(P>0.05)。进一步将以上因素纳入Cox多因素分析,氟维司群使用前化疗线数显著影响患者PFS(P=0.008,HR=2.75,表2)。

表2 患者临床病理特征对于PFS的影响Tab. 2 The influence of the 62 patients’ clinicopathological characteristics on progression free survival
2.4不良事件
12例患者注射部位疼痛3级,1例患者出现臀部注射部位血肿,对症治疗后约1个月吸收,无后遗症。其余未见严重不良事件。
3 讨论
既往研究显示,氟维司群250 mg在二线内分泌治疗中与阿那曲唑1 mg疗效相当,PFS差异无统计学意义[8],而氟维司群500 mg无论在PFS还是OS均优于氟维司群250 mg[4-5],因此目前氟维司群的常规推荐剂量为500 mg。
氟维司群500 mg同样在一线治疗中也获得了非常好的疗效,与阿那曲唑1 mg相比,TTP和OS均显示出明显的优势[9],已有的回顾性分析结果也显示,早期一线应用的疗效优于二线及以后的治疗[10-11]。在本回顾性分析中,超过90%的患者在辅助治疗阶段应用过他莫昔芬或芳香化酶抑制剂,应用氟维司群中位PFS为4.9个月,与以往报道数据类似,但一线、二线及二线以上治疗的PFS分别为5.6、4.9及4.8个月,差异无统计学意义(P=0.624)。
在影响PFS因素的单因素分析中,因为入组患者数较少,未能显示出明确的显著相关因素,但一些观察到的临床数据仍然能给我们一些提示:ER阳性者较ER阴性者(孕激素受体阳性)PFS长,分别为4.9和3个月,说明ER对于指导内分泌治疗的意义大于孕激素受体;HER-2阴性者较HER-2阳性者PFS长,分别为4.8与3个月,说明HER-2阳性者与ER通路之间存在一些交叉影响;转移数目小于3个的较大于等于3个的PFS长,分别为5.6和3个月,说明肿瘤负荷小的更容易从内分泌治疗中获益;未行辅助化疗的较行辅助化疗的PFS长,分别为10.3与4.5个月,说明恶性度低分期早的患者(这些患者往往不需要辅助化疗)即使复发后仍然更容易从内分泌治疗中获益;氟维司群治疗前无化疗者较多线化疗后的PFS长,无化疗、一线化疗后、二线及以上化疗后的PFS分别为5.6、3.7和3.3个月,说明早期应用内分泌治疗的重要性,而且在多因素分析中也支持这个结果;但是DFS时间大于等于5年者较小于5年的PFS却短,分别为3.6和5.6个月,差异无统计学意义,有可能是因为本研究中仅16例患者为一线治疗,其他绝大多数患者后续治疗较复杂,影响了DFS的因素。本研究62例患者无严重不良事件出现,安全性高,耐受性好。
总之,本研究显示对于复发转移性乳腺癌,氟维司群500 mg无论是一线应用还是在多线内分泌及化疗失败后应用,均能获得较好的疗效,且对有内脏转移者同样有效。
[1] CARDOSO F, COSTA A, NORTON L, et al. ESO-ESMO 2ndinternational consensus guidelines for advanced breast cancer (ABC2) dagger[J]. Ann Oncol, 2014, 25(10): 1871-1888.
[2] LONGX, NEPHEWKP. Fulvestrant (I C I 182,780)-dependent interacting proteins mediate immobilization and degradation of estrogen receptor-alpha[J]. J Biol Chem, 2006, 281(14): 9607-9615.
[3] ROBERTSON J F, NICHOLSON R I, BUNDRED N J. Comparison of the short-term biological effects of 7alpha-[9-(4,4,5,5,5-pentafluoropentylsulfinyl)-nonyl]estra-1,3,5, (10)-triene-3,17beta-diol (Faslodex) versus tamoxifen in postmenopausal women with primary breast cancer [J]. Cancer Res, 2001, 61(18): 6739-6746.
[4] DI LEO A, JERUSALEM G, PETRUZELKA L, et al. Results of the CONFIRM phase Ⅲ trial comparing fulvestrant 250 mg with fulvestrant 500 mg in postmenopausal women with estrogen receptor-positive advanced breast cancer[J]. J Clin Oncol, 2010, 28(30): 4594-4600.
[5] DI LEO A, JERUSALEM G, PETRUZELKA L, et al. Final overall survival: fulvestrant 500 mg vs 250 mg in the randomized CONFIRM trial[J]. J Natl Cancer Inst, 2014, 106(1): 337.
[6] EISENHAUER, E A, THERASSE P, BOGAERTS J, et al. New response evaluation criteria in solid tumours: revised RECIST guideline (version 1.1)[J]. Eur J Cancer, 2009, 45(2): 228-247.
[7] National Cancer Institute. NCI common terminology criteria for adverse events (CTCAE)v.4.03[EB/OL].http://evs.nci. nih.gov/ftp1/CTCAE/About.html, 2015-01-14.
[8] HOWELL A, ROBERTSON J F, ABRAM P, et al. Comparison of fulvestrant versus tamoxifen for the treatment of advanced breast cancer in postmenopausal women previously untreated with endocrine therapy: a multinational, double-blind, randomized trial[J]. J Clin Oncol, 2004, 22(9): 1605-1613.
[9] ROBERTSON J F, LINDEMANN J P, LLOMBART-CUSSAC A, et al. Fulvestrant 500 mg versus anastrozole 1 mg for the first-line treatment of advanced breast cancer: follow-up analysis from the randomized ‘FIRST’ study [J]. Breast Cancer Res Treat, 2012, 136(2): 503-511.
[10] 姜航, 王涛, 张少华, 等. 氟维司群治疗曾接受过芳香化酶抑制剂治疗的复发转移性乳腺癌的临床研究[J].中国癌症杂志, 2013, 23(3): 224-228.
[11] 赵燕南, 张淑娟, 陈潇雨, 等. 500 mg氟维司群治疗绝经后雌激素受体阳性转移性乳腺癌患者的疗效和安全性[J]. 中华乳腺病杂志(电子版), 2015, 9(5): 292-297.
Efficacy analysis of fulvestrant 500 mg treatment for patients with hormone receptor-positive advanced breast cancer
SONG Guohong, DI Lijun, SHAO Bin, ZHANG Ruyan, RAN Ran, WANG Huan, LEI Wen, WAN Fengling, LI Huiping
(Key Laboratory of Carcinogenesis and Translational Research, Ministry of Education, Department of Breast Oncology, Peking University Cancer Hospital and Institute, Beijing100142, China)
Correspondence to: LI Huiping E-mail: huipingli2012@hotmail.com
Advanced breast cancer; Fulvestrant; Hormone receptor-positive; Progression free survival
10.19401/j.cnki.1007-3639.2016.11.014
R737.9
A
1007-3639(2016)11-0957-04
李惠平E-mail:huipingli2012@hotmail.com
(2016-05-03
2016-09-10)
