腐植酸作用下γ⁃六氯环己烷在冰相中的光转化
2016-12-14包思琪康春莉钟宇博姚志富黄冬梅王宇寒
包思琪,康春莉,钟宇博,周 林,姚志富,黄冬梅,王宇寒,田 涛
(吉林大学环境与资源学院,地下水资源与环境教育部重点实验室,长春130021)
腐植酸作用下γ⁃六氯环己烷在冰相中的光转化
包思琪,康春莉,钟宇博,周林,姚志富,黄冬梅,王宇寒,田涛
(吉林大学环境与资源学院,地下水资源与环境教育部重点实验室,长春130021)
研究了腐植酸(HA)存在下冰相体系中γ⁃六氯环己烷(γ⁃HCH)的光转化规律.结果表明,HA浓度对γ⁃HCH的光转化率呈现低浓度促进而高浓度抑制的现象;盐离子浓度、及对γ⁃HCH的光转化率均有促进作用;低浓度Fe3+对γ⁃HCH的光转化率有促进作用,当Fe3+的浓度增大到50 μmol/L时,呈现抑制效应;γ⁃HCH在不同pH值条件下光转化速率的大小顺序为碱性>中性>酸性.冰相中HA通过产生单线态氧(1O2)、羟基自由基(·OH)及三重激发态(HA∗)加速γ⁃HCH的光转化.HA存在下γ⁃HCH的光转化产物主要是五氯环己烯、邻二氯苯和对二氯苯、一氯苯,光转化过程中1O2通过消耗中间产物间接加速了γ⁃HCH的光转化过程.
γ⁃六氯环己烷;腐植酸;光转化;冰
冰雪作为地球上非常丰富的物质,在冰雪中发生的化学反应对于有机污染物的归宿及大气组成至关重要[1].研究者们普遍认为,水溶液冻冰后会形成微囊、晶粒边界、纹脉、节点和气⁃冰界面(QLL层)[2],这些统称为类似液体层(LLL层).Kahan等[3~6]研究发现,QLL层这一无序结构部分具有独特的性质.溶液结冰时,大多数有机和无机溶质会进入QLL中而使浓度增大[7,8],这种现象被称为冷冻浓缩效应.冷冻浓缩效应能够加快冰中的反应,甚至改变污染物的降解途径及产物[9].Jonathan等[10]研究发现,添加有光敏剂玫瑰红(RB)的糠醇、色氨酸和双酚A在冰相中的降解率分别是水相中降解率的6400倍、8300倍和50倍.Grannas等[7]研究了冰相温度和溶质浓度对吡啶亲核取代芳香族硝基苯甲醚反应的影响,由于冷冻浓缩效应,在-37℃时,反应速率提高了约40倍,反应速率受温度和离子强度的影响.这种加速现象对于二阶或高阶反应、低浓度反应和反应活化能小的反应尤其重要[11].污染物在冰雪中发生的化学反应能够影响大气及融雪后水流经过的土壤和地表水的化学成分,影响着环境中有机污染物的归趋[12~14].光化学反应是冰雪中污染物最主要的转化途径,因此,研究冰相中有机污染物的光转化具有十分重要的意义.
光化学反应除了直接光转化外,由光敏剂引发的间接光转化也会有效促进有机污染物的降解.腐植酸(HA)作为一种重要的天然光敏剂,能够吸收可见光生成三重激发态及各种活性氧自由基(包括羟基自由基、单线态氧及过氧化氢),从而诱导有机物发生间接光化学降解[15].此外,由于腐植酸广泛存在于土壤、河流、湖泊及海洋水体和沉积物中,因此对全球碳循环,有机物和无机物在自然界的分布、迁移、转化和归宿等行为有非常重要的影响[16,17].
有机氯农药γ⁃六氯环己烷(γ⁃HCH)是一种优先控制污染物,已被列入斯德哥尔摩公约受控物质清单.环境中的γ⁃HCH主要是通过微生物降解和光化学降解而减少,然而在冰相中微生物作用相对较弱,此时光化学降解发挥了重要的作用.本文选取γ⁃HCH为目标污染物,研究了HA存在下冰相体系中有机污染物的光转化规律,进一步揭示了环境中有机污染物在自然冰相环境中的迁移转化机制,为研究持久性有机污染物的全球归趋模式提供了理论依据.
1 实验部分
1.1 试剂与仪器
γ⁃HCH(纯度>98.6%),德国Dr.Ehrenstorfer公司;腐植酸(HA,化学纯),天津市光复精细化工研究所;正己烷和异丙醇(色谱纯),美国天地Tedia公司;磷酸二氢钾、磷酸氢二钾、硫酸铁、硝酸钠、亚硝酸钠和叠氮化钠(分析纯),北京化工厂.
GC⁃2010plus气相色谱仪,日本岛津公司;Agilent 6890N气相色谱⁃质谱联用仪(GC⁃MS),美国安捷伦科技公司;UVmini⁃1240紫外分光光度计,美国Perkin Elmer公司;80 W荧光高压汞灯,上海飞利浦亚明照明有限公司;pHS⁃3C型精密酸度计,上海雷磁仪器厂;Frestech BC/BD⁃261卧式转换型冷藏/冷冻箱,河南新飞电器公司;ST⁃92型照度计,北京师范大学光电仪器厂.
1.2 实验过程
1.2.1 实验方法 将HA和γ⁃HCH的混合溶液分装于若干玻璃管(10 mm×150 mm)中(λ>280 nm),每管装6 mL,使用玻璃塞密封,分别置于冰柜中于-15℃冰冻光照或置于通风橱中于15℃室温光照.当考察其它因素对γ⁃HCH光转化的影响时,则向溶液中添加相应的组分.使用80 W高压汞灯对制备好的样品进行光照,样品距光源12 cm,光强为2.2×104lx.样品分别光照一定时间后取出3个平行样进行测试,取平均值.
1.2.2 γ⁃HCH及其光转化产物分析 在恒温(25℃)条件下将取出的样品融化,取5 mL融化后的样品溶液于萃取瓶中,加入2 mL正己烷,振荡萃取5 min后,静置30 min,取正己烷相进行分析.γ⁃HCH的浓度采用气相色谱仪测定.γ⁃HCH产物分析同样是加正己烷振荡萃取,静置1 d后分离出有机相,进行氮吹浓缩富集.使用气相色谱⁃质谱联用仪分析反应产物.GC和GC⁃MS的分析条件参见文献[18].
2 结果与讨论
2.1 冰相中γ⁃HCH光转化率的影响因素
2.1.1 反应体系和HA浓度的影响 为了验证HA存在下γ⁃HCH在水相(15℃)和冰相(-15℃)中光转化的差别,分别做了水相、冰相中γ⁃HCH的光转化实验,结果见图1.由图1可见,冰相中γ⁃HCH的光转化率比水相中的大,这是由于在冰相中存在冷冻浓缩效应,能够使γ⁃HCH浓缩富集,从而达到更大程度的光转化.同时,在结冰过程中,溶解氧被排出,溶解氧对γ⁃HCH的抑制作用减弱,进一步加速了γ⁃HCH的光转化.
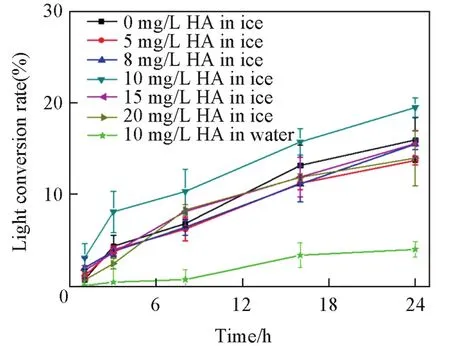
Fig.1 Conversion rate of γ⁃HCH in different concentra⁃tion of humate in ice and water(cγ⁃HCH=60 μg/L)
分别将水相和冰相中γ⁃HCH的光转化反应数据进行准一级动力学拟合,以ln(ct/c0)对t作图,得到光转化反应的表观率常数(k,h-1)和半衰期(t1/2,h):

式中:c0和ct(μg/L)分别为反应初始时刻和t时刻样品中的γ⁃HCH浓度.具体结果如表1所示.

Table 1 The first order kinetics equation and parameters of light conversion of γ⁃HCH
由图1可知,当HA浓度由0增加至20 mg/L时,γ⁃HCH的光转化率呈现先增加后减小的趋势,这主要是由于HA的光敏化作用及光屏蔽作用引起的.HA在光照过程中会吸收可见光而形成单线态氧(1O2)、羟基自由基(·OH)及三重激发态(HA∗),从而诱导γ⁃HCH发生光转化;HA还是一种光屏蔽剂,会导致γ⁃HCH光转化率的减小.因此,当HA浓度由0增加至10 mg/L时,HA的光敏化作用大于光屏蔽作用,γ⁃HCH的光转化率随着HA浓度的增加而增加;然而,随着HA浓度继续增大,HA的光屏蔽作用成为主导作用,导致γ⁃HCH的光转化率随着HA浓度的增加而减小.综上所述,10 mg/L HA时γ⁃HCH光转化率最大,光照24 h后γ⁃HCH光转化率为19.55%,因此在以下实验中HA浓度均采用10 mg/L.
为了验证HA的光屏蔽作用,对不同浓度的HA溶液进行了190~800 nm波段的吸光度测定.由图2可以看出,随着HA浓度的增大,不同波段下的吸光度均随之增大,这一现象验证了HA的光屏蔽作用,同时也证实了随着HA浓度继续增大,HA的光屏蔽作用成为主导作用,导致γ⁃HCH的光转化率随着HA浓度的增加而减小.
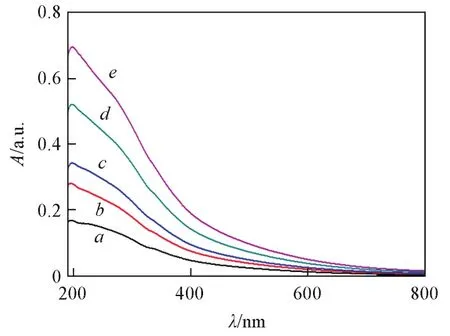
Fig.2 UV⁃Vis spectra of HA of different con⁃centrationsc/(mg·L-1):a.5;b.8;c.10;d.15;e.20.
2.1.2 pH值的影响 根据文献[19]报道,盐离子会对溶液结冰后表面上形成的LLL层的厚度和性质产生影响,从而影响冰相的化学反应.在研究pH值的影响时,若使用一般方法(添加H2SO4和NaOH)调节pH值,在pH值不同的情况下,溶液中盐离子浓度也不相同,从而有可能影响结论的准确性.因此,本实验采用磷酸盐缓冲溶液(PBS)来控制体系的pH值,在保持磷酸盐离子总量不变的情况下,通过改变磷酸氢二钾和磷酸二氢钾的比例调节pH值,以消除盐离子浓度的影响.
图3为不同浓度磷酸盐缓冲溶液作用下,pH值对γ⁃HCH光转化的影响.可见,在上述2个体系中,γ⁃HCH的光转化率均随着pH值的增大而增大.当pH=6时,γ⁃HCH的光转化率比pH=7和pH=8时的低,即在酸性条件下γ⁃HCH的光转化率比在中性和碱性条件下的小,且γ⁃HCH在碱性条件下的光转化率比中性条件下的略高.这是由于γ⁃HCH在光转化过程中脱氯会形成酸,而OH-能够将酸中和,从而有利于光转化过程中脱氯的继续进行[20].同时,由于HA在光敏化过程中会敏化产生·OH和1O2等活性物种,酸性条件下不利于·OH的生成,而中性、碱性条件更利于·OH的生成[21,22],因此,中性和碱性条件能够促进γ⁃HCH的光转化作用.

Fig.3 Light conversion rate of γ⁃HCH at different pH values in icecγ⁃HCH=60 μg/L,cHA=10 mg/L.(A)cPBS=0.005 mol/L;(B)cPBS=0.05 mol/L.
通过对比图3(A)与(B)可以发现,在pH值相同的条件下,γ⁃HCH在0.05 mol/L磷酸盐缓冲体系中的光转化率比其在0.005 mol/L磷酸盐缓冲体系中的大.即随着磷酸盐离子浓度增大,γ⁃HCH光转化率也增大.Grannas等[7]提出了LLL层存在的假定及LLL层占比公式:

由式(3)可知,LLL层的厚度与溶质浓度呈正相关,因此,当冰相中离子浓度增大时,LLL层厚度增加,使更多的γ⁃HCH进入LLL层中,从而加快了γ⁃HCH的光转化过程.
2.1.3 Fe3+的影响 铁是自然界中含量最高、分布最广泛的元素之一.铁及其有机络合物的电子容易转移,且对光有一定的吸收,因此具有显著的光化学作用.分别在添加了0.5,5,50 μmol/L Fe3+的冰相中研究了Fe3+对γ⁃HCH光转化率的影响,结果如图4所示.当加入低浓度Fe3+时,Fe3+对γ⁃HCH光转化起到促进作用.加入5 μmol/L Fe3+时,γ⁃HCH的光转化率增加至26.19%,这是因为HA上存在羧基(—COOH),加入Fe3+后,酚羟基(—OH)或2个相邻—COOH基团会与Fe3+形成Fe3+⁃HA配合物,Fe3+⁃HA配合物在光照条件下发生氧化还原反应,生成Fe2+和弱氧化性自由基;随后Fe2+被HA生成的H2O2氧化,生成·OH,促进了γ⁃HCH的光转化[23,24].反应式如下:

然而,当Fe3+浓度继续增大,γ⁃HCH的光转化率则出现减小的现象,这是因为Fe3+在200~400 nm波长区间有很强的光吸收,所以体系中的Fe3+会对光子产生竞争效应,从而对γ⁃HCH的光转化产生抑制作用[25].

Fig.4 Light conversion rate of γ⁃HCH with different concentrations of Fe3+in icecγ⁃HCH=60 μg/L,cHA=10 mg/L.


2.2 冰相中活性基团在γ⁃HCH光转化中的作用
2.2.11O2的作用 研究发现,冰中1O2的浓度是水溶液中的10000倍[28].叠氮钠(NaN3)是一种普遍使用的水溶性猝灭剂,能够有效地猝灭1O2.为了验证冰相中1O2在γ⁃HCH光转化中的作用,加入NaN3作为1O2的猝灭剂.由图6可知,γ⁃HCH光转化率随着NaN3的加入而降低,当加入0.1 mmol/L NaN3时,光照24 h后γ⁃HCH转化率为未加入NaN3时的67.55%.由实验结果可以得出,1O2参与了γ⁃HCH的光转化过程,并且对γ⁃HCH的光转化有促进作用.
继续增大NaN3浓度至1 mmol/L时,γ⁃HCH转化率则接近未加入NaN3时的转化率,这是由于NaN3不仅有猝灭1O2的作用,同时也作为盐离子促进γ⁃HCH的光转化,二者综合作用使γ⁃HCH的光转化率又增大至原来的数值.

Fig.6 Light conversion rate of γ⁃HCH with different concentrations of NaN3in icecγ⁃HCH=60 μg/L,cHA=10 mg/L.

Fig.7 Light conversion rate of γ⁃HCH with different concentrations of isopropanol in icecγ⁃HCH=60 μg/L,cHA=10 mg/L.
2.2.2 ·OH的作用 HA在光照下不仅会生成1O2,同时也会生成·OH.为了验证·OH在γ⁃HCH光转化中的作用,向反应体系中加入·OH的猝灭剂异丙醇.由图7可知,加入异丙醇后γ⁃HCH转化率减小.对比加入0.01和0.10 mmol/L异丙醇的γ⁃HCH的光转化率可知,0.01 mmol/L异丙醇就能够猝灭10 mg/L HA在光照下产生的·OH.综上所述,·OH参与了γ⁃HCH的光转化过程,并且对γ⁃HCH的光转化有促进作用.同2.2.1节中的结果相比,1O2对γ⁃HCH光转化的促进作用大于·OH的作用.继续增大异丙醇浓度至1.00 mmol/L,γ⁃HCH转化率则增大,并甚至大于未加入异丙醇时的转化率,这是由于异丙醇提供电子的能力比较强,加入后促进了γ⁃HCH的光转化.
2.3 冰相中γ⁃HCH的光转化机理
在冰相中γ⁃HCH的光转化产物中检测出了五氯环己烯(产物Ⅰ)、邻二氯苯(产物Ⅱ)、对二氯苯(产物Ⅲ)及一氯苯(产物Ⅳ),4种产物在总测出物中的比率为17.97%,约等于冰相中γ⁃HCH光照24 h后的光转化率.文献[27,29,30]报道在对γ⁃HCH的直接光转化产物中检测到了苯酚、一氯苯酚、五氯环己烯及四氯环己烯.与之前的实验结果相比较,HA存在下γ⁃HCH的光转化产物中没有检测到这些酚类产物.这是因为HA在光照条件下光敏化生成1O2,虽然1O2不能直接作用于γ⁃HCH光转化反应,但极易氧化酚类物质.酚类产物被1O2迅速氧化消耗,因此没有被检测到.由以上分析可以得出,1O2对γ⁃HCH光转化反应的促进作用可能主要体现在对γ⁃HCH初级或次级光转化产物的降解,通过消耗γ⁃HCH光转化产生的中间产物,使γ⁃HCH的中间产物无法积累,从而间接加速了γ⁃HCH的光转化过程.结合检测到的物质和γ⁃HCH及其产物的分子构型,推测冰相中HA存在下γ⁃HCH的光转化途径如Scheme 1所示.
3 结 论
研究了在HA存在下γ⁃HCH在冰相中的光化学反应.结果表明,HA浓度对γ⁃HCH的光转化率呈现低浓度促进而高浓度抑制的现象;盐离子浓度、及对γ⁃HCH的光转化率均有促进作用;低浓度Fe3+对γ⁃HCH的光转化率有促进作用,当Fe3+的浓度增大到50 μmol/L时,呈现抑制效应;γ⁃HCH在不同pH值条件下光转化速率的大小顺序为碱性>中性>酸性;冰相中HA通过产生单线态氧(1O2)、羟基自由基(·OH)及三重激发态(HA∗)加速了γ⁃HCH的光转化;GC⁃MS对产物的分析结果表明,HA存在下γ⁃HCH的光转化产物主要是五氯环己烯、邻二氯苯和对二氯苯、一氯苯.光转化过程中1O2通过消耗中间产物间接加速了γ⁃HCH的光转化过程.
[1] Kahan T.F.,Kwamena N.O.A.,Donaldson D.J.,Atmos.Chem.Phys.,2010,10(22),10917—10922
[2] Mcneill V.F.,Grannas A.M.,Abbatt J.P.D.,Ammann M.,Ariya P.,Bartels⁃Rausch T.,Domine F.,Donaldson D.J.,Guzman M.I.,Heger D.,Kahan T.F.,Klan P.,Masclin S.,Toubin C.,Voisin D.,Atmos.Chem.Phys.,2012,12(20),9653—9678
[3] Kahan T.F.,Donaldson D.J.,Environ.Sci.Technol.,2010,44(10),3819—3824
[4] Kahan T.F.,Donaldson D.J.,J.Phys.Chem.A,2007,111(7),1277—1285
[5] Kahan T.F.,Zhao R.,Atmos.Chem.Phys.,2010,10(2),843—854
[6] Kahan T.F.,Zhao R.,Jumaa K.B.,Donaldson D.J.,Environ.Sci.Technol.,2010,44(4),1302—1306
[7] Grannas A.M.,Bausch A.R.,Mahanna K.M.,J.Phys.Chem.A,2007,111(43),11043—11049
[8] O’concubhair R.,Sodeau J.R.,Acc.Chem.Res.,2013,46(11),2716—2724
[9] Bartels⁃rsusch T.,Jacobi H.W.,Kahan T.F.,Thomas J.L.,Thomson E.S.,Abbatt J.P.D.,Ammann M.,Blackford J.R.,Bluhm H.,Boxe C.,Domine F.,Frey M.M.,Gladich I.,Guzman M.I.,Heger D.,Huthwelker T.,Klan P.,Kuhs W.F.,Kuo M.H.,Maus S.,Moussa S.G.,McNeill V.F.,Newberg J.T.,Pettersson J.B.C.,Roeselova M.,Sodeau J.R.,Atmos.Chem.Phys.,2014,14(3),1587—1633
[10] Jonathan P.B.,Cort A.,Environmental Science:Processes and Impacts,2014,16(4),748—756
[11] Klan P.,HoloubekI.,Chemosphere,2002,46(8),1201—1210
[12] Bower J.P.,Anastasio C.,J.Phys.Chem.A,2013,117(30),6612—6621
[13] Takenaka N.,Bandow H.,J.Phys.Chem.A,2007,111(36),8780—8786
[14] Domine F.,Bock J.,Voisin D.,Donaldson D.J.,J.Phys.Chem.A,2013,117(23),4733—4749
[15] Ou X.X.,Sun H.J.,Wang C.,Zhang F.J.,Liu N.,J.Henan Agr.Sci.,2012,41(2),18—20(欧晓霞,孙红杰,王崇,张凤杰,刘娜.河南农业科学,2012,41(2),18—20)
[16] Thomsen M.,Lassen P.,Dobel S.,Hansen P.E.,Carisen L.,Moqensen B.B.,Chemosphere,2002,49(10),1327—1337
[17] Zhao N.,Lu Y.Z.,Li G.J.,Chem.Res.Chinese Universities,2013,29(6),1180—1184
[18] Xue H.H.,Tang X.J.,Kang C.L.,Liu J.,Shi L.,Wang H.L.,Yang T.,Water Sci.Technol.,2013,68(11),2479—2484
[19] Cho H.,Shepson P.B.,Barrie L.A.,J.Phys.Chem.B,2002,106(43),11226—11232
[20] Xue H.H.,The Photochemistry of Hexachlorocyclohexane in Water,Snow and Ice,Jilin University,Changchun,2012(薛洪海.六六六在水、冰和雪中的光化学行为,长春:吉林大学,2012)
[21] Yang D.M.,Yuan J.M.,Xia H.,Environ.Prot.Chem.Ind.,2014,34(1),24—27(杨德敏,袁建梅,夏宏.化工环保,2014,34(1),24—27)
[22] Tang X.J.,Wang Y.X.,Kang C.L.,Liu H.F.,Chen B.Y.,Qiu S.L.,Chem.J.Chinese Universities,2015,36(9),1719—1723(唐晓剑,王依雪,康春莉,刘汉飞,陈柏言,裘式纶.高等学校化学学报,2015,36(9),1719—1723)
[23] Zhan M.J.,Yang X.,Xian Q.M.,Kong L.R.,Chemosphere,2006,63(3),378—386
[24] Ou X.X.,Chen S.,Quan X.,Zhao H.M.,Chemosphere,2008,72(6),925—931
[25] Wang F.L.,Chen P.,Su H.Y.,Wang Y.F.,Ma J.S.,Yao K.,Li F.H.,Liu G.G.,Lv W.Y.,J.Environ.Sci.China,2016,36(8),2859—2868(王枫亮,陈平,苏海英,王盈霏,马京帅,姚琨,李富华,刘国光,吕文英.环境科学学报,2016,36(8),2859—2868)
[26] Boxe C.S.,Colussi A.J.,Hoffmann M.R.,Murphy J.G.,Wooldridge P.J.,Bertram T.H.,Cohen R.C.,J.Phys.Chem.A,2005,109(38),8520—8525
[27] He C.,Photochemical Reactions of γ⁃HCH Under Simulated Sunlight in Ice Phase,Jilin University,Changchun,2013(何冲.模拟太阳光作用下冰相中γ⁃HCH的光化学反应,长春:吉林大学,2013)
[28] Bower J.P.,Anastasio C.,Atmos.Environ.,2013,75,188—195
[29] Guo Z.X.,Rose Bengal⁃sensitized Photodegradation of γ⁃Hexachlorocyclohexane in Ice,Jilin University,Changchun,2013(郭志新.玫瑰红作用下γ⁃HCH在冰相中的光敏化降解,长春:吉林大学,2013)
[30] Widchaya R.,Araya T.,Ratchaneekorn W.,Chem.Res.Chinese Universities,2014,30(1),149—156
(Ed.:S,Z,M)
†Supported by the National Natural Science Foundation of China(No.41073063).
Photoconversion of γ⁃Hexachlorocyclohexane in the Presence of Humic Acid in Ice†
BAO Siqi,KANG Chunli,ZHONG Yubo,ZHOU Lin,YAO Zhifu,HUANG Dongmei,WANG Yuhan,TIAN Tao∗
(Key Laboratory of Groundwater Resources and Environment,Ministry of Education,College of Environment and Resources,Jilin University,Changchun 130021,China)
The photoconversion regularity of γ⁃hexachlorocyclohexane(γ⁃HCH)in snow and ice in the presence of humic acid(HA)were studied.The results showed that the photoconversion efficiency of γ⁃HCH was promoted at low initial concentration of HA,but inhibited at high concentration of HA.Salt ion concentra⁃ tion,andall promoted the photoconversion efficiency of γ⁃HCH.The photoconversion efficiency of γ⁃HCH was promoted at low initial concentration of Fe3+,but inhibited when the concentration of Fe3+reached 50 μmol/L.The sequence of photoconversion rate of γ⁃HCH at different pH was alkaline>neutral>acidic.HA accelerated the photoconversion of γ⁃HCH by producing singlet oxygen(1O2),hydroxyl free radical(·OH)and triple excited state(HA∗)in ice.Photoproducts of γ⁃HCH in the presence of HA are mainly pentachloro⁃cyclohexene,p⁃dichlorobenzene and o⁃dichlorobenzene,1⁃chlorobenzene,and1O2indirectly accelerated the photoconversion of γ⁃HCH by consuming the intermediate products.
γ⁃Hexachlorocyclohexane(γ⁃HCH);Humic acid(HA);Photoconversion;Ice
O644
A
10.7503/cjcu20160414
2016⁃06⁃08.网络出版日期:2016⁃11⁃18.
国家自然科学基金(批准号:41073063)资助.
联系人简介:田 涛,男,博士,讲师,主要从事环境化学方面的研究.E⁃mail:tiantao@jlu.edu.cn
