胆甾类分子钳人工受体的研究进展
2016-12-14卢奕江杜育芝段亚欣徐润平姚鑫叶鹏
卢奕江,杜育芝,段亚欣,徐润平,姚鑫,叶鹏
(浙江理工大学化学系,浙江杭州310018)
胆甾类分子钳人工受体的研究进展
卢奕江,杜育芝,段亚欣,徐润平,姚鑫,叶鹏
(浙江理工大学化学系,浙江杭州310018)
人工受体的识别性能研究是生物有机化学和超分子化学富有挑战的前沿课题之一,分子钳作为一类重要的新型人工受体受到了广泛的关注。该文重点综述了胆甾类分子钳对阴离子、阳离子、中性离子和手性分子的识别作用,以及识别性能的检测方法,并对其应用前景进行了展望。
分子钳;甾体;分子识别;人工受体;手性分子
分子识别(molecular recognition)是客体分子与受体之间的选择性结合,其在生命活动中起着十分重要的作用。一些早期的人工受体,如冠醚、环糊精和环蕃等大环化合物,它们的活性官能团有限,即使对其进行化学修饰,也难以满足对更多类型底物进行识别的要求[1]。分子钳(molecular tweezer)又称分子裂缝,是一种新型的人工受体,其结构上有着相当于天然受体的空腔,可以根据实际需要,设计相应形状、大小以及官能团,并通过对其分子钳手臂的进一步化学修饰,提供一个与客体分子恰好互补的微环境[2]。识别的推动力主要包括氢键、静电引力、范德华力、疏水作用和π-π堆积作用等非共价键作用力。
分子钳的种类根据分子骨架的不同大致可分为胍盐类分子钳[3-7]、芳杂环类分子钳[8-12]、杯芳烃类分子钳[13-17]以及胆甾类分子钳等。文章对胆甾类分子钳人工受体的手性识别性能研究作了着重阐述。
1 胆甾类分子钳
胆甾因其刚性的甾体骨架具有不对称性,是构建新型分子钳的理想结构单元。胆甾骨架中指向凹面中心的羟基以及侧链的羧基可以通过不同的化学修饰构建多种类型的分子钳人工受体。胆甾的结构通式可表示为图1。
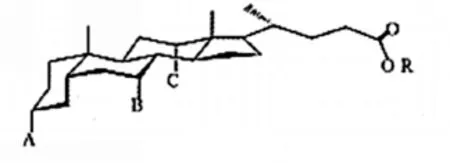
图1 胆甾的结构通式
1.1对阴离子的识别
阴离子在生命活动中起着重要的作用,如携带基因信息和参与酶促反应[18-19]。工业生产中产生的废液也常常含有大量阴离子,会对环境造成污染。设计合成人工受体用于阴离子结合、传感、运输和提取是超分子化学领域备受关注的研究热点[20-23]。
赵志刚等构建了一类手性不对称脲石胆酸分子钳(如图2),通过紫外滴定实验发现,随着卤素阴离子的不断加入,主体溶液的吸光度呈现规律性的下降(或上升),表明分子钳对卤素阴离子产生了识别配合作用;并且分子钳与所有卤素阴离子均能形成1∶1型超分子化合物,识别选择性为I->Cl->Br-,结合常数Ka为102~103 L/mol[24]。该识别作用的主要推动力是不对称脲上的酰胺氮氢质子与卤素阴离子之间形成的氢键作用。相比于I-,Cl-和Br-的离子半径较小,而分子裂穴较大,导致主客体分子之间的形状匹配较差,所形成氢键的距离较远,作用力较弱,因此I-的结合常数最大;并且在电荷密度上Cl-大于Br-,故Cl-形成氢键的能力较大,其结合常数大于Br-。
Mamra Chahar等将胆甾双咪唑衍生物进行了闭环修饰,合成了a、b、c和d 4种受体(如图3),并使用核磁滴定实验考察了其对卤素阴离子的识别能力[25]。研究发现所有受体与卤素阴离子均能形成1∶1型超分子化合物。其中受体a和c对Cl-具有选择性,受体b和d对F-具有良好的选择识别性能,并且受体d与F-的亲和力是受体b的2倍。

图2 手性不对称脲石胆酸分子钳

图3 胆甾双咪唑受体
1.2对阳离子的识别
金属阳离子广泛存在于生命体活动中,如它们参与酶及DNA的代谢过程并且维持着生物体内的水和电解质平衡,是人体细胞不可缺少的[26]。在工业生产中使用的铅、汞及镉等剧毒重金属,如果被过度排放到自然界,会对人和环境造成巨大的危害[27-28]。因此,设计能高效识别有毒重金属离子的新型人工受体是十分有意义的。
赵志刚等通过点击化学方法合成了一系列鹅去氧胆酸类分子钳(如图4),紫外滴定实验表明:随着金属阳离子不断加入,主体的吸光度呈规律性的下降,故主客体之间产生了识别配合作用[29]。此外,主体与客体之间形成了1∶1型超分子化合物,其对Hg2+的识别能力明显高于Cu2+、Mg2+和Pb2+。对汞离子的识别作用较好可能是由于汞离子在形状大小上与分子裂穴更为匹配。
1.3对中性离子的识别
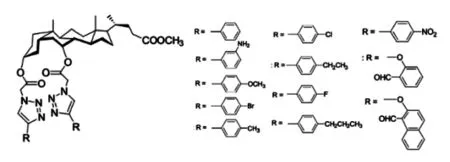
图4 鹅去氧胆酸类分子钳
胆甾在结构上具有以下特点:(1)刚性的凹面结构;(2)具有多个手性中心;(3)α面亲水,β面疏水;(4)胆甾骨架中多个指向凹面中心的羟基和侧链羟基可以进行不同的化学修饰。
杨学军等采用微波技术设计合成了一系列脱氧胆酸分子钳(如图5)[30]。各分子钳对客体苯胺、邻甲氧基苯胺、间甲氧基苯胺和对甲氧基苯胺分别进行了识别。经紫外滴定实验发现:往主体溶液中不断加入客体溶液,主体的吸光度会呈规律性下降,表明主客体分子之间产生了识别配合作用;且在同一溶剂(CHCl3)中,对不同客体溶液的识别性能存在差异,表现为苯胺>对甲氧基苯胺>间甲氧基苯胺>邻甲氧基苯胺。
分子钳的手性识别推动力主要来自于主客体之间的氢键、π-π堆积和范德华力等非共价键作用力的共同作用。同时主客体在形状大小以及空间几何上的匹配度,分子钳的刚柔性,手臂结构不同所造成的微环境效应等,在手性识别过程中也起着十分重要的作用。
Davis等合成了亲脂性胆甾胍盐受体1、2 (如图6),并研究了这些受体对N-乙酰基α-氨基羧酸的手性识别能力,其中受体2对N-乙酰基α-氨基羧酸的手性拆分能力较好,其对映选择性结合常数KL/KD高达10[33-35]。
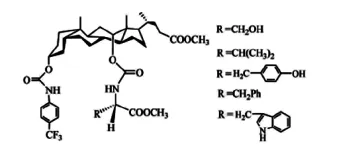
图5 脱氧胆酸分子钳
1.4手性识别
手性分子在生物系统中起着重要的作用,如蛋白质、激素、酶和DNA等都是天然的手性分子。人工受体对手性分子的识别可以提供关于生物现象中主客体相互作用的有用信息[31]。氨基酸作为肽、蛋白质和DNA的重要组成成分,是生物系统中非常重要的分子,其在结构上是彼此相似的,但有着不同的侧链,对氨基酸手性识别的研究是十分有意义的课题[32]。
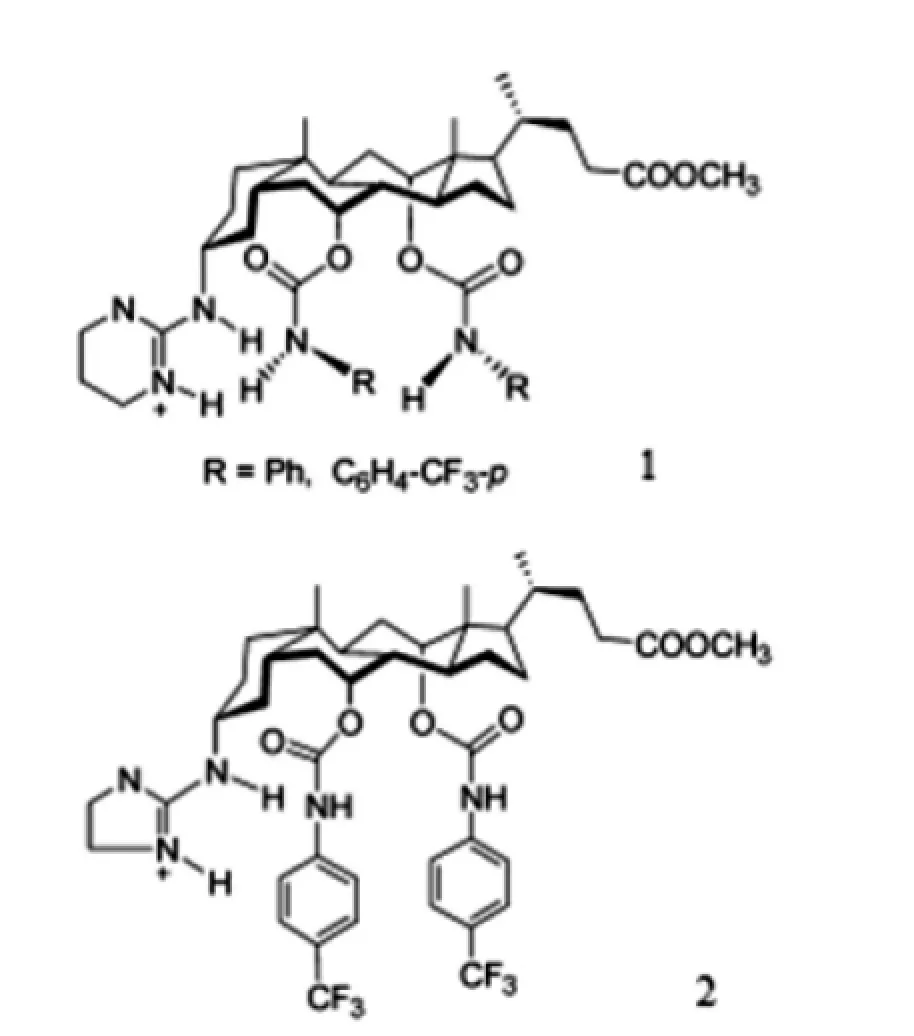
图6 胆甾胍盐受体1,2
Liu等合成了一系列水溶性人工受体(如图7)[36]。其中受体3具有三中心多重氢键,可提供更多的氢键识别位点,其在甲醇/水(1∶1)的溶液中对L-谷氨酸有十分优异的手性识别能力,其结合常数Ka高达5.61×105L/mol。而受体4和5对L-谷氨酸没有手性拆分能力,可能是因为受体4和5的氢键识别位点较少,且分子裂穴较大,无法对L-谷氨酸进行较好的识别匹配。
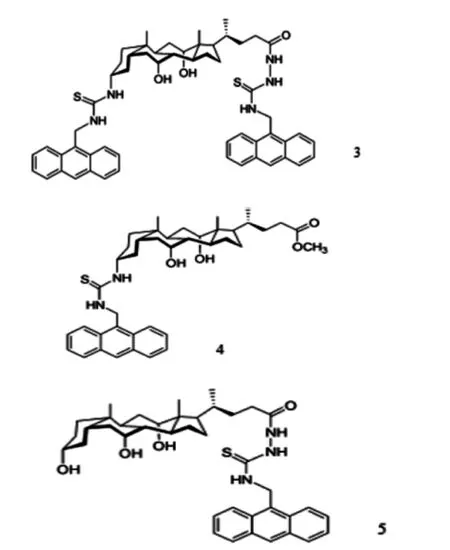
图7 水溶性人工受体3~5
薛翠花等以脱氧胆酸为骨架,在三光气作用下将苯胺及其衍生物与胆甾桥连,合成了新型的脱氧胆酸分子钳6~9(如图8),并研究了分子钳手臂上不同基团所形成的微环境效应对识别性能的影响[37]。这类受体对亮氨酸和苯丙氨酸均显示出识别能力,且D-氨基酸甲酯>L-氨基酸甲酯,亮氨酸甲酯>苯丙氨酸甲酯。受体8相对7在手臂上引入了硝基,意在增加识别位点,增强其对氨基酸的识别配合作用,但实验结果表明受体8对苯丙氨酸甲酯的识别性能不如6和7。原因可能是引入的硝基体积较大,在一定程度上阻碍了苯丙氨酸甲酯进入分子钳的裂穴。
Hao Wang等对胆甾进行修饰合成了受体10和11(如图9),利用核磁滴定法考察了其对D/L-氨基酸的手性拆分能力[38]。实验结果表明,受体10和11对所考察客体中的D-氨基酸均显示出了优良的识别能力,主客体间形成1∶1型超分子配合物,且受体10对氨基酸的KD/KL均大于受体11,其中受体10对D/L-苏氨酸的手性识别性能最佳。

图8 新型脱氧胆酸分子钳6~9

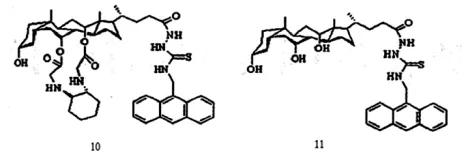
图9 胆甾受体10,11
2 识别性能的检测方法
分子钳主体对客体分子识别性能的测试,目前主要有以下3种方法:(1)紫外分光光度滴定法;(2)核磁共振法;(3)分子模拟。
2.1紫外分光光度滴定法
紫外光谱滴定实验中,以无水氯仿为溶剂,配制一定浓度的主体分子钳溶液和客体分子溶液。主体溶液浓度不变,往其中不断加入浓度不同的客体分子溶液,主体溶液的最大吸光度呈规律性下降或上升,这表明主客体分子之间产生了识别配合作用,紫外滴定曲线如图10。利用主体溶液吸光度的变化,可求得主客体识别配合的结合常数。主客体形成的超分子配合物化学计量比为1∶1,可利用方程1来表达其配合作用;当客体浓度远远大于主体浓度时,根据修饰的Hildebrand-Benesi[39]方程2,以1/ΔA对1/[G]0作图,可得到线性关系图,如图11所示。由直线的截距和斜率计算出配合物的稳定常数Ka和自由能变化(-ΔG0),由此可对识别性能进行比较。

式中:[H]0为主体溶液初始浓度;[G]0为客体溶液总浓度;ΔA为加入客体前后主体溶液的吸光度差;Δε为主客体配合前后的摩尔消光系数差。
2.2核磁共振法
核磁共振法是研究主客体间非共价键作用力的重要手段之一,利用核磁共振法可检测主客体在形成超分子配合物前后的化学位移。一般情况下,当主客体形成超分子配合物后,其中参与氢键作用的相关质子的化学位移会向低场移动,若质子的化学位移向高场移动则其参与π-π堆积作用,故利用1H NMR谱可以初步了解主体分子钳对客体分子识别作用的推动力以及识别模式[40]。

图10 紫外滴定曲线
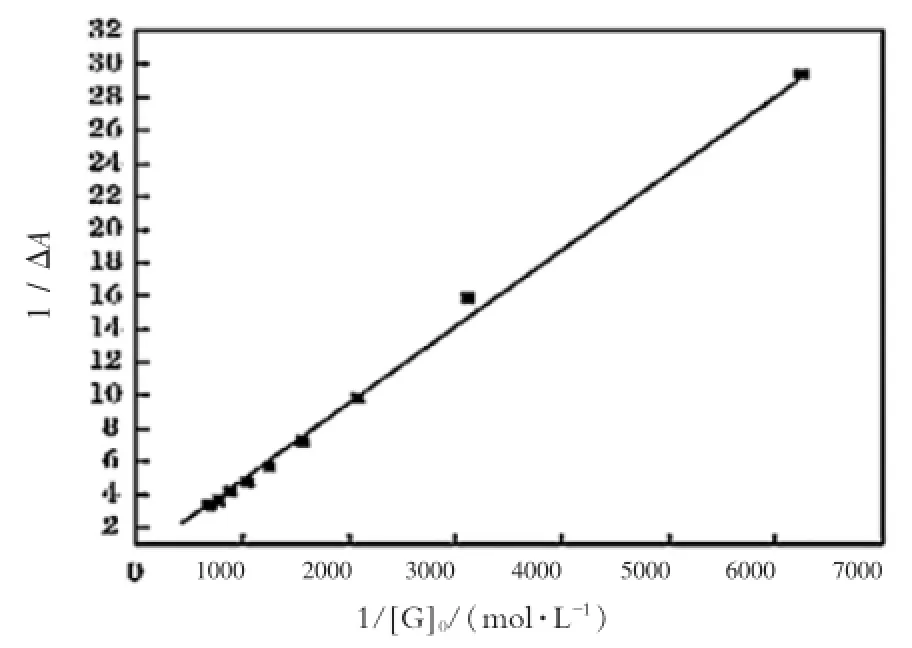
图11 1/ΔA与1/[G]0的线性关系图
2.3分子模拟分析
分子模拟又称“计算机模拟”,是一种在计算机上进行模拟分析的实验。许多通过实验方式较难得到或无法得到的数据,利用分子模拟却可以轻松地获取,这是由于通过计算机可以清晰地观察到分子的微观结构和计算材料的力学性能等[41]。因此分子模拟技术可用来优化以往的结构分析、化学合成和物性检测等实验,从而为新型材料与分子的设计提供理论基础[42]。
通过Chem 3D程序(MM2)可分别对主客体间所形成的各种配合物进行系统的构象搜寻和结构最优化。应用Chem 3D程序(MM2)进行分子构象模拟,可得到受体的多种构象异构体,从中找出最低能量构象图。通过比较可看出客体的大小和形状是否适合进入主体裂穴,诱导其产生配合作用。
3 结语
分子钳作为一类新型人工受体,其优点在于可以根据不同种类客体分子设计具有相应识别结构的受体。通过多种隔离基的选择,使其能与客体分子进行良好的识别作用。分子钳可与客体分子形成1∶1型超分子化合物,对阴离子、阳离子和生物分子等具有良好的识别配合性能。这些识别性能上的差异,与主客体分子形状的匹配程度及其功能基团的相互作用等结构因素相关。
近年来,分子钳的发展十分迅速,在新药设计、不对称催化、拆分手性化合物、生物传感器以及分子器件等领域展示出了它独特的光彩,引起了越来越多人的重视。但目前分子钳的合成还较为困难,分子识别效果也需要进一步提高。此外,分子钳结构对其识别性能的影响尚缺乏系统的理论支撑,难以准确预测所合成分子钳对客体分子的识别性能,从而极大地限制了分子钳的发展。因此,分子钳的合成优化及识别机理的深入研究将是这一领域的重点研究方向。
[1]J Rebek,B Askew,M Killoran,et al.Convergent functional groups.3.a molecular cleft recognizes substrates of complementary size,shape,and functionality [J].J Am Chem Soc,1987,109(8):2426-2431.
[2]J M Lehn.Perspectives in supramolecular chemistry—from molecular recognition towards molecular information processing and self-organization[J].Angew.Chem. Int.Ed.Engl.,1990(29):1304-1319.
[3]陆国元,胡宏纹.手性双环胍剪刀分子对有机阴离子的络合效应[J].中国科学(B辑化学),1996,26(4): 289-294.
[4]Antonio Echavarren,Amalia Galan,Jean Marie Lehn,et al.Chiral recognition of aromatic carboxylate anions by an optically active abiotic receptor containing a rigid guanidinium binding subunit[J].J.Am.Chem.Soc., 1989,111(13):4994-4995.
[5]Carsten Schmuck.Side chain selective binding of N-acetyl-α-amino acid carboxylates by a 2-(guanidiniocarbonyl)pyrrolereceptorinaqueoussolvents[J]. Chem.Commun.,1999,9(9):843-844.
[6]Carsten Schmuck.Carboxylate binding by 2-(guanidiniocarbonyl)pyrrole receptors in aqueous solvents:improving the binding properties of guanidinium cations through additional hydrogen bonds[J].Chem.Eur.J., 2000(6):709-718.
[7]Amalia Galan,David Andreu,Antonio M Echavarren,et al.A receptor for the enantioselective recognition of phenylalanine and tryptophan under neutral conditions [J].J.Am.Chem.Soc.,1992,114(4):1511-1512.
[8]Shigeo Kohmoto,Katsuya Sakayori,Keiki Kishikawa,et al. Molecular cleft possessing a cholic acid moiety as a podant and its conformation[J].J.Chem.Soc.,Perkin Trans.,1999(2):833-836.
[9]T Ross Kelly,Martin P Maguire.A receptor for the oriented binding of uric acid type molecules[J].J.Am. Chem.Soc.,1987,109(21):6549-6551.
[10]Suk Kyu Chang,Andrew D Hamilton.Molecular recognition of biologically interesting substrates:synthesis of an artificial receptor for barbiturates employing six hydrogen bonds[J].J.Am.Chem.Soc.,1988,110(4): 1318-1319.
[11]Shyamaprosad Goswami,Rakhi Mukherjee.Molecular recognition:asimpledinaphthyridinereceptorfor urea[J].Tetrahedron Lett.,1997(38):1619-1622.
[12]Goodman M S,Rose S D.Photosensitized pyrimidine dimersplittingbyamethoxyindoleboundtoa dimer-recognizing macrocycle[J].J.Org.Chem.,1992(57):3268-3270.
[13]黄志镗,杨联明.杯芳烃研究进展[J].化学进展, 1994,6(3):173-177.
[14]Volker Bohmer Calixarenes.Macrocycles with(Almost) unlimited possibilities[J].Angew.Chem.Int.Ed. Engl.,1995(34):713-745.
[15]TimmermanP,VerboomW,ReinhoudtDN.Resorcinarenes[J].Tetrahedron,1996,52(8):2663-2704.
[16]戈云,刘莉,王云艳,等.新型间苯二酚杯芳烃硫脲衍生物对阴离子的识别[J].化学学报,2005,63(6):533-537.
[17]Miroslav Dudic,Pavel Lhotak,Ivan Stibor,et al.Calix[4] arene-porphyrin conjugates as versatile molecular receptors for anions[J].Org.Lett.,2003,5(2):149-152.
[18]He JJ,Quiocho F.A nonconservative serine to cysteine mutation in the sulfate-binding protein,a transport receptor[J].Science,1991(251):1479-1481.
[19]Beer PD,Gale PA.Anion recognition and sensing:the state of the art and future perspectives[J].Angew. Chem.Int.Ed.,2001(40):486-516.
[20]Gale PA,Perez-Tomas R,Quesada R.Towards predictable transmembrane transport:QSAR analysis of the anion binding and anion transport properties ofthioureas[J].Acc.Chem.Res.,2013(46):2801-2813.
[21]Duke RM,Veale EB,Pfeffer FM,et al.Colorimetric and fluorescent anion sensors:an overview of recent developments in the use of 1,8-naphthalimide-based chemosensors[J].Chem.Soc.Rev.,2010(39):3936-3953.
[22]Fowler C J,Haverlock T J,Moyer B A,et al.Enhanced anion exchange for selective sulfate extraction overcoming the hofmeister bias[J].J.Am.Chem.Soc., 2008,130(44):14386-14387.
[23]Caballero A,Zapata F,Beer P D.Interlock host molecules for anion recognition and sensing[J].Coord.Chem.Rev.,2013(257):2434-2455.
[24]刘兴利,赵志刚,周彩娥.手性不对称脲石胆酸分子裂缝对阴离子的识别研究[J].化学研究与应用,2007,19(4):396-400.
[25]Mamta Chahar,Pramod S Pandey.Design of steroidbased imidazolium receptors for fluoride ion recognition[J].Tetrahedron,2008,64(27):6488-6493.
[26]T W Clarkson.Environmental contaminants in the food chain[J].Am.J.Clin.Nutr.,1995(61):682S-686S.
[27]Paul B Tchounwou,Wellington K Ayensu,Nanuli Ninashvili,et al.Review:environmental exposure to mercury and its toxicopathologic implications for public health[J].Environ.Toxicol.,2003(18):149-175.
[28]安琳,蔡亚华,颜朝国.对叔丁基杯[n]芳烃酰胺衍生物的合成及其对某些金属离子的萃取性能[J].应用化学,2005,22(9):980-983.
[29]赵志刚,王晓红,石治川,等.通过点击化学方法合成鹅去氧胆酸分子钳及其识别性能研究[J].有机化学,2014(34):1110-1117.
[30]杨学军,赵志刚,李晖,等.脱氧胆酸手性分子钳的微波合成及其对中性分子的识别性能研究[J].化学研究与应用,2008,20(11):1447-1452.
[31]Donald J Cram.The design of molecular hosts,guests, and their complexes[J].Angew.Chem.Int.Ed.Engl.,1988(27):89-112.
[32]Axel Metzger,Karsten Gloe,Holger Stephan,et al.Molecular recognition and phase transfer of underivatized amino acids by a foldable artificial host[J].J.Org. Chem.,1996,61(6):2051-2055.
[33]Anthony P Davis,Laurence J Lawless.Steroidal guanidinium receptors for the enantioselective recognition of N-acyl α-amino acids[J].Chemical Communications,1999(1):9-10.
[34]Laurence J Lawless,Adrian G Blackburn,Alan J Ayling, et al.Steroidal guanidines as enantioselective receptors for N-acyl α-amino acids.Part 1.3α-Guanylated carbamates derived from cholic acid[J].J.Chem. Soc.,Perkin Trans.,2001(1):1329-1341.
[35]Beatriz Baragana,Adrian G Blackburn,Perla Breccia,et al.Enantioselective transport by a steroidal guanidinium receptor[J].Chem.Eur.J.,2002(8):2931-2936.
[36]Shun-Ying Liu,Lei Fang,Yong-Bing He,et al.Cholicacid-based fluorescent sensor for dicarboxylates and acidic amino acids in aqueous solutions[J].Org. Lett.,2005,7(26):5825-5828.
[37]薛翠花,牟其明,陈淑华.氨基甲酸酯型脱氧胆酸分子钳对氨基酸甲酯的手性识别研究[J].化学学报, 2002,60(2):355-359.
[38]HaoWang,Wing-HongChan,AlbertWMLee.Cholicacidbased fluorescent probes for enantioselective recognition of trifunctional amino acids[J].Org.Biomol.Chem.,2008,6: 929-934.
[39]薛翠花,胡蓉,牟其明,等.胆甾类分子钳对氨基酸衍生物的对映选择性识别[J].化学学报,2000,58(6):717-721.
[40]Klarner FG,Kahlert B.Molecular tweezers and clips as synthetic receptors.molecular recognition and dynamics in receptor-substrate complexes[J].Acc.Chem. Res.,2003(36):919-932.
[41]杨小震.计算机与应用化学[M].北京:化学工业出版社,1999.
[42]朱伟平.分子模拟技术在高分子领域的应用[J].塑料科技,2002(5):23-25.
10.13752/j.issn.1007-2217.2016.03.002
2016-04-08
