β-环糊精增敏催化动力学光度法测定亚硝酸根
2016-12-12赵桦萍
赵桦萍
(齐齐哈尔大学 化学与化学工程学院,黑龙江 齐齐哈尔 161006)
分析监测
β-环糊精增敏催化动力学光度法测定亚硝酸根
赵桦萍
(齐齐哈尔大学 化学与化学工程学院,黑龙江 齐齐哈尔 161006)
在磷酸介质中利用亚硝酸根催化条件下溴酸钾氧化甲基红的褪色反应,建立了β-环糊精(β-CD)增敏催化动力学光度法,对亚硝酸根进行测定。该方法最佳反应条件为:0.05 mol/L甲基红溶液加入量8.0%(φ,下同),0.1 mol/L溴酸钾溶液加入量12.0%,1.0 mol/L稀磷酸加入量12.0%,0.15 mol/L β-CD溶液加入量16.0%,反应温度40 ℃,反应时间15 min。亚硝酸根测定的线性范围为8.0×10-6~6.0×10-4g/L,线性回归方程的相关系数为0.996 6,检出限为4.0×10-7g/L。亚硝酸根的加标回收率为99.0%~102.0%,水样测定结果的相对标准偏差为2.4%~3.2%。加入β-CD后测定亚硝酸根的灵敏度增加了2.5倍。
甲基红;溴酸钾;催化动力学光度法;亚硝酸根;β-环糊精;增敏作用
亚硝酸盐广泛存在于水、土壤以及粮食、蔬菜中。水中的亚硝酸盐主要来源于工业废水以及生活污水中含氮有机物的分解。亚硝酸盐是一种具有化学活性的有害物质,它不仅会导致体内血红素的交换能力下降,还会转化为一氧化氮,与二级胺和三级胺反应后形成致癌的亚硝胺。人体如果过量摄入亚硝酸盐就会中毒甚至死亡[1]。因此,亚硝酸盐是水质以及食品检测的重要项目。国家标准中采用Griess法测定亚硝酸根,该方法所用的偶联试剂盐酸萘乙二胺的性质不稳定,测定条件不易控制,且价格昂贵,气味难闻,还可致癌。因此,寻找新的亚硝酸盐测定方法成为人们研究的热点[2-6]。
β-环糊精(β-CD)可对某些显色反应起到增敏作用[7-10]。本工作以β-CD为增敏剂,建立了催化动力学光度法测定亚硝酸根的新方法。该法灵敏度高,
操作简单,避免使用有害试剂,用于水中亚硝酸根的测定,结果令人满意。
1 实验部分
1.1 试剂、材料和仪器
甲基红、溴酸钾、磷酸、亚硝酸钠、β-CD:分析纯;蒸馏水。
自制水样:亚硝酸钠与蒸馏水配制。
实际水样:某化肥厂处理后的废水。
721型可见分光光度计:北京普析通用仪器有限公司。
1.2 实验方法
我患了乳腺癌。目前病情已得到控制,但癌细胞随时都有转移的可能,我不知道还能活到什么时候。我是家里的独生女,父母快四十了才有了我。我还没有成家,刚买了一套两居室,把父母从农村老家接来不过才三个月而已。
取两支25 mL比色管,分别依次加入0.05 mol/L甲基红溶液2.0 mL,0.1 mol/L溴酸钾溶液3.0 mL,1.0 mol/L磷酸溶液3.0 mL,一支加入1.0×10-6g/L亚硝酸钠溶液4.0 mL,一支不加,用蒸馏水稀释至刻线,摇匀。将两支比色管同时放入40 ℃的恒温水浴锅中加热15 min,迅速取出,用流水冷却2 min,用1 cm比色皿载样,以蒸馏水为参比,采用可见分光光度计测定反应体系于不同波长下的吸光度。按照上述方法配制不加亚硝酸钠的空白溶液和加入亚硝酸钠的试液各一份,在每份溶液中各加入0.15 mol/L β-CD溶液4.0 mL,用蒸馏水稀释至刻线,摇匀,分别测定每一种溶液的吸光度。
改变各溶液的加入量、反应温度、反应时间,重复上述实验,测定反应体系于波长520 nm处的吸光度,以确定最佳反应条件。
2 结果与讨论
2.1 不同反应体系的可见吸收光谱
不同反应体系的可见吸收光谱见图1。
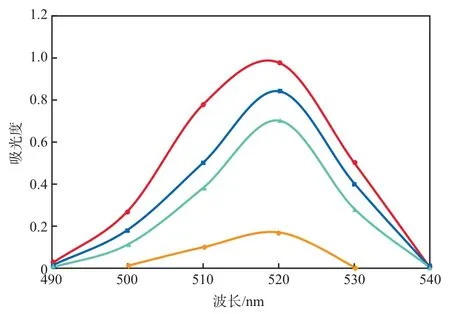
图1 不同反应体系的可见吸收光谱
由图1可见:各反应体系的吸收曲线形状类似,最大吸收波长均为520 nm;由吸收曲线位置的高低可以看出亚硝酸根对溴酸钾氧化甲基红的褪色反应具有催化作用,且β-CD可增敏该催化氧化反应。因此,本实验在磷酸介质中利用亚硝酸根催化条件下溴酸钾氧化甲基红的褪色反应,建立β-CD增敏催化动力学光度法,对亚硝酸根进行测定,测定波长为520 nm。
2.2 反应条件的优化
以反应前后反应体系吸光度的差值∆A来评价褪色效果。
2.2.1 甲基红溶液加入量
在溴酸钾溶液加入量3.0 mL、稀磷酸加入量3.0 mL、β-CD溶液加入量4.0 mL、反应温度40℃、反应时间15 min的条件下,甲基红溶液加入量对∆A的影响见图2。由图2可见,甲基红加入量为2.0 mL时褪色效果最好。因此,选择甲基红溶液加入量为2.0 mL。
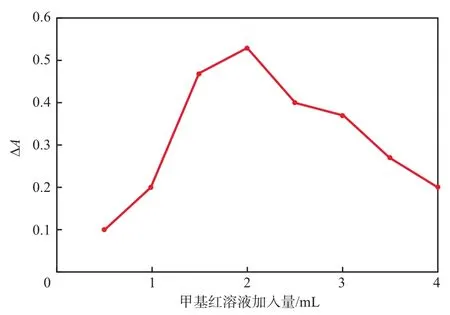
图2 甲基红溶液加入量对∆A的影响
2.2.2 溴酸钾溶液加入量
在甲基红溶液加入量2.0 mL、稀磷酸加入量3.0 mL、β-CD溶液加入量4.0 mL、反应温度40℃、反应时间15 min的条件下,溴酸钾溶液加入量对∆A的影响见图3。由图3可见,溴酸钾加入量为3.0 mL时褪色效果最好。因此,选择溴酸钾溶液加入量3.0 mL。
2.2.3 稀磷酸加入量
在甲基红溶液加入量2.0 mL、溴酸钾溶液加入量3.0 mL、β-CD溶液加入量4.0 mL、反应温度40 ℃、反应时间15 min的条件下,稀磷酸加入量对∆A的影响见图4。由图4可见,稀磷酸加入量为3.0 mL时褪色效果最好。因此,选择稀磷酸加入量为3.0 mL。
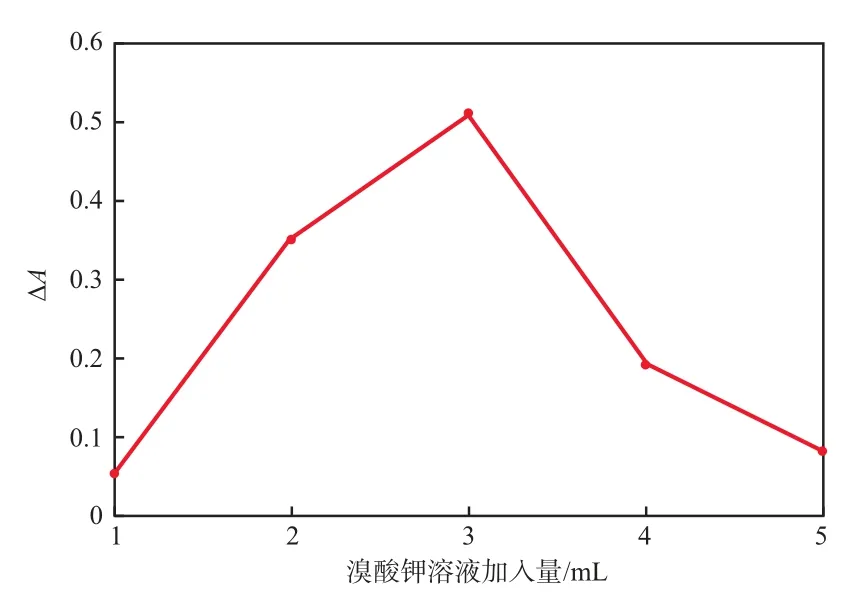
图3 溴酸钾溶液加入量对∆A的影响
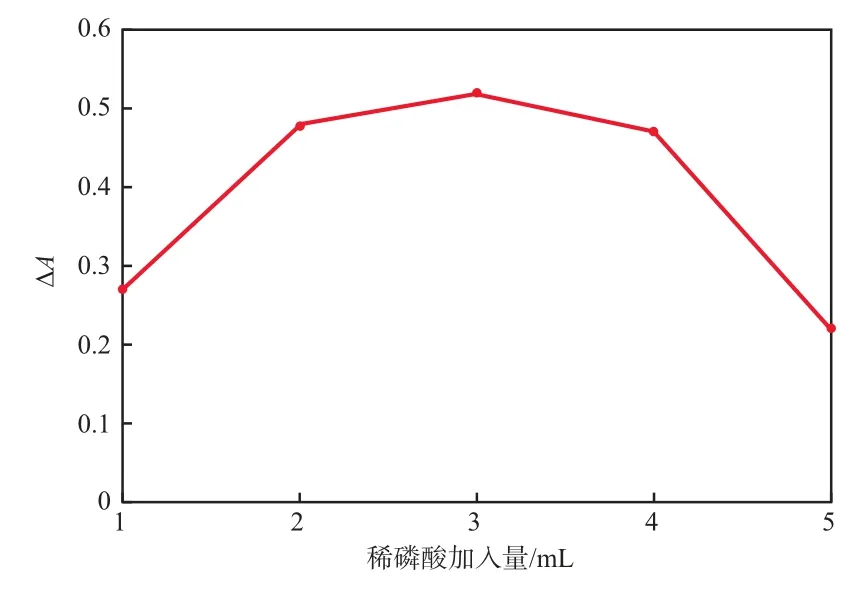
图4 稀磷酸加入量对∆A的影响
2.2.4 β-CD溶液加入量
在甲基红溶液加入量2.0 mL、溴酸钾溶液加入量3.0 mL、稀磷酸加入量3.0 mL、反应温度40 ℃、反应时间15 min的条件下,β-CD溶液加入量对∆A的影响见图5。由图5可见,β-CD溶液加入量为4.0 mL时褪色效果最好。因此,选择β-CD溶液加入量为4.0 mL。
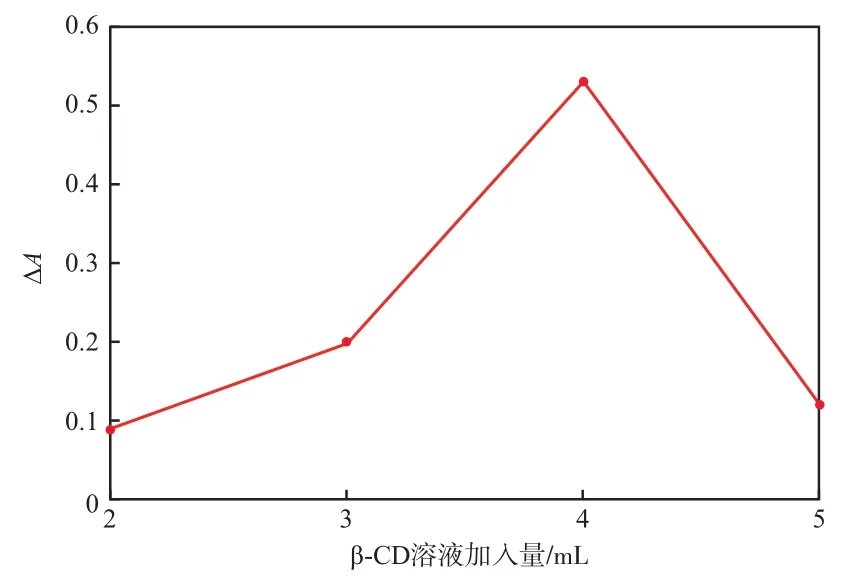
图5 β-CD溶液加入量对∆A的影响
2.2.5 反应温度
在甲基红溶液加入量2.0 mL、溴酸钾溶液加入量3.0 mL、稀磷酸加入量3.0 mL、β-CD溶液加入量4.0 mL、反应时间15 min的条件下,反应温度对∆A的影响见图6。由图6可见,反应温度为40 ℃时褪色效果最好。因此,选择反应温度为40 ℃。
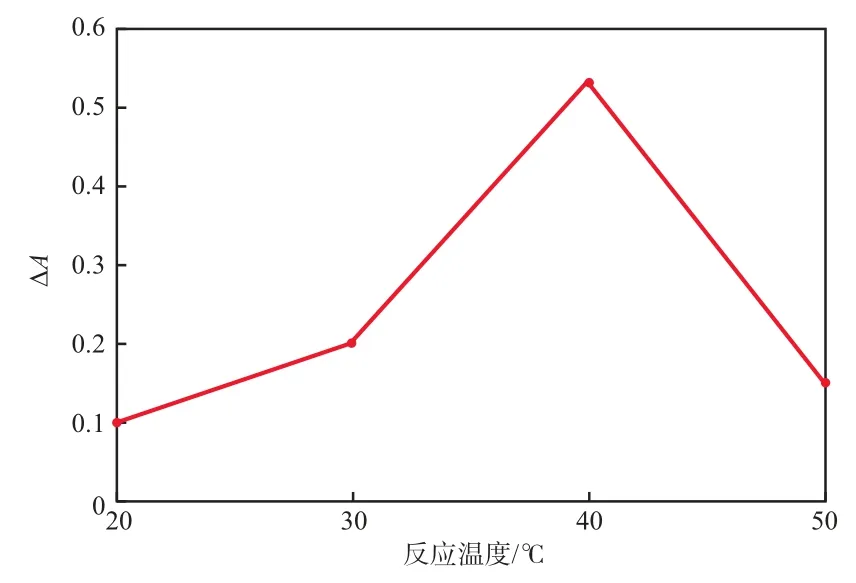
图6 反应温度对∆A的影响
2.2.6 反应时间
在甲基红溶液加入量2.0 mL、溴酸钾溶液加入量3.0 mL、稀磷酸加入量3.0 mL、β-CD溶液加入量4.0 mL、反应温度40 ℃的条件下,反应时间对∆A的影响见图7。由图7可见,反应时间为15 min时褪色效果最好。因此,选择反应时间为15 min。
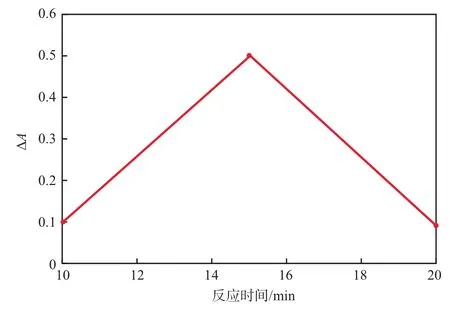
图7 反应时间对∆A的影响
2.3 线性回归方程的建立
在上述最佳反应条件下,移取不同量的亚硝酸钠溶液进行反应。以亚硝酸根质量浓度(ρ,g/L)为横坐标,∆A为纵坐标,绘制工作曲线,求得线性回归方程,并按3倍信噪比确定检出限。结果表明:亚硝酸根质量浓度在8.0×10-6~6.0×10-4g/L范围内符合比尔定律;线性回归方程为∆A=1 550ρ + 0.021,相关系数为0.996 6;亚硝酸根的检出限为4.0×10-7g/L。
未加β-CD体系的线性回归方程为∆A=440ρ+ 0.011。由两方程对应的工作曲线斜率可以看出,加入β-CD后,测定亚硝酸根的灵敏度增加了2.5倍。
2.4 共存离子的影响
当亚硝酸根质量浓度为1.0×10-4g/L时,分别
加入不同量的干扰离子进行干扰实验。将测定结果的相对误差限定在±5%以内。实验结果表明:共存离子对亚硝酸根测定结果无干扰的含量上限为:1 000倍的NH4+,Ca2+,K+,Na+,Bi3+,Mg2+;500倍的Pb2+,Sn2+,Zn2+,Cl-;100倍的Cu2+,Fe2+; 50倍的Br-,I-。
2.5 水样的测定与加标回收
按照上述实验方法测定水样中的亚硝酸根,同时进行加标回收实验,并与Griess法进行比较,结果见表1。

表1 水样的测定与加标回收实验结果(n=6)
由表1可见,亚硝酸根的加标回收率为99.0%~102.0%,水样测定结果的相对标准偏差为2.4%~3.2%。对本实验和Griess法的测定结果进行F检验和t检验,两者无显著性差异。
3 结论
a)在磷酸介质中利用亚硝酸根催化条件下溴酸钾氧化甲基红的褪色反应,建立了β-CD增敏催化动力学光度法,对亚硝酸根进行测定。
b)该方法最佳反应条件为(反应体系总体积25 mL):0.05 mol/L甲基红溶液加入量2.0 mL(8.0%(φ,下同)),0.1 mol/L溴酸钾溶液加入量3.0 mL(12.0%),1.0 mol/L稀磷酸加入量3.0 mL,0.15 mol/L β-CD溶液加入量4.0 mL(16.0%),反应温度40 ℃,反应时间15 min。
c)亚硝酸根测定的线性范围为8.0×10-6~6.0×10-4g/L,线性回归方程为∆A=1 550ρ+0.021,相关系数为0.996 6,检出限为4.0×10-7g/L。亚硝酸根的加标回收率为99.0%~102.0%,水样测定结果的相对标准偏差为2.4%~3.2%。加入β-CD后测定亚硝酸根的灵敏度增加了2.5倍。
[1]赵桦萍.肉制品中亚硝酸盐的测定[J].食品研究与开发,2014,35(1):80-82.
[2]王亚珍,何如意.表面活性剂增敏苏丹红D褪色反应光度法测定亚硝酸根[J].华中师范大学学报:自然科学版,2013,47(5):666-670.
[3]崔英,谢国红.催化动力学光度法测定水中痕量亚硝酸根[J].化工环保,2010,30(3):270-273.
[4]张莹琪,郭秤德,田丹丹,等.微乳液增敏罗丹明B氧化褪色光度法测定微量亚硝酸根[J].化工环保,2014,34(6):595-598.
[5]熊善波,阳庆华,丁捷,等.基于分光光度法检测酱腌菜中亚硝酸盐的条件优化[J].中国调味品,2014,39(9):123-127.
[6]柴红梅,白亮,王雷,等.溴酸钾氧化孔雀石绿和甲基红的褪色光度法测定NO2-的研究[J].安徽农业科学,2013,41(28):11264-11265.
[7]刘奇,魏静娟,王爱军.β-环糊精增敏中性红荧光猝灭法测定痕量亚硝酸根[J].分析试验室,2011,30(7):6-9.
[8]赵永亮,管景帅,温金娥,等.β-环糊精研究进展[J].河南工业大学学报:自然科学版,2014,35(4):97-102.
[9]赵桦萍,靳凤丹,肖忠峰.β-环糊精增敏动力学光度法测定痕量硒[J].食品研究与开发,2013,34(1):94-96.
[10]周群刚,唐建华,谢莲,等.β-环糊精增敏荧光分光光度法检测血浆亚甲蓝[J].临床检验杂志,2011,29(5):344-345.
(编辑 魏京华)
Determination of nitrite by β-cyclodextrin-sensitized catalytic kinetic spectrophotometry
Zhao Huaping
(College of Chemistry and Chemical Engineering,Qiqihar University,Qiqihar Heilongjiang 161006,China)
The β-cyclodextrin-sensitized catalytic kinetic spectrophotometric method for determination of nitrite was developed based on the fading reaction of methyl red oxidized by potassium bromate and catalyzed by nitrite in phosphoric acid.The optimum reaction conditions of the method are as follows:methyl red solution(0.05 mol/L)dosage 8.0%(φ,the same below),potassium bromate solution(0.1 mol/L)dosage 12.0%,phosphoric acid(1.0 mol/L)dosage 12.0%,β-cyclodextrin solution(0.15 mol/L)dosage 16.0%,reaction temperature 40 ℃ and reaction time 15 min.The linear range for determination of nitrite is 8.0×10-6-6.0×10-4g/L,the correlation coefficient of linear regression equation is 0.996 6,and the detection limit is 4.0×10-7g/L.The recovery of standard addition for nitrite is 99.0%-102.0%,and the relative standard deviation of determination results of the water sample is 2.4%-3.2%.The sensitivity of nitrite determination is increased by 2.5 times in the presence of β-cyclodextrin.
methyl red;potassium bromate;catalytic kinetic spectrophotometry;nitrite;β-cyclodextrin;sensitization effect
O657.32
A
1006-1878(2016)02-0226-04
10.3969/j.issn.1006-1878.2016.02.020
2015-10-21;
2016-01-11。
赵桦萍(1966—),女,黑龙江省齐齐哈尔市人,硕士,教授,电话 15084590032,电邮 15084591092@163.com。
