氨基酸及肉碱非衍生化串联质谱法检测系统的性能验证
2016-12-07田明新张道杰崔小昭常海涛孙佳惠计娓娓卢东裕
田明新,张道杰,崔小昭,常海涛,孙佳惠,计娓娓,卢东裕
(北京圣元惠仁医学检验所生化遗传室 101101)
·论 著·
氨基酸及肉碱非衍生化串联质谱法检测系统的性能验证
田明新,张道杰,崔小昭,常海涛,孙佳惠,计娓娓,卢东裕
(北京圣元惠仁医学检验所生化遗传室 101101)
目的 按照ISO15189-2012《医学实验室质量和能力的要求》对Waters公司ACQUITY TQD 串联质谱仪及其配套试剂、PerkinElmer公司NeoBaseTMNon-derivatized MSMS kit在测定氨基酸和肉碱方面进行性能验证。方法 按照美国临床实验室标准化协会指南文件EP15-A2《用户对精密度和准确度性能的核实实验——批准指南》提供的方法,对检测系统进行正确度和精密度验证;按照卫生部行业标准WS/T408-2012《临床化学设备线性评价指南》提供的方法,对其进行线性范围验证。结果 6种氨基酸和7种肉碱的相对偏倚为0.13%~11.34%,均小于1/2允许总误差;批内精密度为0.55%~4.78%,均小于1/4允许总误差;期间精密度除缬氨酸低水平外,为2.52%~7.95%,小于1/3允许总误差;瓜氨酸、苯丙氨酸、游离肉碱在厂家给出的线性范围内呈一阶线性,缬氨酸呈二阶线性,其余呈三阶线性。结论 氨基酸及肉碱非衍生化串联质谱法配套检测系统的性能特征验证通过,可按照常规临床化学检测系统进行管理和要求。
串联质谱仪; 性能验证; 正确度; 精密度; 线性范围
根据国家卫生和计划生育委员会临床检验中心数据,2013年参加其组织的室间质评实验室中采用非衍生串联质谱PerkinElmer NeoBase 试剂盒与衍生非配套试剂盒进行氨基酸和肉碱检测的实验室比例为8∶16,2014年为20∶21,2015年为34∶17。非衍生串联质谱法因其前处理时间短,试剂对环境污染小等优点逐渐取代衍生化方法[1-2],而试剂盒产品因其在研发阶段由厂家负责优化和验证[3],且可溯源至参考物质或参考方法[4],也正逐步取代自配试剂。然而,对于串联质谱仪与其配套试剂所组成的检测系统能否能满足实验室预期用途[5],按照国际标准化组织(ISO)提供的医学实验室专用指南ISO15189-2012《医学实验室质量和能力的要求》,需用户进行独立验证[6]。但实际上,却少有实验室进行验证,个别进行验证的实验室,所采用的方法也过于简单或陈旧,没有依据最新国际相关标准、国家标准及行业标准执行,造成其在串联质谱遗传代谢病筛查、诊断领域存在不少问题。基于以上现状,本实验室特对Waters公司ACQUITY TQD 串联质谱仪及其配套试剂、PerkinElmer公司NeoBaseTMNon-derivatized MSMS kit所组成的氨基酸和肉碱配套检测系统,按照最新标准进行性能验证[7-8]。验证内容包括正确度、精密度和线性范围,验证对象包括瓜氨酸(CIT)、亮氨酸(LEU)、蛋氨酸(MET)、苯丙氨酸(PHE)、酪氨酸(TYR)、缬氨酸(VAL)和游离肉碱(C0)、丙酰肉碱(C3)、异戊酰肉碱(C5)、辛酰肉碱(C8)、十二碳酰肉碱(C12)、十六碳酰肉碱(C16)和十八碳酰肉碱(C18)共13种。
1 资料与方法
1.1 一般资料 样本均为滤纸干血斑标本。正确度验证样本来源于国家卫生和计划生育委员会临床检验中心新生儿遗传代谢病串联质谱筛查的氨基酸和酰基肉碱室间质评样本。精密度验证样本来源于美国疾病预防控制中心室间质评样本。线性范围验证样品来源于本实验室既往检测过的患者标本。
1.2 仪器与试剂
1.2.1 检测系统 仪器为美国Waters公司的串联质谱系统(包括串联质谱仪ACQUITY TQD、高效液相色谱仪1525μ、自动进样器2777C);试剂为美国PerkinElmer公司的非衍生化多种氨基酸、肉碱和琥珀酰丙酮测定试剂盒(包括氨基酸内标准品、酰基肉碱内标准品、干血斑质控品、V型底耐热微孔板、V型截底洁净微孔板、铝箔制微孔板封套、黏性微孔板封套)和溶剂包(包括萃取液和流动相)。
1.2.2 辅助仪器试剂 孵育振荡器(Thermo IEMS Incubator/Shaker HT)、甲醇,均为美国Thermo Fisher公司产品。
1.3 方法
1.3.1 正确度验证方法 选取国家卫生和计划生育委员会临床检验中心2015年第2次室间质评标本AA201522、AA201525和AC201522、AC201525,其中AA201522和AA201525为6项氨基酸低水平和高水平正确度验证标本,AC201522和AC201525为7项肉碱低水平和高水平正确度验证标本。用直径3.2 mm打孔器在滤纸干血斑上各打1孔取样,至于V型截底洁净微孔板,每孔加入内标工作液100 μL,45 ℃密封振荡45 min,提取75 μL萃取液转移至V型底耐热微孔板,铝箔覆盖,上机检测,每标本每天重复测定2次,共5 d。
1.3.2 精密度验证方法 选取美国疾病预防控制中心2015年第2次室间质评标本AA1522、AA1524和AC1562、AC1564,其中AA1522和AA1524为6项氨基酸精密度验证的低水平和高水平标本,AC1562和AC1564为7项肉碱精密度验证的低水平和高水平标本。前处理与正确度验证试验相同,上机后每标本每天重复测定3次,共5 d。
1.3.3 线性范围验证方法 选取本实验室既往检测过的高值和低值可覆盖厂家线性范围的氨基酸、肉碱滤纸干血斑标本,部分项目不能覆盖厂家线性范围时,只验证本实验室检测到的最高或最低水平范围。用直径3.2 mm打孔器在高值和低值滤纸干血斑上各打4孔取样,置于V型截底洁净微孔板,每孔加入内标工作液100 μL,45 ℃密封振荡45 min,每孔吸取75 μL,将4孔高值标本萃取液H和4孔低值标本萃取液L分别混合,按4L、3L+1H、2L+2H、1L+3H、4H配制成5个水平的萃取液,各转移100 μL至V型底耐热微孔板,铝箔覆盖,上机检测,每个水平重复测定4次,1 d内完成。
1.4 统计学处理

(1)
(2)
(3)
(4)
(5)

1.4.2 精密度验证 采用MicrosoftExcel2007软件按照CLSIEP15-A2《用户对精密度和准确度性能的核实实验——批准指南》提供的方法计算批内精密度(CVR)和期间精密度(CVL),将CVR和CVL分别与厂家声明值(CVR1/4 TEA,CVL为1/3 TEA)比较。小于厂家声明值,验证通过;否则计算CVR和CVL验证值,并与之进行比较,小于验证值则判定通过,否则判定未通过。
CVR、批内标准差(SR)、CVL、期间标准差(SL)、批间标准差(SB)、批内精密度验证值(CVR-验)、期间精密度验证值(CVL-验)、期间精密度有效自由度T计算如式(6)至式(13)。
(6)
(7)
(8)
(9)
(10)
(11)
(12)
(13)
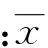

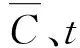
(14)
(15)
(16)
(17)
df=L×R-Rdf
(18)
(19)

2 结 果
2.1 正确度验证 CIT、TYR、C5、C12、C18水平及MET、VAL、C8低水平和LEU、C0、C16高水平验证区间均涵盖靶值,即用验证区间验证法通过正确度验证;其余项目进一步计算Bias,通过比较均小于标准相对偏倚,即用TEA验证法通过正确度验证。全部13个项目正确度验证均通过。
2.2 精密度验证 除VAL低水平CVL外均小于厂家声明值,即用厂家声明值验证法通过精密度验证;VAL低水平CVL大于厂家声明值,需计算其验证值并进行比较。通过比较,VAL低水平CVL小于验证值,故用验证值再验证法通过精密度验证。全部13个项目精密度验证均通过。
2.3 线性范围验证 CIT、LEU、PHE、VAL线性范围上、下限验证均通过;MET、TYR、C0、C3、C5、C8、C12、C16、C18线性范围下限验证通过,上限由于PerkinElmer公司给出线性范围超出本实验室检测标本水平范围,暂未进行验证,目前仅验证至本实验室可检测的最高水平范围,且验证通过。见表1、表2。

表1 氨基酸性能验证结果
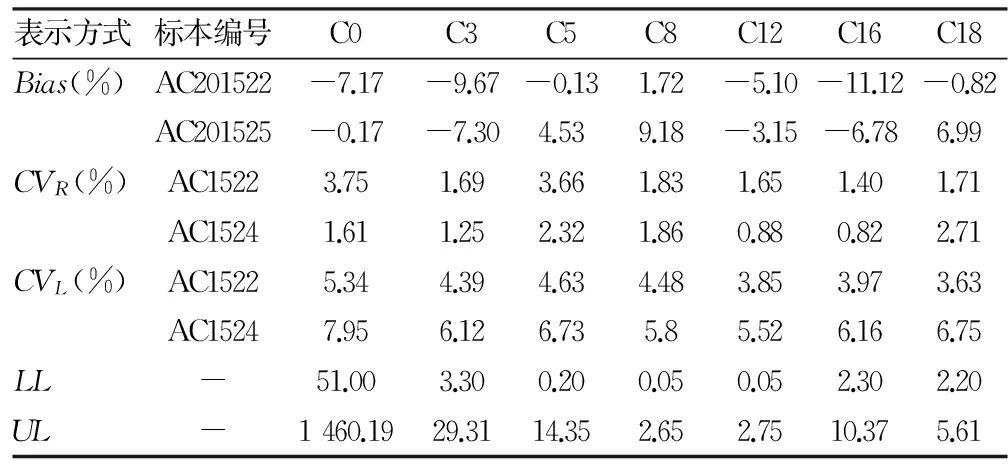
表2 肉碱性能验证结果
3 讨 论
本研究通过对正确度和精密度的验证发现,Waters公司ACQUITY TQD 串联质谱仪及其配套试剂PerkinElmer公司NeoBaseTMNon-derivatized MSMS kit所组成的氨基酸和肉碱检测系统,其Bias为0.13%~11.34%,均小于1/2TEA,但不同检测项目的偏倚范围相差较大,即使同一检测项目其高值和低值偏倚程度也无规律可循,可能与各检测项目的内标准品稳定性不同有关;CVR为0.55%~4.78%,除VAL低水平外批间精密度为2.44%~7.87%,CVL为2.52%~7.95%,符合临床化学检测系统期间精密度大于批间精密度大于批内精密度的一般规律。VAL低水平CVL虽然大于厂家声明值,但是小于其验证值,故通过精密度验证。
线性范围验证试验方案的设计重点在于如何获取系列水平样本。有学者采用打孔后取1、1/2、1/4、1/8血斑获取系列水平样本[9],但该法由于打卡后血斑太小(3.2 mm)而不易于获取理想水平标本。本研究通过摸索,找到获取系列水平标本方法:将高、低水平滤纸干血斑标本分别打4孔,正常孵育振荡,提取萃取液后再将高、低水平萃取液按不同比例混合制成所需水平梯度水平样本。此外,通过对线性范围验证发现,厂家提供某些产品项目的线性范围较窄,不能覆盖日常检测标本的水平范围。如厂家的CIT线性范围为28~1 716 μmol/L,功能敏感性为4.7 μmol/L,而本实验室标本中CIT最低水平值为1.77 μmol/L,不仅低于厂家线性范围下限,也低于功能敏感性,且其他检测项目也有类似现象。故厂家的线性范围或可报告范围还需进一步扩展[10],实验室也应根据实际情况各自建立线性范围。
综上所述,本研究对氨基酸及肉碱串联质谱法配套检测系统的性能特征进行验证,认为虽在标本类型[11]、前处理、检测原理等方面与常规临床化学设备显著不同,但该检测系统仍可按照常规临床化学检测系统的相关标准进行管理和要求[12]。
[1]张捷,胡晓舟.液相色谱与串联质谱在检验医学中的应用[J].中华检验医学杂志,2005,28(8):873-874.
[2]韩连书,高晓岚,叶军,等.串联质谱分析干血滤纸片酰基肉碱方法的建立[J].中华检验医学杂志,2005,28(1):88-91.
[3]李水军.液相色谱-质谱联用技术临床应用[M].上海:上海科学技术出版社,2014.
[4]费阳,王薇,王治国.室间质量评价计划与临床检验的标准化/一致化[J].中华检验医学杂志,2015,38(5):359-360.
[5]张秀明.浅析定量检验程序分析性能验证试验方案设计[J].中华检验医学杂志,2015,38(6):428-430.
[6]中国合格评定国家认可委员会.ISO 15189-2012.医学实验室质量和能力认可准则[S].北京:中国合格评定国家认可委员会,2012.
[7]CLSI.EP 15-A2-2005 User verification of performance for precision and trueness,approved guideline-second edition[S].Wayne,PA,USA:CLSI,2005.
[8]中华人民共和国卫生部.WS/T 408-2012.临床化学设备线性评价指南[S].北京:中华人民共和国卫生部,2012.
[9]田国力,龚振华,王燕敏.非衍生化串联质谱法检测酰基肉碱方法的应用[J].检验医学,2011,26(9):598-601.
[10]王志国.临床检验方法确认与性能验证[M].北京:人民卫生出报社,2009.
[11]段义飞,崔亚利,江永梅.干血斑用于新生儿遗传代谢病筛查的方法学进展[J].中华检验医学杂志,2015,38(4):220-222.
[12]尚世强,杨建滨.新生儿疾病筛查和诊断的发展及存在的问题与思考[J].中华检验医学杂志,2015,38(4):217-219.
Verification of the performance of non-derivatized tandem mass spectrometry method in detecting the amino acids and carnitines
TIANMingxin,ZHANGDaojie,CUIXiaozhao,CHANGHaitao,SUNJiahui,JIWeiwei,LUDongyu
(DepartmentofBiochemicalGeneticsofBeijingShengyuanHuirenClinicalLaboratoryLtd.,Beijing101101,China)
Objective To verify the performance of Waters ACQUITY TQD tandem mass spectrometry and PerkinElmer NeoBaseTMNon-derivatized MSMS kit in detecting the amino acids and carnitines.And ISO15189-2012 Medical laboratories-Requirements for quality and competence were the reference.Methods The accuracy and precision were verified according to Clinical and Laboratory Standards Institute documents,EP15-A2 User Verification of Performance for Precision and Trueness:Approved Guideline.The linear ranges were verified according to industry regulations of Ministry of Health,WS/T 408-2012 Linear Evaluation Guideline of Clinical Chemistry Equipment.Results The relative bias of 6 kinds of amino acids and 7 kinds of carnitines were from 0.13% to 11.34%,which were all lower than 1/2 total error.The within precisions were from 0.55% to 4.78%,which were all lower than 1/4 total error.And the intermediate precisions were from 2.52% to 7.95%,which were all lower than 1/3 total error except valine low level.The linear ranges of citrulline,phenylalanine and free carnitine were into first order linear within the linear range provided by the company.Valine was into second order linear and the rest amino acids were into third order linear.Conclusion The verification of performance of non-derivatized tandem mass spectrometry method in detecting the amino acids and carnitines are passed,and it can be managed and requested in accordance with the routine clinical chemical detection system.
tandem mass spectrometer; performance verification; accuracy; precision; linear range
田明新,女,主管技师,主要从事遗传代谢病检验方面的研究。
10.3969/j.issn.1673-4130.2016.21.027
A
1673-4130(2016)21-3021-04
2016-02-07
2016-04-27)
