格氏试剂制备十九酸
2016-12-05段建利杨志刚
段建利, 杨志刚
(武汉大学 药学院, 省级药学实验教学示范中心, 湖北 武汉 430071)
格氏试剂制备十九酸
段建利, 杨志刚
(武汉大学 药学院, 省级药学实验教学示范中心, 湖北 武汉 430071)
利用格氏试剂和二氧化碳反应制备十九酸。所得十九酸粗品用重结晶的方法纯化,气相色谱仪检测得到含量99%以上的十九酸。实验将格氏试剂、重结晶、含量检测方法有机串联起来,并引入正交设计,获取最优的重结晶条件,使学生在掌握基本有机合成技能的同时了解如何合理有效地安排实验,有助于培养学生的科研能力、激发学生的科研兴趣。
格氏试剂; 十九酸; 重结晶; 正交设计
1 十九酸简介
十九酸也叫正十九烷酸,英文名称为nonadecanoic acid,分子式为C19H38O2,属于长链饱和奇碳脂肪酸。自然界中,十九酸的含量极少,但其应用却极为广泛。十九酸甲酯化后形成十九酸甲酯,是气相色谱法分析脂肪酸含量常用的内标物[1-3]。以十九酸为原料合成的两性表面活性剂,对强酸中的钢铁材料具有较好的缓蚀性[4-5]。十九酸作为磁记录媒质的润滑剂,可显著提高其运行特性和运行耐久性[6]。橡胶中加入十九酸或其金属盐后,摩擦系数降低,抗磨损性提高[7]。Fukuzawa等人的研究表明,灵芝孢子中,抑制HL-60细胞增殖的活性物质,主要是长链脂肪酸,以十九酸的活性最强[8]。十九酸对各种人肿瘤细胞株都有细胞毒活性,而且对人巨噬细胞也有细胞毒性[9]。
根据文献报道,化学合成十九酸的方法主要有以下几种:
(1) 以1-十八醇为原料,经卤代、氰基化,然后水解,得到十九酸[10]。
(2) 利用Arndt-Eistert反应,以十八酸为原料,经氯代、重氮化、银盐催化的Wolff重排、水解,得到十九酸[11]。
(3) 1-二十烯在氧化剂作用下双键断裂,生成十九酸[12]。
(4) 以有机卤代物和二氧化碳为原料,利用电合成法制备十九酸[13]。
以卤代烷烃和二氧化碳反应来制备羧酸,不仅简单、快速,而且成本也很低廉[14]。本实验选用钢瓶装普通二氧化碳气体与格氏试剂反应来制备十九酸。普通二氧化碳气体中,除了二氧化碳外,还有少量的氧气及水分,在反应过程中一定会引入杂质,因此,本实验引入有机合成中常用的纯化方法——重结晶,来除去反应中的杂质,得到含量99%的十九酸。
2 实验目的
(1) 利用格氏试剂与二氧化碳反应,制备十九酸。
(2) 了解实验室实现低温反应的操作方法。
(3) 熟悉重结晶纯化化合物的实验操作方法。
(4) 熟悉化合物的熔点测定。
(5) 掌握采用正交设计法快速筛选最优实验条件的方法。
(6) 了解气相色谱法检测强极性化合物含量的原理,掌握气相色谱检测强极性化合物含量的操作方法。
3 实验原理
本实验以1-溴十八烷为起始原料,四氢呋喃为溶剂,碘和1, 2-溴乙烷为引发剂,与镁条反应,生成格氏试剂。然后,在反应液中通入二氧化碳气体,待反应完成后,缓慢滴加稀硫酸,过滤,旋干,得到粗品。最后,通过重结晶,得到含量99%的十九酸。
由于反应过程中通入的二氧化碳里含有氧气和水分,而且格氏试剂也可能与1-溴十八烷反应,因此可能引入下列杂质:
为了尽可能减少水解产物的形成,反应过程中必须在冷凝管上加装干燥管并通氮气。
4 仪器和试剂
仪器:电磁加热搅拌器(C-MAGHS7,IKA®),熔点仪(X-4,上海精密科学仪器有限公司),气相色谱仪(GC-14C,日本岛津)。
试剂:1-溴十八烷、镁条、1, 2-溴乙烷、四氢呋喃、钢瓶装二氧化碳(普通)、硫酸、三氟化硼乙醚甲醇溶液,正己烷,均为分析纯。色谱级正己烷。
5 气相色谱仪检测条件
色谱柱:DB-Wax石英毛细管柱(30m×0.248mm×0.25μm)。检测器:氢火焰检测器。载气:氮气流速:30mL/min,空气流速:400mL/min,氢气流速:45mL/min。检测器温度:260 ℃,进样口温度:250 ℃。程序升温:初始温度170 ℃,15 ℃/min升温至230 ℃,再以1 ℃/min升温至235 ℃。进样量:1μL。定量方法:面积归一化法。
6 实验内容
6.1 十九酸粗品的合成
在装有100mL恒压滴液漏斗、球形冷凝管(配干燥管)和磁子的250mL干燥三口瓶中,依次加入剪碎的镁条(0.96g,0.04mol)、1, 2-溴乙烷(2-3滴)和经干燥处理的四氢呋喃(10mL)。1-溴十八烷(13.7mL,0.04mol)用经干燥处理的THF(30mL)溶解后,倒入恒压滴液漏斗中。先将约1/5的1-溴十八烷溶液滴加到三颈瓶中,控制油浴温度,缓慢升温至溶液微沸,开启搅拌,将剩余的1-溴十八烷溶液缓慢滴加到反应瓶中。滴加完毕后,再回流反应1h,使镁条几乎反应完全。
将反应液冷却至室温后,放入冰盐浴中,控制反应液温度-5 ℃以下,通入二氧化碳气体,并快速搅拌。注意控制二氧化碳气体的流速,使反应液的温度维持在0 ℃以下。通入二氧化碳气体的时间为1h。然后,缓慢滴加10%硫酸溶液45mL并剧烈搅拌。
硫酸溶液滴加完毕后,将反应液倒入200mL水中,搅拌0.5h,析出大量固体,抽滤,滤饼用水洗至白色,干燥,称重,得十九酸粗品11.3g,气相色谱仪检测十九酸含量为86.3%。
6.2 十九酸粗品的精制
重结晶过程中,对最终产品的含量和收率的影响因素很多,主要影响因素包括:粗品质量和溶剂体积的比例、结晶温度、降温速率和结晶时间。因此,本实验采用L9(34)正交设计表对重结晶条件进行优化,以十九酸的含量为评价指标,获取最佳条件,实验结果见表1。K值表示同因素条件下各水平的实验结果总和,K′值表示同因素条件下各水平的实验结果平均值。

表1 十九酸粗品重结晶条件筛选表
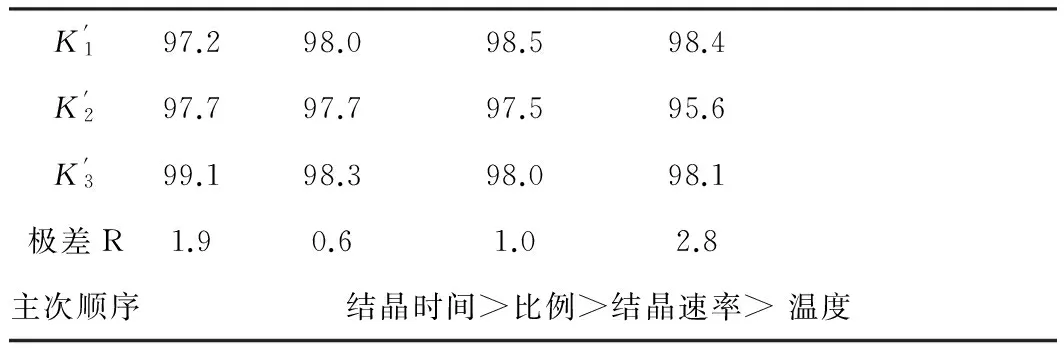
表1(续)
从表中可以看出,最佳重结晶条件为:粗品质量和溶剂体积为1∶6,结晶温度为10 ℃,降温速率10 ℃/10 min,结晶时间为0.5 h。在这4个因素中,结晶时间对十九酸的含量影响最大,而结晶温度对十九酸的含量影响最小。在最佳重结晶条件下的实验结果为:十九酸收率78.8%,含量99.5%。
6.3 十九酸的快速甲酯化
50 mL反应瓶中,依次加入准确称取的十九酸1.0 g,三氟化硼乙醚甲醇溶液1.5 mL,加热至70 ℃,反应10 min。从冷凝管上端口加入色谱纯正己烷7 mL,继续反应2 min。停止加热,冷却至室温,将反应液倒入分液漏斗中,分取有机相,旋干,气相色谱仪检测含量。
7 教学要求
7.1 预习要求
(1) 查阅参考文献,了解化学合成十九酸的方法。
(2) 了解格氏试剂制备和使用过程中的注意事项。
(3) 熟悉气相色谱仪的原理和操作方法。
7.2 实验结果要求
(1) 利用格氏试剂,制备十九酸粗品。
(2) 正确使用L9(34)正交设计表,并提供相应的数据和分析结果。
(3) 根据气相色谱仪检测结果,用面积归一化法给出精制后的十九酸含量。
7.3 思考和讨论
(1) 除了二氧化碳意外,还有哪些无机气体也可以参与有机合成反应?
(2) 利用正交设计表安排实验的好处是什么?还有其他类似的方法吗?
8 结语
格氏试剂是有机合成中最常用的试剂之一,本实验利用格氏试剂与二氧化碳制备十九酸,将无机气体二氧化碳作为反应原料,增加实现的新颖性,并利用重结晶的方法得到高纯的十九酸,使学生在掌握格氏试剂制备和使用的同时,对有机合成中常用的纯化方法有一定的了解。
十九酸含量采用气相色谱检测,需要注意的是,气相色谱检测的是十九酸甲酯的含量,进而计算出十九酸的含量,而不是直接检测十九酸的含量,使学生明白,气相色谱检测化合物时,对化合物有哪些具体的要求。
本实验将有机合成和产品分析结合在一起,使学生意识到仪器分析并不是简单的按键操作,需要对样品进行前处理并对所得数据进行分析,才能获取所需结果。
References)
[1] 廖启斌, 李文权, 陈清花, 等.海洋微藻脂肪酸的气相色谱分析[J]. 海洋通报, 2000, 19(6):66-71.
[2] Abdulkadir S, Tsuchiya M. One-step Method for Quantitative and Qualitative Analysis of Fatty Acids in Marine Animal Samples[J]. Journal of Experimental Marine Biology and Ecology, 2008, 354(1):1-8.
[3] 张志超,余新威,方力,等.气相色谱法同时测定海产品中37种脂肪酸含量[J].中国卫生检验杂志, 2014, 24(12):1710-1713.
[4] 杜先献,申美娜,杨世珖,等.两性表面活性剂的合成及性质的研究[J].高等学校化学学报,1986,7(6):522-524.
[5] 杜先献,杨世珖,陈玉康,等.2-(2’-二甲胺基乙氧基,脂肪酸盐酸盐的合成及性能的研究[J]. 化学试剂,1983,5(6):383-384.
[6] Taketoshi S,Jota I,Hiroshi Y.Magnetic Recording Medium Using Saturated Fatty Acid and Perfluoropolyether Ester as Lubricants:Japan, JP:2000357314[P].2000-12-26.
[7] Yoshiaki Y, Shigeru H, Yoshiyuki M. Rubber Antifriction Compositions[P]. Japan, JP 61261327, 1986-11-19.
[8] Fukuzawa M,Yamaguchi R,Hide I, et al.Possible Involvement of Long Chain Fatty Acids in the Spores ofGanodermalucidum(Reishi Houshi) to Its Anti-tumor Activity[J]. Biological & Pharmaceutical Bulletin,2008,31(10):1933-1937.
[9] Yoo J C,Han J M,Nam S K,et al.Characterization and Cytotoxic Activities of Nonadecanoic Acid Produced byStreptomycesscabieisubsp.chosunensisM0137 (KCTC 9927) [J]. Journal of Microbiology (Seoul, Republic of Korea), 2002, 40(4):331-334.
[10] Levene P A,Taylor F A.The Synthesis of Normal Fatty Acids from Stearic Acid to Hexacosantic Acid[J].the Journal of Biological Chemistry,1924,59(3):905-921.
[11] Vandenheuvel F A, Yates P.The Application of the Arndt-Eistert Reaction to the Synthesis of Fatty Acids of High Molecular Weight[J].Canadian Journal of Research, Section B: Chemical Sciences,1950,28B(9):556-560.
[12] Lee D C, Lamb S E, Chang V S. Carboxylic Acids from the Oxidation of Terminal Alkenes by Permanganate: Nonadecanoic Acid[J].John Wiley & Sons Inc, 2003,60(3):11.
[13] Sock O,Troupel M,Perichon J.Electrosynthesis of Carboxylic Acids from Organic Halides and Carbon Dioxide[J].Tetrahedron Letters,1985,26(12):1509-1512.
[14] Evano G.Carboxylic Acids: Synthesis from Organic Halides[J].Cheminform, 2008,39(44):2878-2891.
Synthesis of nonadecanoic acid using Grignard reagen
Duan Jianli, Yang Zhigang
(Provincial Demonstration Center of Experimental Pharmaceutical Teaching, School of Pharmaceutical Sciences, Wuhan University, Wuhan 430071, China)
Nonadecanoic acid is synthesized by reacting of the Grignard reagent and carbon dioxide. The crude nonadecanoic acid is purified through recrystallization, and then detected using gas chromatograph. The content of purified nonadecanoic acid is over 99%. The Grignard reagent, recrystallization, determination of the target compound are involved in this experiment, moreover, orthogonal design is used to acquire the optimum recrystalliztion conditions. Students can obtain elementary organic synthesis method, and learn how to arrange the experiment effectively. This experiment is helpful for students to cultivate their ability in scientific research and stimulate their research interest.
Grignard reagent; nonadecanoic acid; recrystallization; orthogonal design
10.16791/j.cnki.sjg.2016.11.052
2016-05-03
国家自然科学基金项目(21402144);武汉大学医学部教学改革研究项目(2015037)
段建利(1979—),男,湖北随州,博士,实验师,主要从事有机化学和药物化学实验教学.
O6-33
A
1002-4956(2016)11-0202-03
