Fe3O4@SiO2@m TiO2介孔多功能纳米复合颗粒的制备及载药能力
2016-12-05彭红霞胡传跃吴腾宴胡继林田修营
彭红霞 胡传跃 吴腾宴 胡继林 田修营
(湖南人文科技学院材料与环境工程学院,娄底417000)
Fe3O4@SiO2@m TiO2介孔多功能纳米复合颗粒的制备及载药能力
彭红霞*胡传跃吴腾宴胡继林田修营
(湖南人文科技学院材料与环境工程学院,娄底417000)
以溶剂热法制备氨基功能化的Fe3O4纳米颗粒为磁核,结合溶胶-凝胶法和模板法在其表面先后包覆上致密的SiO2层和介孔TiO2层,制备了磁性-发光-微波热转换性-介孔结构为一体的多功能核-壳结构纳米复合颗粒,并对其结构、性能及载药能力进行了研究。XRD分析表明:Fe3O4表面包覆上了无定形结构的SiO2和TiO2。TEM照片表明:所得的纳米复合颗粒具有明显的核壳结构和完美的球形,构成核的Fe3O4颗粒的尺寸在40~50 nm之间,Fe3O4@SiO2@mTiO2核壳结构纳米复合颗粒的尺寸为60~70 nm,壳层厚度约10 nm,并可观察到壳层中清晰的孔状结构。磁性、荧光光谱和微波热转换特性分析表明:该复合颗粒同时具有良好的发光性、磁性和微波热转换特性。N2气吸附及药物负载率分析表明,该复合颗粒具有较高的比表面积(640m2·g-1)和介孔结构(孔径约2.8 nm)并且具有较高的药物负载率。
Fe3O4@SiO2@mTiO2;介孔;磁性;荧光性;微波热转换性;药物负载
癌症已经成为人类健康生活的重大威胁,由于抗癌药物在抑制癌细胞的同时对正常细胞有较大损伤,因此科学家们一直致力于开发靶向可控释放的纳米颗粒作为药物载体,进而降低抗肿瘤药物对人体正常细胞的毒副作用,同时提高抗肿瘤药物对肿瘤的治疗效果[1-3]。
在对肿瘤的临床治疗中,较为理想的可控药物传输系统不仅要求其自身具有良好的生物相容性和较高的药物负载率,而且还要求其在人体的血液循环系统中具有较好的稳定性,并且药物分子在到达病灶部位后能可控释放[4-5]。为了提高抗肿瘤药物分子对肿瘤的治疗效果,探索一种有效的药物可控释放(定时、定点、定量释放)的方法显得尤为重要。
近年来,介孔复合纳米材料以其独特的结构,在医药领域的应用研究中得到了广泛的关注。大量的文献报道表明[6-7],介孔二氧化硅用于药物载体的比例较高。例如:曹等[8]利用溶胶-凝胶法制备出了具有pH值响应功能的介孔二氧化硅纳米颗粒;Lee等[9]则是通过同样的方法制备了Fe3O4@mSiO2并进行了生物实验;Argyo等[10]系统性地研究了多功能介孔二氧化硅作为药物输送载体的药理。介孔Fe3O4@mSiO2纳米颗粒利用其介孔结构的物理吸附作用进行药物装载,且其具有磁响应性,可以对药物进行靶向控制释放,故介孔Fe3O4@mSiO2纳米颗粒作为较理想的药物载体具有潜在的应用价值。但该纳米颗粒不具有发光特性,无法实现药物负载和释放过程的跟踪与检测。Yan等[11]结合溶胶-凝胶法和模板法制备了兼具磁性、荧光和介孔性能的Fe3O4@mSiO2-YVO4∶Eu3+纳米颗粒,实现了介孔Fe3O4@mSiO2磁性纳米颗粒中引入发光功能,拓展了无机材料在医学领域中的应用空间[12]。但该复合颗粒结构复杂,而且沉积在介孔二氧化硅表面的发光材料会堵塞孔道,使其载药率降低。
TiO2是一种半导体量子点,它具备半导体量子点发光材料的一些重要特征:激发波长范围宽、荧光量子产率高、荧光强度较强及生物相容性好等,这些优点利于其进行特异性连接,并可进行体内荧光成像[13]。此外,TiO2纳米颗粒具有较强的微波吸收性和微波-热转换特性,可以用作非侵袭局部加热热源,用微波照射时,该纳米粒子的加热速度快,可自动达到热平衡,无脂肪过热等问题[14]。
无定形mTiO2同mSiO2一样,具有规则有序的孔道、易于改性的表面和稳定的化学性质等[15],与此同时它还具备mSiO2不具备的重要功能,即发光和微波热转换特性等优点。由于荧光猝灭作用,在磁性材料和发光层中间放置一层致密的二氧化硅层是十分有必要的[16]。这种多功能纳米复合材料结构相对简单,在外部磁场进行操纵的同时可以利用成像技术实时监控药物释放过程,通过微波刺激可实现药物的可控释放,另外,mTiO2规则有序的孔道可以大大提高其载药量。因此,它的出现可实现疾病诊断和治疗的一体化,并且将进一步提高诊断和治疗的效率,减少抗癌药物的毒副作用。
综上所述,本文提出了一种新的思路,即将兼具发光和微波-热转换特性的材料制备成介孔结构与磁性材料进行组装,合成一种在一个实体内兼具多种功能的多功能纳米颗粒,这样不仅简化了载体的结构,而且还能在提高载药量的同时达到靶向可控药物释放的目的。采用溶剂热法制备出磁性核材料,即氨基功能化的Fe3O4纳米颗粒,然后结合溶胶-凝胶法和模板法将SiO2和mTiO2先后包覆在Fe3O4纳米颗粒的表面,制备出具有磁性、发光和微波热转换特性的Fe3O4@SiO2@mTiO2介孔复合纳米颗粒(见图1),并且研究了其性能及药物负载能力。

图1 Fe3O4@SiO2@mTiO2介孔多功能纳米复合颗粒的制备及载药过程示意图Fig.1 Illustration of the process of creating and loading drugmesoporous Fe3O4@SiO2@mTiO2multifunctional nanoparticles
1 实验部分
1.1主要试剂
三氯化铁(FeCl3·6H2O)(纯度>99.0%,北京朝阳区通惠化工厂),无水乙酸钠(纯度>99.0%,北京益利精细化学品有限公司),乙二胺(纯度96.0%,国药集团化学试剂有限公司),乙二醇(纯度:96.0%,北京化工厂),钛酸四丁酯(C16H36O4Ti,分析纯,国药集团化学试剂有限公司),正硅酸乙酯(Si(OC2H5)4纯度:99%,国药集团化学试剂有限公司),十六烷基三甲基溴化胺(CTAB,纯度:9.0%,天津市科密欧化学试剂开发中心)。
1.2样品的制备
磁性Fe3O4颗粒的制备:采用文献[4]的方法。
Fe3O4@SiO2复合纳米颗粒的制备:取0.05 g Fe3O4加入到一定量的去离子水和乙醇的混合溶液中,超声20 min,然后滴加1.0 mL氨水,而后边搅拌边滴加0.2 mL正硅酸乙酯,室温下继续搅拌8 h,所得到样品用去离子水和乙醇分别清洗3次,在50℃下干燥6 h。
Fe3O4@SiO2@mTiO2复合纳米颗粒的制备:取0.05 g Fe3O4@SiO2加入到30 mL溶有0.15 g CTAB的乙醇溶液中,超声20 min,加入0.4 mL钛酸四丁酯,搅拌1 h,然后边搅拌边缓慢加入2 mL去离子水,继续搅拌3 h,利用磁分离收集,所得到样品用去离子水和乙醇各洗涤3次,在80℃下干燥。最后300℃煅烧3 h,去除模板剂而得到Fe3O4@SiO2@ mTiO2样品。
Fe3O4@SiO2@mTiO2复合纳米颗粒的药物装载:将0.3 g Fe3O4@SiO2@mTiO2分散于50 mL 0.04 g· mL-1IBU溶液中,室温下搅拌6 h。收集共3次的上清液,用紫外-可见分光光度计对上清液进行吸光度测量,测定负载在复合纳米颗粒表面的IBU的含量,计算载药率公式如下:载药率M=Mads/Madd(Mads是纳米颗粒表面已负载的药物质量;Madd是载药过程中加入的初始药物的质量)
1.3样品的表征
采用日本JEOL公司的JEM-2010型透射电镜观察粒子的形貌和尺寸。用日本Bruker D8FOCUS多晶粉末X射线衍射(XRD)仪进行物相分析,其X射线源为Cu靶Kα1辐射,λ=0.154 056 nm,电压为30 kV,电流为20mA,衍射角为10°~80°,步长为10° ·min-1,扫描速率为0.1°·s-1。采用日本HITACHI公司的F-4500型荧光光谱仪对样品的发光性能进行测试。测量范围为200~800 nm,扫描速率为1 200 nm· min-1,步长为0.2 nm,用150W氙灯作激发源。样品的磁性用美国Quantum Design公司的MPMS磁学测量系统(MPMSSQUID XL)进行测定。样品的微波-热转换特性用微波反应器(MCR-3,上海将来实验设备有限公司)进行测定。氮气吸附与解吸等温曲线在液氮温度(77K)下采用ASAP 2010M测得。
2 结果与讨论
2.1X射线衍射(XRD)分析
图2是所合成样品的XRD图,由图2a可见,所有衍射峰的位置和相对强度与尖晶石型Fe3O4(PDF #65-3107)标准谱非常吻合,未出现杂峰,表明所制备的样品为尖晶石型Fe3O4。图2c为纯TiO2纳米颗粒的XRD谱图,在2.0°~25.0°处只见一个宽峰,表明所制备的样品为无定形结构的TiO2。图2b为Fe3O4@SiO2@mTiO2纳米颗粒的XRD图,从该图可清晰地看出2.0°~25.0°处出现无定形结构SiO2和TiO2的衍射峰,SiO2和TiO2的衍射峰重叠。从图2b还可以看到2θ=30°、36°、44.5°、57°和63°处的Fe3O4的特征衍射峰。实验结果表明,SiO2和TiO2成功沉积在Fe3O4纳米颗粒的表面上,未出现任何杂峰,表明在合成过程中核与外壳之间没有发生反应。

图2 样品的XRD图Fig.2 XRD patterns of the samples
2.2红外光谱(FTIR)分析
图3是样品Fe3O4,(b)Fe3O4@SiO2@TiO2-IBU和(c)IBU的红外光谱图。在图3a中,575 cm-1处出现了Fe3O4中的Fe-O振动吸收峰;在2 938和2 862 cm-1处出现了亚甲基的2个C-H振动吸收峰;3 440 cm-1处出现了-OH的振动吸收峰;并且在1 634和2 358 cm-1处分别出现了氨基的N-H剪式振动吸收峰和亚胺盐N-H的振动吸收峰,说明乙二胺成功修饰在Fe3O4粒子的表面上[16]。在样品Fe3O4@ SiO2@TiO2-IBU的谱图(图3b)中,除了551和571 cm-1处出现了Fe-O的振动峰外,463 cm-1处出现了Ti-O的振动吸收峰;3 440 cm-1处出现了-OH的振动吸收峰;在1 108 cm-1附近出现了Si-O-Si的反对称振动吸收峰[17];952 cm-1附近出现了Si-O的对称伸缩振动吸收峰[17];进一步表明TiO2和SiO2成功沉积在Fe3O4纳米颗粒的表面上。而且,在1 748,1 448和2 903 cm-1处分别出现了布洛芬的C=O,C-C和C-H特征吸收峰[18],但是其强度比纯IBU(图3c)的有所减弱,且未出现额外的新的化学键吸收峰,表明通过药物负载过程纳米载体与药物分子之间并未形成新的化学键,而是IBU通过氢键作用成功地吸附在了纳米载体表面。

图3 样品的红外光谱图Fig.3 FTIR spectra of the samples
2.3TEM和EDS分析
为了更清晰地观察复合颗粒的形貌以及包覆层的厚度,对其进行了透射电镜分析,如图4所示。由图4a可见,Fe3O4颗粒为均匀的球形,粒径分布较均匀,表面光滑,粒径在40~50 nm。由图4b可见,复合颗粒仍为球形结构,球形样品内部与边缘明显的衬度对比说明制备的复合颗粒具有核壳结构。复合颗粒的尺寸约为70 nm,壳层厚度约10 nm。与包覆前的Fe3O4相比较,包覆后的颗粒尺寸明显增大。说明成功获得了Fe3O4@SiO2@mTiO2复合颗粒,其中含有0.05 g的Fe3O4,0.012 g的SiO2和0.029 g的mTiO2。而且,可以通过改变反应时间和反应物初始浓度来实现各部分含量(即不同壳层厚度)的控制。另外,从放大图4c可以看出,TiO2壳层中清晰的孔状结构,并且从高分辨率透射显微镜(图4d)可以看出,除了核部Fe3O4的晶格线(0.251 8 nm,对应于Fe3O4的(311)晶面间距)外,未观察到其他明显的晶格线,这进一步证实了TiO2和SiO2壳层为无定形构型。图5为复合颗粒的能量色散谱图。从图中可以明显看到O、Si、Ti和Fe元素的峰,Cu元素的峰是由基片产生的,结合XRD分析,进一步说明了样品为Fe3O4@SiO2@mTiO2复合物。

图4 Fe3O4(a),Fe3O4@SiO2@mTiO2(b,c,d)复合颗粒样品的透射照片Fig.4 Transmission images of Fe3O4(a),Fe3O4@SiO2@ mTiO2(b,c)nanoparticles

图5 Fe3O4@SiO2@mTiO2的EDS谱图Fig.5 EDSspectrum of the Fe3O4@SiO2@mTiO2
2.4荧光光谱分析
采用日本HITACHI公司的F-4500型荧光光谱仪对样品进行了荧光分析。首先将相同质量的的3个样品分别固定在石英玻片为载体,激发光和样品表面的夹角为45°的固体支架上。激发源为150W,激发波长为254 nm时,分别测得3个样品的发射光谱。样品(a)mTiO2,(b)Fe3O4@SiO2@mTiO2和(c)Fe3O4@mTiO2的发射光谱如图6所示。由图6可见,3个样品均在395 nm处即紫外区具有发光峰,归属于mTiO2的本征跃迁,主要源于mTiO2自由激子复合引起的发光[19]。从图可见,Fe3O4@mTiO2纳米颗粒的紫外发光强度与纯mTiO2纳米颗粒相比有所减弱,这可能是由于Fe3O4与mTiO2的功能函数不同,Fe3O4与mTiO2直接接触时,在其二者之间可能存在一定的电子转移,使得复合颗粒中mTiO2组分的荧光被部分淬灭,从而导致发光强度减弱。同时,从谱图中也可以看出,Fe3O4@SiO2@mTiO2纳米颗粒发射峰强度比Fe3O4@mTiO2纳米颗粒发射峰强度较强,由于SiO2层在磁性核与发光壳层之间具有一定的屏蔽作用而致[17]。并且,Fe3O4@SiO2@mTiO2纳米颗粒的发光强度介于二者之间表明致密的SiO2层起到了隔层作用,即减弱了荧光淬灭效应。尽管Fe3O4@SiO2@mTiO2纳米颗粒的发光强度有所减弱,但在生物医学应用中仍具有足够的荧光强度。

图6 样品(a)mTiO2,(b)Fe3O4@SiO2@mTiO2和(c)Fe3O4@mTiO2的发射光谱Fig.6 Emission spectra of the samples:(a)mTiO2;(b)Fe3O4@SiO2@mTiO2;(c)Fe3O4@mTiO2
2.5磁学性质分析
图7分别给出了(a)Fe3O4纳米颗粒,(b)Fe3O4@ SiO2和(c)Fe3O4@SiO2@mTiO2复合颗粒的磁滞回线图,外加磁场为10 kOe,温度为300 K。由图可以清楚的看到样品具有相似的磁性质,有微弱的磁滞现象,矫顽力很小可以忽略不计。3种样品的饱和磁化强度分别为81.2、32.4和18.7 emu·g-1。包覆后饱和磁化强度明显降低可能是因为Fe3O4@SiO2和Fe3O4@SiO2@mTiO2复合颗粒中引入非磁性物质,使磁性Fe3O4质量分数降低,从而导致磁性降低。随着引入的非磁性物质的增多,磁性降低越多[17]。尽管Fe3O4@SiO2@mTiO2复合颗粒的饱和磁化强度比Fe3O4磁核小很多,但在磁分离等应用中仍具有足够的磁饱和强度。Fe3O4@SiO2@mTiO2复合颗粒在水溶液中的磁响应性如图7的插图所示。由照片可见,当有外加磁场接近分散在水中的Fe3O4@SiO2@ mTiO2复合颗粒时,这些纳米颗粒迅速被吸引并堆积在靠近磁场的小瓶一侧,结果证复合粒子具有很好的磁响应能力。
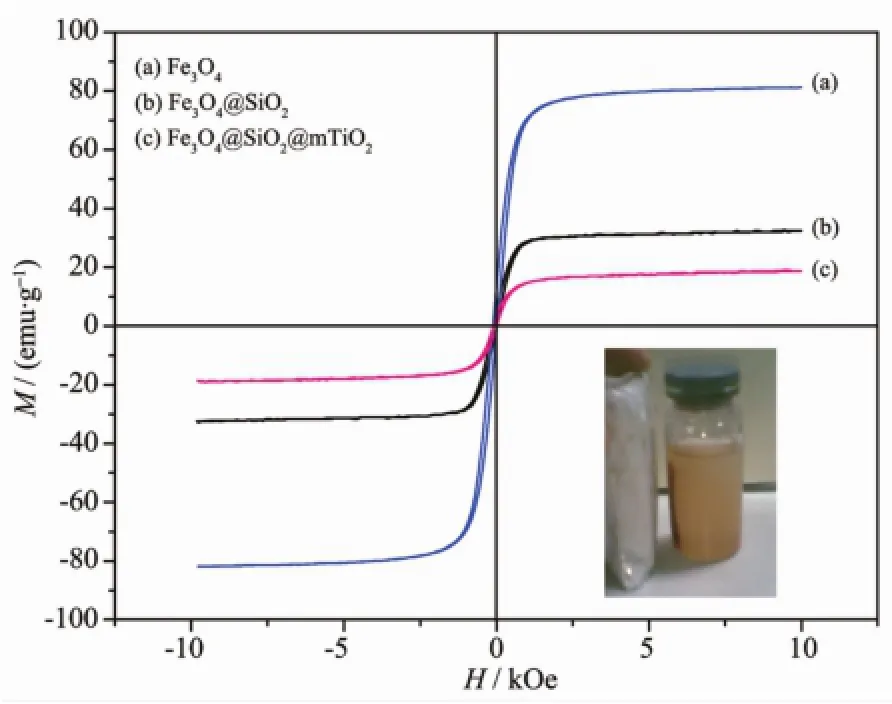
图7 样品(a)Fe3O4;(b)Fe3O4@SiO2;(c)Fe3O4@SiO2@ mTiO2的磁滞回线Fig.7 Measured magnetic hysteresis loops of samples:(a)Fe3O4;(b)Fe3O4@SiO2;(c)Fe3O4@SiO2@mTiO2

图8 在微波辐射下生理盐水溶液,Fe3O4和Fe3O4@ SiO2@mTiO2溶液的温度变化曲线Fig.8 Heating profile of sodium chloride solution, Fe3O4and Fe3O4@SiO2@mTiO2in sodium chloride solution
纳米颗粒的微波-热转换作用产生的热量与微波强度以及微波照时间相关。为了检测该纳米颗粒的微波热响应性能,我们对合成的纳米颗粒以及作为溶剂的生理盐水溶液分别做了微波热转换性能测试,如图8所示。首先称取相同质量的Fe3O4和Fe3O4@SiO2@mTiO2分散在相同体积的生理盐水中,在2.45 GHz的医用微波频段的微波照射下测量微波照射吋间随温度的变化情况,为了直接说明纳米颗粒的微波热转换性能,用生理盐水作为空白对比试验。从图8可以看出,当用微波(2.45 GHz,8W)照射10min后,生理盐水溶液和Fe3O4溶液的温度分别达到36.5和30.8℃。而Fe3O4@SiO2@mTiO2溶液的温度达到45.0℃,此温度足以诱导靶细胞的死亡和控制释放药物。微波照射时,该纳米颗粒有效地将电磁能转化为热能,使其温度升高[20]。实验结果表明,Fe3O4@SiO2@mTiO2纳米颗粒具有良好的微波-热转换效应。
2.6吸附平衡等温线分析
为了表征实验制备的纳米复合颗粒的介孔特性,我们进行了液氮的吸附-解吸附性能测试,Fe3O4@SiO2@mTiO2复合颗粒的液氮的吸附-解吸附等温曲线如图8所示。根据国际理论和应用化学联合会的分类方法,复合颗粒的吸附-解吸附等温曲线显示为典型的带有HI迟滞环的Ⅳ型等温曲线,出现该类型的吸附-解吸附曲线是由于材料中存在孔径比较均一的介孔发生毛细凝聚现象导致的[21]。这说明通过去除CTAB模板后成功地将介孔TiO2包覆在了Fe3O4@SiO2表面。根据吸附数据计算得到Fe3O4@SiO2@mTiO2复合颗粒的BET表面积和总孔容体积分别为640m2·g-1和0.29 cm3·g-1。根据测试数据绘制的孔径分布如图9插图所示,由图可知Fe3O4@SiO2@mTiO2复合颗粒的介孔孔径平均为2.8 nm,且孔径大小分布比较均一。液氮的吸附-解吸附测试结果表明实验制备合成的Fe3O4@SiO2@mTiO2复合颗粒具有高的比表面积和较为均一的介孔形貌,这与高倍透射电镜的分析结果相吻合,高的表面积和大的孔容体积有利于高效、大容量的装载药物分子,是一种十分有效的药物纳米载体。

图9 Fe3O4@SiO2@mTiO2样品的孔径分布图(a)和等温吸附线(b)Fig.9 Pore diameter distribution(a)and N2adsptiondesorption isotherms(b)of Fe3O4@SiO2@mTiO2
2.7药物装载研究
为了研究纳米复合纳米颗粒的药物装载性能,从而确定其是否适合用于药物载体,本次实验选择了布洛芬(IBU)作为模型药物,该分子含有羧基基团易于与其他分子结合。在接近人体体液的生理盐水溶液中进行药物装载实验。IBU药物分子中的羧基与TiO2壳层上吸附的H2O分子形成氢键,从而实现了药物分子在纳米颗粒表面的装载。
实验使用紫外-可见分光光度法来测定布洛芬的负载量[18]。在220 nm处的峰值被选择为布洛芬的特征峰,根据Beer-Lambert定律定量,绘制出吸光度对浓度的校准曲线图。如图10所示为布洛芬药物装载量随时间变化的函数曲线(室温,pH=7)。在开始的2 h内,药物的装载率约为58%。随着时间的增加,在220 nm处的吸收带强度降低,这表明布洛芬装载量增加。随后装载的20 h,紫外-可见光谱显示在220 nm处的吸收峰没有进一步的明显变化。此时,约60%的布洛芬已被负载在Fe3O4@SiO2@ mTiO2纳米复合颗粒的表面和孔道内。实验结果表明,该纳米复合颗粒具有较好的药物负载能力。而且从样品的FT-IR图谱分析也可看出药物分子成功负载在纳米载体的表面上。另一方面,IBU和纳米颗粒之间的氢键相对较弱,易于断开,通过调整溶液的温度,可实现药物释放的控制[4]。

图10 释放过程溶液的紫外光谱(a)和Fe3O4@SiO2@ m TiO2在生理盐水中释药曲线(b)Fig.10 Ultraviolet spectrum of the solution in release process(a)and release curves of Fe3O4@SiO2@mTiO2loaded with drugs in physiological saline(b)
3 结论
(1)本文采用溶剂热法和溶胶-凝胶法制备了Fe3O4@SiO2纳米颗粒,进一步在纳米粒子表面通过模板法包覆上一层介孔TiO2,从而制备出具有磁性、荧光性、微波热转换性以及介孔性能于一体的多层核壳结构的Fe3O4@SiO2@mTiO2纳米复合颗粒。
(2)磁性、荧光性、微波热转换性以及介孔性质的分析结果表明该纳米颗粒具有高的饱和磁化强度(18.66 emu·g-1),优良的微波热响应特性、发光性能和高比表面积(640m2·g-1),大的孔容体积(0.29 cm3·g-1)。
(3)以布洛芬(IBU)为模板药物,研究了其载药能力。研究结果表明,该纳米颗粒具有较好的药物装载能力,是一种性能优异的新型纳米载体。该多功能纳米颗粒可潜在应用于靶向药物传输与可控释放、微波热疗以及污水处理等领域。
[1]XiongW,Mazid R,Yap LW,et al.Nanoscale,2014,6:14388 -14396
[2]Lauth V,MaasM,Rezwan K J,etal.J.Mater.Chem.B,2014, 2:7725-7729
[3]Shang H B,Chen F,Wu J,et al.RSC Adv.,2014,4:53122-53128
[4]Peng H X,CuiB,ZhaoWW,etal.ExpertOpin.Drug Deliv., 2015,12(9):1-7
[5]Qiu H J,Cui B,Li G M,et al.J.Phys.Chem.C,2014,118 (27):14929-14933
[6]Hu S,Wu G,Huang Z J,etal.Nanosci.Nanotechnol.,2010, 10(11):7592-7596
[7]Wang T,He JP,Zhou JH.J.Solid State Chem.,2010,183: 2797-2800
[8]CHAO Jie(曹杰),HE Ding-Geng(何定庚),HE Xiao-Xiao(何晓晓),et al.Chem.J.Chinese Universities(高等学校化学学报),2012,33(5):914-918
[9]Lee J,Lee N,Kim T,et al.Acc.Chem.Res.,2011,44:893-902
[10]Argyo C,Weiss V,Brauchle C,et al.Chem.Mater.,2014, 26:435-441
[11]Yang P P,Quan ZW,Hou Z Y,et al.Biomaterials,2009, 30:4786-4792
[12]HEQuan-Guo(贺全国),WUWei(吴伟),CHEN Hong(陈洪). Chem.Sensors(化学传感器),2007,27(1):9-14
[13]Obregón SKubacka A,Fernández-García M.J.Catal.,2013, 299:298-303
[14]Liu JW,Che R C,Chen H J.Small,2012,88:1214-1220
[15]Wu J,Liu Y,LiW,et al.J.Mater.Chem.B,2014,2:7764-7771
[16]Yu XG,Shan Y,LiGC.etal.J.Mater.Chem.,2011,21:8104
[17]PENG Hong-Xia(彭红霞),LIU Gui-Xia(刘桂霞),DONG Xiang-Ting(董相廷),et al.Chinese J.Inorg.Chem.(无机化学学报),2012,287:1305-1309
[18]Wang Y S,Peng H X,Cui B.Mater.Chem.Phys.,2014,146: 330-335
[19]LIDan-Chen(李旦振),ZHEG Yi(郑宜),FU Xian-Zhi(付贤智).Chin.J.Mater.Res.(材料研究学报),2000,14(6):1005-1009
[20]Zhu C L,Zhang M L,Qiao Y J.J.Phys.Chem.C,2010, 11439:16229-16234
[21]Fu J,Zheng R,Fang J,et al.J.A lloy Compd.,2015,650: 463-469
Synthesis of M esoporous Fe3O4@SiO2@m TiO2Multifunctional Nanoparticlesw ith the Capability for Drug Loading
PENG Hong-Xia*HU Chuan-Yue WU Teng-Yan HU Ji-Lin TIAN Xiu-Ying
(College ofMaterials&Environment Engineering,Hunan University of Humanities, Science and Technology,Loudi,Hunan 417000,China)
In this paper,Fe3O4@SiO2@mTiO2(m was short for mesoporous)core-shell structured nanoparticles with luminescence,magnetic,microwave to heat responsive properties and high specific surface area(640 m2·g-1) were synthesized by Sol-gel method and template method.XRD patterns showed that the SiO2and mesoporous TiO2are coated on the surface of Fe3O4particles after calcined at 300℃.TEM images showed that the obtained nanoparticles have obvious core-shell structure and spherical morphology.The diameter of Fe3O4@SiO2@mTiO2nanoparticles is about 60~70 nm,the shell shows a gray color with an average thickness of about 10 nm.The nanoparticles not only have the large accessible pore size(2.8 nm)for the physical adsorption of drugmolecules and showed good luminescent properities,strongmagnetic and uniquemicrowave to heat responsive properties.
Fe3O4@SiO2@mTiO2;mesoporous;magnetic;lum inescent;microwave to heat responsive properties;drug loading
O614.81+1;O614.41+1
A
1001-4861(2016)07-1154-07
10.11862/CJIC.2016.159
2015-12-10。收修改稿日期:2016-05-22。
湖南省教育厅科学研究重点(No.13A047)资助项目。
*通信联系人。E-mail:penghongxia1@126.com
