冠醚双浊点选择性萃取环境水样和食品中的痕量铅
2016-12-01毛艳丽崔琬晶夏晋晨刘莹莹
毛艳丽 韩 娟 崔琬晶 王 赟 唐 旭 夏晋晨 刘莹莹
1(河南城建学院,市政与环境工程学院,平顶山 467036) 2(江苏大学,食品与生物工程学院,镇江 212013)
冠醚双浊点选择性萃取环境水样和食品中的痕量铅
毛艳丽1韩 娟*2崔琬晶3王 赟3唐 旭3夏晋晨3刘莹莹3
1(河南城建学院,市政与环境工程学院,平顶山 467036)2(江苏大学,食品与生物工程学院,镇江 212013)
3(江苏大学,化学化工学院,镇江 212013)
建立了冠醚双浊点萃取(DCH18C6-DCPE)测定环境水样和食品中痕量铅的方法。本方法包括两步浊点萃取,第一步是二环己基十八冠六(DCH18C6)选择性萃取铅形成疏水性络合物进入L64富集相;第二步是向一步浊点萃取得到的L64富聚相中加入适量EDTA溶液,基于铅与EDTA的结合能力更强,使得铅被反萃入水相。通过单因素与响应曲面实验优化得到最佳条件为:L64浓度为2.06%(w/w),K2HPO4浓度为8.13%(w/w),DCH18C6浓度为207.2 μg/mL,反萃温度为70℃,萃取时间为10 min,富集倍数为18。在优化条件下,测得铅的线性范围为0.05~0.3 μg/mL,相关系数为0.998,铅的萃取率为98.8%,检出限为2.8 μg/L,日内精度RSD<4.6%,日间精度RSD<6.8%。对实际环境水样和食品进行加标回收实验,回收率为97.3%~102.2%,相对标准偏差RSD<3.7%,结果令人满意,说明本方法对于实际样本的检测具有可行性。
二环己基十八冠六(DCH18C6); 双浊点萃取; 温敏型三嵌段聚合物L64; 铅
1 引 言
铅作为重金属污染物之一,能通过复杂食物链在人体内蓄积,当浓度达到一定量后, 会损害神经系统、消化系统,造血系统等组织系统,甚至还会影响智力发育[1,2]。因此检测食品和环境水样等实际样品中铅的含量尤为重要。
浊点萃取(CPE)[3~6]因具有操作设备简单、绿色环保、萃取效率高等优点,广泛用于萃取富集金属离子。但是浊点萃取中表面活性剂粘度高,不便于仪器检测[7]和疏水性物质的干扰问题[8]一直未得到解决。在此基础上,双浊点萃取(DCPE)[9,10]体系逐渐受到研究者关注。DCPE有效解决了CPE的弊端,提高了分析方法的准确性和选择性。此外萃取结束后的表面活性剂可以回收再利用,不仅降低了实验成本,而且更加符合绿色化学的理念。
目前,常用的络合剂大多集中在APDC[11], DDTC[12], PAN[13]和EDTA等,而这些络合剂是没有选择性的,故不能达到选择性萃取铅离子的目的。冠醚[14,15]作为一种金属离子的络合剂,因其空腔的直径大小与阳离子直径相匹配所以成功实现了金属离子的选择性络合[16,17]。在浊点萃取过程中,常用的表面活性剂为曲拉通和PONPE系列[18~20]。然而,这些表面活性剂的结构中含有苯基,干扰荧光和紫外的测定,并对人体有一定的危害和刺激。本研究将高分子表面活性剂温敏型嵌段共聚物—聚氧乙烯-聚氧丙烯-聚氧乙烯(简称PEO-PPO-PEO)作为表面活性剂应用到双浊点萃取技术中。PEO-PPO-PEO可根据PEO/PPO的组成及聚合物分子质量表现出良好的可设计性,此外,随着温度的升高,PEO-PPO-PEO水溶液会形成水相和聚合物富集相的两相体系[9]。由于它们具有独特的核壳结构、低毒性、可设计性和较小的生物免疫响应等特点,已在制药和生物领域广泛应用[21, 22]。
本研究构建二环己基十八冠六(DCH18C6)-双浊点萃取体系,结合火焰原子吸收法,选择性测定了环境水样和食品中的痕量铅。
2 实验部分
2.1 仪器与试剂
TAS-FFH 986火焰原子吸收光谱仪(北京普析通用仪器公司),DF-101S恒温磁力搅拌器(巩义市予华仪器有限公司),25-μL微量进样器(上海安亭微量进样器厂),pH计(PHS-3C,上海理达仪器厂)。
表1 3种PEO-PPO-PEO温敏聚合物的物理参数
Table 1 Physical parameters of three kind of polyoxyethylene-polyoxypropylene-polyoxyethlene (PEO-PPO-PEO)

名称Name平均分子量Averagemolecularweight浊点Cloudpoint(1%)亲水亲油平衡值Hydrophiliclipophilicbalance(HLB)L64290057℃~61℃13L31110037℃3.5L44220045℃~55℃12
PEO-PPO-PEO(L64, L31和L44,武汉新大地环保材料有限公司),具体物理参数见表1;Pb(NO3)2, EDTA, K2HPO4, K3PO4和K2CO3(分析纯,国药集团化学试剂有限公司);DCH18C6(分析纯,北京百灵威化学技术有限公司)。2.2 实验方法
第一步萃取:向10 mL离心管中加入1 mL L64和9 mL含有Pb2+及DCH18C6的样品溶液,再加入一定浓度的K2HPO4,充分振荡混合后,将离心管置于25℃恒温水浴锅中10 min,然后离心,加速其分相,用长针头将下相水溶液吸出弃去。
第二步萃取:向L64富集相中加入0.5 mL一定浓度的EDTA溶液,充分振荡混合后,将离心管置于70℃恒温水浴锅中10 min,然后以3000 r/min离心5 min,分相后,将上相吸出,直接注入仪器分析测定。
2.3 样品预处理
池塘水样品取自镇江。将水样放置于棕色瓶中,用0.45 μm滤膜过滤。
菠菜和枸杞购于镇江某超市,使用前将2.0 g菠菜、枸杞放入10 mL浓HNO3中,待消化完全后,将锥形瓶放在电热板上缓慢加热至黄烟冒尽,再加入3 mL H2O2,继续加热至溶液为无色透明,用蒸馏水稀释定容至50 mL,4℃储存待用。
2.4 实验量化参数
Pb2+的萃取率:E(%)=CaVa/CdVd;方法富集因子: EF=Ca/Cd
其中,Ca和Cd分别表示Pb2+在二次萃取EDTA相和初始样品相中的浓度;Va和Vd分别表示二次萃取EDTA相和初始样品相的体积。
3 结果与讨论
3.1 实验条件优化
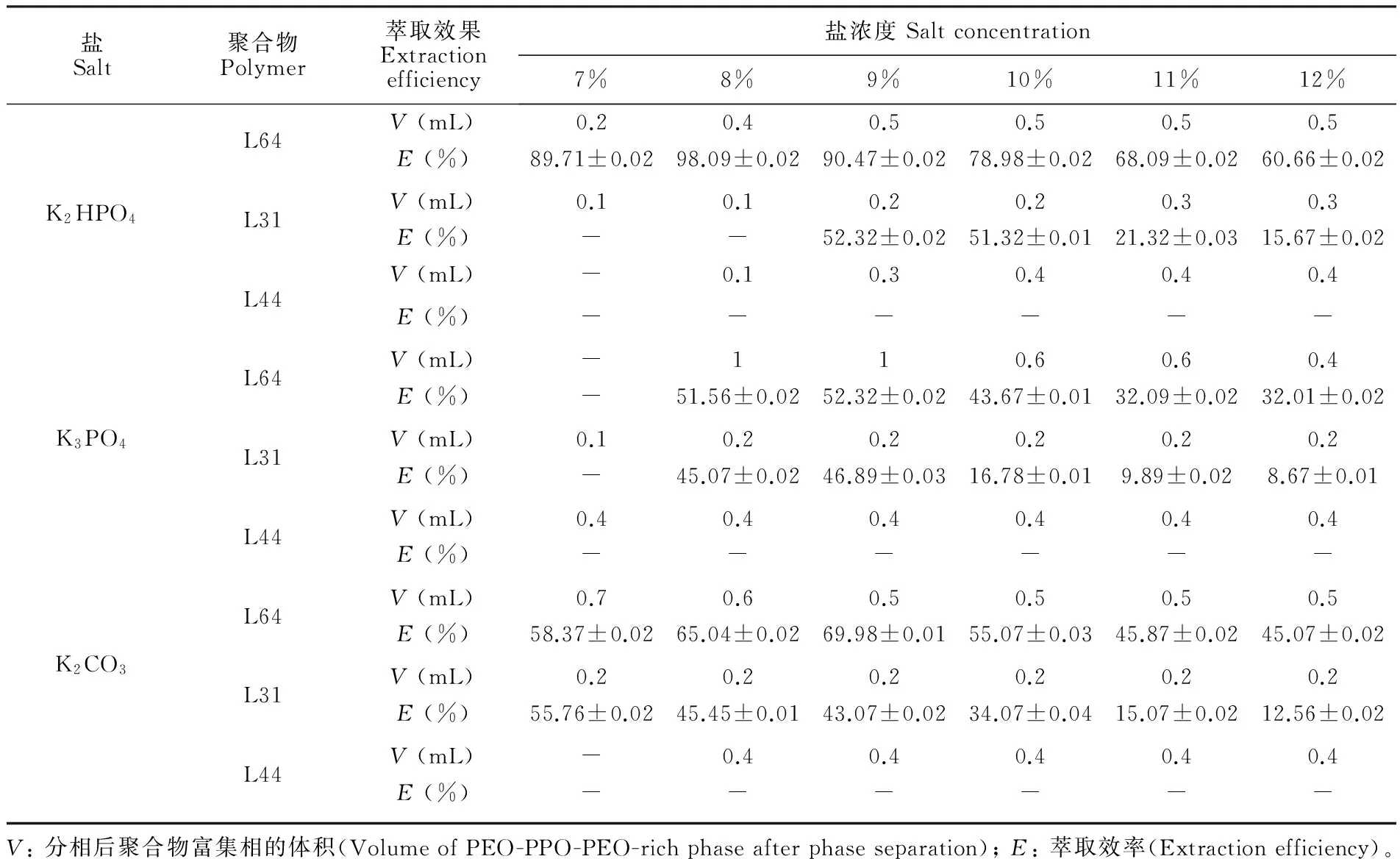
3.1.1 温敏型嵌段聚合物和盐的种类的优化 在PEO-PPO-PEO浓度为2.0%,DCH18C6浓度为200 μg/mL,EDTA的浓度为2.0 mg/mL,第二步萃取温度为70℃,升温时间为10 min的实验条件下,考察温敏型嵌段聚合物和盐的种类对Pb2+萃取效率的影响。由之前的研究[2]可知,在pH≈9.0,Pb2+和冠醚才能形成稳定络合物。因此,实验考察了K2HPO4, K3PO4和K2CO3作为体系的分相盐。在研究的盐浓度的范围内,经测定,K2HPO4体系为pH 8.95~9.26,K3PO4体系为pH 9.56~10.65,K2CO3体系的pH为9.67~10.98。温敏型嵌段聚合物L31, L44和L64的预设浓度均为20% (V/V),K2HPO4, K3PO4和K2CO3的考察浓度均设为7%, 8%, 9%, 10%, 11%和12% (m/V), 通过比较分相体积(V)和Pb2+的萃取效率(E)选取分相盐和聚合物(表2)。结果表明, K2HPO4, K3PO4和K2CO3这3种盐对L31和L44的分相效果均不佳,而仅对L64的分相情况均较好; 只有K2HPO4和L64组成的体系对Pb2+的萃取效果最好。因此本实验选择的分相盐为K2HPO4,聚合物为L64。
3.1.2 K2HPO4浓度的影响 在 L64浓度为2%,DCH18C6浓度为200 μg/mL,EDTA的浓度为2.0 mg/mL,第二步萃取温度为70℃,升温时间为10 min的实验条件下,考察K2HPO4浓度(7%~12%)对Pb2+萃取效率的影响(图1a)。对于K2HPO4-L64体系,随着K2HPO4浓度增加,Pb2+的萃取率从85.71%提高到98.98%,之后便呈下降趋势。这主要是因为盐在溶液中争夺水,增加盐浓度会减少下相中水的含量,进而促进L64进入上相,因此上相L64的浓度随盐浓度增加而增大,但当L64的浓度过大时,会阻碍络合的传质,降低萃取效率。所以本实验K2HPO4的浓度确定在7%~9%。
表2 聚合物和盐种类对Pb2+萃取效果的影响
Table 2 Effect of different salt and different copolymer on extraction efficiency of Pb2+
盐Salt聚合物Polymer萃取效果Extractionefficiency盐浓度Saltconcentration7%8%9%10%11%12%K2HPO4K3PO4K2CO3L64L31L44L64L31L44L64L31L44V(mL)0.20.40.50.50.50.5E(%)89.71±0.0298.09±0.0290.47±0.0278.98±0.0268.09±0.0260.66±0.02V(mL)0.10.10.20.20.30.3E(%)--52.32±0.0251.32±0.0121.32±0.0315.67±0.02V(mL)-0.10.30.40.40.4E(%)------V(mL)-110.60.60.4E(%)-51.56±0.0252.32±0.0243.67±0.0132.09±0.0232.01±0.02V(mL)0.10.20.20.20.20.2E(%)-45.07±0.0246.89±0.0316.78±0.019.89±0.028.67±0.01V(mL)0.40.40.40.40.40.4E(%)------V(mL)0.70.60.50.50.50.5E(%)58.37±0.0265.04±0.0269.98±0.0155.07±0.0345.87±0.0245.07±0.02V(mL)0.20.20.20.20.20.2E(%)55.76±0.0245.45±0.0143.07±0.0234.07±0.0415.07±0.0212.56±0.02V(mL)-0.40.40.40.40.4E(%)------V:分相后聚合物富集相的体积(VolumeofPEO-PPO-PEO-richphaseafterphaseseparation);E:萃取效率(Extractionefficiency)。
3.1.3 L64浓度的影响 以K2HPO4浓度为8%,DCH18C6浓度为200 μg/mL,EDTA的浓度为2.0 mg/mL,第二步萃取温度为70℃,升温时间为10 min为实验条件,考察L64浓度(0.5%~3.0%)对Pb2+萃取效率的影响(图1b)。随着L64用量增加,Pb2+的萃取率由81.90%提高到99.05%,当L64浓度为2.0%, 萃取率最大(99.05%),之后萃取率呈下降趋势。实验表明,L64的浓度太小时,目标物不能完全萃取,导致萃取率降低,;然而当L64浓度过大时,表面活性剂粘度大,会阻碍Pb2+的萃取,也会使萃取率下降。综合考虑,选择L64的浓度范围在1.5%~2.5%。
3.1.4 DCH18C6浓度的影响 以L64浓度为2%,K2HPO4浓度为8%,EDTA的浓度为2.0 mg/mL,第二步萃取温度为70℃,升温时间为10 min为实验条件,考察DCH18C6浓度(50~300 μg/mL)对Pb2+萃取效率的影响(图1c)。DCH18C6浓度在150~250 μg/mL范围内,Pb2+萃取效率较好。在此范围内,Pb2+与DCH18C6形成稳定的络合物,使络合物被有效地萃取入L64富集相,从而保证Pb2+的萃取率。
3.1.5 EDTA浓度的影响 EDTA在第二步浊点萃取中充当的角色是金属离子的反萃剂,加入反萃取剂的目的是破坏DCH18C6与Pb2+形成的络合物,然后将Pb2+反萃到EDTA水溶液中。以L64浓度为2%,K2HPO4浓度为8%,DCH18C6浓度为200 μg/mL,第二步萃取温度为70℃,升温时间为10 min为实验条件,考察EDTA浓度(0.5~3.0 mg/mL)对Pb2+萃取效率的影响。第一步浊点萃取后,向L64富集相中加入不同浓度的EDTA, 其萃取效果(图1d)表明,Pb2+的萃取率先从64.29%上升到最大值99.52%,之后基本不变,保持在98%左右。因此EDTA浓度选择为2.0 mg/mL,结果令人满意。
3.1.6 第二步浊点萃取温度和升温时间的影响 实验考察了第二步浊点萃取温度和加热时间对Pb2+萃取的影响。以L64浓度为2%,K2HPO4浓度为8%,DCH18C6浓度为200 μg/mL,EDTA的浓度为2.0 mg/mL,升温时间为10 min为实验条件,考察第二步浊点萃取温度(60℃, 65℃, 70℃, 75℃, 80℃)对Pb2+萃取效率的影响。在60℃和65℃时,分相较少,约为0.2 mL,同时萃取率也较小(65%)。在70℃~80℃范围内,其分相体积保持在0.6 mL左右,萃取率在70℃时达到最大值98.6%。因此,实验选择第二步萃取温度为70℃。
在70℃条件下,固定其它条件,考察了5~30 min的升温时间对Pb2+萃取效率的影响。在保证高萃取率的前提下,尽量选择较短的升温时间。综合考虑,本实验选择升温时间为10 min 。
3.1.7 BBD响应曲面实验优化 实验采用Design-Expert 8.0建立三因素三水平 BBD的响应曲面设计法优化实验影响因素。在单因素实验基础上,选择影响最明显的3个变量:K2HPO4浓度(7.0%~9.0%),L64 浓度(1.5%~2.5%),DCH18C6浓度(150~250 μg/mL)。其它影响因素保持不变。
实验设计的DCH18C6-DCPE响应曲面图见图2,图中给出了K2HPO4浓度、L64 浓度以及DCH18C6浓度三个因素之一取零水平时,其它两个因素对Pb2+萃取效率的影响。根据实验设计法得到最佳的条件为:K2HPO4浓度取8.13%,L64浓度取2.06%,DCH18C6浓度取207.23 μg/mL,预测萃取率为99.20%。根据最佳实验条件,做3次重复实验,得到Pb2+的萃取率为98.78%,与实验设计的预测值非常接近。因此,利用BBD设计建立的优化模型能够确定实验的优化条件,并得到满意的效果。

图1 DCH18C6-DCPE体系中影响Pb2+萃取率和富集因子的因素Fig.1 Effect of several factors on extraction efficiency (E) and enrichment factor (EF) of Pb2+ in dicyclohexyl-18-crown-6-dual cloud point extraction method (DCH18C6-DCPE)

图2 DCH18C6-DCPE选择性萃取Pb2+的响应曲面图Fig.2 Response surface plots for selective extraction of Pb2+ in DCH18C6-DCPE
3.2 金属干扰离子的影响 为了确保实验体系测定Pb2+的准确性,在最佳实验条件下,讨论干扰离子(Na+, K+, Ca2+, Mg2+, Zn2+, Fe3+, Cd2+, Co2+, Mn2+, Cu2+和 Ni2+)的影响。Pb2+的浓度为70 μg/L。结果见表3。1.0×105倍的Na+和K+, 2.0×104倍的Ca2+和Mg2+, 100倍的Cd2+, Co2+, Mn2+, 50倍的Zn2+和Ni2+, 10倍的Fe3+和Cu2+对Pb2+的萃取几乎没有影响, 由于实际样品中共存金属离子的浓度很低, 因此, 本方法可以准确测定实际样品中Pb2+的含量, 不会受到其它金属离子的干扰。
表3 共存干扰离子对萃取Pb2+的影响
Table 3 Effect of coexisting ions on extraction of Pb2+

共存离子Coexistingions质量比aMassratioPb2+回收率Recovery(%)Na+1.0×10598.67±1.07K+1.0×10599.12±0.85Ca2+2.0×10497.34±1.47Mg2+2.0×10499.36±1.22Cd2+100100.35±1.50Fe3+1097.13±0.81Zn2+5099.37±1.70Co2+10098.90±1.11Mn2+100100.56±1.84Ni2+5099.87±1.07Cu2+10101.16±1.41a共存离子/Pb2+(Coexistingions/Pb2+)。
3.3 金属离子的选择性
为了评价DCH18C6-DCPE的选择性,本实验讨论了7种食品和水样中常有的,而且可能影响Pb2+的萃取和测定的共存金属离子(Co2+, Fe3+, Cu2+, Ni2+, Cd2+, Zn2+, Mn2+),与Pb2+按1∶1比例混合。共存金属离子对Pb2+的干扰主要是由于其它金属离子与金属螯合剂发生反应,从而降低了金属螯合剂对目标物的萃取。如果螯合剂能够从金属离子的混合溶液中选择性萃取Pb2+,则可避免其它金属离子对Pb2+的干扰,结果见图3。在同样的实验条件下,本体系对其它金属离子的萃取率几乎为0。结果表明,以DCH18C6为螯合剂的实验体系具有选择性萃取Pb2+的能力,结果令人满意。
3.4 实验方法性能分析
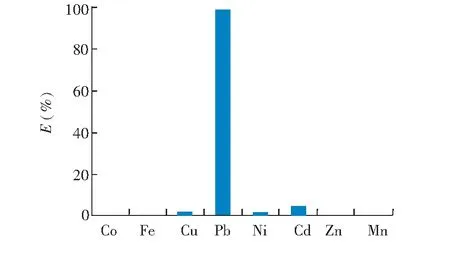
图3 DCH18C6-DCPE体系的选择性Fig.3 Selectivity of DCH18C6-DCPE technique
在优化条件下,得到方法标准曲线的线性范围为0.05~0.3 μg/mL,相关系数R=0.998,检出限为2.8 μg/L,采用70 μg/L Pb2+标准溶液平行测定6次,得到日内精度RSD<4.6%,日间精度RSD<6.8%,萃取率E为98.78%,富集因子EF为18。
3.5 环境水样和食品分析
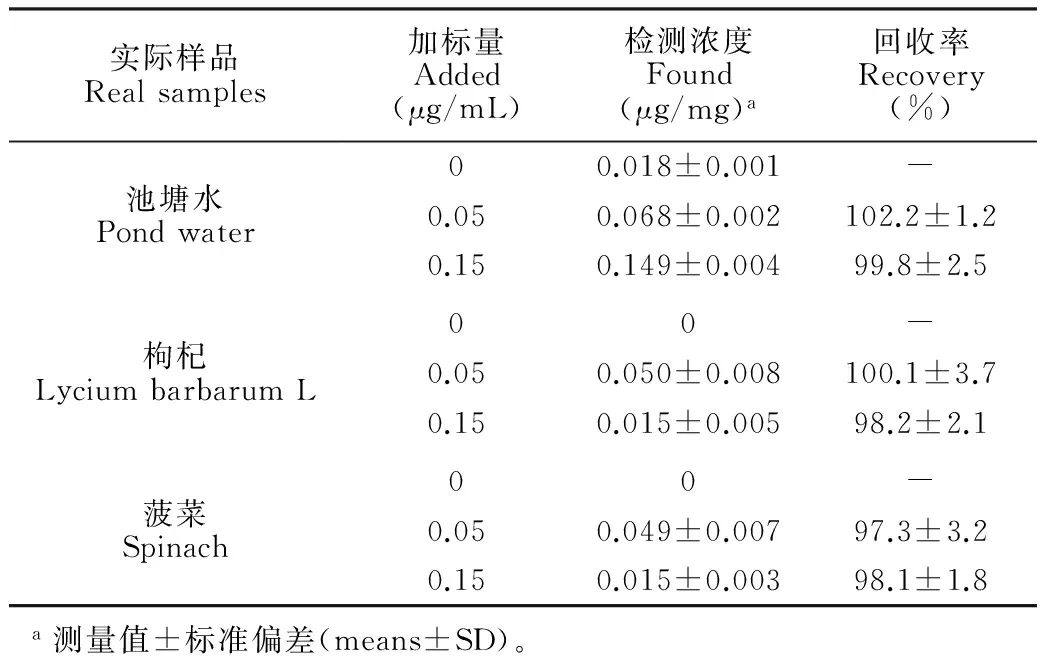
取池塘水、枸杞、菠菜样品溶液,分别加入两组不同浓度混合金属离子溶液:第一组为0.05 μg/mL Pb2+,Co2+,Ni2+,Cd2+;10.00 μg/mL Fe3+, Cu2+,Zn2+,Mn2+,第二组溶液为0.15 μg/mL Pb2+,Co2+,Ni2+,Cd2+;20.00 μg/mL Fe3+,Cu2+,Zn2+,Mn2+。按照最佳条件进行萃取。结果见表4,回收率为97.3%~102.2%,相对标准偏差RSD<3.7%,结果令人满意。由此可见,本方法可用于环境水样和食品中痕量Pb2+的选择性萃取。
表4 环境水样和食品中选择性萃取Pb2+的分析结果
Table 4 Analysis result of selective extraction of Pb2+from water and food
实际样品Realsamples加标量Added(μg/mL)检测浓度Found(μg/mg)a回收率Recovery(%)池塘水Pondwater枸杞LyciumbarbarumL菠菜Spinach00.018±0.001-0.050.068±0.002102.2±1.20.150.149±0.00499.8±2.500-0.050.050±0.008100.1±3.70.150.015±0.00598.2±2.100-0.050.049±0.00797.3±3.20.150.015±0.00398.1±1.8a测量值±标准偏差(means±SD)。
3.6 与其它浊点萃取方法的比较
将本实验方法与其它浊点萃取方法进行了比较,结果见表 5。本方法的检出限均优于其它浊点萃取方法,富集因子优于文献[24],但低于文献[25]和[26],这可能是由于样品体积的原因。若将样品体积增加到50 mL,本方法应该可以得到更高的富集因子。此外,本实验采用双浊点萃取方法可以有效避免表面活性剂对Pb2+测定以及仪器的影响。由此表明,与其它方法相比,本方法不仅性能好,而且更加符合环保理念。
表5 环境水样和食品中选择性萃取Pb2+的分析结果
Table 5 Analysis result of selective extraction Pb2+from water and food

方法Method表面活性剂Surfactant螯合剂Chelatingagent样品体积Samplevolume(mL)检出限LOD(μg/L)富集因子Enrichmentfactor参考文献ReferenceCPE-FAASTritonX-114TANa154.515.1[24]CPE-FAASTritonX-1141-PTSCb503.4225[25]CPE-FAASTritonX-1142-GBIc501129.6[26]DCH18C6-DCPE-FAASL44DCH18C6102.818本方法Thismethoda1-(2-联氮噻吩)-2-萘酚,1-(2-Thiazolylazo)-2-naphthol;b1-苯基氨基硫脲,1-Phenylthiosemicarbazide;c2-胍啶苯并咪唑,2-Guanidi-nobenzimidazole。
1 Zulkali M M D, Ahmad A L, Norulakmal N H.Bioresour.Technol., 2006, 97(1): 21-25
2 CAO Meng-Si, CHEN Jin-Yao, ZHANG Li-Shi.JournalofHygieneResearch, 2014, 43(6): 1051-1056
曹梦思, 陈锦瑶, 张立实. 卫生研究, 2014, 43(6): 1051-1056
3 CHEN Jian-Bo, LIU Wei, Cui Yan-Mei, ZHAO Dao-Yuan, YANG Ming-Min.ChineseJ.Anal.Chem., 2008, 36(3): 401-404
陈建波, 刘 伟, 崔艳梅, 赵道远, 杨明敏. 分析化学, 2008, 36(3): 401-404
4 SUN Bo-Si, Ren Ting, ZHAO Li-Jiao, ZHONG Ru-Gang.SpectroscopyandSpectralAnalysis, 2012, 32(10): 2847-2852
孙博思, 任 婷, 赵丽娇, 钟儒刚. 光谱学与光谱分析,2012, 32(10): 2847-2852
5 ZHOU Xiao, WANG Hui-Qi, FAN Shu-Juan, JIA Qiong.ChineseJ.Anal.Chem., 2013, 41(12): 1905-1909
周 晓, 王荟琪, 范树娟, 贾 琼. 分析化学, 2013, 41(12): 1905-1909
6 Ojeda C B, Rojas F S.MicrochimicaActa, 2012, 177(1-2): 1-21
7 Paleologos E K, Giokas D L, Karayannis M I.Trend.Anal.Chem., 2005, 24: 426-436
8 Wei W, Yin X B, He X W.J.Chromatogr.A, 2008, 1202: 212-215
9 Yin X B.J.Chromatogr.A, 2007, 1154(1): 437-443
10 Arain S S, Kazi T G, Arain J B, Afridi H I, Brahman K D.Microchem.J., 2014, 112: 42-49
11 Melquiades F L, Parreira P S, Yabe M J, Corazza M Z, Funfas R, Appoloni C R.Talanta, 2007, 73: 121-126
12 Kocot K, Zawisza B, Sitko R.Spectrochim.ActaPartB, 2012, 73: 79-83
13 Soylak M, Unsal Y E, Kizil N, Aydin A.FoodChem.Toxicol., 2010, 48: 517-521
14 Shamsipur M, Mashhadizadeh M H, Azimi G.Sep.Purif.Technol., 2002, 27: 155-161
15 Guo X J, Zhu Y D, Wei M J, Wu X M, Lü L H, Lu X H.Chin.J.Chem.Eng., 2011, 19(2): 212-216
16 Izatt R M, Pawlak K, Bradshaw J S.Chem.Rev., 1991, 91: 1721-2085
17 Hiraoka M.CrownCompounds:TheirCharacteristicsandApplications, Kodansha, Tokyo, 1982
18 Pan T, Xu M, Chen X, Sun G, Guo J.Sep.Sci.Technol., 2013, 48(7): 1040-1048
19 Pourreza N, Elhami S.Anal.Chim.Acta, 2007, 596(1): 62-65
20 Aranda P R, Gil R A, Moyano S, de Vito I E, Martinez L D.Talanta, 2008, 75(1): 307-311
21 D′Errico G, Paduano L, Khan A.J.ColloidInterfaceSci., 2004, 279(2), 379-390
22 Li L, Lim L H, Wang Q, Jiang S P.Polymer, 2008, 49, 1952-1960
23 Wang Y, Liu Y, Han J, Wang L, Chen T, Ni L.AnalyticalMethods, 2015, 7(6): 2339-2346
24 Silva E L, dos Santos Roldan P.J.Hazard.Mater., 2009, 161:142-147
25 Citak D, Tuzen M.FoodChem.Toxicol., 2010, 48:1399-1404
26 Dallali N, Zahedi M M, Yamini Y.ScientiaIranica, 2007, 14(4): 291-296
(Received 7 August 2015; accepted 13 September 2015)
This work was supported by the National Natural Science Foundation of China (Nos.31470434, 21406090)
Selective Extraction of Lead from Water and Food Samples by Dicyclohexy-18-crown-6-Dual Cloud Point Extraction Method
MAO Yan-Li1, HAN Juan*2, CUI Wan-Jing3, WANG Yun3, TANG Xu3, XIA Jin-Chen3, LIU Ying-Ying2
1(SchoolofMunicipalandEnvironmentalEngineering,HenanUniversityofUrbanConstruction,Pingdingshan467036,China) 2(SchoolofFoodandBiologicalEngineering,JiangsuUniversity,Zhenjiang212013,China)3(SchoolofChemistryandChemicalEngineering,JiangsuUniversity,Zhenjiang212013,China)
A new extraction method, dicyclohexyl-18-crown-6 (DCH18C6)-dual cloud point extraction method (DCH18C6-DCPE), was developed for extraction and determination of Pbin environmental water and food samples. The DCH18C6-DCPE method included two cloud point extraction (CPE) steps. At the first CPE procedure, DCH18C6 was used as selective chelating agent of Pb2+, and the formed hydrophobic complex (Pb-DCH18C6) was entrapped in a thermoseparating triblock copolymer (L64) rich phase. At the second CPE stage, the L64-rich phase was treated with a certain amount of Ethylene Diamine Tetraacetic Acid (EDTA) solution, and Pb2+was back extracted into the aqueous phase for analysis due to its stronger combining capacity with EDTA. The single factor experiment and response surface methodology design were used to obtain the optimal condition, namely 2.06% L64 (m/m), 8.13% K2HPO4(m/m), 207.23 μg/mL DCH18C6, 70℃ of extraction temperature, and 10 min of extraction time. Under the optimized conditions, the calibration curve was linear in the range of 0.05-0.3 μg/mL (R2=0.998), the extraction efficiency of Pbwas 98.8%, and the limit of detection (LOD) was 2.8 μg/L. Besides, the precisions of inter-day RSD<4.6% and intra-day RSD<6.8% were obtained. Moreover, the proposed method was successfully applied to the determination of Pb2+in water and food samples with the recoveries of 97.3%-102.2% and a relative standard deviation (RSD) lower than 3.7%. The results indicated that the proposed method was effective for the determination of Pb2+in real samples.
Dicyclohexyl-18-crown-6; Dual cloud point extraction; Thermoseparating triblock copolymer L64; Lead
10.11895/j.issn.0253-3820.150630
本文系国家自然科学基金资助项目(Nos.31470434, 21406090)和江苏出入境检验检疫局科技计划项目(No.2015KJ27)
2015-08-07 收稿;2015-09-13接受
* E-mail: hanjuan@ujs.edu.cn
