系列大环草酰胺配合物的合成与表征——推荐一个综合化学实验
2016-11-24张瑞红杨光明
张瑞红 杨光明
(南开大学化学学院,天津300071)
·化学实验·
系列大环草酰胺配合物的合成与表征——推荐一个综合化学实验
张瑞红*杨光明
(南开大学化学学院,天津300071)
采用加热回流和溶剂热两种方法合成了三种大环草酰胺系列配合物,并对所得配合物进行单晶结构解析。使用元素分析、红外光谱、电子光谱、ESR谱对配合物进行了表征和性质研究。该实验原料简单易得,实验方法简便易行,可操作性强,有利于培养学生的实践能力和创新能力。
回流;溶剂热;大环草酰胺;配合物;表征
www.dxhx.pku.edu.cn
实验教学改革的一项重要内容是实验教学内容的提升或改变。如今将科研成果转化为本科或研究生实验教学内容已经受到很多教育工作者的重视,越来越多的成功转化实例被报道[1-4]。这些实例均立足于学科研究前沿和热点领域,不仅使教学内容更加丰富和深入,还可以拓宽学生的知识面,激发学生学习的兴趣,提高学生学习的热情和积极性。该实验项目来源于笔者的科研课题,我们经过反复实践,把这个项目转化为具有开放型特色的综合性实验。该实验涉及配合物合成中的两种常用方法,配合物单晶结构作图的两种软件以及配合物结构表征和性质研究的常用技术手段,知识要点多,学科覆盖面广,同时具有很好的可操作性,有利于培养学生的实践能力和创新能力。
1 实验目的
(1)了解配合物合成基本策略。
(2)掌握配合物合成及单晶培养基本方法。
(3)了解配合物结构表征手段和方法。
2 实验原理
大环草酰胺配合物合成反应原理如下:
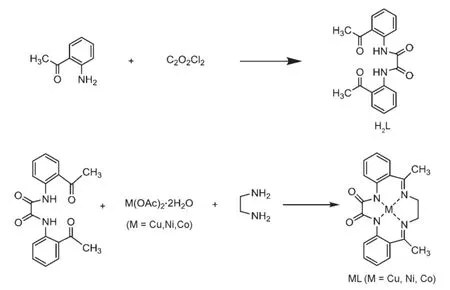
所得配合物一方面作为大环配合物中的一种,对于揭示生命现象的化学本质,对于新材料、新技术的开发具有重要意义;另一方面通过外延的羰基氧原子桥联另一个金属离子,从而使得多金属配合物的合成更加可控。同时因含有的草酰胺基团可有效地传递顺磁离子间的磁交换作用,使得该类配合物成为一种合成多核配合物的优良多原子桥基配体。
3 实验用品
(1)试剂:2-氨基苯乙酮、甲苯、草酰氯、无水乙醇、碳酸氢钠、水合醋酸铜、氢氧化钠、甲醇、乙二胺、水合醋酸镍、水合醋酸钴、氮气。
(2)仪器:电磁搅拌器、烧杯、布氏漏斗、滴管、圆底烧瓶、球形冷凝管、量筒、水热釜、Perkin-Elemer 240型元素分析仪、Shimadzu IR-408型红外光谱仪、Jasco V-570型紫外-可见分光光度计、BurkerEMX-6/1型电子自旋共振谱仪、Rigaku and Rigaku/MSC(2005)型X射线衍射仪。
4 实验内容
4.1配体二乙酰草酰二苯胺(H2L)的合成
室温下,将13.5 g(0.1 mol)2-氨基苯乙酮溶解在500 mL甲苯溶液中,搅拌下向此溶液中缓慢滴加草酰氯至无新的沉淀产生为止,搅拌一小时后过滤,将得到的白色固体依次用甲苯、无水乙醇、饱和NaHCO3以及水洗涤,真空干燥,得到二乙酰草酰二苯胺(H2L)乳白色固体粉末。
4.2配合物的合成
大环草酰胺配合物是参照文献通过模板反应方法合成的[5]。
配合物1(CuL(MeOH)):将0.324 g(1 mmol)二乙酰草酰二苯胺(H2L),0.199 g(1 mmol)水合醋酸铜,0.08 g(2 mmol)NaOH的混合物加入到20 mL甲醇溶液中,搅拌下再滴入约0.12 g(2 mmol)乙二胺,加热回流8 h,静置冷却至室温,过滤得到红色针状晶体,将红色针状晶体用甲醇重结晶得到适合X射线分析的红色块状晶体。产率83%-87%。
配合物2(NiL):采用与配合物1相似的方法合成,在相同条件下用水合醋酸镍代替水和醋酸铜,加热回流后得到红色针状晶体,将所得滤液放置一周后得到适合X射线分析的红色块状晶体。产率78%-82%。
配合物3(CoL):取0.0324 g(0.1 mmol)H2L放入25 mL水热釜中,加入18 mL无水乙醇,0.0249 g(0.1 mmol)水合醋酸钴,通入N210 min,滴入0.018 g(0.3 mmol)乙二胺,立即密封。于110°C下反应48 h,程序降温至室温,过滤得到适合X射线分析的深红色菱形晶体。产率42%-47%。
4.3配合物的表征及性质研究
4.3.1单晶结构解析
三种配合物的X射线单晶衍射数据解析由指导教师完成。对配合物1和2使用Diamond软件作图,如图1、图2所示。对配合物3使用XP作图软件作图,如图3所示。
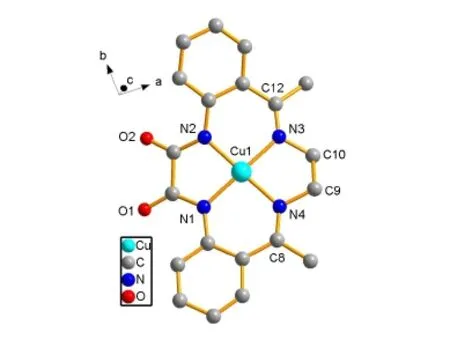
图1 由Diamond软件作出的配合物1(CuL(MeOH))的晶体结构图
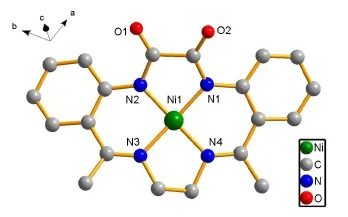
图2 由Diamond软件作出的配合物2(NiL)的晶体结构图
4.3.2元素分析
对配合物1-3中的C、H、N的含量进行了元素分析,实验结果与理论值相当吻合,这一结果也进一步验证了晶体结构解析的正确性。如表1所示。
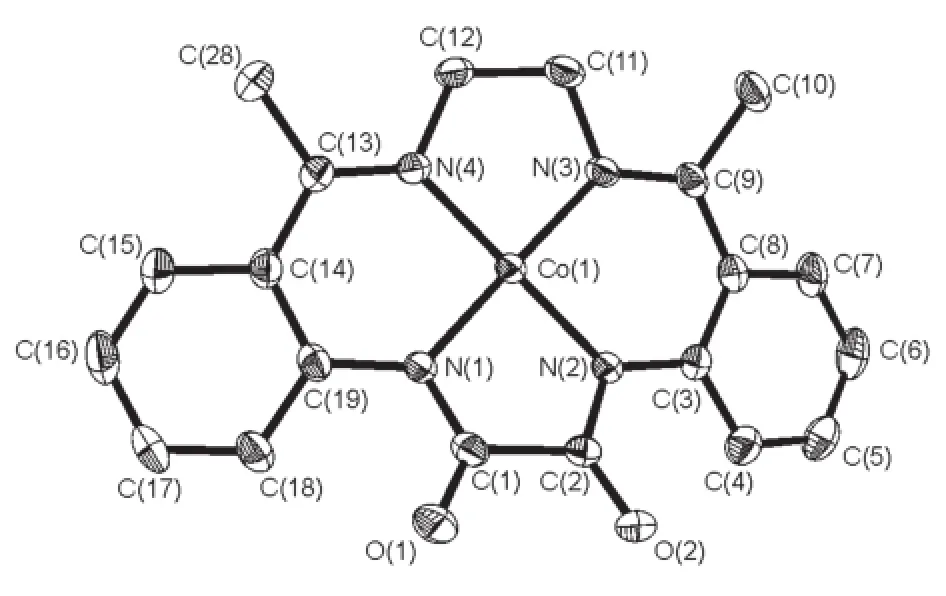
图3 由XP软件作出的配合物3(CoL)的晶体结构图
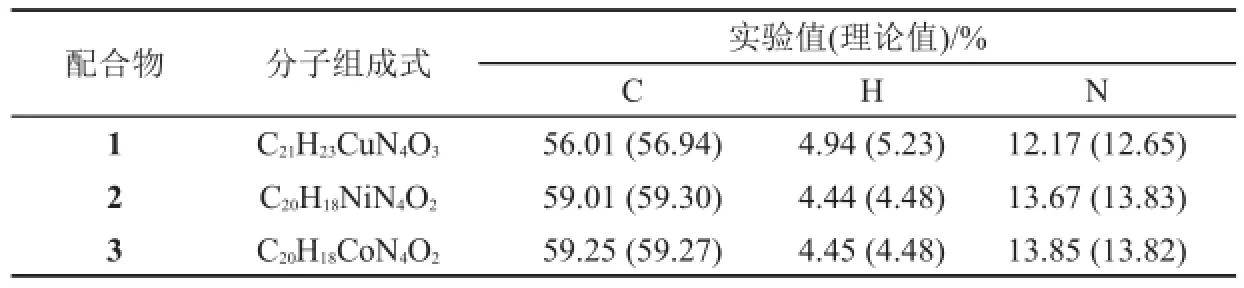
表1 配合物的元素分析数据
4.3.3红外光谱分析
(1)配体二乙酰草酰二苯胺(H2L)的红外光谱。
配体H2L在1675 cm-1处出现酮的νC=O特征吸收峰,1645、1610和1590 cm-1处为酰胺的νC=O特征吸收峰,在1450-1400 cm-1处有苯环的νC=C特征吸收峰,在3200和1500 cm-1处为酰胺的νN―H特征吸收峰。
(2)配合物的红外光谱。
配合物1-3的红外光谱特征峰非常相似(表2),与配体H2L相比,未出现酮的νC=O特征吸收峰和酰胺νN―H的特征吸收峰,在1640-1660 cm-1处的强吸收峰可以归属为草酰胺基团νC=O的吸收峰,在1530-1550 cm-1处的吸收峰可以归属为亚胺νC=N的特征峰,这与文献报导的草酰胺基团和亚胺的特征吸收峰相吻合[6-8]。
4.3.4配合物的电子光谱分析
室温下,在DMF溶液中测定了配合物1和2的电子光谱。配合物1在500 nm以下的紫外区和高频可见区有较强的吸收带,可以归属为配体内部的π-π*跃迁及金属到配体的电荷转移跃迁(MLCT);配合物1在515 nm处较弱的吸收峰可归属为Cu(II)离子自旋允许的d-d跃迁[9,10]。配合物2在425 nm处的中强峰可归因为金属到配体的电荷转移跃迁和四方场中Ni(II)离子的d-d跃迁的叠加作用[11,12]。
4.3.5配合物的电子顺磁共振(ESR)谱分析
在室温下测定了配合物1的X波段多晶粉末电子顺磁共振(ESR)谱。用WINEPR和SimFonia程序对配合物1的谱图进行了较好的拟合,拟合结果见图4。通过拟合结果可以看出在整个磁场范围内,实验值与理论值均非常吻合。拟合结果为g||(2.20)>g⊥(2.15)>2.02,表明Cu(II)离子处于拉长的平面四边形环境,未成对电子处于轨道上,该结果与单晶结构解析结果相一致。

表2 配合物的主要红外光谱数据
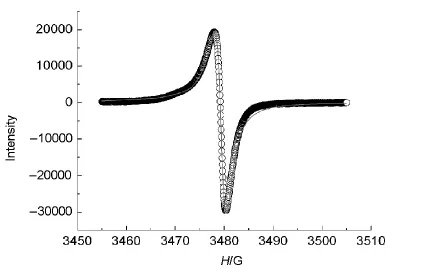
图4 配合物1的X波段多晶粉末电子顺磁共振(ESR)谱
5 注意事项
(1)反应釜内的液体填充量不得超过四分之三。反应前反应釜一定要拧紧,反应中切勿打开烘箱,反应结束后要等反应釜温度降到室温才能打开反应釜。
(2)实验中需要用到氮气钢瓶,操作时需谨慎小心。
6 思考题
(1)用XP作图软件作配合物1和2的晶体结构图,用Diamond作图软件作配合物3的晶体结构图,比较这些结构图,阐述两种作图软件的优缺点。
(2)讨论常见配合物的合成方法及表征手段。
(3)试从该类单核配合物出发提出合成多核配合物的策略和可能的多核配合物结构。
7 结束语
本实验采用二乙酰草酰二苯胺作为配体,采用加热回流及溶剂热两种合成方法,分别与Cu(II)盐、Ni(II)盐、Co(II)盐反应,得到系列配合物。分别用Diamond和XP两种作图软件作出配合物单晶结构图,利用元素分析、红外光谱、电子光谱、ESR谱对配合物进行表征和性质研究。实验所需原料及合成方法均较简单,可操作性强,可使学生较容易地掌握学科前沿知识,对于培养学生实践和创新能力也有积极意义。
本实验项目所涉及实验内容已在我校实验教学中心综合化学实验室所开设的开放实验中反复实践多次,实验重复性很好,取得了很好的教学效果。综合化学实验室每年招收数量不等的各年级本科生进入实验室,为学生提供了利用课余时间锻炼和提高化学实验技能的场所,培养化学研究的兴趣,增强个人动手能力、团结协作能力、分析和解决问题的能力、科研创新能力,建造了良好的实验平台。
[1]傅水根.中国大学教学,2007,No.4,4.
[2]于兵川,吴洪特,童金强.实验室研究与探索,2009,28(1),133.
[3]曹小华,喻国贞,雷艳红,刘新强,谢宝华.化学教育,2009,No.11,15.
[4]石先莹.大学化学,2015,30(5),26.
[5]Black,D.S.C.;Bos Vanderzalm,C.H.;Hartshorn,A.J.Inorg.Nucl.Chem.Lett.1976,12(8),657.
[6]Taylor,R.;Kennard,O.Acc.Chem.Res.1984,17(9),320.
[7]Baker,A.;Hamer,A.;Livingstone,S.Transition Met.Chem.1984,9(11),423.
[8]Nakamoto,K.Infrared and Raman Spectra of Inorganic and Coordination Compounds(Part B),5th ed.;John Wiley:New York,1997.
[9]Lloret,F.;Journaux,Y.;Julve,M.Inorg.Chem.1990,29(20),3967.
[10]Rillema,D.P.;Brubaker,C.H.Inorg.Chem.1969,8(8),1645.
[11]Cervera,B.L.;Sanz,J.J.;Ibanez,M.;Vila,G.;Lloret,F.;Julve,M.;Ruiz,R.;Ottenwaelder,X.;Aukauloo,A.;Poussereau,S.;Journaux,Y.;Cano,J.C.;Munoz,M.J.Chem.Soc.Dalton Trans.1998,No.5,781.
[12]Yokoi,H.Bull.Chem.Soc.Jpn.1974,47(12),3037.
Synthesis and Characterization of Macrocyclic Oxamide Complexes
ZHANG Rui-Hong*YANG Guang-Ming
(School of Chemistry,Nankai University,Tianjin 300071,P.R.China)
Three macrocyclic oxamide complexes were synthesized by reflux and solvothermal methods. The structures were determined by X-ray crystallography.The complexes were characterized by means of elemental analyses,IR spectra,electronic spectra and ESR spectra.The experimental raw materials are simple and easy to obtain.The experimental methods are simple and easy to operate.It can train students'practical and innovative abilities.
Reflux;Solvothermal;Macrocyclic oxamide;Complex;Characterization
G64;O6-3
10.3866/PKU.DXHX201601034
,Email:zhangrh@nankai.edu.cn
